Describir la experiencia con la administración de toxina botulínica tipo A (OnabotA) en el tratamiento de la migraña crónica (MC) en Segovia durante 16 meses, evaluar su beneficio y buscar marcadores clínicos que sirvan para predecir una mejor respuesta al tratamiento.
Pacientes y métodosEstudio prospectivo de pacientes con MC que recibieron infiltraciones con OnabotA durante 16 meses. Se evaluó la eficacia de OnabotA comparando la reducción en el número de días de cefalea, en la intensidad y efectos adversos. Se comparó el efecto del tratamiento con el factor tiempo mediante un análisis de la varianza de dos vías (ANOVA). Se estudió la correlación del efecto del tratamiento con el resto de las variables mediante un modelo de regresión lineal para buscar marcadores clínicos que sirvan para predecir una mejor respuesta.
ResultadosSe incluyó a 69 pacientes que cumplían criterios de MC. Se les realizó una media de 2 infiltraciones. La edad media fue de 43 años, el 88,4% fueron mujeres. La frecuencia de los días de cefalea y su intensidad se redujeron de forma significativa (p<0,005) y esta mejoría se mantuvo a lo largo del tiempo. Se encontró una correlación negativa entre la reducción de la intensidad y el número de tratamientos previos a la administración de la toxina.
ConclusiónEl efecto beneficioso de la OnabotA en la MC se mantiene en el tiempo, siendo un tratamiento seguro y bien tolerado. No debe retrasarse su uso en MC refractaria, ya que su beneficio podría ser mayor cuanto antes se administre.
The purposes of this study were to describe our 16-month experience with onabotulinumtoxinA (OnabotA) for the treatment of chronic migraine (CM) in the Spanish province of Segovia, evaluate its benefits, and determine clinical markers of good response to treatment.
Patients and methodsProspective study of patients with CM who received OnabotA for 16 months. The effectiveness of OnabotA was evaluated based on the reduction in the number of headache days, pain intensity, and side effects. We used two-way analysis of variance (ANOVA) to assess the effects of treatment according to the time factor. We studied the correlation between treatment effects and other variables using a linear regression model to establish the clinical markers of good response to treatment.
ResultsWe included 69 patients who met the diagnostic criteria for CM. Patients underwent an average of 2 infiltrations. Mean age was 43 years; 88.4% were women. The number of headache days and pain intensity decreased significantly (P < .005); improvements remained over time. We found a negative correlation between the reduction in pain intensity and the number of treatments before OnabotA.
ConclusionThe beneficial effects of OnabotA for CM continue over time. OnabotA is a safe and well-tolerated treatment whose use for refractory CM should not be delayed since early treatment provides greater benefits.
La migraña crónica (MC) es un trastorno neurológico muy complejo que produce una gran discapacidad e impacto en la calidad de vida de los que la padecen1. La Clasificación Internacional de las Cefaleas (tercera edición [ICHD-III]) define la MC como un mínimo de 15 días de cefalea al mes, durante más de 3 meses, de los cuales 8 días o más cumplen criterios de migraña con o sin aura o responden al tratamiento específico de migraña2. Su complejidad se basa en que en su patogenia están implicadas múltiples vías sensitivas, redes emocionales, sistemas autonómicos y funciones corticales. Representa una prevalencia entre el 1,4 y el 2,2%3.
La administración de la toxina botulínica tipo A (OnabotA) en el tratamiento preventivo de la MC ha supuesto un gran cambio en el manejo terapéutico de estos pacientes. Los datos definitivos que confirmaron la eficacia de este tratamiento en MC se derivan del programa PREEMPT. En estos estudios se demostró la eficacia de la toxina tanto en la disminución de frecuencia de días de cefalea al mes como en la disminución del uso de medicación y mejoría en la calidad de vida. Además, no solo demostró su eficacia, sino también la seguridad, la tolerabilidad y la baja incidencia de efectos adversos que se obtienen al aplicar este tratamiento4-6. Estudios posteriores al 2010 han seguido confirmando su eficacia, seguridad, mejoría en calidad de vida, ahorro en costes y efecto a largo plazo7,8.
Aunque el efecto analgésico de la toxina en la MC no está totalmente aclarado, las teorías al respecto parecen que no solo lo explican por su capacidad de inhibir la liberación de acetilcolina a nivel presináptico, produciendo un efecto relajante a nivel de la musculatura pericraneal, sino que además se conocen el papel y la importancia de otras vías implicadas en este efecto analgésico. La toxina produce inhibición de liberación de mediadores nociceptivos, como el péptido relacionado con el gen de la calcitonina, glutamato y sustancia P de terminaciones periféricas aferentes. Esto produce una inhibición de la inflamación neurogénica y secundariamente de la sensibilización periférica de fibras nociceptivas, con lo que se reducen las señales dolorosas periféricas al sistema nervioso central y, de esta forma, se reduce la sensibilización central, que es lo que finalmente explica la cronificación de la migraña9,10.
El objetivo de este estudio ha sido describir la experiencia con la administración de la OnabotA en el tratamiento de la MC en el Complejo Asistencial de Segovia durante un período de 16 meses, evaluando el beneficio del tratamiento en la reducción de la intensidad y la frecuencia de los días de cefalea e intentando identificar posibles marcadores clínicos que sirvan para predecir una mejor respuesta al tratamiento.
Pacientes y métodosDiseño del estudioSe realizó un estudio prospectivo con una muestra de pacientes pertenecientes a la consulta de neurología general del Complejo Asistencial de Segovia (mayores de 18 años) en el periodo comprendido entre el 1 de octubre del 2013 y el 1 de abril del 2015, que cumplían criterios de MC según la última clasificación internacional de las cefaleas (ICHD-III)2.
Se procedió a realizar infiltraciones de OnabotA según el protocolo PREEMPT (155 unidades [U] en 31 puntos) cada 3-4 meses durante 16 meses. Se recogieron las siguientes variables: demográficas (edad y sexo) y clínicas (antecedentes psiquiátricos, tratamientos preventivos previos, número de días de cefalea al mes e intensidad de los episodios). Se instruyó a los pacientes en el uso de un diario de cefaleas para recoger el número de días con dolor, así como en el uso de la escala visual analógica (EVA) para evaluar en cada paciente y de forma individual la intensidad de los episodios. Además, se recogieron el número de infiltraciones realizadas a cada paciente y los efectos adversos debido a la infiltración con OnabotA, tanto el tipo de efecto como su duración y resolución.
Se evaluó la eficacia de OnabotA comparando la respuesta después de cada ciclo con la situación basal, es decir, antes de la primera infiltración. Esta evaluación se llevó a cabo a través de los siguientes parámetros: cambio en el número de días de cefalea, mejoría subjetiva de los pacientes, según la EVA y efectos adversos por la infiltración de OnabotA.
Análisis estadísticoEl análisis estadístico se realizó con el programa SPSS v15.0.
Se comparó el efecto del tratamiento con el factor tiempo comparando los parámetros basales y tras cada periodo de tratamiento mediante un análisis de la varianza de 2 vías (ANOVA). Se consideró estadísticamente significativo si el valor de p era menor de 0,006. Se estudió la correlación del efecto del tratamiento con el resto de las variables mediante un modelo de regresión lineal, con el fin de buscar marcadores clínicos que puedan servir en la práctica clínica diaria para predecir una mejor respuesta del tratamiento en estos pacientes.
ResultadosSe incluyó a 69 pacientes que cumplían criterios de MC. La edad media de la muestra fue de 43,2±15,2 años (con un rango entre 18-80 años), el 88,4% fueron mujeres. Tenía antecedentes psiquiátricos el 20,3% (incluyendo trastornos de ansiedad y depresivos) y había recibido tratamientos previos el 82,6%. La distribución de los tratamientos preventivos recibidos antes de la administración de la OnabotA se resumen en la tabla 1; de los pacientes incluidos, 12 de los 69 pacientes (17,4%) no habían recibido ningún tratamiento preventivo previo, 24 (34,8%) habían recibido uno, 21 (30,4%) 2, 8 (11,6%) 3 y 4 pacientes (5,8%) 4. Además, 8 pacientes (11,6%) habían recibido toxina previamente con una dosis media de 94,4±21,5 U (IC del 95%, 76,4-112,3), antes de ser aplicado el protocolo PREEPMT (155 U).
Distribución de tratamientos preventivos
| Tratamientos | Pacientes, n (%)a |
|---|---|
| Betabloqueantes | 17 (29,8) |
| Antagonistas del calcio | 15 (26,3) |
| Anticomiciales | 30 (52,6) |
| Antidepresivos | 44 (77,2) |
A los pacientes incluidos en el estudio se les realizó una media de 2 infiltraciones con OnabotA, con un rango entre 1 y 5. De entre los 69 pacientes, 50 recibieron 2 infiltraciones, 28, 3, y 14, 4 en el periodo de estudio. Un paciente recibió una quinta infiltración, pero no se le incluyó en el estudio por no haber tenido lugar la revisión para poder comprobar el resultado de la última infiltración dentro del periodo de estudio.
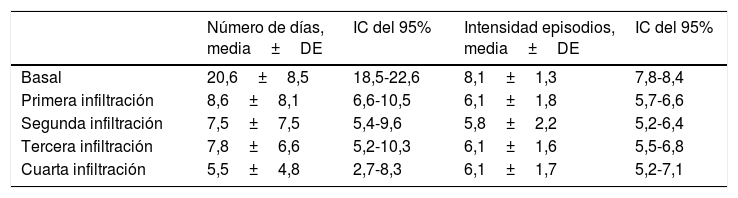
Partiendo de una media de 20,6±8,5 días de cefalea al mes, observamos que en la primera infiltración el número de días se redujo a 8,6±8,1, en la segunda a 7,5±7,5, en la tercera a 7,8±6,6 y en la cuarta a 5,5±4,8. Y, partiendo de una media de 8,1±1,3 de intensidad de los episodios de cefalea al mes, según la EVA, observamos que en la primera infiltración la intensidad se redujo a 6,1±1,8, en la segunda a 5,8±2,2, en la tercera a 6,1±1,6 y en la cuarta a 6,1±1,7. Los cambios respecto a la frecuencia y la intensidad de los episodios se resumen en la tabla 2. Con estos resultados se comprobó una reducción porcentual de días de cefalea del 48,5% y una reducción porcentual respecto a la intensidad del 20,7%.
Número de días de cefalea e intensidad de los episodios en cada infiltración
| Número de días, media±DE | IC del 95% | Intensidad episodios, media±DE | IC del 95% | |
|---|---|---|---|---|
| Basal | 20,6±8,5 | 18,5-22,6 | 8,1±1,3 | 7,8-8,4 |
| Primera infiltración | 8,6±8,1 | 6,6-10,5 | 6,1±1,8 | 5,7-6,6 |
| Segunda infiltración | 7,5±7,5 | 5,4-9,6 | 5,8±2,2 | 5,2-6,4 |
| Tercera infiltración | 7,8±6,6 | 5,2-10,3 | 6,1±1,6 | 5,5-6,8 |
| Cuarta infiltración | 5,5±4,8 | 2,7-8,3 | 6,1±1,7 | 5,2-7,1 |
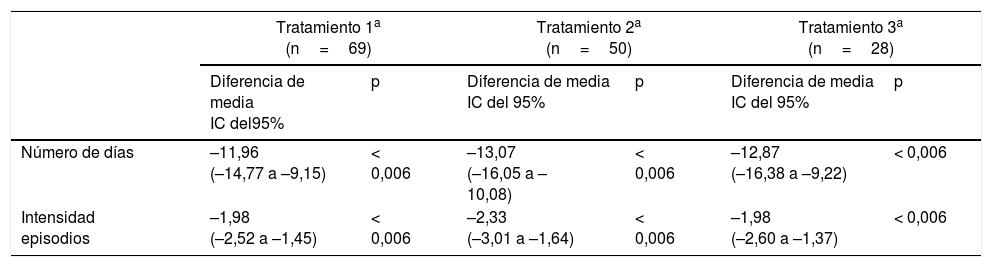
Para evaluar el efecto del tratamiento y el factor tiempo, se realizó un estudio comparativo de las variables «número de días de cefalea» e «intensidad de los episodios» y de sus cambios con respecto al valor basal para todos los pacientes incluidos en el estudio. Los valores de p se calcularon comparando los parámetros basales y tras cada ciclo de tratamiento mediante un análisis de la varianza de 2 vías (ANOVA). Se consideró estadísticamente significativo si el valor de p era menor de 0,006. Se comprobó que el número de días de cefalea y la intensidad de los episodios se reducían de forma significativa tras el tratamiento y se mantenían a lo largo del tiempo en todas las infiltraciones, sin diferencias entre las administraciones. Estos resultados se resumen en la tabla 3.
Comparación de efecto del tratamiento con el factor tiempo
| Tratamiento 1a (n=69) | Tratamiento 2a (n=50) | Tratamiento 3a (n=28) | ||||
|---|---|---|---|---|---|---|
| Diferencia de media IC del95% | p | Diferencia de media IC del 95% | p | Diferencia de media IC del 95% | p | |
| Número de días | –11,96 (–14,77 a –9,15) | < 0,006 | –13,07 (–16,05 a –10,08) | < 0,006 | –12,87 (–16,38 a –9,22) | < 0,006 |
| Intensidad episodios | –1,98 (–2,52 a –1,45) | < 0,006 | –2,33 (–3,01 a –1,64) | < 0,006 | –1,98 (–2,60 a –1,37) | < 0,006 |
Se realizó por separado un análisis de los 28 pacientes que habían recibido 3 infiltraciones y se comprobó que el número de días se reducía de forma significativa tras el tratamiento (mantenido a lo largo del tiempo en las tres infiltraciones, sin diferencias entre ellas) y la intensidad de los episodios también se reducía de forma significativa tras el tratamiento (en las 3 infiltraciones), sin diferencias entre ellas (p<0,005).
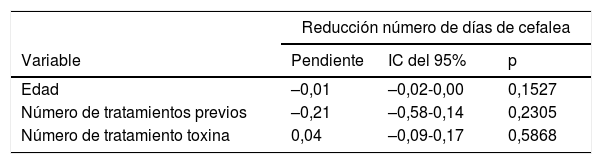
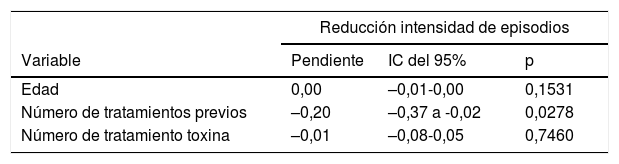
Para evaluar la existencia de marcadores que pudieran predecir una mejor respuesta al tratamiento se realizó un análisis de la correlación entre la variable «reducción del número de días de cefalea y el resto de variables» del estudio mediante un modelo de regresión lineal, en el que se evaluó la pendiente de la recta de regresión. Se consideró estadísticamente significativo un valor de p<0,05. No se encontró relación de la reducción en el número de días con ninguna variable (tabla 4), pero sí con la reducción de la intensidad, donde se demostró que existía una correlación negativa entre la reducción de la intensidad de los episodios y el número de tratamientos previos a la administración de la toxina (pendiente –0,20, IC del 95%, –0,37 a –0,02, p=0,0278), es decir, cuantos menos tratamientos se hubieran pautado al paciente antes del inicio de la toxina, mayor fue la reducción de la intensidad de los episodios de migraña (tabla 5).
De los 69 pacientes, 26 fueron excluidos a lo largo del periodo de estudio por las siguientes razones: 17 pacientes (24,63%) por falta de mejoría (tras 2 infiltraciones de media), uno por embarazo (tras la segunda infiltración), 2 por deseos de embarazo (tras la segunda y tercera, respectivamente), 4 por trastornos psiquiátricos o deterioro cognitivo en estudio (tras la primera infiltración) y 2 no fueron localizados tras la primera infiltración.
Respecto a los efectos adversos, solo se registraron 3 casos con ptosis leves; todos ellos se resolvieron en menos de una semana.
DiscusiónLa MC representa un trastorno muy complejo y es considerada, según la Organización Mundial de la Salud, como una de las patologías que mayor discapacidad produce11,12.
Es un trastorno caracterizado por la persistencia del dolor y refractariedad a los tratamientos preventivos, lo que condiciona una gran discapacidad e impacto en la calidad de vida de aquellos pacientes que la presentan12. Debido a la gran repercusión y las implicaciones que conlleva, es importante compartir la experiencia con tratamientos eficaces en estos pacientes en la vida real y en las condiciones de nuestra práctica clínica diaria. Se deben diseñar estudios con criterios de inclusión y respuestas a los tratamientos similares, para evitar errores o datos no concluyentes. La selección correcta de los pacientes es la clave para el éxito del tratamiento con toxina en MC.
La OnabotA fue aprobada en 2010 para el tratamiento preventivo de la MC, basándose en los resultados obtenidos en el programa PREEMPT con 1.354 pacientes que recibieron infiltraciones con toxina botulínica cada 12 semanas durante 24 semanas seguido de una fase abierta de 32 semanas. Se trató de un ensayo clínico multicéntrico doble ciego, controlado con placebo y llevado a cabo en 2 fases y consiguió demostrar la eficacia, seguridad y tolerabilidad de la OnabotA en el tratamiento preventivo en la MC en adultos4–8,13.
Nuestra serie es un estudio prospectivo que evalúa la eficacia y tolerabilidad del tratamiento con OnabotA en la vida real, es decir, en pacientes con MC que acuden a nuestra consulta de neurología del Complejo Asistencial de Segovia. Hemos seguido el protocolo PREEMPT utilizando el paradigma de inyección de 155 U de OnabotA en 31 puntos repartidos en cabeza y cuello13. Nuestros resultados muestran una mejoría significativa que se mantiene a lo largo del tiempo, con una reducción porcentual en los días de cefalea del 48,5% y en la intensidad de los episodios del 20,7%. A diferencia del estudio original, hemos valorado con la EVA la intensidad del dolor, en lugar de los días de mayor severidad de la cefalea o la repercusión en las actividades de la vida diaria.
Comparando los datos de nuestra serie con el estudio original PREEMPT6, hemos obtenido resultados demográficos similares y, por tanto, comparables en la práctica clínica real. Nuestra serie presentaba una edad media de 43,2 años y un predominio femenino (88,4% fueron mujeres), siendo en el estudio original la edad media de 41,1 años y el 87,6% mujeres. La MC en nuestra serie vuelve a demostrar que es una patología más frecuente en mujeres, de acuerdo también con otros trabajos publicados13,14.
En el estudio original se incluyó a pacientes con un mínimo de 20 días de cefalea6. En nuestra serie el número basal de días de cefalea, antes de iniciar el tratamiento con OnabotA, también fue de 20,6 días. Se consiguió una reducción porcentual en días de cefalea del 48,5%. En el estudio original se realizó una valoración diferente de la eficacia del tratamiento a la que hemos llevado a cabo nosotros. Los autores mostraron de forma significativa una reducción como mínimo del 50% de días de cefalea en el 47,1%6.
Como en otras series publicadas en estos 2 últimos años, que demuestran una amplia experiencia en el tratamiento, no solo hemos obtenido una diferencia significativa en la reducción de días de cefalea tras el tratamiento con OnabotA, sino una evidencia del mantenimiento de este beneficio a lo largo del tiempo10,14–18.
Como novedad respecto a otros estudios publicados hasta ahora y, respecto al estudio original PREEMPT6, hemos obtenido correlación con el número de tratamientos previos, de tal forma, que cuanto antes se administre mayor puede ser el beneficio conseguido. En otros trabajos recientes no se ha conseguido identificar factores predictores clínicos de una respuesta favorable a OnabotA19. Por este motivo, con nuestros resultados podemos recomendar el uso precoz de la OnabotA en la MC refractaria y no retrasar el inicio del tratamiento en estos casos, ya que su beneficio podría ser mayor cuanto antes se administre.
La seguridad y tolerabilidad de la OnabotA fue excelente en nuestra serie, tal y como han reflejado también otros estudios similares14,20,21. Observamos solo 3 casos de ptosis leves (4,3%), similar a otros estudios, incluido el estudio original PREEMPT, que fue del 3,3%6. Nuestros casos se resolvieron en menos de una semana. También hemos podido demostrar que el beneficio se mantiene, es decir, que repetidas inyecciones a lo largo del tiempo son capaces de aumentar el beneficio obtenido después del primer ciclo22.
No hay que olvidar que además hay estudios publicados que muestran que la aplicación de OnabotA en el tratamiento preventivo de la MC es un recurso coste-efectivo y ya es totalmente indiscutible el posicionamiento en este tratamiento en la actualidad23,24.
Nuestro trabajo tiene algunas limitaciones, entre las que destacamos el taman¿o muestral y la ausencia de un grupo control, ya que está basado en una serie de pacientes de la práctica cli¿nica habitual, en la que no podemos contar con un grupo placebo. Aun así aportamos como novedad con nuestra serie la recomendación de no retrasar el uso de la OnabotA en la MC refractaria, ya que su beneficio podría ser mayor cuanto antes se administre.
ConclusiónLa selección de pacientes es la llave para el éxito del tratamiento con OnabotA en el manejo de MC. El efecto beneficioso de la OnabotA en la MC se mantiene en el tiempo, siendo además un tratamiento seguro y bien tolerado. No debe retrasarse su uso en MC refractaria, ya que su beneficio podría ser mayor cuanto antes se administre.
FinanciaciónEl trabajo ha sido financiado por la Fundación del Colegio de médicos de Segovia.
Conflicto de interesesNo otros conflictos de intereses.
Ha sido presentado en la última LXVII Reunión Anual de la SEN 2015 (comunicación oral).