El glioblastoma es el tumor cerebral más frecuente. A pesar de los avances en su tratamiento, el pronóstico sigue siendo pobre, con una supervivencia media en torno a los 14 meses. Los costes directos, aquellos asociados al diagnóstico y el tratamiento de la enfermedad, han sido descritos ampliamente. Los costes indirectos, aquellos derivados de la pérdida de productividad debido a la enfermedad, han sido descritos en escasas ocasiones.
Material y métodoRealizamos un estudio retrospectivo, incluyendo a los pacientes diagnosticados entre el 1 de enero del 2010 y el 31 de diciembre del 2013 de glioblastoma en el Hospital Universitario Donostia. Recogimos datos demográficos, relativos al tratamiento ofertado y la supervivencia. Calculamos los costes indirectos a través del método del capital humano, obteniendo datos de sujetos comparables según sexo y edad, y de mortalidad de la población general a través del Instituto Nacional de Estadística. Los salarios pasados fueron actualizados a euros de 2015 según la tasa de inflación interanual y los salarios futuros fueron descontados en un 3,5% anual en forma de interés compuesto.
ResultadosRevisamos a 99 pacientes, 46 mujeres (edad media 63,53 años) y 53 hombres (edad media 59,94 años). En 29 pacientes se realizó una biopsia y en los 70 restantes se realizó una cirugía resectiva. La supervivencia global media fue de 18,092 meses. Los costes indirectos totales fueron de 11.080.762 € (2015). El coste indirecto medio por paciente fue de 111.926 € (2015).
DiscusiónA pesar de que el glioblastoma es un tipo relativamente poco frecuente de tumor, que supone el 4% de todos los tipos de cáncer, su mal pronóstico y sus posibles secuelas generan una mortalidad y morbilidad desproporcionadamente altas. Esto se traduce en unos costes indirectos muy elevados. El clínico debe ser consciente del impacto del glioblastoma en la sociedad y los costes indirectos deben ser tenidos en cuenta en los estudios de coste-efectividad para conocer las consecuencias globales de esta enfermedad.
Glioblastoma is the most common primary brain tumour. Despite advances in treatment, its prognosis remains dismal, with a mean survival time of about 14 months. Many articles have addressed direct costs, those associated with the diagnosis and treatment of the disease. Indirect costs, those associated with loss of productivity due to the disease, have seldom been described.
Material and methodWe conducted a retrospective study in patients diagnosed with glioblastoma at Hospital Universitario Donostia between January 1, 2010 and December 31, 2013. We collected demographics, data regarding the treatment received, and survival times. We calculated the indirect costs with the human capital approach, adjusting the mean salaries of comparable individuals by sex and age and obtaining mortality data for the general population from the Spanish National Statistics Institute. Past salaries were updated to 2015 euros according to the annual inflation rate and we applied a discount of 3.5% compounded yearly to future salaries.
ResultsWe reviewed the records of 99 patients: 46 women (mean age 63.53) and 53 men (mean age 59.94); 29 patients underwent a biopsy and the remaining 70 underwent excisional surgery. Mean survival was 18.092 months for the whole series. The total indirect cost for the series was €11 080 762 (2015). Mean indirect cost per patient was €111 926 (2015).
DiscussionAlthough glioblastoma is a relatively uncommon type of tumour, accounting for only 4% of all cancers, its poor prognosis and potential sequelae generate disproportionately large morbidity and mortality rates which translate to high indirect costs. Clinicians should be aware of the societal impact of glioblastoma and indirect costs should be taken into account when cost effectiveness studies are performed to better illustrate the overall consequences of this disease.
El glioblastoma (GB) es el tumor primario más frecuente y más agresivo del sistema nervioso central1,2. Su incidencia varía entre 0,59 y 3,69 por 100.000 habitantes y año, y suponen aproximadamente un 1,4% del total de casos de cáncer diagnosticados1,3,4. El tratamiento de primera línea del GB consiste en la extirpación quirúrgica máxima de la lesión sin afectar áreas elocuentes, seguida de quimiorradioterapia con temozolomida y de 6 ciclos de quimioterapia secuencial también con temozolomida, según el denominado protocolo Stupp2,4-6.
El gran impacto de las enfermedades neurológicas sobre el coste sanitario depende de su prevalencia e incidencia, del número y la complejidad de las técnicas necesarias para su diagnóstico y tratamiento, y de la discapacidad y dependencia que generan7,8. En el caso del GB, la lesión cerebral permanente que provoca y su resistencia a la mayor parte de tratamientos generan una morbimortalidad desproporcionadamente elevada, con una supervivencia a los 5 años entre el 0,05 y el 4,7%, según las diferentes series publicadas1,3.
El objetivo del presente estudio es proporcionar al clínico información relativa al impacto económico de la enfermedad sobre el sistema de salud y sobre la sociedad y facilitar la toma de decisiones para que la distribución de los recursos disponibles se realice de una manera racional7. Los estudios publicados en nuestro entorno en relación con el coste sanitario del GB se centran habitualmente en los costes directos que derivan del tratamiento quirúrgico, radioterápico y quimioterápico, bien con temozolamida o con implantes de carmustina tópica6,9. Los costes indirectos, asociados a la pérdida de productividad, han sido analizados con menor frecuencia y deben, también, ser tomados en consideración a la hora de calcular el impacto económico total de dicha enfermedad10.
Material y métodoEl presente estudio contó con la aprobación del Comité de Ética de nuestro centro, con el código de proyecto: UND-CGM-2015-01. Todos los pacientes incluidos firmaron un consentimiento informado específico para la recogida y la divulgación de datos con propósito científico.
Realizamos un estudio retrospectivo, recogiendo sistemáticamente todos los pacientes diagnosticados de GB en nuestro centro durante un periodo de 4 años (entre el 1 de enero del 2010 y el 31 de diciembre del 2013) según los criterios descritos por la Organización Mundial de la Salud (OMS) publicados en 200711, a partir de la base de datos del Servicio de Anatomía Patológica. La estrategia de tratamiento propuesta a cada paciente fue determinada por un equipo multidisciplinar, que incluye a neurocirujanos, oncólogos médicos, oncólogos radioterápicos, neurólogos, radiólogos, farmacéuticos y patólogos12.
Se revisaron las historias clínicas, recogiendo datos epidemiológicos relativos al tratamiento administrado, fechas de diagnóstico y último contacto con el paciente o fallecimiento, según correspondiera. Los datos fueron incluidos en una base de datos Microsoft Access 2013 (Microsoft Corporation, Washington, EE.UU.). El análisis estadístico se llevó a cabo en Microsoft Excel 2013 (Microsoft Corporation, WA) y SPSS v.21 (IBM Corporation, Nueva York, EE. UU.).
Todos los costes se expresan en euros correspondientes al año 2015 (€ 2015). Para el cálculo de costes se obtuvo el salario medio anual por trabajador según sexo, edad y año, disponible a través de Instituto Nacional de Estadística13. Para trasladar los costes pasados a € 2015 se empleó como referencia la tasa de inflación interanual. Para la estimación de los costes futuros expresados en € 2015 se empleó el salario medio constante correspondiente al año 2015 y se aplicó una tasa de descuento en forma de interés compuesto del 3,5% anual, tomando como referencia la recomendación de las guías del National Institute for Clinical Excellence (NICE)14 para este tipo de estudios publicadas en 2013. Además de ello, los costes futuros fueron ajustados en función del riesgo de muerte de la población en general según sexo y edad, igualmente accesible a través del INE13.
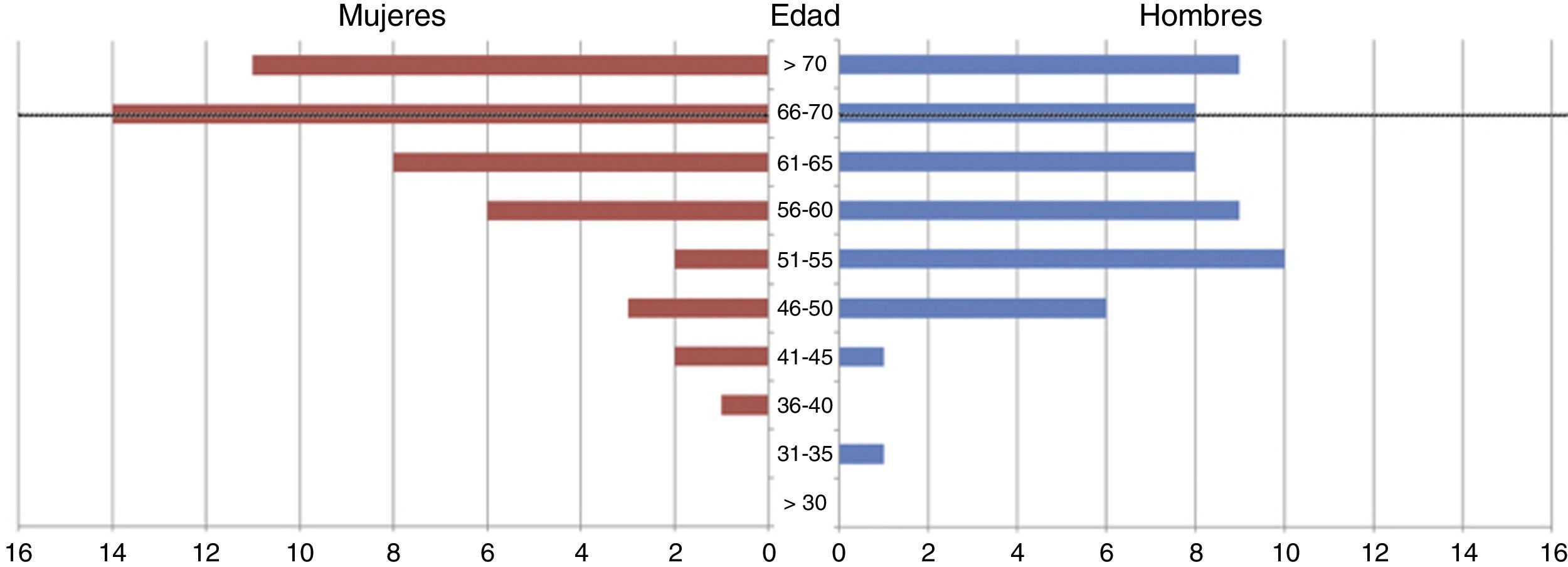
ResultadosSe recogieron los datos de un total de 99 pacientes consecutivos. La edad media desviación típica [SD] fue de 61,61 ± 9,89 años (rango 31-80). En la distribución por sexos encontramos un 46,46% de mujeres (n=46) y un 53,53% de hombres (n=53) (fig. 1). La edad media ± SD en el grupo de las mujeres (media 63,53 ± 9,69 años) fue algo mayor que en el grupo de los hombres (media 59,94 ± 9,84).
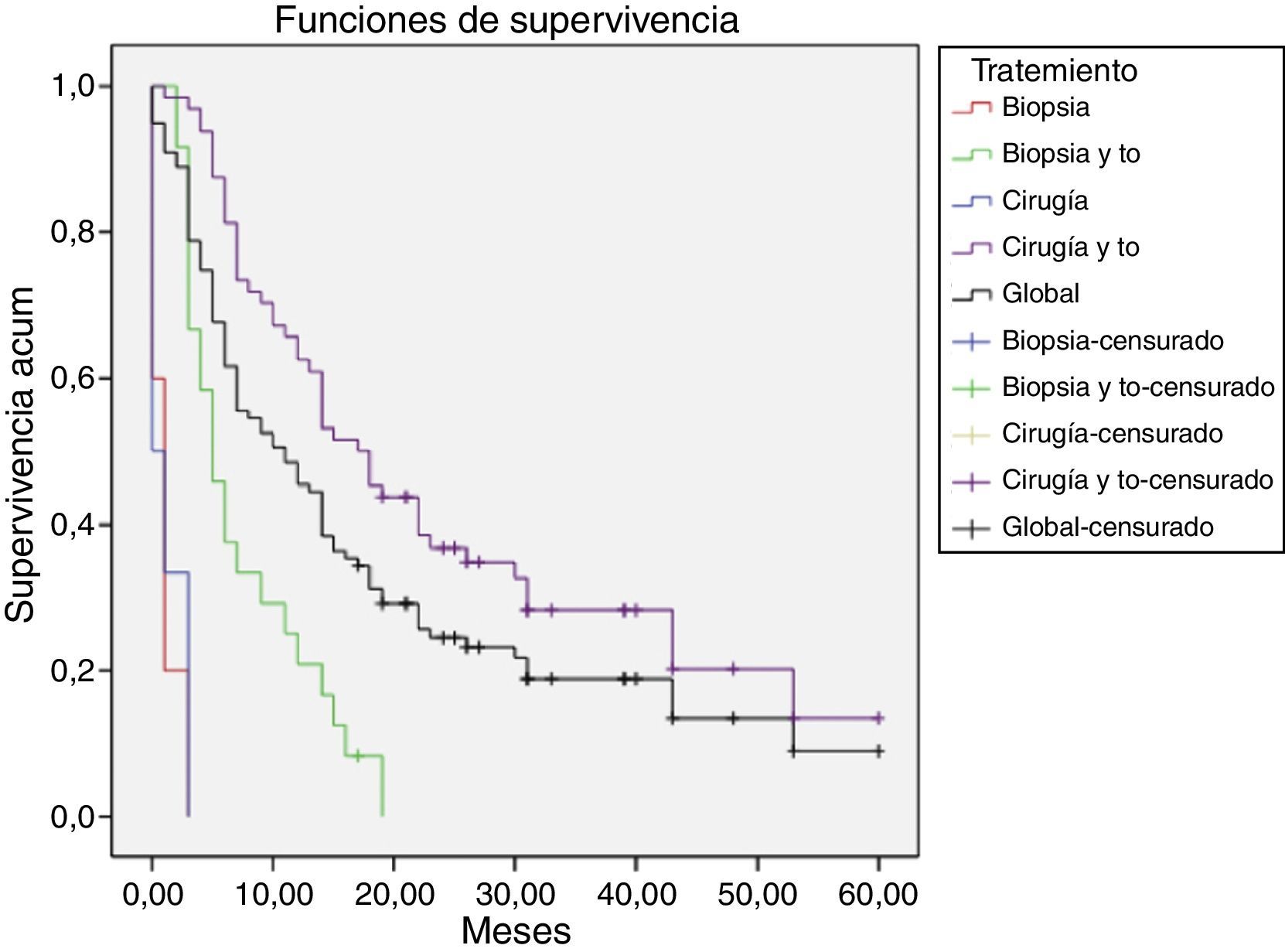
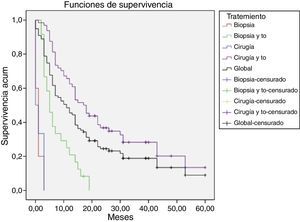
Los 99 pacientes acumularon un total de 111 intervenciones quirúrgicas. La mortalidad operatoria fue de un 8,08% (8 pacientes). Un total de 11 pacientes (11,11%) no recibieron tratamiento complementario alguno, bien por complicaciones posquirúrgicas, decisión del paciente, una situación funcional pobre con un índice de Karnofsky bajo o por progresión tumoral inmediata al tratamiento quirúrgico. En el momento de la conclusión del estudio 86 pacientes (86,86%) habían fallecido. La mediana de seguimiento fue de 39 meses (media 39,72 ± 18,3, rango 18,2-63). La mediana de supervivencia fue de 10,9 meses y la media global fue de 18,1 meses (intervalo de confianza del 95% [IC del 95%], 14,2-21,97) (tabla 1, fig. 2). Encontramos diferencias significativas (Mantel-Cox p<0,001) en función del tratamiento aplicado a cada paciente, alcanzando una supervivencia media de 24,64 meses en aquellos pacientes en los que se realizó una exéresis quirúrgica de la lesión y se llegó a administrar algún tipo tratamiento oncológico.
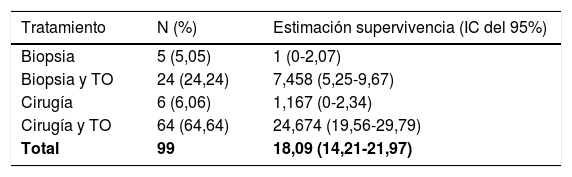
Estimación de supervivencia media (meses) de Kaplan-Meier en función del tratamiento recibido
| Tratamiento | N (%) | Estimación supervivencia (IC del 95%) |
|---|---|---|
| Biopsia | 5 (5,05) | 1 (0-2,07) |
| Biopsia y TO | 24 (24,24) | 7,458 (5,25-9,67) |
| Cirugía | 6 (6,06) | 1,167 (0-2,34) |
| Cirugía y TO | 64 (64,64) | 24,674 (19,56-29,79) |
| Total | 99 | 18,09 (14,21-21,97) |
TO: tratamiento oncológico.
El 58,58% de los pacientes estudiados (n=58) contaban en la fecha del fallecimiento con una edad no superior a 67 años, por lo que se encontraban en edades productivas de la vida (fig. 1). El coste indirecto total en nuestra serie, según el método descrito, fue de 11.080.762,84 € 2015. El coste medio por paciente fue de 111.926,90 ± 148.958,47 € 2015.
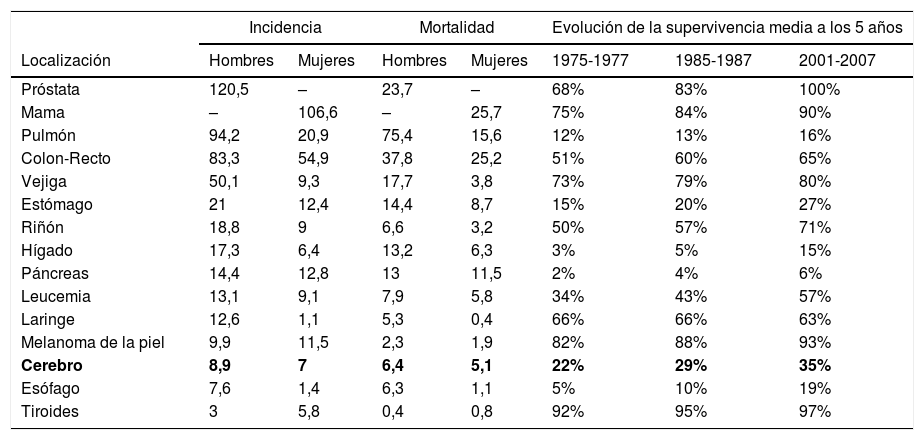
DiscusiónEn el presente trabajo analizamos los pacientes diagnosticados de GB en los años 2010-2013 en nuestro centro. Según los datos disponibles a partir de la OMS, correspondientes al año 2012 para España15, las neoplasias cerebrales malignas tienen una incidencia de 7.9/100.000 habitantes y año. Dicha incidencia se encuentra muy por debajo de otros tumores, como el cáncer de mama, que es el más frecuente en mujeres, el cáncer de próstata, que es el más frecuente en hombres, o el cáncer de colon y pulmón, que son los más frecuente en ambos sexos (tabla 215,16). La mortalidad debida al cáncer está encabezada por el cáncer de mama y el de colon en mujeres, y por el cáncer de pulmón y de colon en hombres (tabla 215,16). Cuando analizamos la supervivencia de los pacientes con neoplasias cerebrales malignas en 5 años, observamos que presentan una de las más bajas, en torno al 35% (tabla 215,16). El GB es la neoplasia cerebral primaria más frecuente pero con una incidencia relativamente baja con respecto a la de otro tipo de cánceres, variando entre 0,59 y 3,69 por 100.000 habitantes y año. A pesar de los avances en el tratamiento quirúrgico y oncológico de estas lesiones, el pronóstico continúa siendo pobre, con una supervivencia a los 5 años entre el 0,05 y el 4,7%1,3,4.
Incidencia, mortalidad y evolución de la supervivencia media de los principales tipos de cáncer según localización
| Incidencia | Mortalidad | Evolución de la supervivencia media a los 5 años | |||||
|---|---|---|---|---|---|---|---|
| Localización | Hombres | Mujeres | Hombres | Mujeres | 1975-1977 | 1985-1987 | 2001-2007 |
| Próstata | 120,5 | – | 23,7 | – | 68% | 83% | 100% |
| Mama | – | 106,6 | – | 25,7 | 75% | 84% | 90% |
| Pulmón | 94,2 | 20,9 | 75,4 | 15,6 | 12% | 13% | 16% |
| Colon-Recto | 83,3 | 54,9 | 37,8 | 25,2 | 51% | 60% | 65% |
| Vejiga | 50,1 | 9,3 | 17,7 | 3,8 | 73% | 79% | 80% |
| Estómago | 21 | 12,4 | 14,4 | 8,7 | 15% | 20% | 27% |
| Riñón | 18,8 | 9 | 6,6 | 3,2 | 50% | 57% | 71% |
| Hígado | 17,3 | 6,4 | 13,2 | 6,3 | 3% | 5% | 15% |
| Páncreas | 14,4 | 12,8 | 13 | 11,5 | 2% | 4% | 6% |
| Leucemia | 13,1 | 9,1 | 7,9 | 5,8 | 34% | 43% | 57% |
| Laringe | 12,6 | 1,1 | 5,3 | 0,4 | 66% | 66% | 63% |
| Melanoma de la piel | 9,9 | 11,5 | 2,3 | 1,9 | 82% | 88% | 93% |
| Cerebro | 8,9 | 7 | 6,4 | 5,1 | 22% | 29% | 35% |
| Esófago | 7,6 | 1,4 | 6,3 | 1,1 | 5% | 10% | 19% |
| Tiroides | 3 | 5,8 | 0,4 | 0,8 | 92% | 95% | 97% |
Los datos epidemiológicos de nuestra serie coinciden con los encontrados por otros autores en contextos similares17,18. En nuestro entorno Graus et al.2 estudió un total de 834 pacientes diagnosticados de GB provenientes de 19 centros españoles. La edad media fue de 62 años con una mayor incidencia en pacientes varones (61,3%) y la mediana de supervivencia de 11,8 meses (IC del 95%, 10,7-12,8). Por su parte, Brodbelt et al.17 analizan en 2015 a 10.743 pacientes diagnosticados de GB en Inglaterra durante el periodo 2007-2011 y describe igualmente una mayor incidencia en el sexo masculino (60,04%), con un pico de incidencia entre los 65 y los 75 años de edad. En este estudio de base poblacional, la mediana de supervivencia fue de 6,1 meses. Típicamente, los estudios de base poblacional muestran supervivencias inferiores en comparación con los estudios hospitalarios puesto que incluyen a todos los pacientes de una población determinada, mientras que las series hospitalarias solamente incluyen a aquellos pacientes que reciben atención médica especializada. Yabroff et al.18 describen una serie de 1.202 pacientes diagnosticados de GB en Estados Unidos, con una mediana de supervivencia de 10 meses (IC del 95%, 9-11) y una supervivencia a los 3 años del 12,6%. Todos los estudios coinciden con el nuestro en que existen diferencias significativas en la supervivencia a favor de los pacientes que reciben tratamiento quirúrgico con posterior quimioterapia y radioterapia adyuvantes en comparación con aquellos que, por alguna razón, no reciben dicho tratamiento. Además del tratamiento recibido, son múltiples los factores descritos asociados a la supervivencia de los pacientes con GB, especialmente la edad en el momento del diagnóstico y la situación funcional expresada habitualmente mediante el Karnofsky Performance Status. Sin embargo, el análisis detallado de los factores pronósticos de los pacientes de nuestra serie excede los objetivos del presente estudio.
Se estima que en España el coste de las enfermedades neurológicas en general supone el 10,4% del gasto sanitario total19 y se prevé que en el 2030 ascienda hasta el 14,4%20. La revisión sistemática llevada a cabo por Pares-Badell et al.21 estimaron que el coste total de las enfermedades neurológicas en España en 2010 (incluyendo las enfermedades mentales) ascendió a 83.749 millones de euros. El coste total de una enfermedad se puede dividir en coste directo, indirecto, intangible e informal. El coste directo se relaciona directamente con la actividad y refleja el sacrificio de recursos sanitarios empleados para su prevención, diagnóstico y tratamiento. Este tipo de costes es el más habitualmente descrito en la literatura y se calcula a partir del gasto generado por el ingreso hospitalario, el tratamiento administrado y el posterior control en consultas. Por tanto, su estimación es menos susceptible a variabilidades de criterio. Estos costes incluyen, también, los relacionados con el transporte de los pacientes, los servicios sociales y los derivados de la adaptación del domicilio por la discapacidad generada7,22-24. Los costes indirectos se pueden considerar costes de oportunidad y representan la pérdida de productividad generada por la enfermedad. Incluyen el fallecimiento, la jubilación prematura, el absentismo laboral y la menor productividad en relación con la posible discapacidad generada7,10,22,24. Los costes informales corresponden a la prestación no remunerada en el cuidado del paciente por parte de la familia y el entorno del paciente. En ocasiones, este tipo de coste se incluye dentro de los costes directos y, debido a su difícil estimación y a que no son analizados en la mayor parte de los estudios, se los denomina también el «sistema invisible de salud»7,10,25. Por último, los costes intangibles corresponden a la pérdida de calidad de vida sufrida por el paciente. En ocasiones, este tipo de costes se incluye dentro de los costes indirectos. En el presente trabajo nos centraremos en el estudio de los costes indirectos, entendiendo los mismos como la pérdida de productividad asociados a la enfermedad.
El tratamiento de primera línea del GB establecido a partir de 2005, según el denominado protocolo Stupp, consiste en la extirpación quirúrgica máxima de la lesión sin afectar áreas elocuentes, seguida de quimiorradioterapia con temozolomida (75mg/m2/di¿a durante el periodo de administración de la radiación hasta 60Gy) y de 6 ciclos de quimioterapia secuencial también con temozolomida (150-200mg/m2/di¿a durante 5 di¿as cada 28 di¿as)5. La complejidad de los procesos tanto diagnósticos como terapéuticos necesarios se asocian a unos costes directos elevados9,26. En 2004 Chang et al.27 estudiaron los costes directos asociados al tratamiento de 7 tipos de cáncer en los Estados Unidos tratados entre los años 1998 y 2000. En dicho estudio, analizaron a un total de 653 pacientes con tumores cerebrales malignos, calculando un incremento medio ± SD en el coste frente a la población control de 46.452 ± 12.492 $. En la distribución de dichos costes los factores más importantes fueron el coste del tratamiento radioterápico y quirúrgico, si bien se trata de un periodo previo a la introducción del tratamiento con temozolamida. En el estudio llevado a cabo en 1996 por Silverstein et al.28 en pacientes diagnosticados de GB se describe un coste directo total de 91.368 $ e igualmente fue el tratamiento radioterápico el que más contribuyó a dicho coste. En ambos estudios se aprecia que los costes directos alcanzan una meseta en torno al año de tratamiento, debido a la corta supervivencia de los pacientes. En nuestro medio, los autores publicaron en 20119 el coste correspondiente al tratamiento quirúrgico de los tumores cerebrales en general que ascendieron a 13.540,56 € de media por paciente.
El cálculo del coste indirecto asociado a una enfermedad presenta dificultades prácticas, en cuanto que debe estimar costes futuros en plazos de tiempo muy dilatados29. Por esta razón, existen distintas aproximaciones para el cálculo del coste indirecto. De entre ellas el más habitual es el cálculo de la ganancia perdida. Para dicho cálculo se emplea el método del capital humano, que pretende estimar el coste potencial o productividad perdida del paciente hasta la edad teórica de jubilación22, tomando como referencia el salario de individuos comparables en la población. Es importante incluir en este tipo de análisis a los pacientes que realizan tareas fuera del mercado laboral o no remuneradas, como pueden ser las amas de casa, los voluntarios, etc., que pueden ser pasados por alto y que hay que tener en cuenta para el cálculo del coste indirecto total de la enfermedad10. Este método de cálculo, si bien es el más corriente, no está exento de crítica, pues algunos autores opinan que tiende a sobreestimar este tipo de costes22,23. Se argumenta que en un mercado en el que existe una oferta de mano de obra ilimitada (al existir trabajadores desocupados) el trabajo perdido será realizado por otro individuo, que bien puede estar previamente desempleado o ser trasladado desde otro puesto. En este caso, la aproximación empleada se denomina coste de fricción y se calcula sobre la base de la disminución de productividad estimada debida a pérdida de experiencia del nuevo trabajador y los costes de su formación10,22. Hay que subrayar que ninguno de estos 2 métodos pretende cuantificar el valor de la vida humana, sino el impacto económico de la enfermedad sobre la sociedad30. En el presente estudio tomamos como referencia los salarios medios de sujetos comparables (en función del sexo y la edad), ajustando dicho salario a la probabilidad de fallecimiento en la población general y aplicando una tasa de descuento de un 3,5% anual en forma de interés compuesto, recomendado para este tipo de estudios en el informe NICE14. Se evidencia, por tanto, la variabilidad existente en la construcción del modelo en función de la tasa de descuento aplicada (que varía aproximadamente entre un 3 y un 5%, según los estudios14), del ajuste en función a la previsión de progresión salarial y de las diferencias de salario según regiones o países.
En 1996 Blomqvist et al.31 cuantificaron en 101.058 $ (78.218 € 1996) el coste indirecto por paciente en pacientes diagnosticados de tumores cerebrales, lo que suponía el 73% del coste total. Esta cifra se aproxima a los resultados presentados en nuestra serie. En nuestro medio, Navarrete-Navarro et al. analizan los costes indirectos asociados a la hemorragia cerebral espontánea, que ascendieron 31.108 € 2007 por paciente32. En la revisión sistemática realizada por Peres-Badell et al. en 201421 se analizan los costes indirectos asociados a distintas enfermedades neurológicas en España. En dicho estudio los costes indirectos de los tumores cerebrales, en general, son los cuartos más cuantiosos (6.826 €/año), solamente por detrás de las enfermedades neuromusculares (14.185 € 2014/año), la esclerosis múltiple (12.160 € 2014/año) y la enfermedad de Parkinson (9.612 € 2014/año). En nuestro caso, a pesar de que la edad media de nuestra serie fue de 61 años, el hecho de que hasta un 58,58% de los pacientes se encontrara laboralmente activo en el momento del fallecimiento justifica un coste indirecto tan elevado. Según estos datos, los costes indirectos del GB serían superiores a los de otras enfermedades neurológicas. La interpretación de estos resultados debe ser siempre cautelosa, ya que las unidades en las que se expresan son euros en los años correspondientes y a que el método de cálculo varía ligeramente entre los estudios según el modelo empleado. Debido a la naturaleza retrospectiva del actual trabajo, hay que destacar que calculamos los costes indirectos únicamente a partir de la fecha de fallecimiento del paciente, por lo que no se tuvo en cuenta el periodo de supervivencia tras el diagnóstico, la cirugía y el tratamiento oncológico posterior.
Limitaciones del estudioEn el trabajo presentado se incluyó únicamente a los pacientes con diagnóstico anatomopatológico de GB. Existe un grupo de pacientes con imágenes radiológicas indicativas de glioma de alto grado en los que, debido a una pobre situación clínica, avanzada edad, deseo expreso del paciente, etc., se descartó un tratamiento oncológico posterior y no se realizó procedimiento quirúrgico alguno. Estos pacientes no fueron incluidos en el presente estudio al carecer de diagnóstico anatomopatológico. El cálculo de los costes indirectos requiere de una estimación del salario futuro, sujeto a variabilidad en función del modelo empleado, lo que limita la comparabilidad entre estudios.
ConclusionesA pesar de la baja incidencia relativa del GB, su coste sanitario es muy elevado. Los costes indirectos representan una parte importante del coste total asociado al GB. En la actualidad no existe un consenso para la estimación de dichos costes. En nuestra serie hasta una 58,58% de los pacientes se encontraban en edades productivas de la vida, acumulando un coste indirecto medio por paciente 111.926,90 € 2015.
FinanciaciónNo se contó con fuentes de financiación para la elaboración del presente estudio.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.
Los autores quieren agradecer a Andoni Mozo, Maite Iñarra, Ana González y al personal de la unidad 2.ª 3.ª del edificio Aránzazu del Hospital Universitario Donostia por su trabajo constante, buen hacer diario y ayuda indispensable en el tratamiento de nuestros pacientes.
El presente estudio no ha sido presentado previamente en la SEN.