El siguiente reporte de manejo anestésico perioperatorio de cardiomiopatía severa y resección de tumor de feocromocitoma ofrece una experiencia clínica y farmacológica con buen resultado, de una patología de alto riesgo con poca literatura mundial. La paciente ingresa en el servicio de urgencias con angustia, taquicardia, tensión arterial lábil, disnea y dolor abdominal severos. Sus estudios clínicos revelan insuficiencia cardiaca, masa suprarrenal y derivados de catecolaminas elevados en sangre, que hacen diagnóstico de cardiomiopatía severa inducida por feocromocitoma; se realiza el manejo médico de la crisis aguda con terapia en unidad de cuidado intensivo, antihipertensivos y sulfato de magnesio y una vez estabilizada se lleva a resección tumoral laparoscópica. Su evolución postoperatoria fue adecuada, con resolución progresiva de los síntomas. La cardiomiopatía secundaria a feocromocitoma es una patología de alta morbimortalidad e inusual frecuencia, producida por la acción de grandes cantidades de catecolaminas liberadas de modo subagudo por necrosis tumoral hemorrágica o manipulación de feocromocitoma, que requiere manejo estricto en su crisis aguda y en la cirugía de resección definitiva. Este reporte muestra la experiencia de la utilidad del sulfato de magnesio, como fármaco coadyuvante en el control de esta patología durante todo el periodo perioperatorio, por su mecanismo de acción y farmacodinamia. Su fácil accesibilidad hospitalaria, buen resultado clínico y soporte científico son factores importantes para ser considerado una opción farmacológica en feocromocitoma.
The following report on the perioperative anesthetic management of severe cardiomyopathy and resection of pheochromocytoma tumors offers a clinical and pharmaceutical experience with a good outcome for a high-risk pathology with little available world literature. The female patient accesses emergency services in distress with tachycardia, labile blood pressure, dyspnea, and severe abdominal pain. Clinical studies reveal heart failure, an adrenal mass, and derivates of high levels of catecholamines in the blood, which leads to the diagnosis of severe cardiomyopathy induced by pheochromocytoma. The medical management for the acute crisis is performed with therapy in the intensive care unit, antihypertensives and magnesium sulfate. Once stabilized, a laparoscopic tumor resection followed. Her postoperative progress was adequate with a progressive resolution of symptoms. Cardiomyopathy secondary to pheochromocytoma is a pathology with high morbimortality and low frequency and is produced by the action of great quantities of catecholamines released subacutely due to hemorrhagic tumor necrosis or manipulation of the pheochromocytoma. It requires strict care in its acute crises and during surgery for its definitive resection. This report shows our experience with the usefulness of magnesium sulfate as a contributory drug in the control of this pathology throughout the perioperative period due to its mechanism of action and pharmacodynamics. Its easy availability in hospitals, the good clinical results it produces, and its scientific backing are important factors that make it a pharmacological option for pheochromocytoma.
El feocromocitoma es un tumor originado en las células cromafines productoras de catecolaminas, encontrado principalmente en la médula adrenal1. Los principales signos clínicos debidos al efecto agudo de catecolaminas secretadas en altas concentraciones son: hipertensión, palpitaciones, cefalea, ansiedad, sudoración y palidez. Las complicaciones potencialmente letales como arritmia, isquemia cardiaca o periférica, miocardiopatía, y enfermedad cerebrovascular, pueden ocurrir por liberación aguda e incontrolada de catecolaminas en la inducción anestésica y/o la cirugía de resección tumoral. Una presentación inusual preoperatoria es la cardiomiopatía severa con hipertensión, compromiso miocárdico hipertrófico o dilatado, edema pulmonar y arritmias2. El manejo adecuado de la crisis aguda se basa en el control de la contractilidad cardiaca con estabilización de ritmo, frecuencia y presión arterial3.
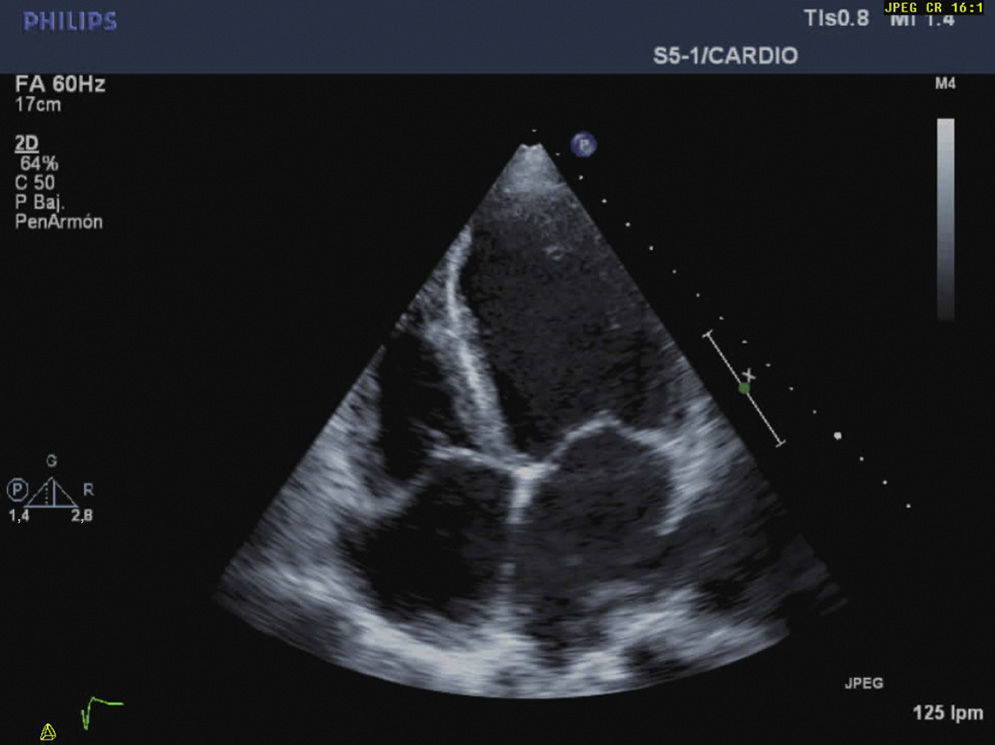
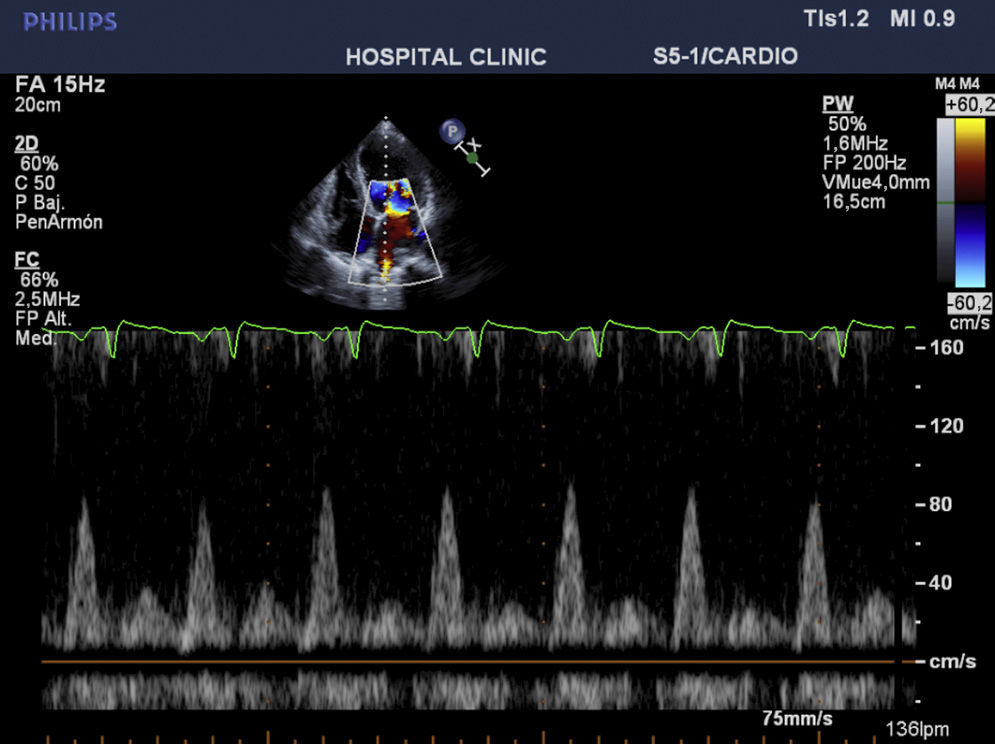
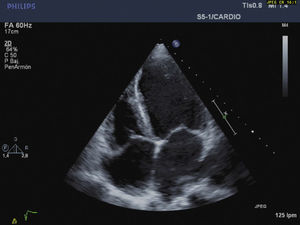
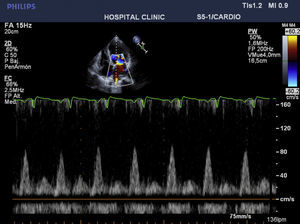
CasoReportamos el caso de una paciente de 42 años de edad, sin antecedentes patológicos importantes, ingresada en la unidad coronaria con síntomas de ansiedad, polipnea, sudoración, dolor y distensión abdominal. A su admisión presentaba presión arterial lábil entre 180/120 y 95/60mmHg, frecuencia cardiaca de 115 × min, soplo sistólico mitral e ingurgitación yugular. El electrocardiograma evidenciaba taquicardia sinusal y elecocardiograma transtorácico: dilatación ventricular izquierda, hipocinesia global severa, patrón diastólico restrictivo con relación E/A de 3,8cm/seg, fracción de eyección de 20%, presión sistólica de arteria pulmonar de 85mmHg e insuficiencia tricuspídea y mitral severas (figs. 1 y 2). Los niveles enzimáticos cardiacos eran normales, así como la arteriografía coronaria.
Ante la escanografía abdominal que reportaba una imagen de tumor suprarrenal derecho con necrosis, se sospechó feocromocitoma e inició dosaxosina 4mg/día y bisoprolol 1,5mg/día. Los niveles plasmáticos de derivados de catecolaminas (metanefrina de 2063 pg/ml [normal<90] y normetanefrina de 1291 [normal<200]), y los estudios funcionales de imágenes confirmaron el diagnóstico. A pesar del tratamiento, durante las dos primeras semanas persistió la inestabilidad de presión arterial e igual compromiso de contractilidad, por lo cual se modificó el fármaco alfabloqueador por fenoxibenzamina y se suspendió el betabloqueador. El ecocardiograma de la semana siguiente reveló solo mínima mejoría de fracción de eyección al 25%. Se decidió iniciar el sulfato de magnesio intravenoso para mejorar contractilidad, función diastólica y disminución de efectos tóxicos del calcio intracelular en el miocardio, a razón de un bolo de 40mg/kg peso e infusión de 15mg/Kg hora. Una semana después, el día prequirúrgico, aunque la fracción de eyección continuaba en el 25%, se observaba una gran mejoría de la función diastólica, presión pulmonar sistólica a 29mmHg, relación E/A en 1,2cm/seg, e insuficiencia mitral y tricuspídea en grado leve.
El día de la cirugía se procedió a preparar para resección laparoscópica de feocromocitoma. Bajo sedación, se realizó monitoría invasiva de presión arterial, encontrando presión arterial media de 105 mmHg y frecuencia cardiaca de 100 por minuto. Se realizó inducción con etomidato 0,2mg/kg, fentanyl 3 mcg/kg, rocuronio 0,6mg/kg e intubación orotraqueal sin complicaciones cardiovasculares. El mantenimiento anestésico se realizó con fentanyl 3 mcg/kg, rocuronio 10 mcg/kg/min y desfluorane 4-5% mac, así como infusión de sulfato de magnesio a 15mg/kg/hora continuado hasta el momento de la resección tumoral completa.
La función cardiaca fue monitorizada con ecocardiografía transesofágica y catéter de arteria pulmonar Swan-Ganz modificado (Edwards CCO/SVO2 746HF8) permitiendo estimación continua de gasto cardiaco, volumen final de diástole (VEFD) y fracción de eyección derechas. El perfil inicial fue: gasto cardiaco de 3,4 l/min, VEFD 240ml, fracción de eyección del 25%, presión venosa central de 22mmHg, resistencia vascular sistémica de 2850 dinas.seg/cm5, resistencia vascular pulmonar de 340 dinas.seg/cm5, por lo que se inició dobutamina a 5 mcg/kg/minuto. La monitorización invasiva permitió determinar progresivamente la mejoría en contractilidad hasta una fracción de eyección final de 42%, con reducción del VEFD hasta 160ml, y realizar aumento titulado de volemia, vigilando la presión venosa central que pasó de valores de 22 a 6 mmHg. Se presentaron dos momentos de crisis hipertensiva a los 30 y 50 minutos de cirugía (presión arterial media: 122 y 160 mmHg, respectivamente) controlados con fentolamina en bolo de 2mg cada uno. El resultado quirúrgico fue satisfactorio con un tiempo quirúrgico de 120 minutos y sangrado de 350cc. La extubación se realizó sin inconvenientes cardiovasculares ni neuromusculares, con evolución posquirúrgica adecuada y soporte inotrópico que se pudo retirar a las 24 horas.
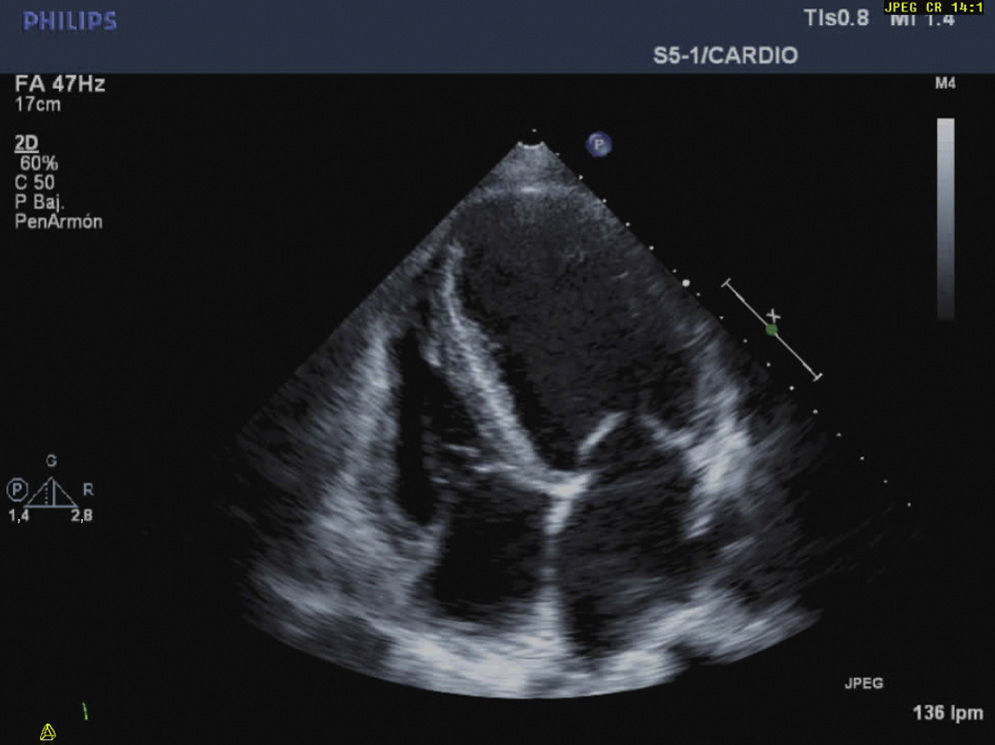
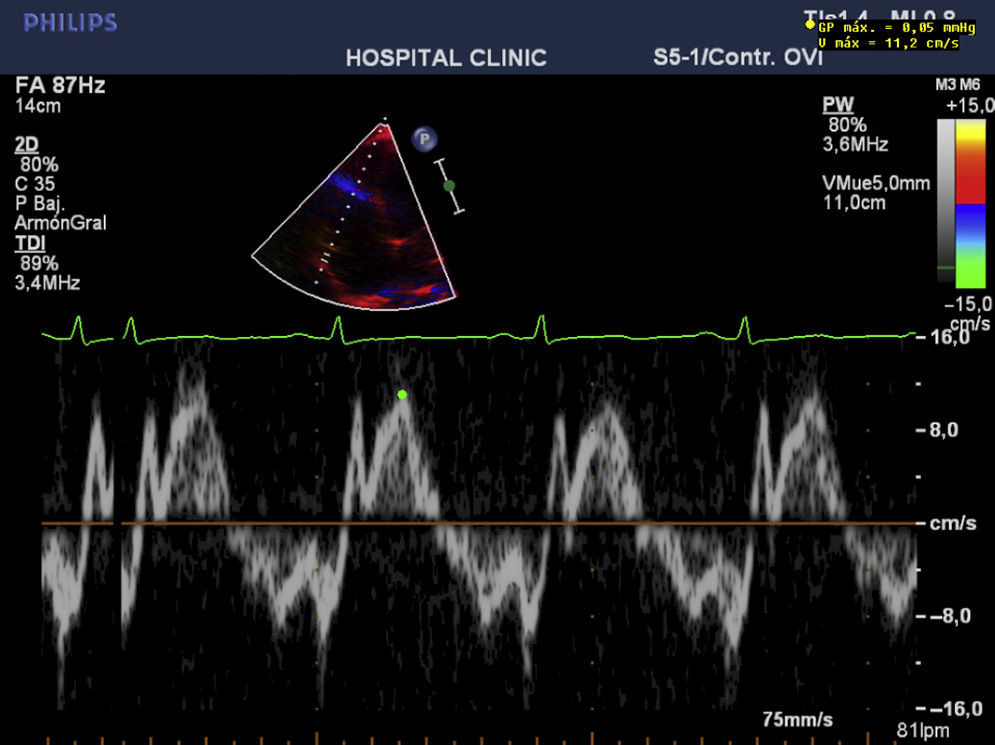
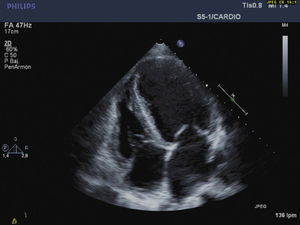
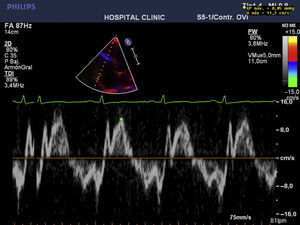
En resumen, es una paciente con cuadro subagudo de falla cardiaca severa, labilidad de cifras tensionales y dolor abdominal severo, con estudios negativos de patología coronaria; la escanografía abdominal y niveles elevados de metabolitos de catecolaminas clarifican el diagnóstico, que guía la lenta mejoría iniciada con alfabloqueadores y la introduccion del sulfato de magnesio. La respuesta cardiovascular a este fármaco fue esencial. Mejoró la contractilidad cardiaca y la presión arterial, logrando optimización fisiológica, que permite la resección tumoral con resultado adecuado (figs. 3 y 4).
Esta paciente con tumor de feocromocitoma comienza con crisis de cardiomiopatía dilatada severa inducida por catecolaminas, cuadro clínico de falla cardiaca izquierda y síntomas abdominales secundarios a necrosis tumoral aguda. Es una presentación infrecuente, de difícil diagnóstico y como consecuencia de elevada morbimortalidad por el inicio tardío de manejo. Las bases diagnósticas fueron la ausencia de antecedentes de enfermedad cardiovascular, con enzimas cardiacas y arteriografía coronaria normales. La cardiomiopatía en feocromocitoma está producida por niveles excesivos de catecolaminas, con sobrecarga intracelular de calcio como injuria principal, lesión tipo isquemia reperfusión con radicales libres, deterioro de la fibra miocárdica4, alteración microvascular y vasoespasmo. Finalmente se presenta un aumento de la demanda miocárdica de oxígeno con una disminución en su aporte por la vasoconstricción coronaria. El paciente puede presentar clínica de disfunción cardiaca hipertrófica o dilatada, edema pulmonar cardiogénico o no cardiogénico, arritmia fatal y muerte súbita5.
Esta fisiopatología celular y de receptores adrenérgicos ha sugerido el sulfato de magnesio como posible terapia para el manejo de las crisis agudas y la cirugía6. Hay una extensa literatura en su eficacia en el manejo de hipertensión y arritmias durante todo el periodo perioperatorio, para lograr la adecuada optimización del paciente. En algunos casos ha sido útil en situaciones donde el labetalol o nitroprusiato no han sido beneficiosos7. La optimización en esta paciente se inicia con bloqueadores adrenérgicos alfa (dosaxosina y fenoxibenzamina), pero ante la poca mejoría de contractilidad miocárdica e inestabilidad de la presión arterial, se introduce el sulfato de magnesio, desde la crisis aguda y durante proceso quirúrgico, hasta la remoción total del flujo del feocromocitoma, asegurando nivel de magnesemia máximo de 4,5 mmol/l. Este fármaco ha sido reportado clínicamente en este contexto en series de casos de adultos8,pediatría9 y embarazo10. El magnesio es un ion que participa en procesos enzimáticos esenciales de síntesis y metabolismo energético, tiene efectos como modulador y estabilizador de las corrientes Na/K en la membrana plasmática, antagonizando el calcio a nivel intracelular y del músculo liso vascular, así como disminuyendo la liberación de catecolaminas desde la médula adrenal, en las terminaciones nerviosas, y bloqueando directamente sus receptores y, en consecuencia, su repercusión hemodinámica sistémica11. Adicionalmente, preserva la célula miocárdica durante el proceso de isquemia-reperfusión, y es antiarrítmico en el contexto de grandes concentraciones de catecolaminas12. El resultado clínico es la mejora de la función miocárdica, sistólica y diastólica, la estabilización del ritmo cardiaco, la vasodilatación progresiva del lecho vascular (principalmente arterial y mínimo venoso) de órganos diana y periferia. En el manejo perioperatorio adicionalmente disminuye la respuesta adenérgica a todos los estímulos como intubación orotraqueal y el estímulo quirúrgico, logrando mejor control hemodinámico perioperatorio6.
El control ecocardiográfico durante la crisis permitió evidenciar la respuesta al magnesio con la mejoría sostenida del patrón restrictivo de la disfunción diastólica (paso de la relación E/A de 3,8 a 1,2cm/seg; aumento de la fracción de eyección del 20 al 25%; y disminución de la presión sistólica de arteria pulmonar de 80 a 29 mmHg), lo cual asociado a la dobutamina facilitó el manejo hemodinámico intraoperatorio. Intraoperatorianente, la mejor monitorización es la ecografía transesofágica, para establecer compromiso global cardiaco, contractilidad y volemia, empleando el catéter de arteria pulmonar solo en casos de compromiso cardiaco severo.
Recientemente se han reportado casos de cardiomiopatía de Takotsubo, síndrome caracterizado por disfunción ventricular izquierda transitoria, con abombamiento apical e hiperquinesia basal simulando síntomas de infarto de miocardio sin enfermedad coronaria significativa; en los casos de feocromocitoma y cardiomiopatía Takotsubo, el patrón más frecuente es el invertido, con aquinesia basal y medioventricular y ápex hiperquinético. Se asocia este síndrome con estrés emocional o físico y estimulación aumentada de catecolaminas, daño al miocardiocito y corazón atontado, lo que sugiere una similitud en la fisiopatología de las dos condiciones: la sobrecarga adrenérgica, siendo el síndrome Takotsubo de pronóstico más favorable que el feocromocitoma. Probablemente, hay otros agentes neurohumorales secretados por las células cromafines tumorales, como el neuropéptido Y, que pueden actuar sinergistícamente con las catecolaminas y empeorar la injuria miocárdica y la evolución13.
El sulfato de magnesio tiene buen perfil de seguridad, con toxicidad y reversión fácilmente manejables. Proporciona estabilidad hemodinámica y facilita el control cardiovascular durante la crisis de cardiomiopatía y la remoción tumoral6,13, representando una opción de primera línea para reducir la morbimortalidad en el manejo de feocromocitoma.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciamientoLos autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.