La cardiomiopatía hipertrófica se define como el engrosamiento de la pared ventricular izquierda que no es explicado por condiciones anormales de la carga y que impone un riesgo de: arritmias, falla cardiaca y muerte súbita.
Objetivoidentificar prevalencia, las características clínicas y el tratamiento de los pacientes con cardiomiopatía hipertrófica atendidos en nuestra institución.
Materiales y métodosSe extrajeron y analizaron los registros de pacientes con cardiomiopatías hipertróficas, definiendo las características generales y explorando las diferencias entre subgrupos, todos los contrastes estadísticos asumieron una confianza del 95%.
ResultadosSe evaluaron 22 casos de la cardiomiopatía hipertrófica, el sexo femenino aportó el 40,9% del total de los casos, la edad promedio fue 54 años. El 77,27% presentaron insuficiencia mitral, el 63,64% reportaron dolor torácico, el 68,18% se encontraban en tratamiento inhibidor de renina y el 95,45% tenían betabloqueador, el grosor promedio del septum fue del 22,77mm, la prevalencia de fibrilación auricular fue del 22,7% y la de enfermedad coronaria del 18%.
ConclusionesLa prevalencia de la cardiomiopatía hipertrófica en el período 2009-2013 fue del 2,35%, relacionado principalmente con la insuficiencia mitral y tenían antecedente de dolor torácico, la prevalencia de la fibrilación auricular en pacientes con cardiomiopatía hipertrófica en el presente estudio fue del 22,7% y la de enfermedad coronaria del 18%.
Hypertrophic cardiomyopathy is defined as the thickening of the left ventricular wall that is not explained by abnormal loading conditions, imposing a risk for arrhythmias, heart failure and sudden death.
We attempt to identify the prevalence, clinical features and treatment of patients with hypertrophic cardiomyopathy assisted within our institution.
Material and methodsRecords of patients with hypertrophic cardiomyopathy were pulled and analysed, defining general features and exploring differences among subgroups; all statistical contrasts assumed a confidence of 95%.
Results22 cases of hypertrophic cardiomyopathy were assessed, 40.9% of whom were female, average age was 54. 77.27% showed mitral insufficiency, 63.4% reported chest pain, 68.18% were receiving renin inhibitor therapy and 95.45% were taking beta blockers. Average septum thickness was 22.77mm, prevalence of atrial fibrillation was 22.7% and coronary disease 18%.
ConclusionPrevalence of hypertrophic cardiomyopathy during the 2009-2013 period was of 2.35%, mostly related to mitral insufficiency and previous history of chest pain; prevalence of atrial fibrillation in patients with hypertrophic cardiomyopathy in our study was of 22.7%, and 28% for coronary disease.
La cardiomiopatía hipertrófica se define como el engrosamiento de la pared ventricular izquierda que no es explicado por condiciones anormales de la carga, tiene un prevalencia a nivel mundial baja, reportándose en un 0,02-0,23%1, en los adultos el 60% de los casos se debe a mutaciones autosómicas dominantes de los genes de la proteína del sarcómero2.
Los pacientes con la miocardiopatía hipertrófica suelen presentar ciertas descompensaciones provocadas por las arritmias. En estos casos, puede ser necesario que el paciente reciba un tratamiento anticoagulante para prevenir los problemas embólicos y es una de las causas más importantes de la muerte súbita en personas jóvenes3. Aunque sea bastante infrecuente, la muerte puede ser incluso la primera manifestación en enfermos de miocardiopatía hipertrófica que no han presentado síntomas previamente4.
El manejo farmacológico de los pacientes con la cardiomiopatía hipertrófica en la ausencia de grandes estudios aleatorizados se realiza de manera empírica con el fin de mejorar los síntomas, mejorar la capacidad vital y disminuir la progresión de la enfermedad1. En los pacientes sintomáticos con obstrucción del tracto de salida del ventrículo izquierdo según las guías mundiales se busca como primera medida la mejoría de los síntomas ya sea con tratamientos farmacológicos, dispositivos electrónicos o cirugía. Siendo el grupo de los betabloqueadores el principal manejo farmacológico empleado5.
En nuestro medio no hay información concreta de la prevalencia y como se trata esta patología, con este trabajo queremos dar a conocer la experiencia de la Fundación Clínica Shaio en el manejo de la cardiomiopatía hipertrófica y si está acorde con lo conocido a nivel mundial.
El objetivo principal de este estudio es conocer la experiencia de la Fundación Clínica Shaio en el manejo médico y quirúrgico de los pacientes con diagnóstico de la cardiomiopatía hipertrófica que ingresaron en los últimos 5 años por consulta externa, urgencias o procedimientos quirúrgicos.
Materiales y métodosSe revisaron las bases de datos de las historias clínicas como soporte informativo para la localización de todos los pacientes que ingresaron a: consulta externa, cirugía, hospitalización y en general todos los servicios de la Fundación Clínica Shaio entre los años 2009 y 2013 con el diagnóstico de la cardiomiopatía hipertrófica obstructiva (CIE10: I421), otras cardiomiopatías hipertróficas (CIE10: I422), otras cardiomiopatías (I428), taquicardia ventricular (CIE10: I472), muerte cardiaca súbita (CIE 10: I461) y los pacientes a los que se les haya realizado los siguientes procedimientos: implantación de cardioversor o desfibrilador por vía infra clavicular (Cód. 379401) e implantación de cardioversor o desfibrilador por vía subcutánea (Cód. 379402). Mayores de 16 años. Como criterios de exclusión se utilizaron la estenosis aórtica severa y la cardiomiopatía hipertrófica secundaria a alteración de origen funcional o anatómica.
La recolección de datos, se realizó mediante la revisión de las historias clínicas de la totalidad de los pacientes atendidos en la Fundación Clínica Shaio en el período comprendido entre 2009 y 2013, verificando que cumplieran con los criterios de inclusión; se elaboró una base de datos en una hoja de cálculo de Microsoft Excel con las variables: edad, sexo, gradiente del tracto de salida del ventrículo izquierdo, grosor del septum, diámetro de la aurícula izquierda, insuficiencia mitral, fibrilación auricular, taquicardia ventricular no sostenida, tratamiento miectomía, tratamiento con dispositivo electrónico, tratamiento inhibidor de renina, tratamiento calcioantagonista, tratamiento betabloqueador, enfermedad coronaria, historia familiar de muerte súbita, historia familiar de miocardiopatía hipertrófica.
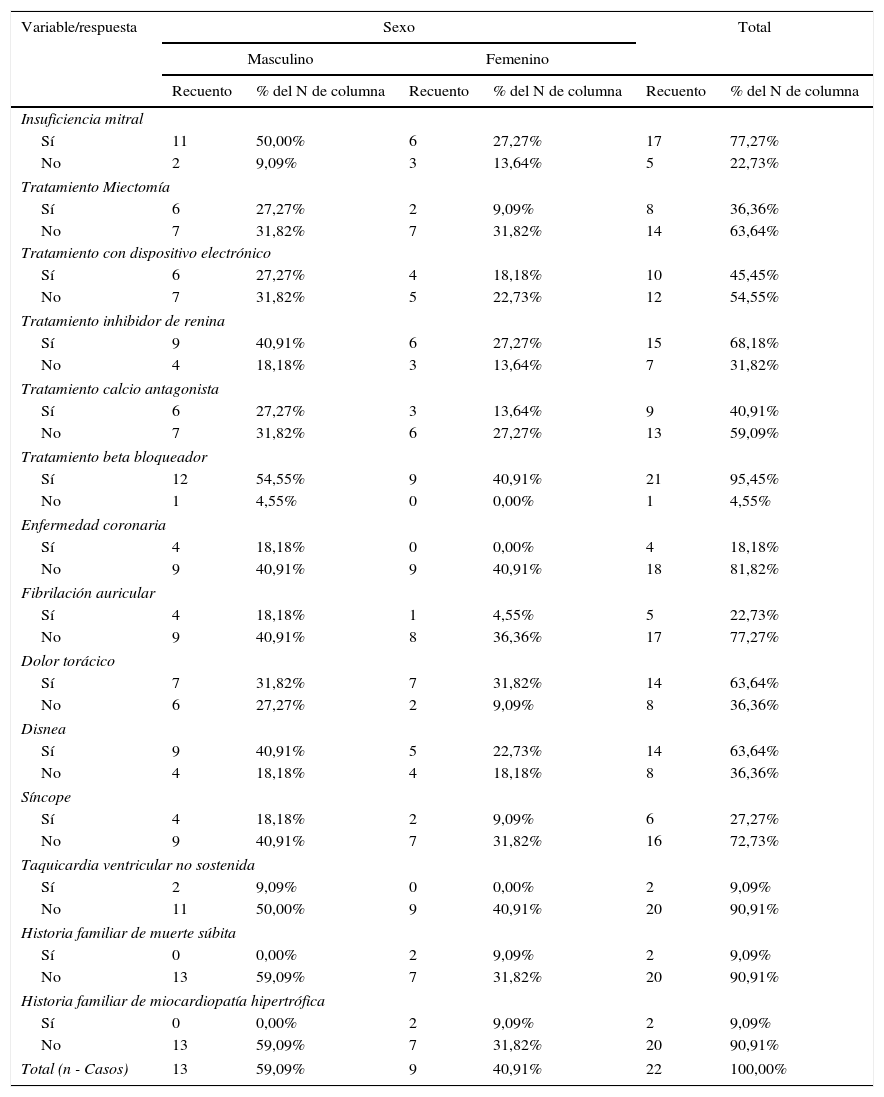
ResultadosSe evaluaron 22 casos de la cardiomiopatía hipertrófica, la prevalencia del período 2009-2013 fue de 2,35%, el sexo femenino aportó el 40,9% de los casos, la mayoría presentaron insuficiencia mitral (77,27%); se encontraban en tratamiento inhibidor de renina (68,18%); betabloqueador (95,45%) y tenían antecedente de dolor torácico (63,64%) (ver tabla 1).
Características generales (variables cualitativas) de los casos valorados
| Variable/respuesta | Sexo | Total | ||||
|---|---|---|---|---|---|---|
| Masculino | Femenino | |||||
| Recuento | % del N de columna | Recuento | % del N de columna | Recuento | % del N de columna | |
| Insuficiencia mitral | ||||||
| Sí | 11 | 50,00% | 6 | 27,27% | 17 | 77,27% |
| No | 2 | 9,09% | 3 | 13,64% | 5 | 22,73% |
| Tratamiento Miectomía | ||||||
| Sí | 6 | 27,27% | 2 | 9,09% | 8 | 36,36% |
| No | 7 | 31,82% | 7 | 31,82% | 14 | 63,64% |
| Tratamiento con dispositivo electrónico | ||||||
| Sí | 6 | 27,27% | 4 | 18,18% | 10 | 45,45% |
| No | 7 | 31,82% | 5 | 22,73% | 12 | 54,55% |
| Tratamiento inhibidor de renina | ||||||
| Sí | 9 | 40,91% | 6 | 27,27% | 15 | 68,18% |
| No | 4 | 18,18% | 3 | 13,64% | 7 | 31,82% |
| Tratamiento calcio antagonista | ||||||
| Sí | 6 | 27,27% | 3 | 13,64% | 9 | 40,91% |
| No | 7 | 31,82% | 6 | 27,27% | 13 | 59,09% |
| Tratamiento beta bloqueador | ||||||
| Sí | 12 | 54,55% | 9 | 40,91% | 21 | 95,45% |
| No | 1 | 4,55% | 0 | 0,00% | 1 | 4,55% |
| Enfermedad coronaria | ||||||
| Sí | 4 | 18,18% | 0 | 0,00% | 4 | 18,18% |
| No | 9 | 40,91% | 9 | 40,91% | 18 | 81,82% |
| Fibrilación auricular | ||||||
| Sí | 4 | 18,18% | 1 | 4,55% | 5 | 22,73% |
| No | 9 | 40,91% | 8 | 36,36% | 17 | 77,27% |
| Dolor torácico | ||||||
| Sí | 7 | 31,82% | 7 | 31,82% | 14 | 63,64% |
| No | 6 | 27,27% | 2 | 9,09% | 8 | 36,36% |
| Disnea | ||||||
| Sí | 9 | 40,91% | 5 | 22,73% | 14 | 63,64% |
| No | 4 | 18,18% | 4 | 18,18% | 8 | 36,36% |
| Síncope | ||||||
| Sí | 4 | 18,18% | 2 | 9,09% | 6 | 27,27% |
| No | 9 | 40,91% | 7 | 31,82% | 16 | 72,73% |
| Taquicardia ventricular no sostenida | ||||||
| Sí | 2 | 9,09% | 0 | 0,00% | 2 | 9,09% |
| No | 11 | 50,00% | 9 | 40,91% | 20 | 90,91% |
| Historia familiar de muerte súbita | ||||||
| Sí | 0 | 0,00% | 2 | 9,09% | 2 | 9,09% |
| No | 13 | 59,09% | 7 | 31,82% | 20 | 90,91% |
| Historia familiar de miocardiopatía hipertrófica | ||||||
| Sí | 0 | 0,00% | 2 | 9,09% | 2 | 9,09% |
| No | 13 | 59,09% | 7 | 31,82% | 20 | 90,91% |
| Total (n - Casos) | 13 | 59,09% | 9 | 40,91% | 22 | 100,00% |
La prevalencia de la fibrilación auricular en los pacientes con la cardiomiopatía hipertrófica en el presente estudio fue del 22,7%, la de enfermedad coronaria en el mismo grupo de pacientes fue del 18%.
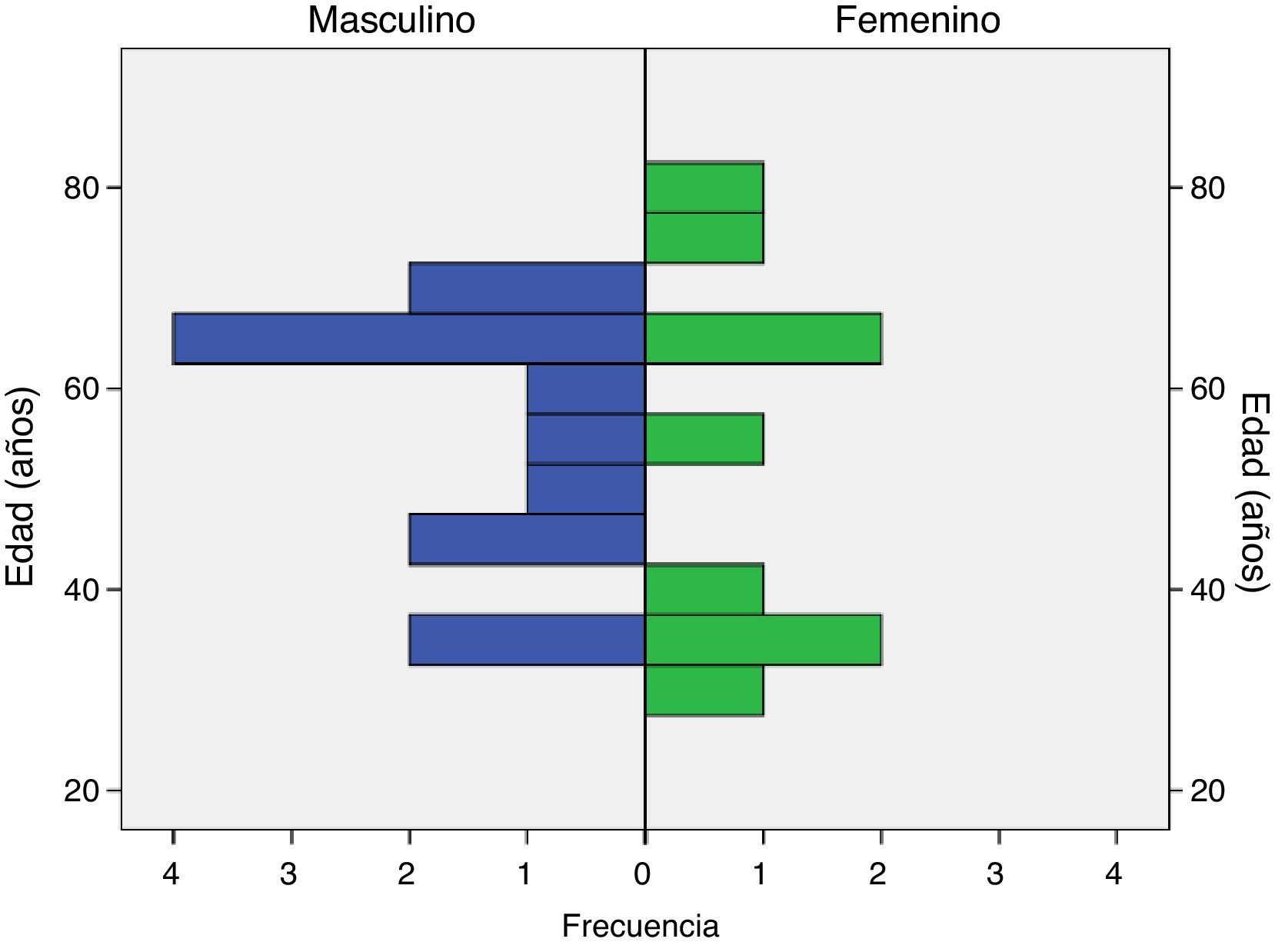
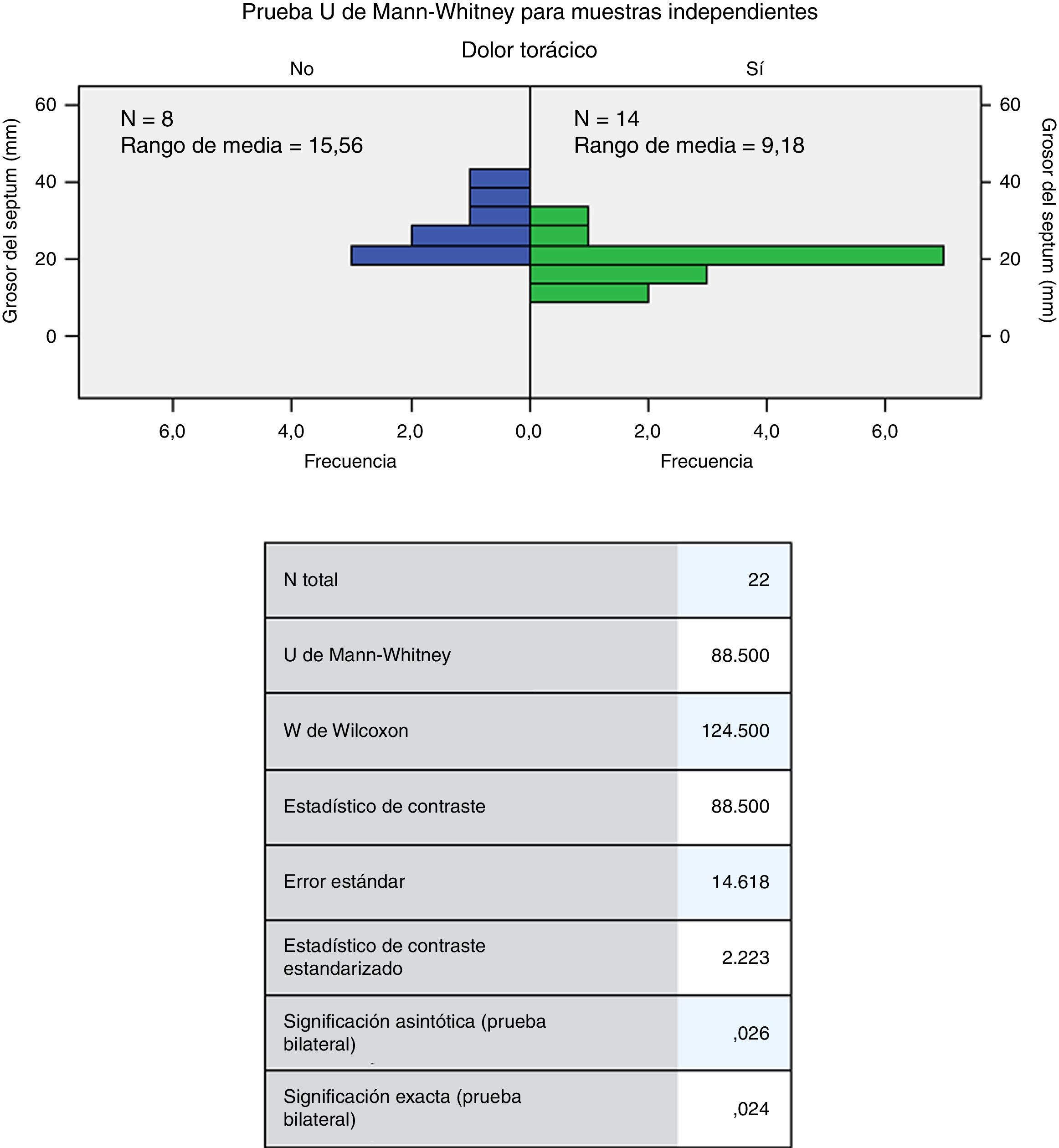
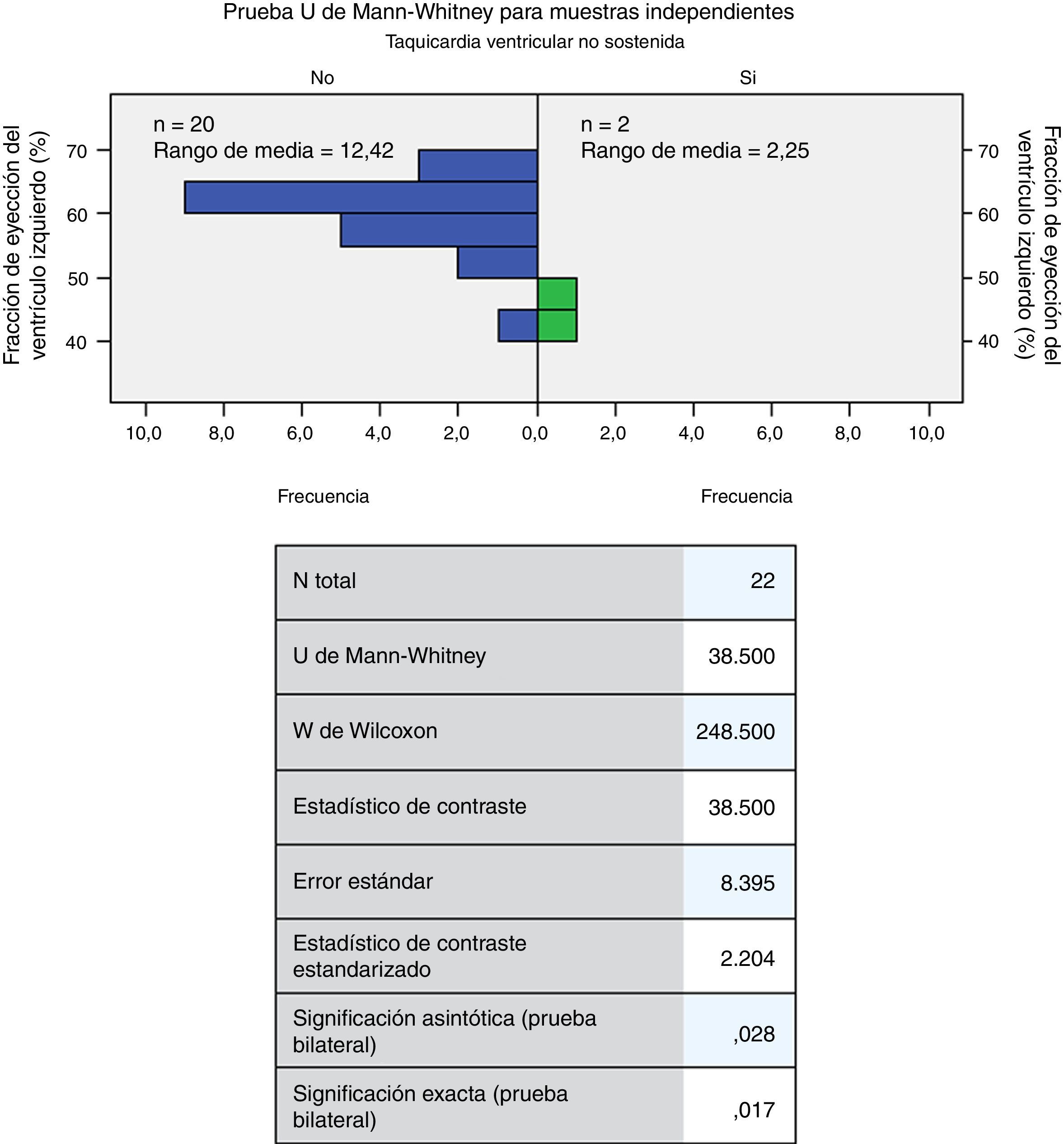
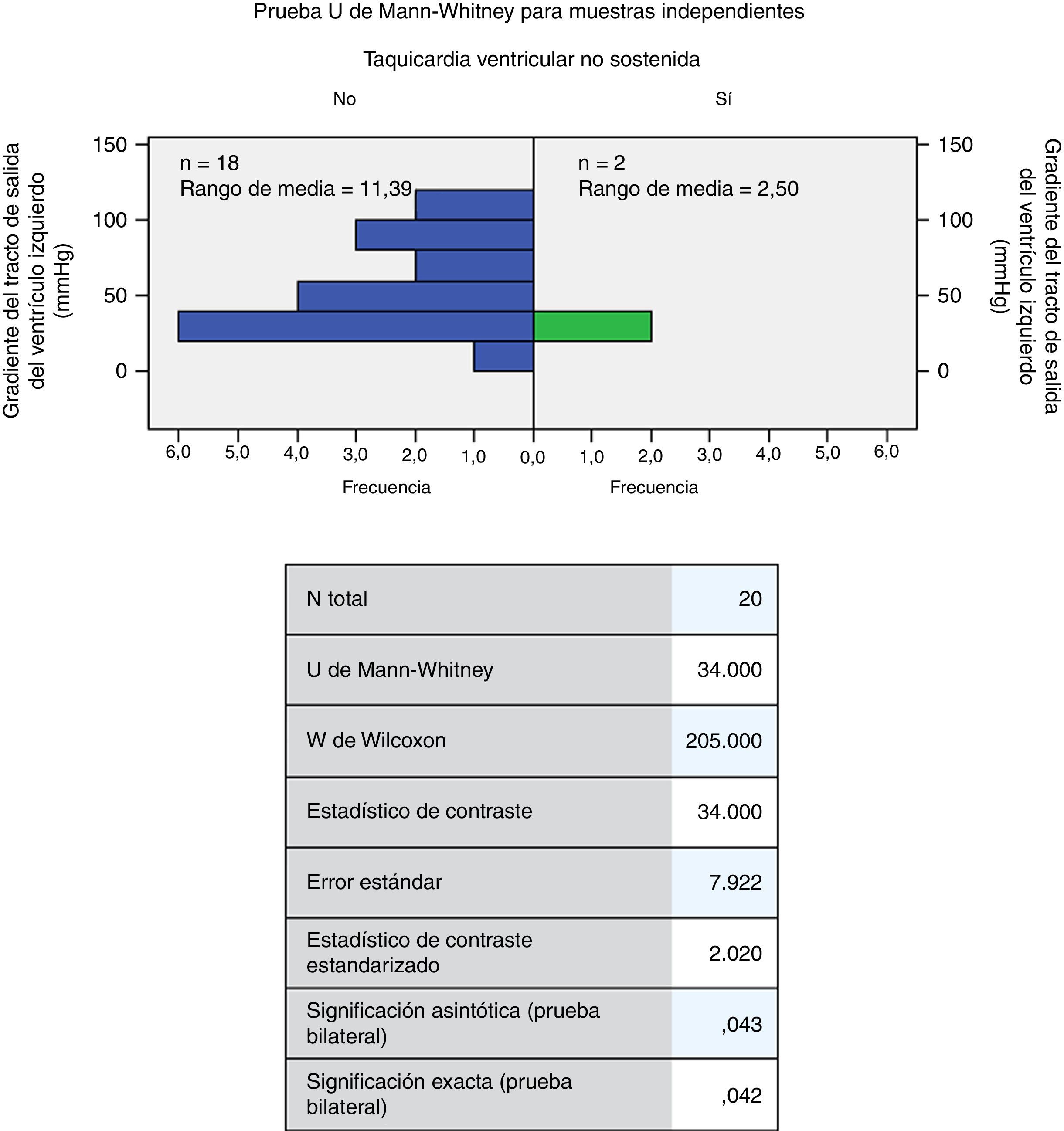
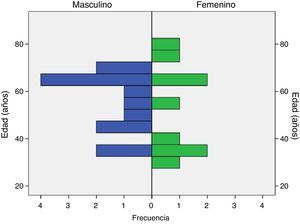
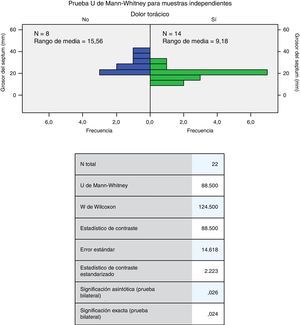
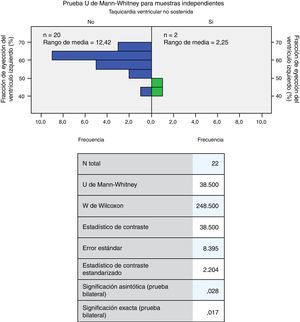
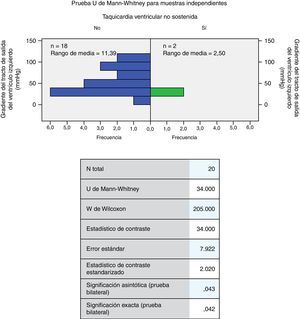
La edad mínima de los individuos fue de 30 años (promedio de 54,73 años) (tabla 2 y fig. 1). La fracción de eyección mínima fue de 40 (media 56,36mmHg); el gradiente mínimo del tracto de salida del ventrículo izquierdo fue de 12 (media de 53,2mmHg); el diámetro máximo de la aurícula izquierda fue de 63 (media de 40,95mm) y el grosor máximo del septum fue de 40 (media de 22,77mm) (tabla 2). A la exploración de diferencias en la distribución de las variables cuantitativas por las cuantitativas (U de Mann-Whitney), se encontraron diferencias significativas entre el grosor del septum y el antecedente de dolor torácico (p=0,026); el antecedente de la taquicardia ventricular no sostenida con la fracción de eyección del ventrículo izquierdo y el gradiente del tracto de salida del ventrículo izquierdo (p=0,017 y 0,042, respectivamente) (figs. 2–4) el resto de las diferencias no fueron estadísticamente significativas.
Características generales (variables cuantitativas) de los casos valorados
| Variable | Mínimo | Máximo | Media | Desviación estándar |
|---|---|---|---|---|
| Edad (años) | 30 | 78 | 54,73 | 15,313 |
| Fracción de eyección del ventrículo izquierdo (%) | 40 | 67 | 56,36 | 7,410 |
| Gradiente del tracto de salida del ventrículo izquierdo (mmHg) | 12 | 110 | 53,20 | 30,227 |
| Diámetro de la aurícula izquierda (mm) | 23 | 63 | 40,95 | 8,109 |
| Grosor del septum (mm) | 11 | 40 | 22,77 | 7,270 |
| N total de casos valorados | 22 |
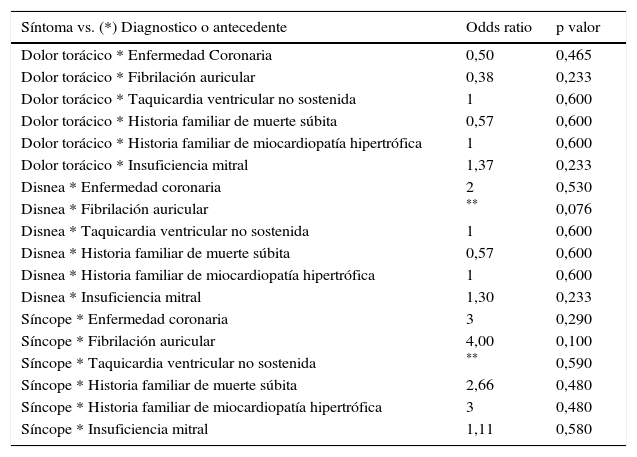
A la exploración de Odds de la presencia de síntomas por los diagnósticos o antecedentes cardiovasculares no se encontraron asociaciones significativas (tabla 3).
Resultados de tablas cruzadas de síntomas vs. diagnóstico o antecedente
| Síntoma vs. (*) Diagnostico o antecedente | Odds ratio | p valor |
|---|---|---|
| Dolor torácico * Enfermedad Coronaria | 0,50 | 0,465 |
| Dolor torácico * Fibrilación auricular | 0,38 | 0,233 |
| Dolor torácico * Taquicardia ventricular no sostenida | 1 | 0,600 |
| Dolor torácico * Historia familiar de muerte súbita | 0,57 | 0,600 |
| Dolor torácico * Historia familiar de miocardiopatía hipertrófica | 1 | 0,600 |
| Dolor torácico * Insuficiencia mitral | 1,37 | 0,233 |
| Disnea * Enfermedad coronaria | 2 | 0,530 |
| Disnea * Fibrilación auricular | ** | 0,076 |
| Disnea * Taquicardia ventricular no sostenida | 1 | 0,600 |
| Disnea * Historia familiar de muerte súbita | 0,57 | 0,600 |
| Disnea * Historia familiar de miocardiopatía hipertrófica | 1 | 0,600 |
| Disnea * Insuficiencia mitral | 1,30 | 0,233 |
| Síncope * Enfermedad coronaria | 3 | 0,290 |
| Síncope * Fibrilación auricular | 4,00 | 0,100 |
| Síncope * Taquicardia ventricular no sostenida | ** | 0,590 |
| Síncope * Historia familiar de muerte súbita | 2,66 | 0,480 |
| Síncope * Historia familiar de miocardiopatía hipertrófica | 3 | 0,480 |
| Síncope * Insuficiencia mitral | 1,11 | 0,580 |
La cardiomiopatía hipertrófica se define por la presencia de un aumento de grosor de la pared ventricular izquierda que no se explica exclusivamente por las condiciones de carga anormales1,5. La prevalencia de CMH se ha estimado en estudios metodológicamente heterogéneos, que reportan una prevalencia de aumento no explicado en el grosor del ventrículo izquierdo en el rango de 0,2 - 0,23% en adultos5,6, se ha determinado que en cerca del 60% de los adolescentes y adultos, la CMH es una enfermedad autosómica dominante, se han reportado mutaciones autosómicas dominantes en más de 11 genes que codifican los componentes proteicos del sarcómero2.
Es una enfermedad cardiaca que presenta un curso y presentación clínica diversa, afectando todos los grupos de edad4, en algunos casos la progresión de la enfermedad conlleva a la muerte prematura7, relacionada principalmente con riesgo de la muerte súbita cardiaca8, se debe realizar una estratificación y evaluar la historia personal de: la fibrilación ventricular, la taquicardia ventricular no sostenida, la historia del síncope (familiar y/o personal) y el grosor mayor a 30mm al ecocardiograma, en donde la estrategia preventiva indica la implantación del cardiodesfibrilador para el control del riesgo3.
El electrocardiograma muestra alteraciones en el 75 a 95% de los casos, evidenciando patrones de fibrilación auricular, aleteo auricular y taquicardia ventricular no sostenida9, además, permite la medición del grosor del ventrículo izquierdo, identificación de los subtipos (apical, septal), la obstrucción dinámica del tracto de salida del VI, evaluación de la función sistólica y a distinguir entre otras posibles causas de la hipertrofia del ventrículo izquierdo1,10.
El manejo depende de la sintomatología de los pacientes, en aquellos que se encuentran asintomáticos, se recomienda tratar: comorbilidades cardiovasculares, estilos de vida con baja intensidad física, no usar vasodilatadores ni diuréticos y una adecuada hidratación1. En los pacientes sintomáticos se debe adicionar el manejo médico específico que incluye betabloqueadores11, que aumentan el aporte de oxígeno y el período de llenado diastólico, así como, calcioantagonistas tipo verapamilo que producen un efecto inotrópico negativo12.
Como última opción se encuentra el manejo invasivo divido en dos modalidades, la ablación con alcohol13 y la miectomía quirúrgica considerado el tratamiento más apropiado al adelgazar el septum, corrigiendo la obstrucción del tracto de salida y la insuficiencia mitral14,15.
En este trabajo se evaluaron los registros de los últimos 5 años de la Fundación Clínica Shaio en el manejo de la cardiomiopatía hipertrófica encontrándose una prevalencia del 2,35% aumentada respecto a la conocida a nivel mundial, con una distribución por género similar con mayor predominio en la población masculina en un 60,1%, encontrando una asociación con insuficiencia mitral en el 77,27%.
Los síntomas más frecuentemente encontrados fueron el dolor torácico en el 63,64% y la disnea el 27,89%, con presentación de síncope en el 27,7% y en menor porcentaje (9,09%) de la taquicardia ventricular no sostenida. Se presentó en un 22,73% la fibrilación auricular asociada.
Respecto al manejo farmacológico el 95,45% de la población recibió manejo betabloqueador y el 40,91% recibió manejo con calcioantagonistas, que comparado con las indicaciones actuales del manejo farmacologico se encuentra acorde con las recomendaciones.
El 45,45% de los pacientes requirieron manejo con dispositivos electrónicos y el 36,6% de los pacientes fueron llevados a miectomía. Los pacientes llevados a miectomía presentaron gradientes del tracto de salida superiores a 50% asociado a síntomas (como indican las publicaciones internacionales del manejo de la cardiomiopatía hipertrófica1,5).
ConclusionesLa prevalencia de la cardiomiopatía hipertrófica en el período 2009-2013 fue del 2,35%, relacionado principalmente con la insuficiencia mitral y tenían antecedente de dolor torácico, la prevalencia de la fibrilación auricular en los pacientes con cardiomiopatía hipertrófica en el presente estudio fue del 22,7% y la de enfermedad coronaria del 18%. Se requiere de estudios adicionales con diseño prospectivo para identificar la efectividad e impacto de las intervenciones.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.