El uso de prótesis vasculares y dispositivos endovasculares ha permitido tratar muchas patologías que antes no se intervenían dado el gran riesgo quirúrgico, como es el caso de los aneurismas de aorta torácica. Los materiales usados para estas reconstrucciones son muy resistentes y de larga duración, pero son muy sensibles a ser colonizados y presentar infección, lo que genera morbimortalidad considerable.
Se presenta el caso de un paciente de 64 años con antecedente de aneurisma del arco aórtico y aorta descendente, tratado en forma extra institucional con prótesis de aorta torácica endovascular y debranchig de las ramas del arco aórtico, con injerto carótido-carotídeo y carótido-subclavio izquierdo en dacrón, por vía pretraqueal, con antecedente de intento de cubrimiento del injerto expuesto con un flap miocutáneo el cual fue fallido por necrosis; ingresó al Hospital Universitario Clínica de San Rafael, con exposición del injerto carótido-carotídeo a nivel cervical, signos locales de infección y sepsis secundaria.
The use of vascular replacements and endovascular devices has led to the treatment of many conditions that could not be operated on due to a high surgical risk, such as aortic aneurysms. The materials used for these reconstructions are very resistant and durable, but are very susceptible to being colonised and infected, which leads to a considerable morbidity and mortality.
The case is presented of a 64 year-old patient with a history of an aortic arch and descending aortic aneurysm. This had been treated in another hospital with a thoracic aortic endovascular repair and debranching of the aortic arch, with carotid-carotid and left carotid-subclavian Dacron graft. The pretracheal route was used, after attempting to cover the exposed graft with a myocutaneous flap that failed due to necrosis. The patient was admitted to the Hospital Universitario Clínica de San Rafael, presenting with a carotid-carotid graft at cervical level, with local signs of infection and secondary sepsis.
El uso de prótesis vasculares y dispositivos endovasculares ha permitido tratar muchas patologías que antes no se intervenían por riesgo quirúrgico altísimo, como es el caso de los aneurismas de aorta torácica. Los materiales usados para estas reconstrucciones son muy resistentes y de larga duración, pero son muy sensibles a ser colonizados y presentar infección, lo que genera muy alta morbimortalidad1,2. La infección protésica se trata con resección o explantación, procedimientos que pueden generar sangrado, falla multiorgánica, sepsis o isquemias tisulares. La incidencia de infección para prótesis vasculares y endovasculares es del 0,5 al 5% y se asocia con la indicación de la intervención, patologías asociadas del paciente, sitio de implantación y técnica quirúrgica.
La infección protésica luego de cirugía de la aorta torácica es mucho menor que la cirugía de la aorta abdominal o procedimientos periféricos, y mucho menor en casos de procedimientos endovasculares, y oscila entre 0,5 y 1%3,4.
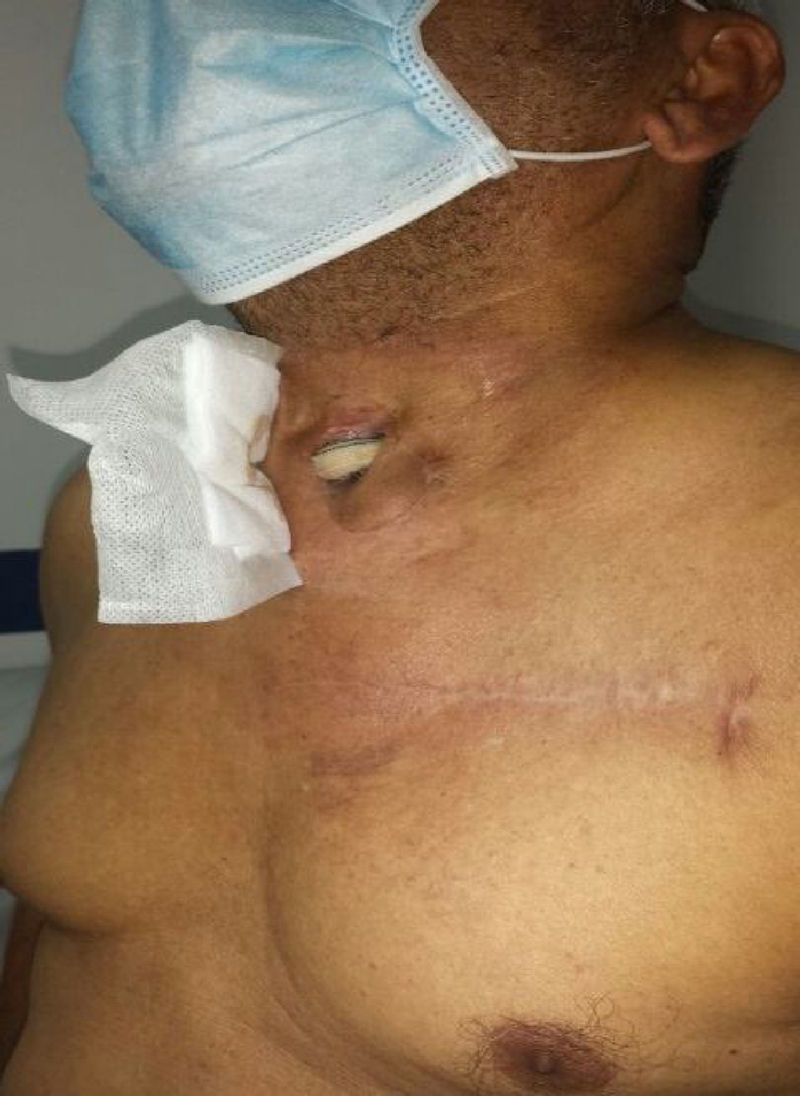
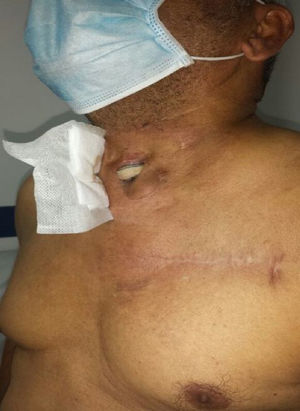
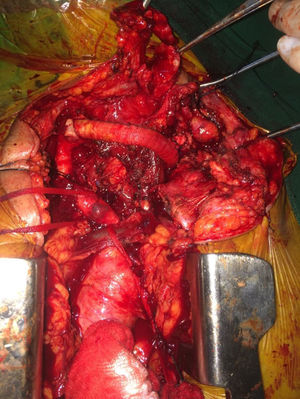
Se presenta el caso de un paciente de 64 años con antecedente de aneurisma del arco aórtico y aorta descendente, manejado de manera extrainstitucional con una prótesis de aorta torácica endovascular y un debranching de las ramas del arco aórtico, con injerto carótido-carotídeo y carótido-subclavio izquierdo en dacrón, por vía pretraqueal, con antecedente de intento de cubrimiento del injerto expuesto con un flap miocutáneo el cual fue fallido por necrosis, quien ingresó al Hospital Universitario Clínica de San Rafael, con exposición del injerto carótido-carotídeo a nivel cervical (fig. 1), signos locales de infección y sepsis secundaria.
AngioTAC de tórax: prótesis endovascular aórtica desde la porción distal del ostium de la arteria carótida común izquierda hasta tercio distal de la aorta descendente sin fugas ni signos de infección; injerto carótido-carotídeo y carótido-subclavio permeable con gas a su alrededor. Leucocitosis de 21.000 con desviación izquierda y PCR (proteína C reactiva) 230mg/l.
Análisis: paciente con sepsis secundaria a infección de injerto de dacrón, expuesto en cuello, en el que se intentó cubrimiento con flap miocutáneo, que fue fallido; requiere explantación del material protésico y reemplazo con material autológo, de otra manera la sepsis no se controlará y el riesgo de sangrado masivo y muerte es muy alto.
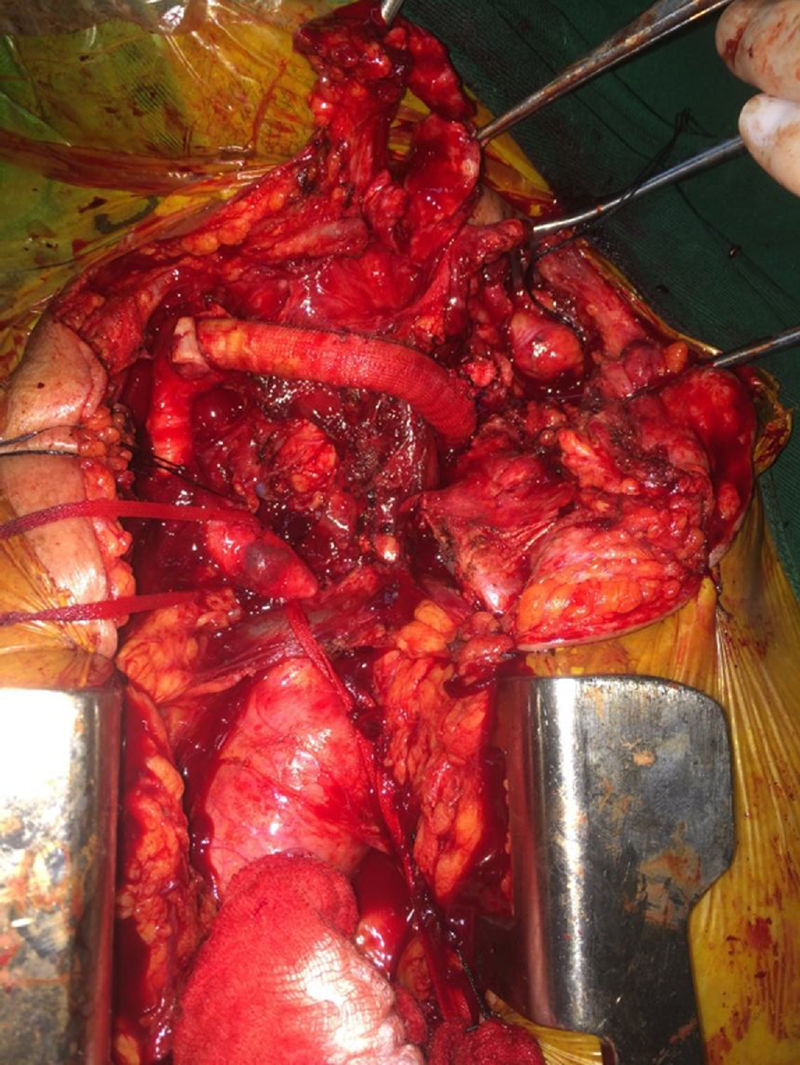
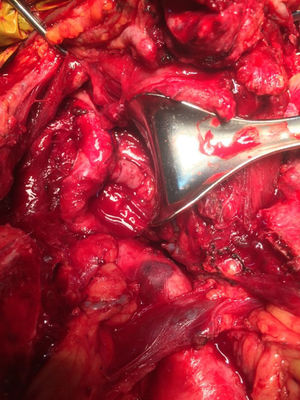
Técnica quirúrgica: se realizó una esternotomía mediana convencional para control de los vasos supraaórticos, más cervicotomía antero-lateral bilateral; se disecó el tronco braquiocefálico y la aorta ascendente; se procedió a disección de arterias carótidas comunes de manera bilateral, encontrando injerto carótido-carotídeo en dacrón severamente infectado con pus a su alrededor pero permeable, e injerto carótido-subclavio izquierdo en continuidad en dacrón en iguales condiciones de infección. Ambos injertos ubicados en el compartimento anterior del cuello, vía pretraqueal (fig. 2).
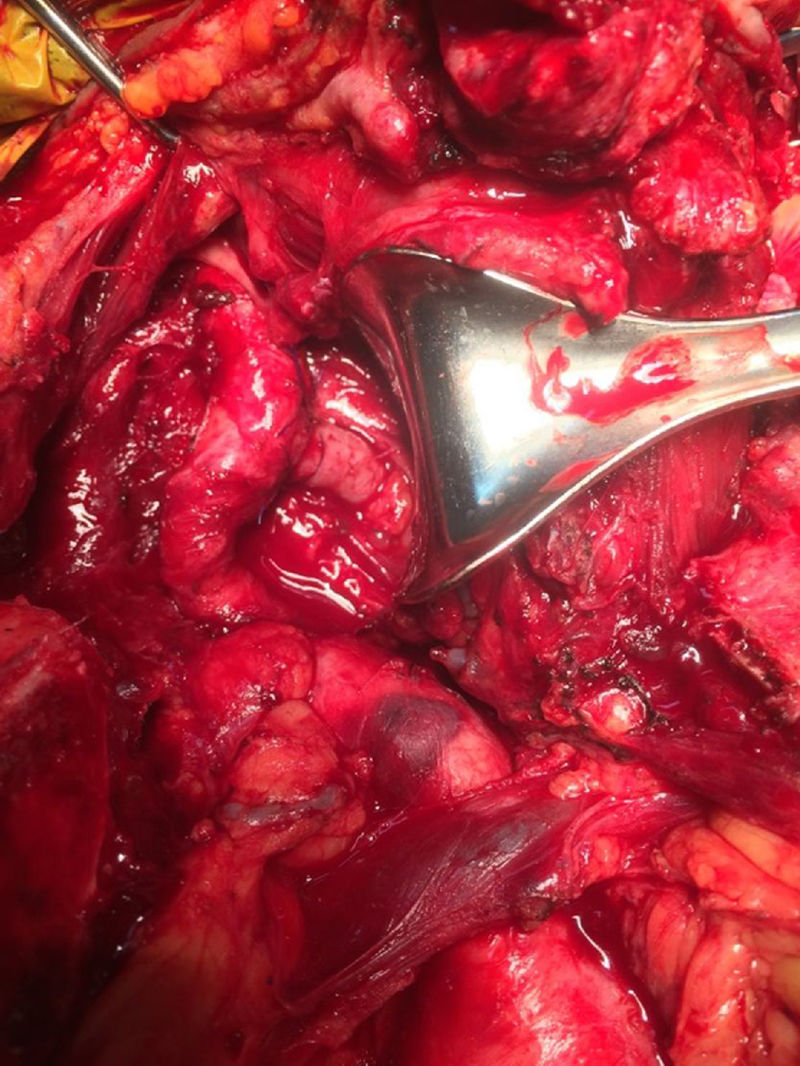
Se procedió a disección cuidadosa de las estructuras comprometidas y a toma de injerto venoso, de vena femoral derecha con técnica de Clagget, preservando la vena safena mayor y su cayado. Se preparó una extensión de injerto de 10cm y se procedió a resección completa del injerto carótido-carotídeo y carótido-subclavio y se colocó un nuevo injerto en vena femoral autóloga por vía retrofaríngea (fig. 3); se resecó el injerto carótido subclavio, ligando la arteria subclavia izquierda y rafia a la arteria carótida común.
Se lavó profusamente la zona quirúrgica, se cerraron las incisiones y se colocaron drenajes. El paciente evolucionó satisfactoriamente, con estancia en UCI de 3 días, lográndose controlar el proceso séptico; se dio manejo antibiótico intrahospitalario por 12 días y se dio de alta a los 14 días de hospitalización, para manejo antibiótico por 6 semanas con ertapenem.
Ha estado en seguimiento durante 9 meses, tiempo durante el cual se ha observado buena evolución, ausencia de signos de infección y permeabilidad de las reconstrucciones arteriales sin lesiones neurológicas centrales o periféricas.
DiscusiónEl tratamiento endovascular de los aneurismas de aorta torácica, fue descrito por primera vez en 1994, por el grupo de Dake et al. En 2005, la FDA aprobó el primer dispositivo a partir de lo cual se han hecho millones de implantes alrededor del mundo para patologías como: aneurismas, disección, hematoma intramural, úlcera aórtica penetrante, transección aórtica traumática, fístula traqueoesogáfica, entre otras. Se ha demostrado, por tanto, en muchos estudios, que ya no está indicada la cirugía abierta para estas patologías, en vista de que la mortalidad es menor en la cirugía endovascular, que en la abierta (2,1 vs. 11,7%), y disminuye el índice de complicaciones, paraplejia (3 vs. 14%), falla ventilatoria (4 vs. 20%) y falla renal (1 vs. 13%)4–6. La cirugía abierta convencional del arco aórtico requiere el uso de circulación extracorpórea e hipotermia y tiene una mortalidad que alcanza el 10 al 20%, de modo que las técnicas endovasculares e híbridas tienen un papel preponderante7.
La introducción y evolución de las técnicas endovasculares y quirúrgicas para las patologías de aorta torácica ha contribuido a aumentar las indicaciones de intervención y a disminuir los índices de morbimortalidad. Al mezclar procedimientos quirúrgicos y endovasculares al tiempo o en estadios, se crean los procedimientos híbridos como debranching o relocalización, que consiste en retirar los ostium de salida de estas arterias y relocalizarlos en una zona más proximal del arco o incluso la aorta ascendente, de tal manera que se puedan implantar así prótesis de manera más proximal.
El concepto de cirugía híbrida para el arco aórtico, tiene tres principios básicos8,9:
- 1.
Relocalización quirúrgica abierta de los grandes vasos del arco aórtico.
- 2.
Creación de una zona de aterrizaje o anclaje adecuada para una prótesis endovascular.
- 3.
Despliegue concomitante de una prótesis endovascular de aorta torácica.
Este tipo de procedimientos ya ha demostrado ser eficaz en el manejo de aneurismas del arco aórtico y aorta descendente. Existen diferentes técnicas, que de manera acumulada, muestran una mortalidad del 5,8%, evento cerebrovascular del 2,8% e isquemia espinal del 2,9%7,8. No hay estadísticas asociadas a la infección de estas reconstrucciones extraanatómicas, a excepción de algunos reportes de caso, en los que se tratan con cirugía de explantación o prótesis endovasculares periféricas como el Viahban (Gore-medical, Flagstaff, AZ, USA)9. En general, la indicación en estos casos es hacer la derivación por vía retrofaríngea, ya que se disminuye el riesgo de infección y es más anatómica. La mortalidad del injerto carótido-carotídeo y la incidencia de evento cerebrovascular intraoperatorio es de menos del 5%; patencia primaria del 88% y secundaria del 92% a 3 años10–12.
Ante infección protésica o de un dispositivo endovascular, se debe individualizar cada caso y tener en cuenta los siguientes factores: presentación clínica (aguda o crónica), localización de la infección, estado general del paciente, tipo de injerto o prótesis comprometida e infección localizada o sistémica. La exploración quirúrgica permite inspeccionar el injerto, tomar muestras, evaluar tejidos adyacentes y controlar sangrados. La mayoría de casos se descubren por aparición de pus en las heridas, y en pocos se presenta estallido del injerto con sangrado masivo, que es la complicación más temida y de mayor mortalidad en este tipo de infecciones11,12.
Los principios generales de tratamiento en estos casos, son13–15:
- 1.
Resecar el material protésico infectado.
- 2.
Mantener la continuidad arterial.
- 3.
Resecar el tejido necrótico e infectado alrededor.
- 4.
Instaurar antibioticoterapia prolongada, de acuerdo con los cultivos.
Las prótesis vasculares se pueden contaminar por tres factores, a saber16,17:
- 1.
Contaminación intraoperatoria, por falla en la técnica aséptica.
- 2.
Infección activa que colonice la prótesis al momento del procedimiento (infección urinaria, neumonías, etc.).
- 3.
Infección propia del aneurisma o del trombo, donde existan bacterias que proliferen al momento de la colocación del injerto y lo invadan.
En este paciente se cumplieron todos los principios, logrando resecar todo el material infectado, desbridar tejidos necróticos y preservar la continuidad arterial por medio de un injerto en vena, que es más resistente a la infección.
ConclusiónPese al uso de antibióticos y los principios en prevención de infecciones quirúrgicas, las infecciones de prótesis vasculares continúan siendo una entidad frecuente; este caso muestra una infección compleja en una patología aneurismática de alto nivel, en cuyo caso el manejo integral con diagnóstico imagenológico y la planeación quirúrgica adecuada, genera buenos resultados y disminuye la morbimortalidad.
Conflictos de interesesNinguno.