La artritis reumatoide (AR) es una enfermedad crónica, inflamatoria, autoinmune y multisistémica, cuyo principal blanco es la membrana sinovial. El manejo adecuado y temprano mejora la evolución y pronóstico de la enfermedad.
ObjetivoEvaluar los resultados clínicos y funcionales en pacientes con AR temprana.
MetodologíaEstudio observacional, con seguimiento longitudinal, de una cohorte de pacientes con AR temprana de menos de 12 meses de evolución, clasificados según los criterios de la Liga Europea Contra el Reumatismo y del Colegio Americano de Reumatología (ACR 2010). Se tuvieron en cuenta los criterios de remisión según la Escala de Actividad de la Enfermedad (DAS28-VSG) y el índice de actividad clínica de la enfermedad. Estado funcional según Cuestionario modificado de Evaluación de la Salud.
ResultadosSe analizaron 99 pacientes. La edad promedio de los pacientes fue de 47,8±15,5 años, el 93% (92) eran mujeres. Todos los pacientes fueron tratados con fármacos antirreumáticos modificadores de la enfermedad sintéticos. Durante el seguimiento a los 3 meses se observó una disminución significativa en los puntajes del DAS28 y actividad clínica de la enfermedad respecto al valor en la visita basal (p<0,05). No se encontraron diferencias significativas en la evolución de pacientes diagnosticados antes y después de 3 meses desde el inicio de los síntomas (p>0,05).
ConclusionesSe evidencia mejoría sustancial de los pacientes con AR temprana tratados durante el primer año de inicio de los síntomas. El seguimiento continuo y periódico de la patología es una herramienta indispensable para evaluar el progreso de la enfermedad y hacer ajustes en el manejo terapéutico.
Rheumatoid arthritis (RA) is a chronic, inflammatory, autoimmune multisystemic disease that affects the synovial joints. An appropriate and earlymanagement improves prognosis and course of the disease.
ObjectiveTo evaluate the clinical and functional outcomes of patients with RA.
MethodologyObservational study with longitudinal follow up in a cohort of patients with early RA, with less than 12 months of evolution, classified according to the European League Against Rheumatism and American College of Rheumatology (ACR 2010) criteria. Remission criteria were taking into account according to Disease Activity Scale (DAS28-VSG), clinical activity disease index, and functional status according to Modified Health Assessment Questionnaire.
ResultsThe analysis included 99 patients with a mean age of 47.8 + 15.5 years, and of which 92 (93%) were women. All patients were treated with synthetic disease-modifying antirheumatic drugs. At 3 months of follow-up, a significant decrease was observed in DAS28 scores and clinical activity disease index compared to the value at baseline values (p<.05). No significant differenceswere found between patients diagnosed before and after 3 months from onset of symptoms (p>.05).
ConclusionsA substantial improvement was observed in patients with early RA treated during first year from onset symptoms. Continuous and periodic monitoring of the pathology is an indispensable tool for evaluating disease progress and making adjustments in the therapeutic management.
La artritis reumatoide (AR) es una enfermedad crónica, inflamatoria, autoinmune y multisistémica, que afecta principalmente la membrana sinovial. La AR se distribuye mundialmente, con mayor prevalencia en mujeres1 y en países desarrollados2. En Latinoamérica, se ha reportado una prevalencia cercana al 0,5%3. En Colombia, no se tienen datos precisos de la prevalencia, aunque se han hecho algunas aproximaciones con población afrocolombiana, con una estimación del 0,4%4.
La definición de AR temprana, varía de acuerdo con el tiempo de evolución. Algunos autores establecen como límite menos de 3 meses, desde el inicio de los síntomas. Sin embargo, para otros autores este tiempo puede llegar a ser de hasta 3 años4,5.
El tratamiento actual de la AR, está orientado a la remisión, es decir, a la ausencia de actividad inflamatoria, o al menos a una reducción significativa o estado de baja actividad de la enfermedad6. En el camino hacia la consecución de este objetivo, los pacientes deben ser estrechamente monitorizados en su evolución, utilizando diferentes indicadores que permiten evaluar la actividad de la enfermedad para determinar las modificaciones necesarias en el tratamiento y alcanzar el resultado esperado.
El tratamiento adecuado, con un control periódico de la actividad de la enfermedad, mejora el pronóstico de la AR. Esto ha sido enfocado en el concepto «tratamiento dirigido al objetivo» (T2T) o tratamiento hacia el blanco, trabajado por un grupo de especialistas internacionales, que recomienda tener como meta alcanzar la remisión o la baja actividad de la enfermedad, mediante la monitorización sistemática7. El presente estudio tiene como objeto evaluar el comportamiento clínico y funcional de los pacientes con AR temprana, tratados en la Clínica de Artritis y Reumatología del Centro Médico Imbanaco (CAR-CMI) y caracterizar demográfica y clínicamente esta población.
Pacientes y métodosTipo de estudioEstudio descriptivo, longitudinal tipo serie de casos, que incluyó pacientes entre 18 y 65 años, que consultaron a la CAR-CMI en el periodo 2004-2014, diagnosticados con AR de acuerdo con los criterios de clasificación de la Liga Europea Contra el Reumatismo (EULAR) y del Colegio Americano de Reumatología (ACR) EULAR/ACR 20108, con un tiempo de evolución de síntomas menor a 12 meses, con al menos una visita de seguimiento durante el primer año. Se excluyeron pacientes con diagnóstico de fibromialgia, lupus eritematoso sistémico y otras enfermedades articulares concomitantes como gota y osteoartrosis severa, también fueron excluidos pacientes con depresión mayor.
Lugar de estudioEl estudio se llevó a cabo en la CAR-CMI, institución prestadora de servicios de salud privada, de alta complejidad, en la ciudad de Cali, Colombia.
Las evaluaciones se realizaron de forma periódica, como parte del seguimiento clínico rutinario de los pacientes. Este estudio fue aprobado por el Comité de Ética de la institución y todos los pacientes firmaron el formato de consentimiento informado para la recolección de la información.
VariablesLa información demográfica, se recolectó mediante un cuestionario multidimensional que incluyó variables como datos de identificación, género, edad, escolaridad, condición marital y estrato socioeconómico. Las variables analíticas fueron: factor reumatoide, anticuerpo antipéptido cíclico citrulinado, anticuerpos antinucleares, velocidad de sedimentación globular (VSG), proteína C reactiva y cuadro hemático. El seguimiento clínico se realizó por medio del DAS28-VSG, CDAI, MHAQ, evaluación global de la actividad de la enfermedad por el paciente y por el médico, y escala visual análoga para dolor. Adicionalmente, se documentó el tipo de tratamiento utilizado.
La remisión clínica fue definida con base en el DAS28-VSG con un punto de corte <2,6. Los criterios de respuesta EULAR fueron tomados en cuenta de la siguiente manera: los buenos respondedores fueron pacientes que tuvieron una disminución en el DAS28-VSG en por lo menos 1,2 unidades con respecto a la evaluación inicial; respuesta moderada en aquellos pacientes con un cambio entre <1,2 y >0,6 unidades, y no respondedores a los que tuvieron cambios ≤0,6 unidades9,10. En la escala CDAI, se consideró una baja actividad de la enfermedad cuando se encontraba entre 2,8-10.
En cuanto a los criterios de respuesta ACR, se asignó un porcentaje de mejoría del número de articulaciones inflamadas, dolorosas y mejoría en 3/5 de las siguientes variables: evaluación global de la actividad de la enfermedad por el paciente y por el médico, EVA, MHAQ y VSG o proteína C reactiva, dando distintos porcentajes con respuesta al 20, 50 o 70%11.
Las modificaciones en el tratamiento de cada paciente, se realizaron de acuerdo con el criterio médico del reumatólogo, con base en los parámetros anteriormente mencionados. Las evaluaciones clinimétricas de los pacientes durante el manejo médico, se realizaron aproximadamente cada 3 meses. Para este estudio, se analizaron las evaluaciones de los pacientes a los 3, 6 y 12 meses de seguimiento. El 85% de los pacientes, tenía información a los 3 meses, el 58% a los 6 y el 53% al año.
Análisis estadísticoSe realizó un análisis descriptivo mediante tablas de frecuencia y medidas de tendencia central y dispersión, para variables cualitativas y cuantitativas, respectivamente. Para la comparación de los resultados clínicos (exámenes de laboratorio, DAS28-VSG, CDAI) y funcionales (escala MHAQ) a través del seguimiento y según el tiempo de evolución (<3 meses), se utilizaron modelos de efectos mixtos de medidas repetidas. Los modelos fueron ajustados en el software estadístico R.3.1.3, a través de estimación por máxima verosimilitud restringida (REML).
ResultadosPoblación de estudioEn el periodo de estudio, se evaluaron 134 pacientes con AR temprana de menos de un año de evolución, de estos fueron incluidos 99 pacientes que cumplieron los criterios de selección, no se incluyeron 35 pacientes debido a que no tenían una evaluación mínima al año. La edad promedio de los pacientes fue de 47,8±15,5 años y el 93% (92) era de sexo femenino. El 85% de los pacientes fue diagnosticado en ≤6 meses desde el inicio de los síntomas y el 46,6% de los pacientes tenía menos de 3 meses de evolución.
Evaluación basalEn la evaluación basal se encontró que la mitad de los pacientes presentaron entre 3 y 12 articulaciones dolorosas. Los anticuerpos antipéptido cíclico citruliano y factor reumatoide fueron positivos en el 77,8 y 77,5% de los sujetos, respectivamente. En la escala DAS28-VSG, se encontró que el 38,8% tenía una actividad de la enfermedad moderada y el 45,9% una actividad alta, la escala CDAI reportó el 37,3 y el 48,4%, respectivamente. El esquema de tratamiento y otras características clínicas se resumen en la tabla 1.
Características basales de los pacientes
| Variables | N=99 |
|---|---|
| Características clínicas | |
| Edad | |
| Media±SD | 47,8±15,5 |
| Sexo n (%) | |
| Femenino | 92 (92,9) |
| Meses de evolución de la enfermedad | |
| Mediana (RIQ) | 4,0 (2,0-6,0) |
| Evolución <3 meses n (%) | 46 (46,5) |
| Meses de seguimiento | |
| Mediana (RIQ) | 12 (3-35) |
| Número de controles | |
| Mediana (RIQ) | 3 (2-4) |
| Número de articulaciones dolorosas | |
| Mediana (RIQ) | 8 (3-12) |
| Número de articulaciones inflamadas | |
| Mediana (RIQ) | 3 (0-8) |
| Actividad global por médico | |
| Media±SD | 4,4±2,4 |
| Actividad global por paciente | |
| Media±SD | 5,1±2,4 |
| DAS28 (n=74) | |
| Media±SD | 4,8±1,4 |
| CDAI | |
| Media±SD | 22 (14-29) |
| EVA | |
| Media±SD | 6,0±2,9 |
| MHAQ | |
| Media±SD | 0,8 (0,3-1,3) |
| Medicamentos a la evaluación inicial | |
| AINE | 59 (59,6) |
| Esteroides | 25 (25,2) |
| Metotrexate (MTX) | 7 (7,1) |
| CQ/HCQ | 16 (16,2) |
| SSZ | 1 (1,0) |
| Características paraclínicas | |
|---|---|
| Hemoglobina (n=84) | |
| Mediana (RIQ) | 13,3 (12,3-14,1) |
| ACCP n (%) | |
| Positivo (n=77) | 77 (77,8) |
| Factor reumatoide n (%) | |
| Positivo (n=89) | 69 (77,5) |
| Anticuerpos antinucleares n (%) | |
| Positivo (n=66) | 6 (9,1) |
| PCR (n=67) | |
| Positivo, mediana (RIQ) | 41 (61,2), 24,0 (14,4-41,5) |
| VSG | |
| Mediana (RIQ) | 26,5 (10,0-38,7) |
El esquema de tratamiento se decidió en la primera visita de confirmación del diagnóstico y la primera evaluación de seguimiento se realizó alrededor de los 3 meses. Todos los pacientes recibieron FARME sintéticos, los cuales incluían terapias combinadas con MTX, CQ/HCQ y SSZ. Solo se tuvo conocimiento de 2 pacientes que cambiaron de régimen de tratamiento a leflunomida más MTX después de 7 y 18 meses de seguimiento y un paciente que requirió terapia biológica con etanercept a los 31 meses de evolución.
El 67% de los pacientes recibió FARME combinando con MTX más CQ/HCQ durante el primer año. A los 3 meses de seguimiento, el 27% de los pacientes recibió monoterapia con MTX o CQ/HCQ. Solo el 3% recibió terapia triple que incluyó MTX, CQ/HCQ y SSZ.
En la primera visita de seguimiento, el 65% de los pacientes era tratado con esteroides con dosis menores de 15mg, al año de seguimiento el 45% de los pacientes evaluados continuaba con esteroides con dosis menores o iguales a 5mg. Al tercer mes, el 22% de los pacientes tenía manejo con antiinflamatorios, disminuyendo a 4,7% en el primer año.
SeguimientoAl momento del diagnóstico, los pacientes tenían una VSG promedio de 29mm/h, con una disminución de 8mm/h a los 3 meses y al año de seguimiento (p<0,05). La evaluación de la actividad global de la enfermedad realizada por el médico (4,4±2,4), reportó valores más bajos en comparación con el reporte realizado por el paciente (5,1±2,4), en la visita basal. Se encontró una disminución durante el seguimiento en la puntuación de la actividad global de la enfermedad, con base en lo reportado por el médico y el paciente (p<0,05). Sin embargo, solo las puntuaciones determinadas bajo el criterio médico variaron significativamente entre los pacientes diagnosticados antes y después de los 3 meses de evolución, encontrando una mayor actividad de la enfermedad en los pacientes diagnosticados en el primer trimestre (p<0,05).
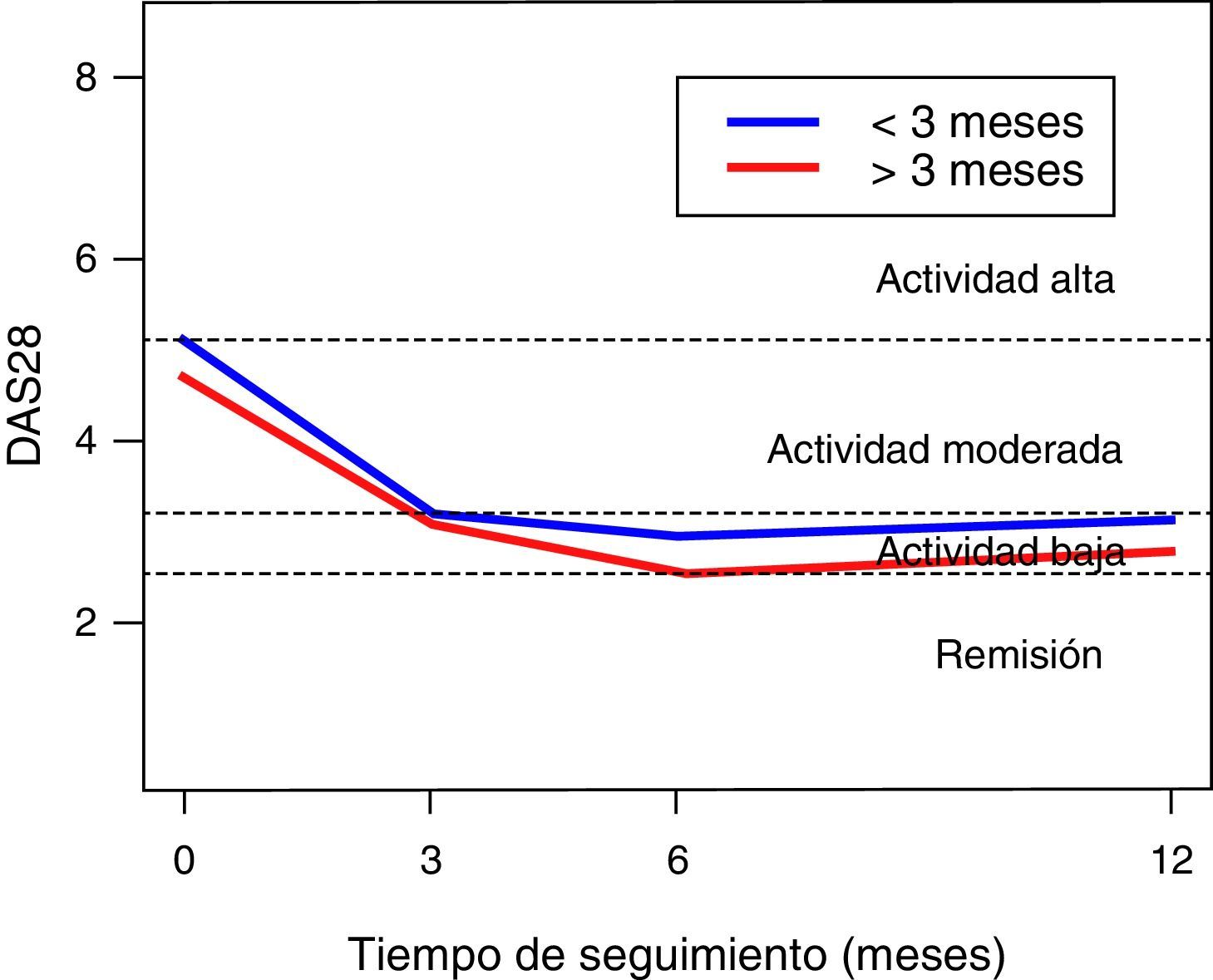
En la escala DAS28-VSG, se observa un cambio significativo de las puntuaciones durante el seguimiento (p<0,001), con una reducción en 1,5 puntos a los 3 meses, de 1,9 a los 6 meses y de 1,6 al año de seguimiento (fig. 1). La escala CDAI, al igual que la escala DAS28-VSG, indica una disminución significativa de la actividad de la enfermedad en los pacientes (p<0,05).
No se encontraron diferencias en los valores de VSG, en la evaluación global de la enfermedad por el paciente y en la escala DAS28-VSG, en los pacientes diagnosticados antes de los 3 meses de evolución. Los datos sugieren mayores puntuaciones en la escala CDAI, en los pacientes diagnosticados en el primer trimestre de evolución de la enfermedad (p: 0,056).
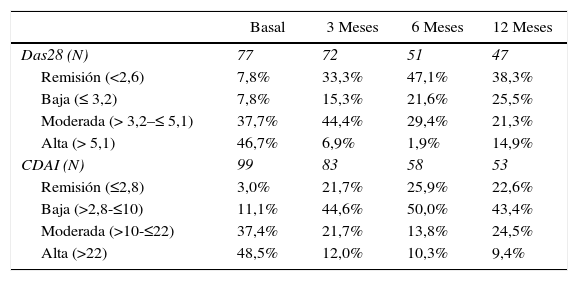
La actividad de la enfermedad, clasificada de acuerdo con las escalas DAS28-VSG y CDAI, se muestra en la tabla 2. Al tercer mes, se encontró que uno de cada 3 pacientes estaba en remisión de la enfermedad, según la escala DAS28-VSG. Se observa una disminución de la proporción de pacientes con actividad alta de la enfermedad, en las 2 escalas, a través del seguimiento.
Porcentaje de remisión (DAS28<2,6) y (CDAI ≤2,8)
| Basal | 3 Meses | 6 Meses | 12 Meses | |
|---|---|---|---|---|
| Das28 (N) | 77 | 72 | 51 | 47 |
| Remisión (<2,6) | 7,8% | 33,3% | 47,1% | 38,3% |
| Baja (≤ 3,2) | 7,8% | 15,3% | 21,6% | 25,5% |
| Moderada (> 3,2–≤ 5,1) | 37,7% | 44,4% | 29,4% | 21,3% |
| Alta (> 5,1) | 46,7% | 6,9% | 1,9% | 14,9% |
| CDAI (N) | 99 | 83 | 58 | 53 |
| Remisión (≤2,8) | 3,0% | 21,7% | 25,9% | 22,6% |
| Baja (>2,8-≤10) | 11,1% | 44,6% | 50,0% | 43,4% |
| Moderada (>10-≤22) | 37,4% | 21,7% | 13,8% | 24,5% |
| Alta (>22) | 48,5% | 12,0% | 10,3% | 9,4% |
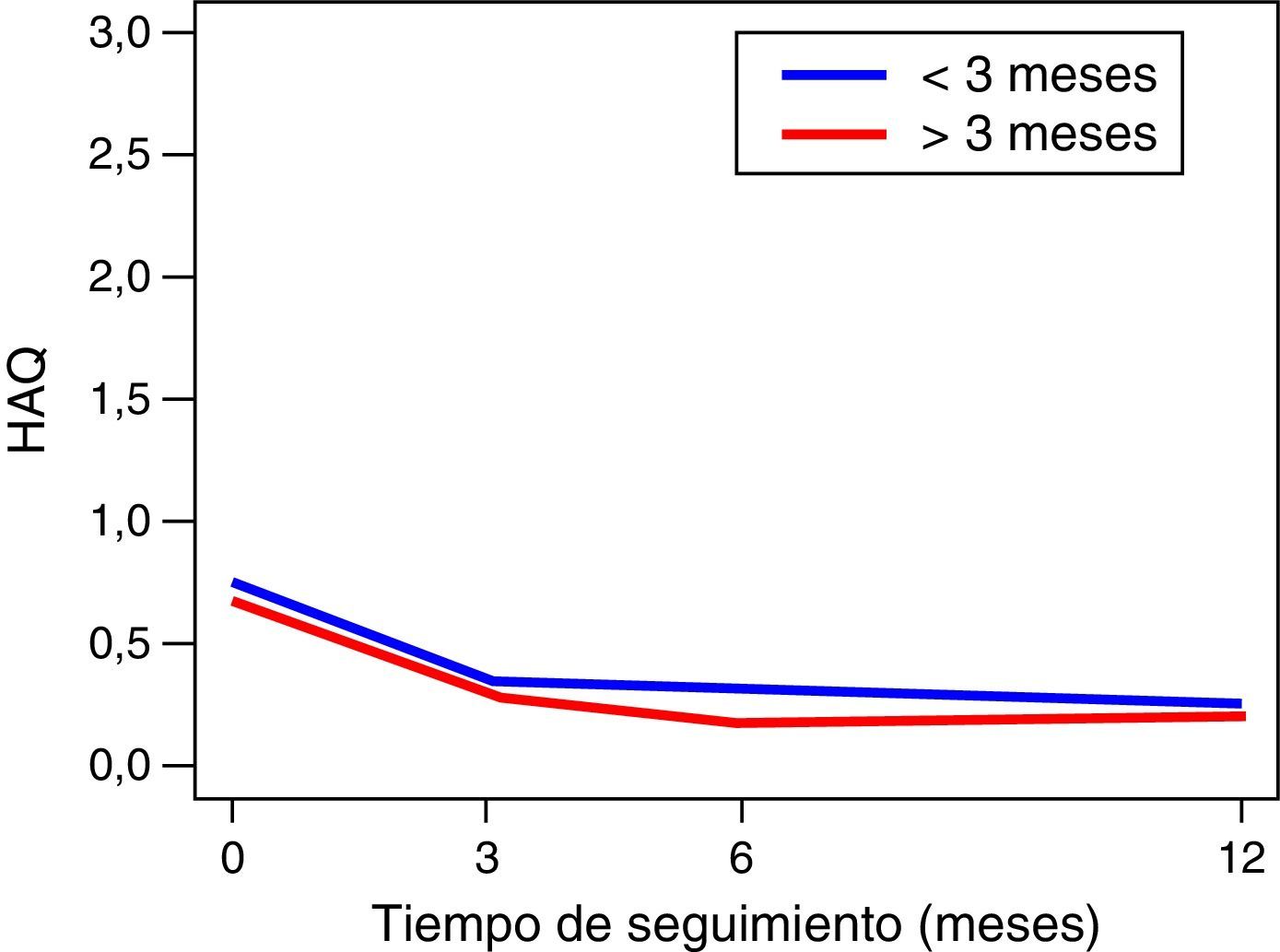
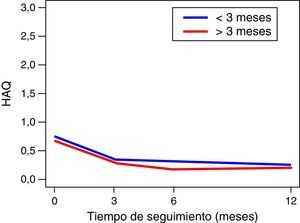
La funcionalidad de los pacientes, evaluada a través del MHAQ, evidenció una mejoría, estadísticamente significativa (p<0,05) en el primer año de seguimiento. Lo anterior, sugiere que los pacientes intervenidos para el control de su enfermedad, logran mejorar su calidad de vida en la realización de actividades cotidianas, como vestirse, comer, caminar, entre otras. No se observaron cambios en la funcionalidad de los pacientes, en las puntuaciones del MHAQ a través del tiempo, en los pacientes diagnosticados antes y después de los 3 meses de evolución (fig. 2).
Respuesta al tratamientoPara la evaluación de la respuesta al tratamiento, los pacientes se clasificaron según los criterios de respuesta EULAR. Se encontró que a los 3 meses de seguimiento, el 32% fueron buenos respondedores, el 48% moderados respondedores y el 20% no respondedores, al tratamiento. Por medio de los criterios ACR 20, 50 y 70, se encontró una respuesta a los 3 meses de tratamiento del 72,8, 45,7 y 22,2%, respectivamente. El 35% de los pacientes que no respondieron al tratamiento suspendieron los medicamentos antes de finalizar el manejo, ocasionando recaídas y reactivación de la enfermedad.
DiscusiónEn este estudio, se encontró que las características demográficas de la población con AR no difieren de lo reportado en estudios previos nacionales e internacionales. Se observó un predominio de la enfermedad en el género femenino12–14 y en edades mayores de 45 años1,15.
Nuestros datos sugieren que la remisión de la enfermedad se alcanza alrededor de los 3 meses, con resultados similares al año de seguimiento, según lo evidenciado con las escalas DAS28-VSG y CDAI. Este es un hallazgo de importancia, dado que controlar la enfermedad por periodos prolongados conlleva a una menor destrucción articular, a una mejoría de la funcionalidad y de la calidad de vida. Estos hallazgos, son similares a los reportados por otros autores16–18, pero más bajos que los indicados en el estudio TICORA19. Nosotros no encontramos diferencias en la evolución de los pacientes que fueron diagnosticados durante el primer trimestre, desde el inicio de los síntomas. Lo anterior, difiere de lo reportado por otros autores, los cuales han considerado que el diagnóstico y manejo muy temprano (<3 meses) de la enfermedad está relacionado con mejores desenlaces16,20.
Las evaluaciones realizadas evidencian la eficacia del manejo de la enfermedad antes de los 12 meses, de acuerdo con la respuesta terapéutica según EULAR y ACR. En la actualidad, se considera que el tratamiento con medicamentos modificadores de la enfermedad, confiere una ventaja significativa en el manejo de la AR21 y más aún, si ha iniciado de forma temprana, mejorando la respuesta funcional y la calidad de vida17,22,23.
El tratamiento inicial de los pacientes con AR manejados en la CAR-CMI, consiste en el uso de esteroides como terapia puente, comenzando con dosis intermedias, las cuales se disminuyen progresivamente en el tiempo, de acuerdo con el efecto terapéutico de los FARME. Aunque en este estudio no se realizó una evaluación de la respuesta de los pacientes según el tipo de terapia utilizada, nuestros resultados evidencian una mejoría de los pacientes que puede ser atribuida al tratamiento inicial. Diferentes estudios han demostrado la eficacia de los esteroides a dosis bajas junto con FARME en AR de menos de 2 años de evolución24–26. La combinación de estos medicamentos ha evidenciado disminuir la sintomatología, mejorar el pronóstico funcional de los pacientes, reducir la progresión radiológica y así mismo reducir la necesidad de terapia biológica para conseguir la remisión clínica.
El manejo terapéutico con FARME, se dio a los pacientes con base en las guías internacionales27,28 y latinoamericanas4,29. Estas, apoyan la utilización temprana de los FARME como primera línea y los biológicos como segunda línea de tratamiento. Lo anterior, se debe a que la terapia biológica puede tener un mayor costo para el paciente y están reservados para aquellos que tienen enfermedad activa persistente y que no responden a las combinaciones convencionales. Nosotros, solo tuvimos información que el 1% de los pacientes requirieron manejo con terapia biológica, después de 3 años de seguimiento. Lo anterior, sugiere un control de la enfermedad temprana con los FARME convencionales. Sin embargo, este porcentaje puede ser mayor, debido al gran número de pérdidas durante el seguimiento. Es importante resaltar que los medicamentos biológicos son eficaces. Sin embargo, la necesidad de un tratamiento a largo plazo y su toxicidad, puede hacerlos menos costo-efectivos e incrementar los costos directos relacionados con los medicamentos30,31. Si bien, lo que interesa es el control de la enfermedad con el uso de terapias disponibles, los análisis económicos apoyan el concepto de terapias con FARME y el escalonamiento de tratamiento rápido cuando hay una respuesta insuficiente, buscando alternativas que generen costo beneficio tanto para los pacientes como para el sistema de salud, este concepto va de la mano con las recomendaciones actuales de EULAR el cual es consistente con el uso racional de los recursos de la sociedad32.
Es importante resaltar que la CAR-CMI cuenta con un programa educativo especial para pacientes con AR, el cual contiene videos educativos, charlas para pacientes, acompañamiento en rehabilitación por parte de fisioterapia, terapia ocupacional y personal capacitado para el tratamiento integral de la patología, el cual busca orientar al paciente en el manejo de su enfermedad y lograr una mayor adherencia a los tratamientos propuestos. Esto se apoya en estudios previos que evaluaron el papel de la educación a los pacientes, la cual brinda beneficios adicionales para el manejo y control de la enfermedad33,34. A pesar de que todos los pacientes entraron al programa de educación, la tercera parte tenía recaídas por suspensión del tratamiento.
Este estudio representa la vida real en la práctica clínica. Los tratamientos fueron planificados y ajustados de acuerdo con la actividad de la enfermedad, conteo de articulaciones inflamadas y dolorosas, funcionalidad, comorbilidades y tolerabilidad al tratamiento. Dado que los datos provienen del seguimiento clínico realizado durante el manejo médico de los pacientes en la CAR-CMI y no fueron estrictamente recolectados para este estudio, pueden existir problemas en la calidad de la información y en algunos casos no se lograron obtener los seguimientos de las variables clínicas y funcionales en el primer año de seguimiento.
Por otro lado, no se estableció un tratamiento estandarizado para el grupo como lo utilizaron otros protocolos, sin embargo, estos datos pueden reflejar el manejo que se da a los pacientes en la práctica clínica.
ConclusionesSe evidencia una mejoría sustancial de los pacientes con AR temprana tratados durante el primer año de inicio de los síntomas. El seguimiento continuo y periódico de la patología es una herramienta indispensable para evaluar el progreso de la enfermedad y hacer ajustes en el manejo terapéutico, lo que conlleva a alterar el curso de la enfermedad y a mejorar la calidad de vida.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónEste trabajo fue financiado con recursos propios de los autores.
Conflicto de interesesLos autores declaran no presentar ningún conflicto de intereses al momento de la redacción del manuscrito.
Los autores agradecen la colaboración que brindó la institución fuente de información, en el apoyo de la recolección de datos de este proyecto, principalmente a los estudiantes de medicina de la Universidad del Valle, Alejandro Correa y Diego Escarpetta.