El modelo de cribado combinado de primer trimestre de aneuploidías fetales es el más extendido a nivel nacional. Sin embargo, aunque está bien establecido que deben realizarse controles de calidad de las medidas bioquímicas, su implantación en las ecográficas es escasa.
El objetivo de este artículo es describir cómo implantar desde el laboratorio un modelo de control de calidad que incluya todos los marcadores que se realizan en el cribado prenatal de aneuploidías.
Material y métodosSe valoró la precisión y el sesgo de los marcadores bioquímicos. En el caso de la TN se ha utilizado el método WIHRI como control de calidad y se ha aplicado el CUSUM a cada ecografista con los valores extraídos de la base de datos del software de cálculo.
ResultadosPara los parámetros bioquímicos el CV se situó por debajo del 4%. El sesgo se situó dentro de especificaciones para las concentraciones de analito, tal y como ocurrió con los MoM excepto en una mensualidad. El control de calidad de la TN mostró que 5 de los 8 ecografistas evaluados no cumplieron con los criterios de calidad establecidos cuando se utilizó el método WIHRI y 6 cuando se aplicó el CUSUM.
ConclusionesAl mostrar desde el laboratorio a los profesionales implicados la dificultad de conseguir medidas veraces de la TN, se ha consensuado el método CUSUM como control de calidad para la misma. El laboratorio enviará un informe a cada ecografista en el momento en el que sobrepase el límite de desviación establecido.
First trimester combined fetal aneuploidy screening is the most widely implemented model at national level. Although it is well established to perform quality control of biochemical measurements, it has been seldom applied to ultrasound measures.
The aim of this paper is to describe how to implement a model of quality control in the laboratory, which includes all markers in prenatal screening for aneuploidy.
MethodsWe have evaluated the precision and bias of biochemical markers. In the case of nuchal translucency (NT), the WIHRI method was employed to control quality, and CUSUM was applied to each ultrasound operator with the values extracted from the computer software database.
ResultsFor the biochemical parameters CV was below 4%. The bias was within the specification for the analyte concentration levels, as was the case for MoMs, except for one month. Quality control of NT showed that 5 of the 8 ultrasound operators evaluated sdid not comply with the quality criteria when using the WIHRI method, and 6 when CUSUM was applied.
ConclusionsAfter showing the difficulty in obtaining accurate NT measurements to the professionals involved, it was possible to reach a consensus on using the CUSUM method for quality control of NT. In this way, the laboratory will be responsible for sending a report to each ultrasound operatorin the cases where the deviation exceeds the established limit.
El cribado prenatal de aneuploidías en el primer trimestre de embarazo es un proceso multidisciplinario en el que participan los laboratorios clínicos y los Servicios de Ginecología y Obstetricia: incluye 2 magnitudes bioquímicas, la fracción β libre de la gonadotropina coriónica humana (fβ-hCG) y la proteína A plasmática asociada al embarazo (PAPP-A) y una medición ecográfica, translucencia nucal (TN)1–5.
Puesto que la TN es el marcador con más influencia en el cálculo de riesgo, la efectividad del cribado depende de la capacidad de obtener mediciones óptimas de la TN. En este sentido inciden estudios que demuestran cómo variaciones de décimas de milímetro en la medida de la TN impactan en el resultado del cálculo de riesgo6–8. Se están realizando grandes esfuerzos para armonizar las medidas de TN9,10 aunque es un cometido difícil, de hecho, se ha propuesto la utilización de medianas específicas por ginecólogo11.
Para obtener medidas de calidad es imprescindible el entrenamiento y la cualificación de los ecografistas que realicen las mediciones12 y no solo es capital la estandarización de las mediciones de TN, también es recomendable la revisión de los parámetros poblacionales y los puntos de corte en los algoritmos de cálculo así como las estrategias de cribado12.
Cuando se implanta un método de detección en la práctica clínica, el responsable se obliga a adoptar medidas de control de la calidad que permitan mantener una eficacia aceptable. Así, el control epidemiológico global de los resultados del cribado, que consiste en monitorizar continuamente las tasas de detección y falsos positivos conseguidas, si bien es el modelo más efectivo para controlar la eficacia, presenta los inconvenientes de que requiere disponer de información sobre el padecimiento o no de cromosomopatía del feto o recién nacido de todas las gestaciones que han participado del programa de detección. Esto, en nuestro sistema, es bastante complejo debido a que no a todos los cribados con riesgo alto se les realiza amniocentesis, por decisión de la gestante, y porque los partos de embarazos de alto riesgo se atienden en hospitales de un nivel superior y no hay garantía de la retroalimentación de la información del resultado del nacimiento. Por otro lado, esta se consigue de forma tardía por lo que se demora la detección de desviaciones.
En cuanto al control de calidad de las mediciones de las magnitudes bioquímicas y ecográficas aisladas, está establecido que es necesario realizar controles de calidad13–15. Sin embargo, aunque se detecta un incremento del interés en cuanto a la necesidad de aplicar controles de calidad aislados en la medida de la TN, su aplicación no está claramente definida ni estandarizada. Como control de calidad de los marcadores bioquímicos en fase analítica, se debe disponer de un control de calidad interno que permita controlar la imprecisión. El objetivo de imprecisión para estas 2 magnitudes se ha situado por debajo del 5% con el fin de que esta no repercuta en el cálculo del riesgo. Igualmente es recomendable participar en un programa de control de calidad externo con el objeto de verificar el sesgo de nuestras medidas. Por último, para evaluar la fase postanalítica es esencial realizar un control periódico de los múltiplos de la mediana (MoM) que idealmente debe ser 1 con una variación del 10% (0,9-1,1) para los marcadores utilizados16. Para el control de calidad de las mediciones de TN se utilizan principalmente 2 métodos. El primero es el utilizado por la Fetal Medicine Foundation (FMF) y se basa en obtener el % de medidas de TN por debajo y por encima del percentil 5 y 95 respectivamente. Esta metodología está ya en desuso y el método que más se utiliza actualmente es el descrito por el Woman and Infant Hospital of Role Island (WIHRI) que adoptó el control de calidad utilizado en los marcadores bioquímicos para la TN (mediana y desviación estándar del logaritmo de los MoM de las medidas de la TN)17. El inconveniente que surge al utilizar esta metodología es la necesidad de gran cantidad de datos y el análisis retrospectivo de los mismos por lo que las desviaciones, si las hubiese, se detectarían a posteriori.
Recientemente se ha propuesto la aplicación del método CUSUM (cumulative sum control chart) como control de calidad para las mediciones de TN18–21. Este método permite realizar una monitorización continua y ecografista-específica, a partir de la suma acumulada de las diferencias entre cada medición y el valor esperado, generando una gráfica con 2 líneas, una superior que monitoriza las mediciones al alza o sobreestimación y otra inferior que monitoriza mediciones a la baja o infraestimación con respecto a la media. Si la media de los valores se corresponde con la media de referencia, las líneas oscilarán en torno a la línea central basal, pero si no es así se producirá una tendencia tanto si se sobreestima como si se infraestima y la línea correspondiente se alejará cada vez más del objetivo. Se establecen unos límites a partir de los cuales se considera que el error en la medición está fuera de los márgenes aceptables. Este método permite detectar pequeños cambios de forma precoz, después de unas 40-70 mediciones (en función de la sensibilidad que se desee y el número de mediciones mínimas para generar una falsa alarma)15,16, sin tener que esperar a un análisis retrospectivo de las mismas.
El objetivo es describir cómo implantar desde el laboratorio un modelo de control de calidad del cribado prenatal de primer trimestre centrándonos en el control de los marcadores bioquímicos y ecográficos.
Material y métodosSe presentan los datos obtenidos del programa de cribado implantado en los Hospitales de Alta Resolución de Écija y Utrera pertenecientes a la Agencia Sanitaria Bajo Guadalquivir (ASBG) en el periodo comprendido entre enero de 2010 y octubre de 2011. Al disponer de un programa de cálculo adaptado para funcionar en una red local, los datos de las mediciones biométricas son introducidos en el programa por los ecografistas de los diferentes centros y los bioquímicos por los facultativos de laboratorio.
Con respecto al control de calidad de las magnitudes bioquímicas fβ-hCG y PAPP-A se ha valorado la precisión y el sesgo del método mediante el control interno y externo, respectivamente.
En el control de calidad externo se analizan 3 niveles enviados mensualmente por la sociedad científica británica United Kingdom National External Quality Assesment Service (UK-NEQAS) para el programa MSS First Trimester con el analizador KRYPTOR BRAHMS y los resultados son introducidos en el programa Ssdwlab5 (SBP [Software & Soft 2007]) junto con datos biométricos y demográficos suministrados por la entidad organizadora, de esta manera se obtienen los MoM de los analitos, así como el riesgo bioquímico y combinado que también es informado (útiles para valorar la calidad del software de cálculo).
Las especificaciones de calidad para las magnitudes bioquímicas son las proporcionadas por la institución organizadora UK-NEQAS; son el +/- 20% del BIAS para las concentraciones y MoM de fβ-hCG y PAPP-A.
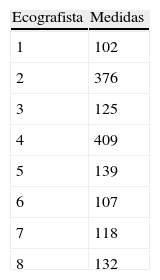
Para el cálculo de datos de control de calidad de las mediciones de la TN por ecografista se ha analizado 1.508 valores procedentes de 1.508 embarazos tomados por 8 ginecólogos (solo se obtuvieron datos de ecografistas que han realizado más de 100 medidas durante ese periodo de tiempo) (tabla 1). Para la valoración de la calidad de las mediciones de TN se ha obtenido la mediana de los MoM y la desviación estándar del logaritmo de TN expresada en MoM mediante el módulo de control de calidad del programa de cálculo SsdwLab5. Se establece como valor ideal 1 con una permisividad de +-10% para la mediana, mientras que para la desviación estándar del log 10 las especificaciones de calidad son de 0,08 a 1,314.
Además, se ha obtenido el CUSUM de cada de cada uno de ellos basándonos en el modelo sugerido por Biau et al.15 y adaptado por Sabriá et al.16 para la utilización de los MoM. El método de la suma acumulada normalizado calcula cada vez que se hace una medición 2 valores St+ y St− que se suman al resultado anterior de la siguiente manera St+ =max {0,St−1++Wt+} y St− = max {0,St−1−+Wt−}, con So+ = 0 y So− = 0 y t=0,1,2,…… Si los datos siguen una distribución normal Wt± es una medida de la desviación del valor diana. Depende del valor medido (Xt), de la media del proceso cuando se considera que esta dentro de control (μo), de la desviación estándar de las series (σ) y del valor que se designe como límite de desviación κ (para detectar desviaciones de σ/2 κ=0,5 g donde g es el número de σ que se quiere detectar), así que se define como: Wt±=Xt−μoσ−κ. Los sucesivos valores de St+ y St− se representan gráficamente vs el número de mediciones. Se establecen 2 límites (H+ y H−), uno superior y otro inferior, de modo que en el momento que o bien la línea de sobreestimación o la de infraestimación sobrepasen dicho límite, el proceso estaría fuera de control. Los valores de los límites se escogen en función del número de mediciones medias necesarias para la detección temprana de desviaciones significativas y para la obtención tardía de falsas alarmas (H+=12, 5 y H−=15). Con estos límites la sensibilidad media es de 63 y 70 medidas y el número de datos necesarios para generar una falsa alarma está por encima de 1.50016.
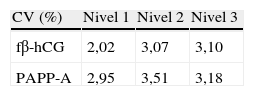
ResultadosAnalizados los datos de control interno de los marcadores bioquímicos se obtiene CV inferior al 4%, que consideramos aceptable, en cada uno de los 3 niveles (tabla 2).
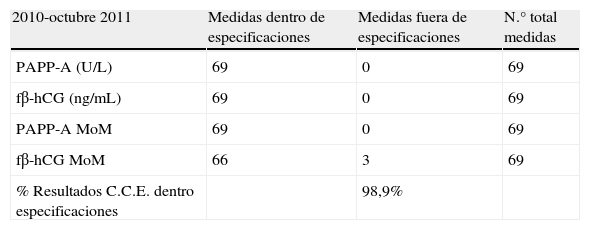
De la revisión de los informes recibidos de la institución organizadora del programa de calidad externo de las magnitudes bioquímica (UK-NEQAS) en las que se incluyen 4 variantes de control, se obtiene que el 98,9% de las medidas cumplen los estándares de calidad (tabla 3).
Resumen de los resultados del control de calidad externo de los marcadores bioquímicos
| 2010-octubre 2011 | Medidas dentro de especificaciones | Medidas fuera de especificaciones | N.° total medidas |
| PAPP-A (U/L) | 69 | 0 | 69 |
| fβ-hCG (ng/mL) | 69 | 0 | 69 |
| PAPP-A MoM | 69 | 0 | 69 |
| fβ-hCG MoM | 66 | 3 | 69 |
| % Resultados C.C.E. dentro especificaciones | 98,9% |
C.C.E.: control de calidad externo.
En cuanto a los resultados de control de la mediana de los MoM referidos al contexto poblacional, tanto la fβ-hCG como la PAPP-A están dentro de la especificación de fluctuación del 10% con respecto al valor ideal; se han tomado los valores desde la actualización de las medianas en abril de 2010 (tabla 4).
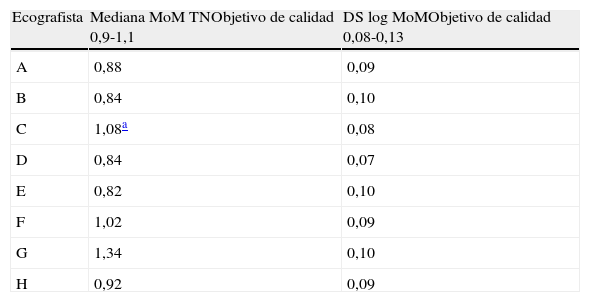
Los resultados del control de calidad de los valores obtenidos en la medida de la TN utilizando la metodología WIHRI muestran que 5 de los 8 ecografistas (62,5%) no cumplen las especificaciones de calidad, 4 (50%) infraestiman la medida de la TN y 1 la sobreestima (12,5%). La mediana de todos los valores obtenidos en la medida es de 0,88 y también está fuera de especificaciones, indicándonos nuevamente que de manera general existe una tendencia a infraestimar las medidas. En cuanto a la imprecisión de las medidas, estimada mediante la desviación estándar del logaritmo MoM de la TN, todos los ecografistas están dentro de especificaciones por lo que la dispersión de los valores es baja (tabla 5).
Resumen del resultado del control de calidad con metodología WIHRI de los resultados de las medidas ecográficas para cada ecografista y para todos los valores
| Ecografista | Mediana MoM TNObjetivo de calidad 0,9-1,1 | DS log MoMObjetivo de calidad 0,08-0,13 |
| A | 0,88 | 0,09 |
| B | 0,84 | 0,10 |
| C | 1,08a | 0,08 |
| D | 0,84 | 0,07 |
| E | 0,82 | 0,10 |
| F | 1,02 | 0,09 |
| G | 1,34 | 0,10 |
| H | 0,92 | 0,09 |
| Mediana MoM TN de todas las medicionesObjetivo de calidad 0,9-1,1 | DS Log MoM de todas las medicionesObjetivo de calidad 0,08-0,13 |
| 0,88 | 0,10 |
Cuando aplicamos el método CUSUM observamos que de los 8 ecografistas evaluados 6 (75%) están fuera de los límites establecidos, 4 infraestiman y 2 sobreestiman.
Si comparamos el método de la suma acumulada con la mediana de los MoM podemos observar que existe buena correlación salvo en un caso en el que la mediana está dentro de especificaciones mientras que en el CUSUM no.
Cuatro de los ecografistas evaluados sobrepasan los límites entre las 40-60 medidas, uno sobrepasa el límite muy por debajo de las 40 medidas (a partir de la 16) y en el otro por encima de las 60 (a partir de la 76).
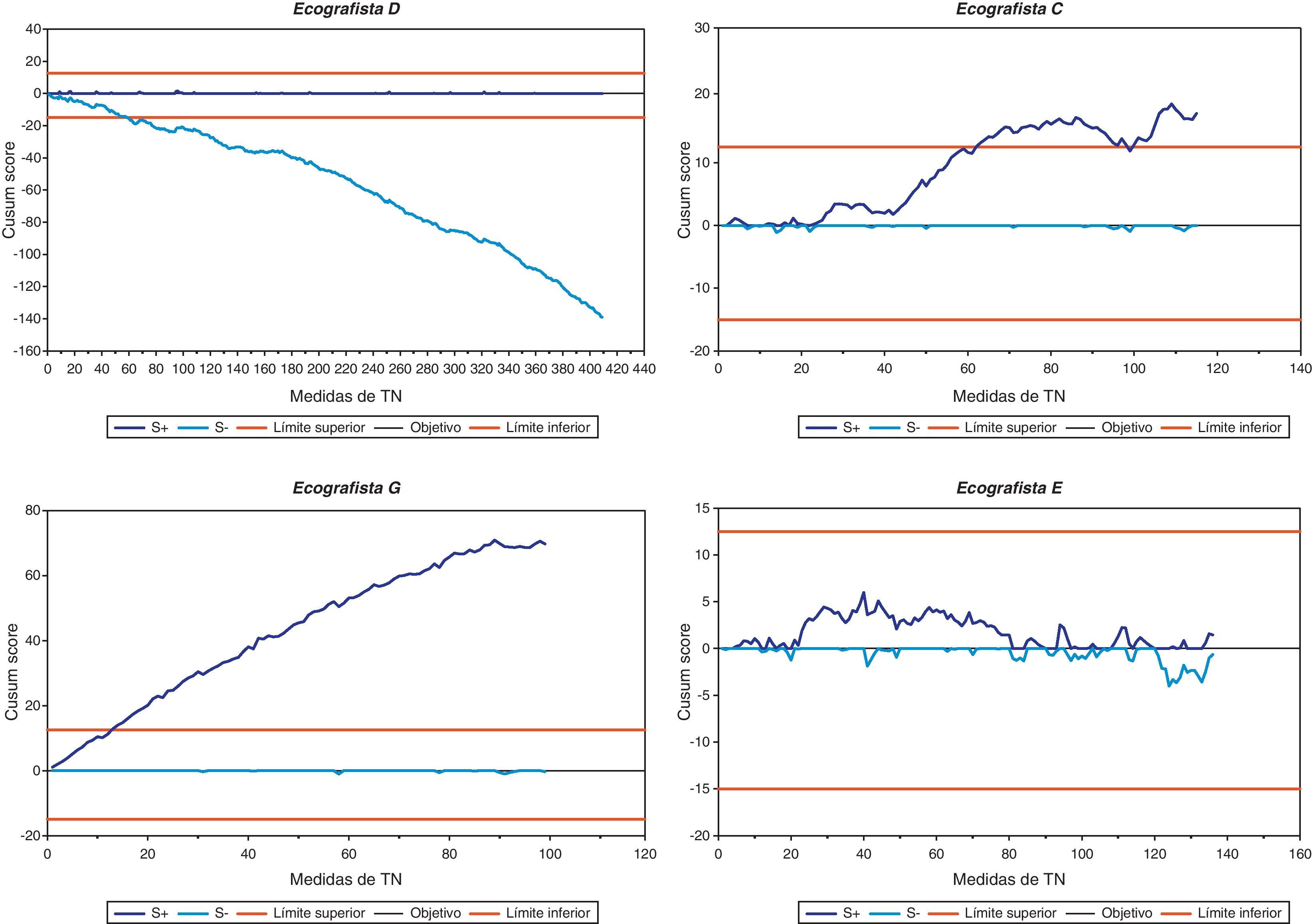
A modo de ejemplo, en la figura 1 se representan las gráficas resultantes de aplicar el método CUSUM de un grupo de ecografistas seleccionados. El ecografista (D) infraestima en sus mediciones sistemáticamente, el ecografista (G) sobreestima sistemáticamente, el ecografista (C) a partir de un punto inicia una tendencia a la sobreestimación y posteriormente se normaliza, el ecografista (E) mide correctamente en el periodo evaluado.
DiscusiónLos datos de control de calidad interno de los marcadores bioquímicos presentan una adecuada precisión.
Los resultados de control de calidad externo están dentro de especificaciones salvo el correspondiente al envío del mes de julio de 2010 en el que los MoM de la fβ-hCG se situó fuera de especificaciones en las 3 medidas (Media BIAS: +25,7%), causado por un ligero incremento en el sesgo de las concentraciones de analito (Media BIAS: +11,2%) aunque cumplen especificaciones cuando nos comparamos con los laboratorios que utilizan nuestro mismo método (por debajo de 2 expresado como índice de desviación estándar). Además el riesgo bioquímico y combinado presentaban una desviación aceptable con respecto al valor de referencia (Running Risk Score (RRS) del riesgo bioquímico: -1 y combinado: 0).
La mediana de los MoM de los marcadores bioquímicos se sitúa en valores aceptables indicándonos que las medianas utilizadas son adecuadas a nuestra población (tabla 5).
En cuanto a los resultados de las medidas de TN nuestros hallazgos muestran la dificultad para conseguir medidas veraces de la TN; ya hemos hablado de la escasa implantación del control de calidad en esta técnica ecográfica. Es preciso señalar también que los modelos de control de calidad más utilizados basados en la mediana de los MoM precisan de un largo análisis retrospectivo.
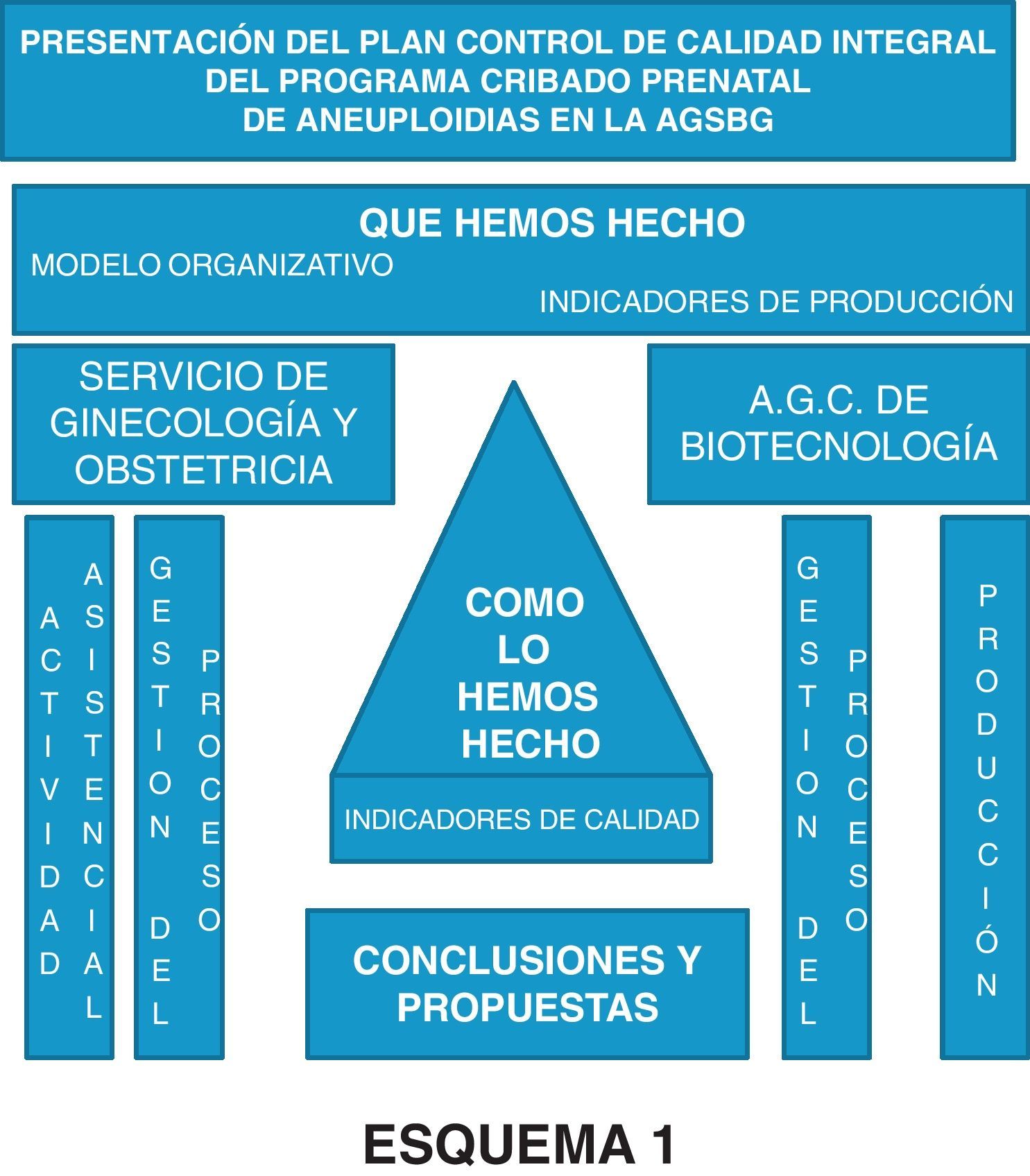
Del análisis y reflexión de esta situación por parte del laboratorio surge la propuesta de explorar cómo recibirían los ginecólogos la utilización del CUSUM como herramienta para monitorizar de manera continua e individualizada sus mediciones ecográficas. Con la colaboración de la Dirección Médica realizamos una sesión clínica que ha tratado de explicar a los ginecólogos los conceptos en que se basa el control de calidad y su utilidad aplicada al cribado prenatal de aneuploidías, construida en base al esquema 1. Tras este paso previo, hemos consensuado:
- •
El envío de un informe individualizado a cada ecografista cuando sobrepase el límite establecido, lo que le permitirá la toma de medidas correctoras a tiempo real, con el propósito de evitar infra o sobreestimaciones que conllevan consecuentemente a una infra o sobreestimación del riesgo de aneuploidías.
- •
La realización de una reunión conjunta anual coordinada por la Dirección Médica para valorar el grado de cumplimiento de los estándares de calidad.
La propuesta de implantación del modelo control de calidad del cribado prenatal de aneuploidías en el primer trimestre de embarazo, lejos de generar sorpresa o conflictos interdepartamentales, ha sido globalmente bien aceptada, ha generado una sinergia beneficiosa y el inicio de una cultura de seguridad y calidad basada en datos objetivos, con lo que se evitarán incidencias y tendencias que influyen negativamente en los resultados. Estudios posteriores deberán corroborar el impacto de estas medidas de control sobre la eficacia del programa de cribado.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.