La neurodegeneración asociada al déficit de pantotenato cinasa es una entidad autosómica recesiva secundaria a las mutaciones del gen pantotenato cinasa 2 (PANK2). Clínicamente se caracteriza por anormalidades progresivas del movimiento y demencia. El tratamiento médico de la enfermedad es limitado y la distonía suele ser refractaria, por lo cual la cirugía estereotáctica con colocación de electrodos cerebrales profundos es una opción terapéutica cada vez más usada en estos pacientes. Describimos una paciente de 32 años de edad con distonía severa asociada a déficit de PANK2. Fue programada para tomografía computarizada estereotáctica y colocación bilateral de electrodos en núcleo pálido medial, bajo anestesia general para tratar la distonía debilitante y la rigidez generalizada asociada a su enfermedad. Durante la intervención se realizó el mantenimiento anestésico con propofol, rocuronio y remifentanilo en perfusión, sin ninguna incidencia a destacar durante el procedimiento. Tras la intervención la paciente fue trasladada a la unidad de cuidados intensivos bajo sedación farmacológica con remifentanilo para proceder a una educción lentamente progresiva. La paciente pudo ser dada de alta tras la colocación del generador y en el seguimiento posterior se ha evidenciado mejoría de los movimientos distónicos.
Anesthesia considerations for deep-brain stimulation in a patient with type-2 pantothenate kinase deficiency (Hallervorden-Spatz disease)
Neurodegeneration associated with pantothenate kinase deficiency is an autosomal recessive condition caused by mutations in the pantothenate kinase 2 gene (PANK2). Clinical characteristics include progressive motor impairment and dementia. Medical treatment is limited and the dystonia tends to be refractory, making stereotactic surgery with placement of deep-brain electrodes an option that is being adopted with greater frequency in these patients. We report the case of a 32-year-old woman with severe dystonia associated with PANK2 protein deficiency. The patient was scheduled for stereotactic bilateral placement of electrodes in the medial globus pallidus, guided by computed tomography and under general anesthesia, to treat the debilitating dystonia and generalized stiffness associated with her condition. Anesthesia was maintained with propofol, rocuronium and remifentanil in perfusion during the intervention, which was uneventful. After the procedure, the patient was transferred to the intensive care unit and sedation was provided with remifentanil to allow slow, gradual emergence from anesthesia. The patient was discharged from hospital after placement of the implanted pulse generator, and subsequent follow-up showed improvement of the dystonia.
La neurodegeneración asociada al déficit de pantotenato-cinasa (PANK) es una entidad autosómica recesiva caracterizada por disfunción extrapiramidal. Era conocida previamente con el epónimo de Hallervorden Spatz quienes describieron por primera vez la enfermedad en cinco hermanas con disartria y demencia progresiva, cuyos cerebros mostraron una degeneración marrón en el globo pálido y la sustancia nigra. Desde que se conocieron las actividades no éticas de Hallervorden y Spatz, la nomenclatura de la enfermedad ha sido reemplazada por PANK (neurodegeneración asociada al déficit de pantotenato cinasa tipo 2)1.
El gen responsable de PANK2 ha sido descubierto en el cromosoma 20 y codifica la pantotenato cinasa la cual es esencial para la síntesis de coenzima A desde el pantotenato e indispensable para la síntesis de ácidos grasos, así como en el metabolismo energético. La alteración en la pantotenato cinasa también lleva al depósito de cisteína en los ganglios basales, así como a la acumulación de hierro en estas áreas. El complejo hierro-cisteína puede causar daño tisular al promover la aparición de estrés oxidativo. Es así como el síndrome de déficit PANK puede ser identificado como un desorden del metabolismo del pantotenato (Vitamina B5)2.
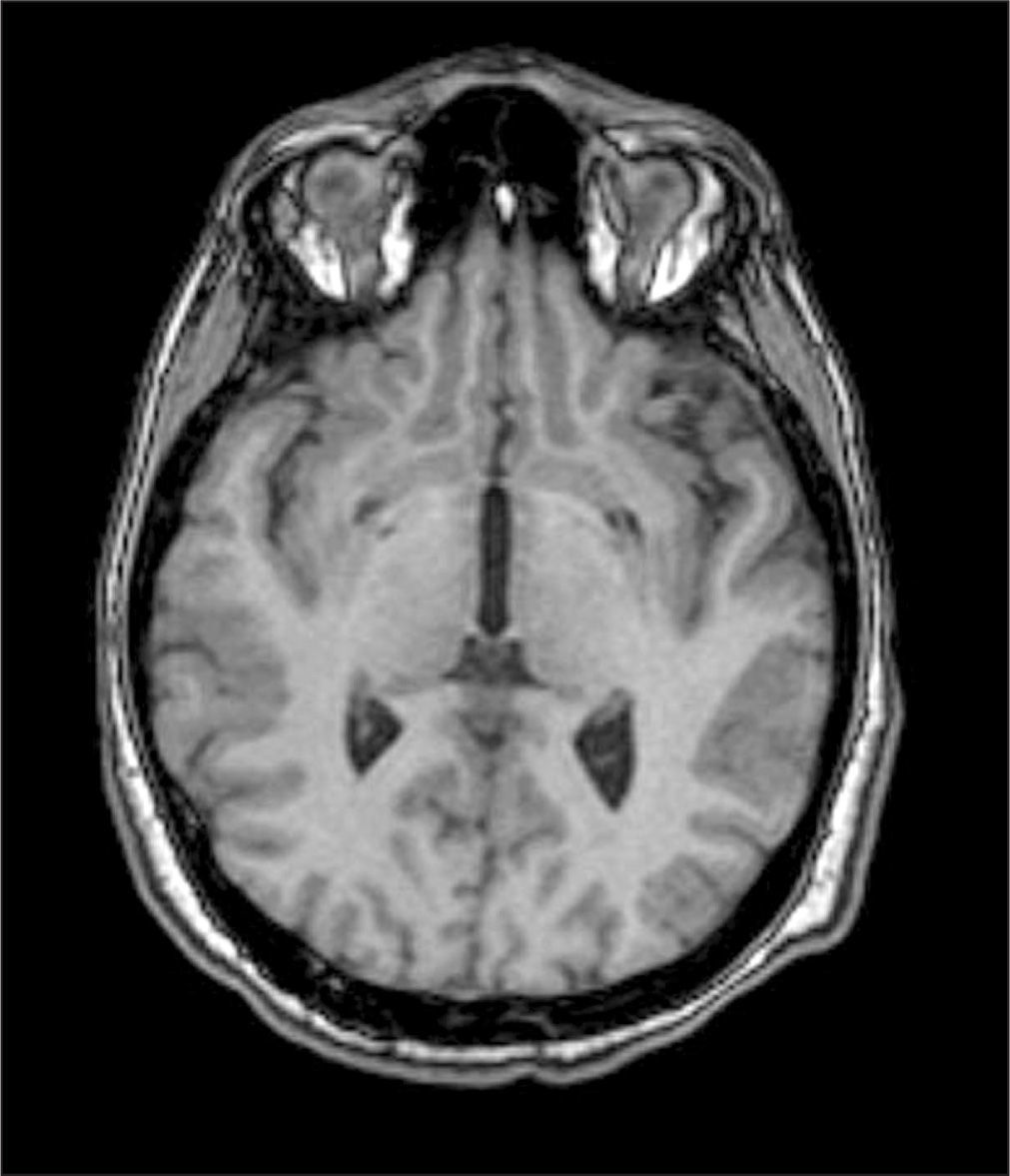
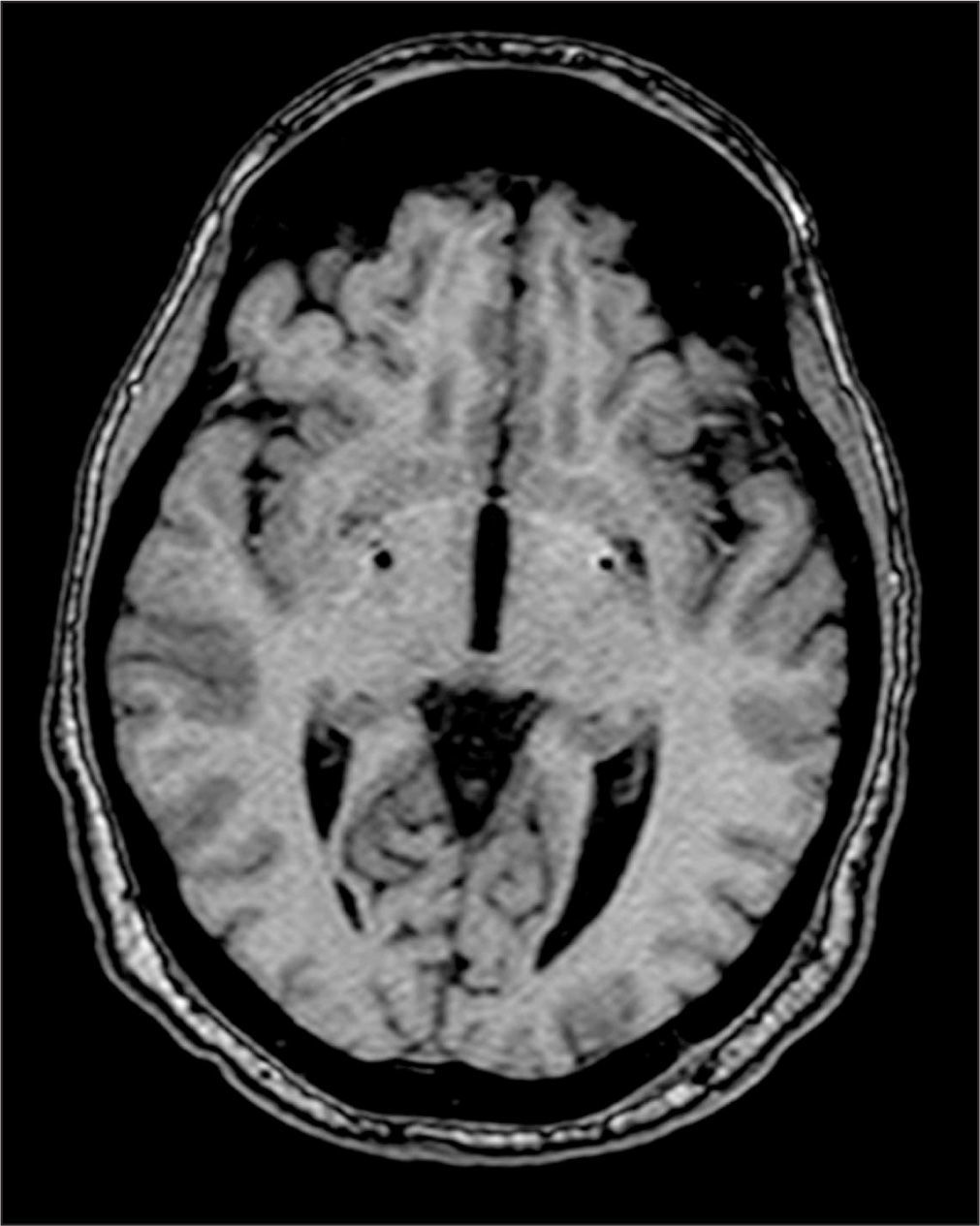
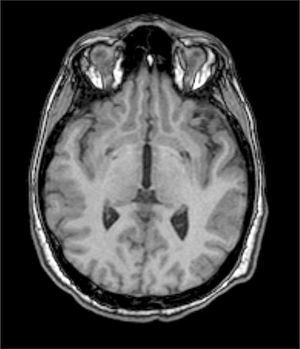
Clínicamente se caracteriza por trastornos del movimiento progresivos y demencia. Los pacientes presentan síntomas motores como parkinsonismo, distonía y corea que se inician tempranamente en la infancia. En la sustancia nigra y en el núcleo pálido se encuentran cambios histopatológicos patognomónicos que incluyen depósitos de hierro, gliosis y edema axonal. Las lesiones características en ojo de tigre de la resonancia magnética nuclear tienen valor en la confirmación diagnóstica y se caracterizan por áreas bilaterales de hiperintensidad dentro de una región de hipointensidad en el núcleo pálido medial3 (Figura 1).
El tratamiento médico de la enfermedad es limitado y la distonía suele ser refractaria. Por ello, se han hecho esfuerzos para proveer opciones terapéuticas alternativas como la cirugía de denervación periférica, la colocación de bombas de baclofeno intratecal o la cirugía funcional estereotáctica4. La experiencia con los enfermos de parkinson cuyos síntomas distónicos asociados mostraban una mejoría notable tras palidotomía o estimulación del núcleo pálido, han hecho que las aproximaciones estereotácticas a los globos pálidos mediales se apliquen como terapia en todas las formas de distonía5. Actualmente, predomina la tendencia a implantar sistemas de electrodos que estimulan a altas frecuencias mediante un generador semejante a un marcapasos cardiaco, como alternativa a inducir lesiones anatómicas. Con esta técnica, los procedimientos quirúrgicos se han hecho más seguros y los efectos secundarios más fáciles de controlar. Además, es una técnica reversible y las características de la estimulación pueden variar a medida que la enfermedad progresa6.
Caso clínicoDescribimos una paciente de 32 años de edad con distonía severa refractaria a tratamiento médico y asociada a déficit PANK2. Fue programada para tomografía computarizada (TC) estereotáctica y colocación de electrodos en núcleo pálido medial, bajo anestesia general, para tratar la distonía debilitante y la rigidez generalizada asociada a su enfermedad.
Los síntomas aparecieron a los 6 años de edad cursando con retraso escolar, trastornos del lenguaje y de la marcha, desarrollando posteriormente retinitis pigmentaria. La alteración del lenguaje y la dificultad para la marcha se hicieron más evidentes apareciendo posteriormente rigidez y distonía generalizada. Tenía movimientos de hiperextensión del cuello y distonía de las cuatro extremidades, por lo que presentaba gran dificultad para la marcha, precisando de ayuda para dar unos pasos. La musculatura orofacial estaba implicada, produciendo dificultad para comer y hablar. La paciente fue diagnosticada a los 18 años de edad, cuando una resonancia magnética cerebral reveló las imágenes típicas diagnósticas3. En los años siguientes, recibió tratamiento con biperideno 4mg al día y levomepromazina 7mg cada 82horas, con discreta mejoría. Previamente a la cirugía presentaba movimientos distónicos dolorosos en cabeza, miembros superiores e inferiores que no respondían a tratamiento médico y cuyos episodios se hicieron cada vez más frecuente [Escala de Burke-Fahn-Marsden7 de 102 (0–120)], por lo que fue propuesta para cirugía estereotáctica8.
La valoración preanestésica revelaba una paciente de 48Kg de peso, con escoliosis moderada y ceguera por la retinitis pigmentaria. Estaba incapacitada para caminar y sentarse, y la comunicación verbal se limitaba a la emisión de sonidos incomprensibles. La paciente presentaba apertura bucal completa continua por espasmos distónicos intensos; Mallampati II. Se mantuvo el tratamiento habitual hasta el día de la intervención y se premedicó con clonazepam 0,5mg en la noche anterior a la cirugía. La analítica preoperatoria era normal.
El día de la intervención, tras la monitorización no invasiva [electrocardiograma (ECG), presión no invasiva (PNI) y pulsioximetría (SpO2), siendo sus tensiones basales de 110/60mmHg], se procedió a inducir la anestesia general endovenosa con fentanilo 100µg, propofol 130mg y rocuronio 50mg. Se intubó con un tubo endotraqueal de 7,0mm sin problemas, iniciándose la ventilación en modo volumen control con una FiO2 al 0,5, volumen corriente (VT) 500mL, frecuencia respiratoria (FR) 12min−1’, presión positiva al final de la espiración (PEEP) 8mmHg. Se cateterizó la arteria radial izquierda, la vena yugular derecha y tras colocación del marco estereotáctico Leksell®, fue trasladada al área de radiología para la realización de una TC craneal. Durante el transporte medicalizado (monitorización y ventilación mecánica), la sedación se mantuvo con infusión de propofol a 1–2mg mL−1 y remifentanilo iv a 0,1µg Kg−1 min−1. Al regresar al quirófano, se continuó con la monitorización de la SpO2, temperatura con termómetro esofágico, capnografía, diuresis, presión arterial invasiva, Doppler precordial, monitor de relajación muscular (TOF), profundidad anestésica (BIS) y presión venosa central a través de la vena yugular derecha mediante monitor (Datex-Ohmeda® S/5 Monitor, Helsinki, Finland).
Se fijó la cabeza de la paciente mediante el marco estéreotáctico y se practicaron incisiones cutáneas bicoronales con dos hemiherraduras, a nivel de donde se realizaron dos orificios de trépano, uno a cada lado de la sutura coronal, guiados estereotácticamente.
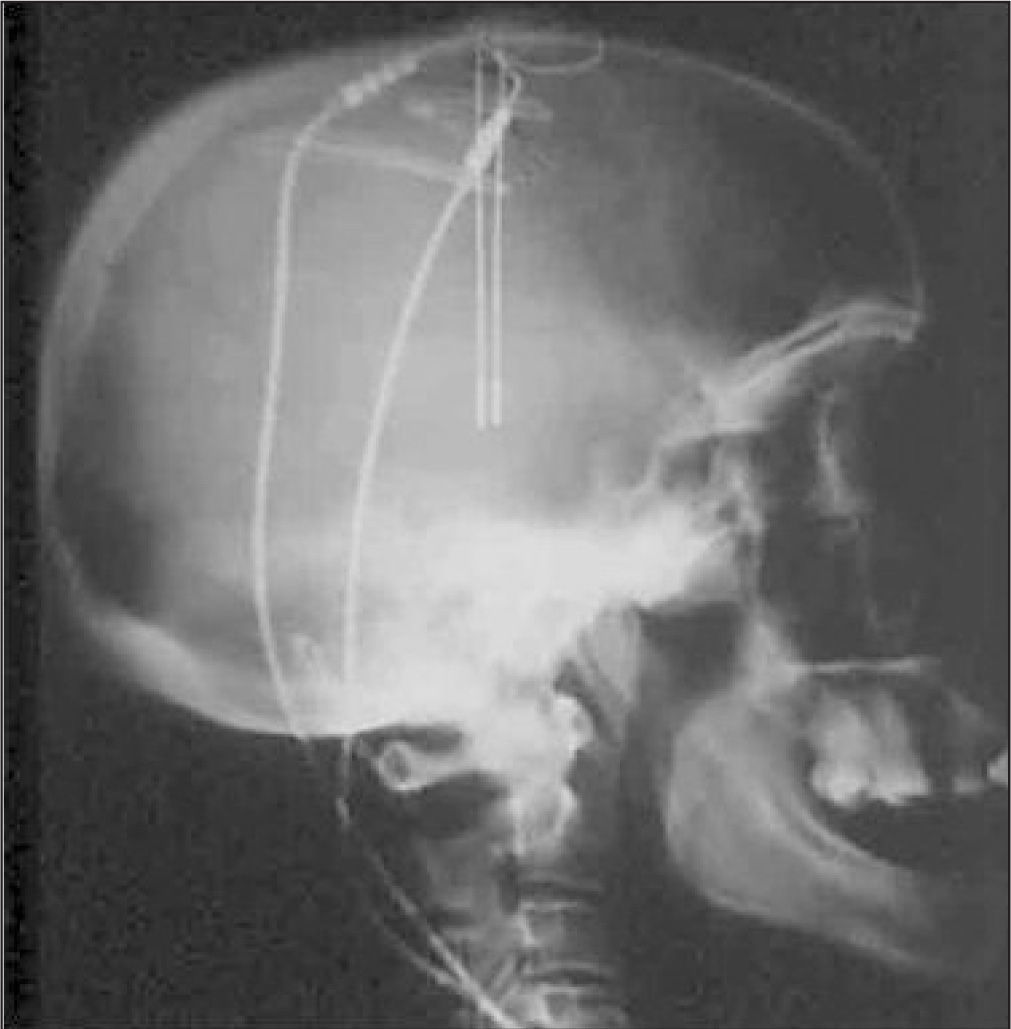
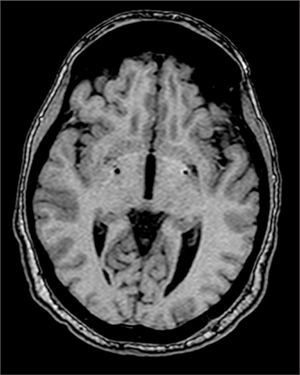
Calculadas las dianas terapéuticas se inició la confirmación de la diana anatómica mediante microrregistro neurofisiológico. La anestesia se mantuvo con remifentanilo a 0,1µg Kg−1 min−1, propofol en TCI (target control infusion) 1–2mg mL−1 y rocuronio 0,1mg Kg−1 h−1 para mantener un TOF de 0/4-1/4 siendo suspendido al iniciarse la implantación de los electrodos. Durante la implantación de los electrodos se mantuvo la anestesia total endovenosa (TIVA) dada la existencia de distonía severa. La paciente se colocó en posición semisentada y la intervención duró 13horas, siendo necesarios 5 trayectos de microrregistro para localizar el pálido medial izquierdo y 6 trayectos para el pálido medial derecho (Figura 2). La principal dificultad residió en la imposibilidad de detectar los potenciales visuales de las cintillas ópticas en su vecindad con la base del globo pálido interno (una referencia fundamental) a causa de la retinitis de la paciente. El sangrado intraoperatorio fue de aproximadamente 400mL, llegando la hemoglobina a un valor de 9dL−1, por lo que se transfundieron dos concentrados de hematíes para garantizar un aporte de oxígeno óptimo y dado que la cirugía estaba siendo técnicamente difícil y el sangrado continuaba. La paciente se mantuvo estable cardiorrespiratoriamente y normotérmica durante la intervención. Tras la intervención, la paciente fue trasladada a la unidad de cuidados intensivos (UCI) bajo sedación farmacológica con remifentanilo. Fue extubada a la hora de su ingreso en la UCI, manteniéndose la perfusión de remifentanilo sin incidencias y observándose la persistencia de movimientos anormales en cabeza y miembros superiores. Al día siguiente la paciente fue trasladada a la sala de hospitalización convencional.
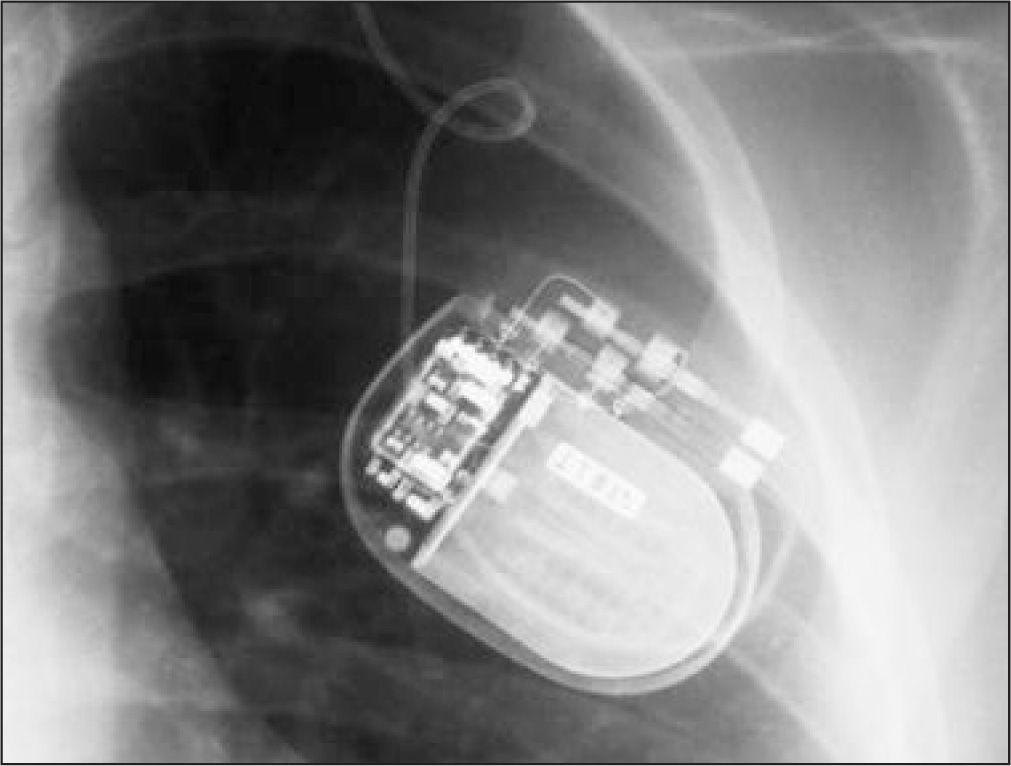
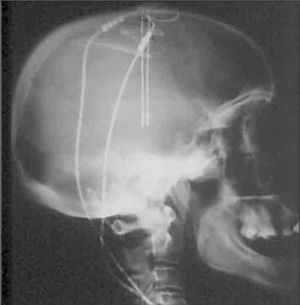
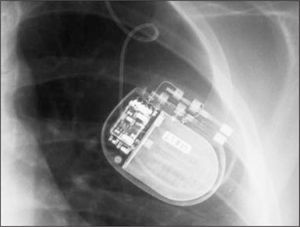
A la semana siguiente se procedió a la implantación subcutánea de un generador de impulsos eléctricos y a su conexión con los electrodos intracerebrales (Figuras 3 y 4), bajo anestesia general endovenosa con propofol TCI, remifentanilo y cisatracurio en perfusión. Se desestimó el uso de una técnica locorregional debido a la flexión y desviación lateral de la cabeza así como a la espasticidad de la paciente. No hubo incidencias a destacar en este procedimiento, la paciente pudo ser extubada en el postoperatorio inmediato sin incidencias. La paciente no presentó complicaciones durante su ingreso y se dio de alta a la semana del ingreso.
Reingresó al cabo de un mes del alta para ajustar las estimulaciones del generador, teniendo a los 6meses una puntuación de Burke-Fahn-Marsden de 73, una mejoría del 30% tanto en los parámetros de discapacidad como en los de severidad. Podía sentarse sin ayuda, los espasmos bucales eran ocasionales y el tono de las cuatro extremidades normal, aunque la capacidad de deambular no se recuperó.
DiscusiónSon varios los aspectos a destacar en el manejo de estos pacientes. Es importante evaluar preoperatoriamente los antecedentes de obstrucción de la vía aérea asociada a la distonía. En nuestro caso no hubo incidentes en el manejo de la vía aérea, quizás debido a que la educción y la extubación tras la intervención quirúrgica de mayor duración no se realizaron en el postoperatorio inmediato, sino una hora después del traslado a la UCI por el riesgo de aparición de distonía cervical y compromiso de la vía aérea. Keegan et al describen el caso de una paciente de 11 años afecta de déficit de la PANK e intervenida bajo anestesia general para la realización de talamotomía esterotáctica en la que se realizó una extubación precoz, que se asoció a un cuadro de obstrucción completa de la vía aérea y tuvo que ser reintubada, presentando además un edema pulmonar por presión negativa5.
Otro aspecto a tener en cuenta, es que estos pacientes con frecuencia son tratados con fármacos de acción anticolinérgica central, como el biperideno, asociados con la aparición de disfunción cognitiva postoperatoria9. Este “síndrome anticolinérgico central” podría aumentar los síntomas distónicos y retrasar la recuperación postquirúrgica10,11. Nuestra paciente estaba en tratamiento crónico con levomepromazina, un neuroléptico que puede producir hipotermia e hipotensión. Por otro lado en la literatura se refiere asociación entre el tratamiento crónico con antipsicóticos y la agravación de la disminución de la temperatura asociada a la anestesia general12, o la aparición de hipotensión por una insuficiente respuesta adrenal frente al estímulo quirúrgico13. En nuestro caso, la paciente no presentó ni hipotermia ni inestabilidad hemodinámica. En estos pacientes es especialmente importante la monitorización intraoperatoria multimodal, tanto hemodinámica como de la relajación muscular, de la temperatura y de la hipnosis, todo ello con el fin de ajustar mejor las dosis de agentes anestésicos y evitar la aparición de inestabilidad hemodinámica e hipotermia. Queremos incidir enque mantuvimos la sedación con remifentanilo en el postoperatorio inmediato, ya que ante la naturaleza de la enfermedad y los antecedentes de empeoramiento de los síntomas con la ansiedad, consideramos recomendable una educción gradual y una extubación en las mejores condiciones posibles.
Nosotros realizamos una anestesia TIVA con propofol, remifentanilo y rocuronio en esta paciente por la severidad de la distonía. A pesar de que algunos grupos consideran que el propofol interfiere con los microrregistros en la cirugía estereotáctica, existen por otra parte reportes que consideran inconsistentes los efectos del propofol sobre las neuronas del globo pálido medial14.
Tras la cirugía los espasmos dolorosos relacionados con la hipertonicidad, las posiciones distónicas y los movimientos anormales disminuyeron sustancialmente tal como en las serie de pacientes presentada por Castelnau et al.15.