La artrosis es la alteración articular lenta y progresiva que ocurre especialmente en los ancianos y que se caracteriza por la destrucción patológica del cartílago y subsecuentes cambios del hueso o tejido subcondral, que incluyen esclerosis y osteofitosis. Sin embargo esta definición ha quedado un poco anticuada a tenor de los conocimientos acerca de la etiopatogenia de la artropatía degenerativa. Por esto la definición debiera ser: "Es un grupo de cambios que pueden tener distintas etiologías, aunque con un resultado similar desde el punto de vista biológico, morfológico y clínico. Este proceso no sólo afecta al cartílago articular, sino también a toda la articulación incluyendo el hueso subcondral, la cápsula articular, la membrana sinovial y los músculos periarticulares. Finalmente, el cartílago articular degenerado presenta fibrilación fisural, ulceración y pérdida completa de espesor de la superficie articular".
La artrosis es la forma más común de enfermedad reumática. Su alta prevalencia especialmente en los ancianos, con afectación física notable, es una de las causas de discapacidad, especialmente con respecto a su comportamiento funcional1. Dentro de las enfermedades que presentan un curso crónico, la artropatía degenerativa afecta al 50% de los adultos que tienen más de 65 años de edad. Si en EE.UU. la padecen alrededor de 20 millones de personas, en España es un proceso frecuente que, de presentar esa misma proporción, afectaría a unos 5 millones de pacientes2.
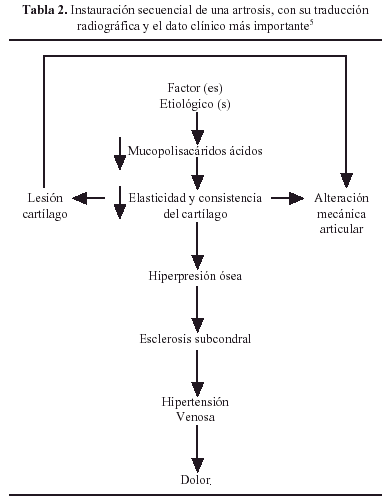
La artrosis se clasificó en 4 estadios según el aspecto radiológico:
1. Preartrosis, sin alteraciones artrósicas.
2. Artrosis precoz, con ligero pinzamiento del espacio articular asociado con esclerosis del hueso subcondral.
3. Artrosis avanzada, con pinzamiento del espacio articular, radiolucencias quísticas y osteofitosis moderada.
4. Artrosis severa, con desaparición del espacio articular y marcada formación de osteofitos.
El aspecto artroscópico se clasificó, según Outerbridge, en 5 grados:
GRADO 0: Sin anormalidades.
GRADO 1: Reblandecimiento y tumefacción del cartílago.
GRADO 2: Fragmentación o fisuración en una zona de 1 cm de diámetro o menos.
GRADO 3: La zona afecta es superior a 1 cm de diámetro.
GRADO 4: Erosionado el cartílago hasta el hueso.
Las lesiones artrósicas de la rótula son frecuentemente del grado 3 de Outerbridge. Sin embargo, en el cóndilo femoral externo predominan las de grado 4 y, además, son las primeras en frecuencia3. La pérdida de la superficie cartilaginosa se afecta en diversa extensión y profundidad, llegando incluso a desprenderse parcialmente, lo que da lugar a una clara artrosis fémoro-rotuliana, cuya reparación completa es impensable de forma espontánea4. Aun sin existir un claro causante de la instauración de la artrosis, se han mencionado diversos factores que pueden facilitar la presencia de la misma, unos locales y otros generales, que son enumerados en la Tabla 1.
Cuando uno o varios de estos factores actúan, se produce la degeneración del cartílago articular, motivado por la sobrecarga y la perturbación mecánica consiguiente. A ello se acompaña la progresión de las lesiones desde la superficie hacia la profundidad del cartílago. Sin embargo, la artrosis afecta a éste, al tejido óseo subcondral, a la cápsula y a la membrana sinovial, y lo hace siguiendo unas normas que es preciso conocer para entender el efecto que se va a instaurar posteriormente5.
INSTAURACIÓN DE LAS ALTERACIONES EN EL CARTÍLAGO ARTICULAR
El cartílago articular se vuelve opaco, de color amarillento, rugoso, blando y menos elástico. Se considera debido a la disminución de mucopolisacáridos ácidos de la sustancia fundamental, lo que desprotege a las fibras colágenas y limita la amortiguación que se precisa cuando se produce una sobrecarga mecánica. Por eso es de consenso prácticamente general que las alteraciones del cartílago son de presentación precoz en la artrosis, por alteraciones en la organización y en el tamaño de las fibras colágenas, que se despegan de las adyacentes. Si se constata la pérdida de matriz cartilaginosa, es responsabilidad de las enzimas lisosómicas y de las metaloproteinasas de la matriz (MPM). En sentido contrario actúa el factor de crecimiento básico de los fibroblastos (FGF), que favorece la reparación o estabiliza el proceso de deterioro cartilaginoso6.
En la artrosis, los condrocitos sufren divisiones activas, produciendo una cantidad elevada de ADN, ARN, colágeno, prostaglandinas (PG), y proteínas no colágenas. Esta hiperactividad aumenta la concentración de PG, que conllevaría un engrosamiento del cartílago, que se conocería como artrosis «compensada», que puede frenar su evolución durante años, pero con un cartílago menos resistente que el normal para la vida ordinaria. Finalmente disminuiría la síntesis de PG, el cartílago perdería altura y se desarrollaría una artrosis «terminal»6.
Al realizarse la carga sobre una articulación que funciona en condiciones normales, se produce una deformación del cartílago y del hueso subcondral, que facilita un máximo contacto de las superficies articulares y un reparto de presiones. Cuando no existe esa elasticidad las presiones se concentran, obligando a la articulación a trabajar en unas condiciones que van a facilitar la sobrecarga articular y la degeneración del cartílago7.
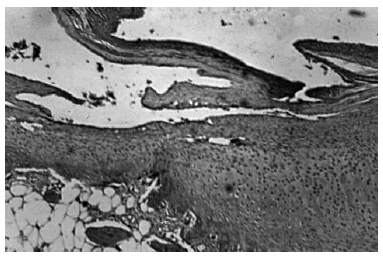
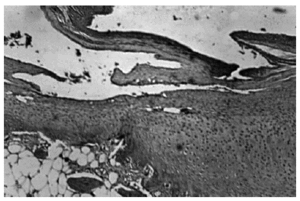
Sin embargo, las alteraciones no se presentan exclusivamente en el cartílago, aunque éste es el que más sufre, ya que se afectan dos de sus funciones más importantes: de una parte la superficie lisa que permitiría un deslizamiento prácticamente sin fricción, que se hace rugosa y con una sobrecarga friccional, y de otra parte porque el reparto de cargas sobre el cartílago y su homónimo pierde el poder de reparto de cargas y sufre un cambio de esfericidad que hace que las fuerzas se concentren en un número menor de puntos, se aboque a una deformidad del mismo y a la rotura de las fibras colágenas, hendiduras o fisuras, que son horizontales pero, si aumentan, se hacen verticales y más profundas (Fig. 1). Algunos fragmentos pueden desprenderse en la superficie, originando erosiones superficiales o úlceras más profundas, con fondo formado por fibras colágenas verticales desprovistas de sustancia fundamental, con aspecto aterciopelado o afelpado (degeneración velvética)3,5.
Figura 1. Anatomía patológica de una artrosis con degeneración y adelgazamiento del cartílago (HEx 20).
TEJIDO ÓSEO SUBCONDRAL
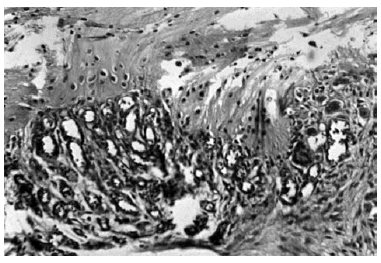
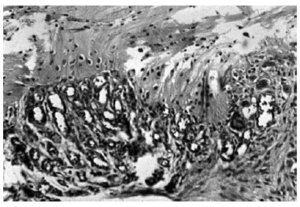
El tejido óseo subcondral presenta ulceraciones más profundas que hacen desaparecer el cartílago, descubriendo el hueso subcondral, de aspecto marmóreo, en el que pueden aparecer islotes de neocartílago en forma de «clavos de tapicero». En la capa profunda se produce la penetración de mamelones conjuntivo vasculares procedentes de la médula ósea subyacente, que atraviesan el tejido subcondral (Fig. 2). En las zonas periféricas y en las zonas no sometidas a presión se forman los condrofitos que, por osificación endocondral, se transforman en osteofitos5.
Figura 2. Neoformación capilar yustacartilaginosa y células gigantes en una rodilla artrósica (HEx 50).
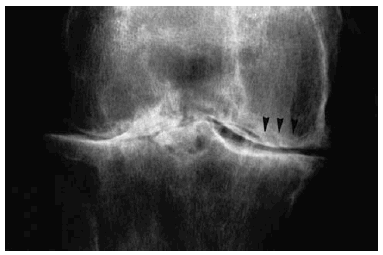
En las zonas de mayor presión articular se produce una marcada disminución del grosor del cartílago, que coincide con el aumento de formación en las zonas de menor presión periféricas. Ello da lugar a la característica deformidad (Fig. 3) y al empeoramiento de las condiciones mecánicas en el funcionamiento articular5. A estas alteraciones se une la constatación bioquímica e histoquímica del descenso de la tasa de mucopolisacáridos ácidos, que va de la superficie a la profundidad cartilaginosa, demostrado por la pérdida de la metacromasia, exceptuando las zonas pericondrocitarias, en que la metacromasia puede permanecer inalterada o estar aumentada, lo que se ha interpretado como un intento de aumento de la síntesis de mucopolisacáridos, demostrado por el aumento de captación del 35S. El aumento de las mitosis en el cartílago también se comprueban por el estudio con Timidina Tritiada, cuya captación está incrementada en el cartílago artrósico5.
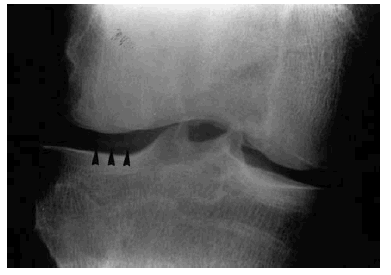
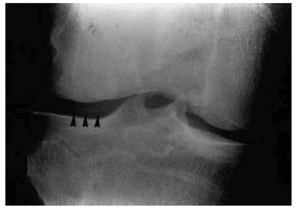
Figura 3. Aspecto radiográfico de una rodilla artrósica con pérdida de la regularidad articular (flechas).
LIGAMENTOS Y MEMBRANA SINOVIAL
Los ligamentos, sobre todo intraarticulares, pueden sufrir una laxitud que hará que la articulación afecta de artrosis tenga una inestabilidad, que facilita se presenten lesiones por la sobrecarga funcional que se ve obligada a soportar, sobre todo, en situaciones de tensión5. La membrana sinovial presenta un cuadro de inflamación crónica, con hiperplasia de su aspecto y aumento del tamaño de las vellosidades, debido a que es irritada por las partículas desprendidas al lesionarse el cartílago. En ocasiones presenta zonas de metaplasia cartilaginosa u ósea, con resultado de la formación de cuerpos libres intraarticulares, aunque éstos también pueden formarse por desprendimiento de fragmentos de la superficie articular o incluso de la fractura de un osteofito5.
El líquido sinovial presenta un volumen normal o discretamente aumentado y tiene características no inflamatorias. Ocasionalmente pueden estar aumentadas la aldolasa, la LDH, las fosfatasas alcalinas, etc., que también lo están en las artropatías inflamatorias. La celularidad es inferior a 2.000 células por μl, con menos de un 25% de polinucleares y predominio de células mononuclares (linfocitos, macrófagos y células sinoviales). La presencia de cristales de ácido úrico orientan hacia la etiología gotosa y los de pirofosfato cálcico a la condrocalcinosis. Tiene alteradas las propiedades viscoelásticas y está reducida la concentración de ácido hialurónico (AH)8.
CÁPSULA ARTICULAR
La cápsula articular sufre una fibrosis con consecutivo engrosamiento, que puede dificultar el retorno venoso que, con el estasis intraóseo a consecuencia del engrosamiento de las trabéculas óseas, es responsable del dolor. El conjunto de lesiones capsulares y sinoviales es uno de los responsables de la disminución de la movilidad de la articulación5.
FACTORES AGRESIVOS
La presencia de uno o varios de los factores considerados agresivos para el cartílago (Tabla 1) inician las alteraciones que van a conducir al deterioro del mismo. El cambio fundamental se inicia con el descenso en la matriz de los mucopolisacáridos ácidos, que lleva a una disminución de la elasticidad y consistencia del cartílago articular. Como consecuencia de ello se inician la fisuración, la esclerosis subcondral y los cambios en la mecánica articular. Subsiguiente a las dos primeras es la ulceración y el progresivo deterioro articular, que llega a la destrucción del mismo, con instauración de cuerpos libres, que van a ser los culpables de la limitación de la movilidad.
Los cambios de la mecánica van a ser los responsables de la irritación sinovial y de la fibrosis cápsulo-sinovial, que, de igual modo, va a limitar la movilidad. También va a provocar una excesiva tracción cápsulo-sinovial que permite desarrollar calcificaciones en las zonas de distensión, dando lugar a los osteofitos en las zonas marginales y de menor presión.
ÉSTASIS VENOSO
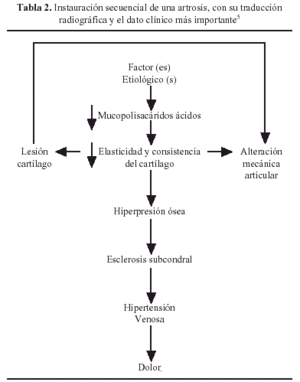
El descenso de la elasticidad y consistencia y la erosión subsiguiente del cartílago hace que el hueso subyacente sufra una hiperpresión que va a dar lugar a una esclerosis subcondral como mecanismo de defensa y autocuración (o en caso contrario dar lugar a los quistes subcondrales por debilidad, isquemia, necrosis y rotura de la pared subcondral). La esclerosis subcondral puede contribuir a la instauración de una hipertensión venosa intraósea, causante del dolor (Tabla 1).
La inflamación sinovial se debe también a la presencia de restos desprendidos del cartílago. La contractura muscular, junto con la fibrosis y retracción capsulares pueden facilitar la subluxación articular que, unida a las alteraciones de funcionamiento mecánico, y los posibles cuerpos libres conducen a la limitación de la movilidad. La fibrosis capsular puede producir estasis venoso, que participa de forma notable en la instauración del dolor (Tabla 2).
Los crujidos habituales, que es un síntoma clínico realmente frecuente, se presentan a consecuencia del rozamiento entre superficies vecinas que han perdido la cubierta cartilaginosa, la crepitación de la membrana sinovial inflamada o el contacto entre los osteofitos5 (Fig. 3).
La hiperpresión ósea puede estar influenciada negativamente por la contracción de los músculos que actúan en o en la vecindad de la articulación. Así durante la deambulación aumenta por 3 la presión del peso del cuerpo en la cadera, y lo hace por 9 en la rodilla7.
Aunque la elasticidad y la absorción de presiones del cartílago es muy favorable en relación a su masa, su grosor es limitado (habitualmente entre 1 y 2 mm). Por eso es importante la descompresión del tejido subcondral y en ello se basaban algunas de las intervenciones que han sido usuales en alguna articulación, como eran las Tenotomías de Voss en la cadera, con sección de las inserciones de los músculos periarticulares contracturados8.
Hay dos funciones muy importantes del cartílago en las superficies articulares. La primera es el contacto de dos superficies lisas y lubricadas, que permiten un deslizamiento sin apenas rozamiento. El coeficiente de fricción es quince veces menor que el que se produce si se frotan dos cubitos de hielo entre sí. La segunda es de protección de la concentración de tensiones sobre el hueso subcondral, ya que el cartílago evita estas concentraciones y las amortigua6.
SITUACIONES QUE FAVORECEN LA ARTROSIS
Según esto, hay dos situaciones en las que se instaura la artrosis: 1. El cartílago y el hueso subcondral son normales, pero las condiciones de trabajo a que se ven sometidos es excesiva. 2. Las condiciones del cartílago y/o del hueso subcondral son deficientes, por lo que se produce un deterioro, aunque el trabajo que se les exija no sea excesivo6,7.
Cuando el trabajo que se le exige a una articulación es excesivo se producen dificultades para el buen funcionamiento de la misma. En este sentido son peligrosos los episodios de compresión-descompresión o los de rozamiento. A esto se debe que algunas articulaciones sean más vulnerables, sobre todo si están sometidas a una sobrecarga de compresión. En ocasiones son pequeños defectos articulares, que hay que valorar muy «in extremis» para considerarlos culpables de la instauración de la artrosis. Es el caso de la cadera por la presencia previa de antecedentes de displasias más o menos importantes, enfermedad de Legg-Calvé-Perthes, luxación previa, epifisiolisis, etc., que cambian de alguna manera el reparto dinámico de las fuerzas que actúan entre los diversos componentes articulares.
También participan en la instauración de cuadros de artrosis algunas patologías que reducen la capacidad de absorción o de deformación del cartílago, tales como la acumulación de polímeros del ácido homogentisínico, típico de la ocronosis, que le endurece. O cuando existe una rigidez de las trabéculas subcondrales, típico de la osteopetrosis. En estas condiciones es fácil que se presenten alteraciones degenerativas generalizadas en etapas precoces, incluso antes de los 40 años, como se puede demostrar experimentalmente si se aumenta la rigidez del hueso subcondral o se le somete a impactos repetidos6.
Aunque en situación de reposo las superficies articulares vecinas no suelen ser congruentes, al producirse el apoyo, se produce una deformación que favorece una mayoritaria e íntima relación entre las capas articulares y una notable disminución de la presión por unidad de medida, que suele hacerse por cm2. Esta modulación de la forma del cartílago para contactar al máximo con su vecino, facilita una lubricación rezumante hidrostática autopresurizada, que es precisa para hacer posible el movimiento. Si se aumenta la carga es preciso añadir a la deformación del cartílago la deformación del hueso subyacente, con objeto de minimizar el deterioro cartilaginoso a consecuencia de la presión concentrada en menor número de puntos.
El hueso subcondral, 10 veces más duro que el cartílago, absorbe los impactos que actúan sobre aquél. Tiene una mayor flexibilidad que el tejido cortical. Cuando la carga sobrepasa ciertos límites, produce la ruptura de las trabéculas y la presentación de microfracturas, cuya reparación produce un remodelado de mayor dureza que influye negativamente en el funcionamiento homogéneo de la articulación, al no poder deformarse y al concentrarse la sobrecarga sobre un menor número de puntos del cartílago articular7.
EQUILIBRIO DE LA FORMACIÓN Y REABSORCIÓN ÓSEA
En los pacientes afectos de artrosis la densidad mineral ósea está incrementada, estando aumentadas la formación y la reabsorción óseas, lo que da como resultado un descenso del endurecimiento del hueso por unidad de masa ósea. El incremento en el número de trabéculas subcondrales, el acercamiento de las trabéculas y el aumento del espesor de la placa subcondral aumentan el endurecimiento del hueso. No está definido si los cambios del cartílago son previos o consecutivos a los del hueso subcondral7.
La degeneración articular puede verse influenciada si el funcionamiento de los músculos periarticulares está afectado sensorial y motoramente, así como con respecto a los impulsos propioceptivos. Ésta puede ser debida a debilidad muscular por desuso o a inhibición refleja de la contracción muscular secundaria a patología intraarticular7. La pérdida del cartílago es la regla en la artrosis. La concentración de colagenasa en el cartílago se incrementa a medida que aumenta la severidad de la artrosis, probablemente por la destrucción de la matriz del colágeno. La pérdida del cartílago está asociada a la carencia de agrecano, por lo que se pierde elasticidad. Los datos bioquímicos incluyen un defecto en la red de colágeno del cartílago, probablemente por la disrupción del «pegamento» que une las fibras colágenas vecinas entre sí en la matriz, y esto es irreversible7.
En el cartílago articular adulto normal las células no se dividen, sin embargo en el cartílago artrósico sí lo hacen, y muy activas metabólicamente, produciendo grandes cantidades de colágeno, proteoglicano e hialuronano. Pero estos productos no se agregan bien ni se estabilizan adecuadamente en la matriz extracelular, con lo que las propiedades mecánicas de la matriz son inferiores a la norma lidad7. Cuando se trata de una artrosis consecutiva a una condrodisplasia familiar secundaria a una mutación en el ADNc, que codifica para el colágeno tipo II, se justifica el factor que un defecto generalizado produce en la matriz del cartílago articular7.
Para comprender las alteraciones que se producen en el cartílago articular hay que recordar su composición normal. Así, hay dos tipos fundamentales de macromoléculas: a) los proteoglicanos (PGl), que son los responsables de la capacidad para resistir las presiones; y b) el colágeno (C) responsable de la resistencia a la tracción y al cizallamiento. Un tercer componente es la familia de las metaloproteinasas de la matriz (MPM), que incluye la estromelisina, la colagenasa y la gelaginasa, que son capaces de degradar todos los componentes de la matriz extracelular a pH neutro. Son secretadas por los condrocitos como proenzimas latentes que deben ser activadas por separación proteolítica de su secuencia N-terminal6.
La artrosis es un complejo proceso de degradación y reparación del cartílago, sinovial, hueso, etc., con componentes secundarios de inflamación. Su proceso etiopatogénico es discutido e incluye dos vertientes. Por una parte es fundamental un cartílago defectuoso que conduce a la artrosis. Por eso la matriz cartilaginosa falla bajo una carga articular normal. Por otra parte, también se produce artrosis si se detecta un efecto de sobrecarga sobre un cartílago articular normal. Así que puede llegarse a la misma consecuencia por dos caminos: el primero por daño sobre la matriz, el segundo por fuerzas que actúan sobre los condrocitos. En el curso evolutivo estos condrocitos reaccionan degradando los enzimas y desarrollando una respuesta reparadora inadecuada. Recientes estudios implican la degradación enzimática del cartílago como un factor fundamental en la progresión de la enfermedad. También se han valorado como causa del deterioro articular los traumas repetidos de pequeña intensidad o uno de gran intensidad. En este último caso si la fuerza se concentra en un punto puede dar lugar a una lesión localizada del cartílago o a una estimulación de remodelación del hueso y gradual desarrollo de un contorno alterado9.
Varias etiologías pueden conducir a una distribución anormal de transmisión de fuerzas, sin antecedente traumático, como son el desarrollo de fallos en el cartílago de crecimiento, escasa profundidad o irregularidad en la formación del acetábulo, cambio de posición del núcleo cefálico con relación al cuello femoral, genu varo o valgo, dismetría de extremidades, etc. La inestabilidad es un motivo de que se realice una transmisión de cargas anormal, lo que produce un desorden en la estructura del colágeno que conduce a la artrosis9.
PAPEL DE LA INTERLEUCINA
Son considerados como factores estimuladores de la síntesis de tejido conectivo los IGF-I y el TGF-β, y como estimuladores de la degradación de la matriz cartilaginosa las citoquinas, como la interleuquina (IL-1) y el factor de necrosis tumoral (TNF-α). Estas dos últimas pueden incrementar la síntesis de proteasas, incluyendo metaloproteasas y activadores del plasminógeno, siendo responsables probablemente, del incremento de síntesis en la sinovial artrósica, correlacionada con la severidad de la inflamación y coincidente con la positividad de los hallazgos de interleuquina 1 en el líquido sinovial9.
El recambio de cartílago normal se realiza por una degradación coordinada por la interleucina (IL-1), que es una citocina producida por células mononucleares (algunas de ellas tapizan la sinovial) sintetizada por los condrocitos. La IL-1 estimula la síntesis y la secreción de MPM latentes y del activador tisular del plasminógeno (PA). El plasminógeno puede ser elaborado por los condrocitos o proceder del líquido sinovial y puede participar, al igual que la estromelisina, en la activación de las MPM latentes. También, la IL-1, añadido a su efecto catabólico, puede inhibir la síntesis de PGl en los condrocitos, dificultando la reparación de la matriz. La interleucina-1 es considerada como directora de la progresión de la rotura del cartílago en la artrosis, que ha sido observado en experimentos de terapia génica7.
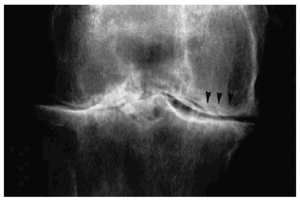
Factores de crecimiento, como el factor de crecimiento insulínico (IGF-1), factor beta transformador de crecimiento (TGF-β), factor de crecimiento de fibroblasto básico (FGF) intentan la reparación que podría curar o frenar la evolución de la artrosis. Su papel sería incrementar la síntesis de proteoglicanos o disminuir su degradación7. No está suficientemente claro si la presencia de cristales de apatita es el resultado o la causa de la lesión artrósica del cartílago. Pero está demostrado que los cristales de pirofosfato cálcico dihidratado (CPPD) o de fosfato cálcico básico (BCP) o de hidroxiapatita cálcica (HC) suelen estar presentes en el líquido sinovial de la articulación artrósica (fig. 4).
Figura 4. Imagen radiológica de la calcificación meniscal por condrocalcinosis (flechas).
Se produce un cierto equilibrio si actúan dos elementos, el inhibidor tisular de las metaloproteinasas (TIMP) y el inhibidor del activador del plasminógeno 1 (PAI-1) sintetizados por los condrocitos y que frenan, respectivamente, la actividad degradativa de las MPM y del PA. Si el TIMP y el PAI-1 son insuficientes, la estromelisina y la plasmina actuarán sobre los sustratos de la matriz. La estromelisina puede degradar el núcleo de los PGl y activar la colagenasa latente. La conversión de la estromelisina latente en una proteinasa activa y muy destructiva por la acción de la plasmina va a dar un segundo mecanismo para la degradación de la matriz6.
En los casos de artrosis pueden favorecer la reparación de la matriz algunos mediadores polipeptídicos, como el factor de crecimiento de la insulina 1 (IGF-1) y el factor βtransformador de crecimiento (TGF-β), que favorecen la síntesis de PGl. Estos factores modulan el metabolismo de los condrocitos, regulando negativamente los receptores de los condrocitos para IL-1, lo que reduce la degradación de PGl6.
EFECTO DEL ESTÍMULO MECÁNICO
El estímulo mecánico también interviene en la modulación del metabolismo de los condrocitos del cartílago normal, inhibiendo la síntesis de proteínas y de proteoglicanos las cargas estáticas, y estimulando la síntesis de matriz las cargas de breve duración o alternantes. También hay que remarcar el estímulo positivo de la IL-1 y el negativo de las MPM, plasmina y catepsinas6. En los inicios de la progresión de la artrosis, se producen cambios en el cartílago, con remodelación ósea, que da como resultado una pérdida de la función de absorción de energía sobre el cartílago (Fig. 4). Debido al incremento de la transmisión de fuerzas pueden verse osteofitos en un intento de redistribuir las presiones en una superficie más amplia10.
Aunque se presentan connotaciones inflamatorias, sobre todo en el proceso progresivo de la enfermedad, no cabe duda que la artrosis tiene una mayor influencia en su presentación por trastornos mecánicos que inflamatorios11. La explicación patogénica de la artrosis incluye dos características de la evolución humana. De una parte el cambio de postura a la bipedestación, y de otra la prolongación del período de vida post-reproductiva, ya que en este último supuesto la reparación del cartílago se hace menos eficaz11. Los datos experimentales sugieren que las pérdidas de proteoglicano de la matriz puede ser reversible, sin embargo la lesión del colágeno de la matriz es más difícil de reparar11.
MARCADORES
Existen varios marcadores moleculares de interés en la artritis reumatoide y en la artrosis. Son fundamentalmente un producto catabólico de la degradación del agrecano, la región de fijación de hialuronano. La proteína oligométrica del cartílago (COMP) parece ser útil como marcador de la artrosis, ya que aumenta con la progresión de la artrosis, manteniéndose invariable en una artrosis no progresiva. La sialoproteína es una proteína específica del hueso que está aumentada si la artrosis es debida a aquélla.
La artrosis es asociada con el incremento de las funciones reparadoras y destructoras del cartílago. Solamente cuando la capacidad reparadora es menor que la degradadora y se produce descompensación en este sentido, se obtiene la artrosis, que es progresiva. Se genera un incremento en la síntesis y en la destrucción del colágeno tipo II. El colágeno tipo IX es reducido, aunque su síntesis puede estar aumentada o reducida12.
El colágeno tipo II y los proteoglicanos pueden identificarse por anticuerpos que identifican estos epítopos de las macromoléculas de la matriz, que no son identificadores en el cartílago normal11. Las fibras colágenas se fragmentan a consecuencia de la desconexión de las uniones entre las mismas, influenciado también por la penetración de agua en su entramado13.
Los condrocitos del cartílago artrósico producen óxido nítrico, que no lo hacen normalmente. Este óxido nítrico, producido en respuesta a los estímulos por citocinas puede actuar inhibiendo la síntesis del colágeno y favoreciendo la secreción de factores proinflamatorios como las metaloproteasas. Una aportación importante es la constatación de que el óxido nítrico induce fenómenos de apoptosis en los condrocitos, que cronifica el proceso14.
Uno de los síntomas más frecuentes de la artrosis es el dolor debido a la inflamación, contra el que es preciso luchar utilizando fármacos que actúan inhibiendo la síntesis de las prostaglandinas, formadas a partir del ácido araquidónico con la influencia del enzima ciclooxenasa, que tiene gran importancia a la hora de plantear el tratamiento más idóneo15.