La detección y descolonización del Staphylococcus aureus previo a la cirugía, se postula como la opción para disminuir el riesgo de infección en artroplastias. El objetivo de este estudio fue evaluar la efectividad de un programa de cribado de S. aureus en la artroplastia total de rodilla (ATR) y en la artroplastia total de cadera (ATC), la incidencia de infección respecto a una cohorte histórica y su viabilidad económica.
Material y métodosEstudio pre-postintervención en pacientes intervenidos de ATR y ATC en al año 2021. Se realizó protocolo de detección de colonización nasal por S. aureus y erradicación si procedía, con mupirocina intranasal, cultivo postratamiento con el resultado de 3 semanas entre cultivo postratamiento y cirugía.
Se evalúan medidas de eficacia, se analizan costes y se comprara la incidencia de infección respecto a una serie histórica de pacientes intervenidos entre enero y diciembre de 2019, realizando análisis estadístico descriptivo y comparativo.
ResultadosLos grupos fueron comparables estadísticamente. Se realizó el cultivo en el 89%, siendo 19 (13%) pacientes positivos. Se confirmó el tratamiento en 18, cultivo control en 14, todos descolonizados; ninguno sufrió infección. Un paciente con cultivo negativo sufrió infección por S. epidermidis. En cohorte histórica: 3 sufrieron infección profunda por S. epidermidis, E. cloacae y S. aureus. El coste del programa fue de 1.661,85€.
ConclusiónEl programa de cribado detectó el 89% de los pacientes. La prevalencia de infección en el grupo intervención era menor que en la cohorte, siendo S.epidermidis el microorganismo causante, diferente a S. aureus descrito en la literatura y en la cohorte. Consideramos que este programa es económicamente viable, siendo sus costes reducidos y asumibles.
Detection and decolonization of Staphylococcus aureus prior to surgery is postulated as an option to reduce the risk of infection in arthroplasties. The aim of this study was to evaluate the effectiveness of a screening program for S. aureus in total knee arthroplasty (TKA) and total hip arthroplasty (THA), the incidence of infection with respect to a historical cohort, and its economic viability.
Material and methodsPre-post intervention study in patients undergoing primary knee and hip prostheses in 2021, a protocol was carried out to detect nasal colonization by S. aureus and eradication if appropriate, with intranasal mupirocin, post-treatment culture with results three weeks between post-treatment culture and surgery. Efficacy measures are evaluated, costs are analyzed and the incidence of infection is compared with respect to a historical series of patients operated on between January and December 2019, performing a descriptive and comparative statistical analysis.
ResultsThe groups were statistically comparable. Culture was performed in 89%, with 19 (13%) positive patients. Treatment was confirmed in 18, control culture in 14, all decolonized; none suffered infection. One culture-negative patient suffered from Staphylococcus epidermidis infection. In historical cohort: 3 suffered deep infection by S. epidermidis, Enterobacter cloacae, S. aureus. The cost of the program is €1661.85.
ConclusionThe screening program detected 89% of the patients. The prevalence of infection in the intervention group was lower than in the cohort, with S. epidermidis being the main microorganism, different from S. aureus described in the literature and in the cohort. We believe that this program is economically viable, as its costs are low and affordable.
Una de las complicaciones más temidas respecto a las artroplastias totales de cadera (ATC) y rodilla (ATR) es la infección protésica, teniendo una prevalencia entre el 1-3% en la artroplastia total de rodilla y un 0,7-2,5% en la de cadera1.
La infección protésica aumenta la estancia hospitalaria, ocasiona múltiples intervenciones, retrasa la recuperación y aumenta el riesgo de mortalidad2. Además, los costes sanitarios directos tras una cirugía de revisión de ATC o ATR se elevan en gran medida, sobre todo cuando se trata de cirugía en 2 tiempos3,4.
Existen diversos factores de riesgo asociados a la infección protésica2; uno de ellos es la colonización por Staphylococcus aureus nasal5 o cutáneo6,7; si bien no está claro si se debe solamente a esta colonización o a la combinación con otros factores6,8, puesto que las infecciones por dicho microorganismo también pueden ocurrir en pacientes no portadores6.
El principal agente etiológico causante de la infección del sitio quirúrgico y protésica es la especie Staphylococcus en más del 60% de los casos8. Dentro de esta, predominan en algunas series los estafilococos coagulasa negativos (SCN) como S. epidermidis y S. haemolyticus, mientras que, en otras como la de Sousa et al., el germen predominante es S. aureus en el 41,2% de los casos; siendo el 17,6% resistente a meticilina (SARM) y el 23,5% sensible (SASM)6. El SARM es más virulento y de tratamiento más complejo9.
S. aureus es un microorganismo comensal que se encuentra en la piel y mucosas del 30% de los pacientes sometidos a artroplastia total6–8, el 1% de los cuales es SARM. Algunos estudios longitudinales demuestran que hasta un 20% de la población son portadores permanentes de S. aureus, y un 30% intermitentes10.
Algunos protocolos, estudios e instituciones recomiendan la descolonización nasal de S. aureus previo a la cirugía con el objetivo de disminuir el riesgo de infección protésica11, aunque no existe un consenso generalizado, ya que suponen implicaciones logísticas y económicas a considerar12.
Respecto al protocolo de descolonización nasal, estudios retrospectivos sugieren que tanto el tratamiento preoperatorio universal con antiséptico tópico, como el examen, la detección y el tratamiento de portadores pueden ser beneficiosos para reducir las infecciones del sitio quirúrgico en general, y específicamente por S. aureus y SARM después de la cirugía ortopédica, sin consenso sobre cuál de los 2 métodos es más eficiente y costo-efectivo9. Existen diferentes alternativas en cuanto al cribado: por un lado, el cultivo estándar en diversas zonas corporales o exclusivamente nasal, con una sensibilidad variable, o las técnicas de detección mediante la reacción en cadena de la polimerasa molecular (PCR) con resultados más rápidos, pero más costosos sin demostrarse una clara ventaja13,14.
El tratamiento usado para la descolonización es la mupirocina intranasal combinada o no con el gluconato de clorhexidina tópico usado en la ducha15. A pesar de que los protocolos de detección y descolonización han demostrado ser altamente exitosos, hay estudios que han demostrado una colonización persistente hasta en un 20% de los casos7,16–18; así, es importante confirmar la descolonización al menos 3 semanas antes de la cirugía11.
Los objetivos del presente estudio son evaluar la efectividad de un programa de cribado y descolonización de S. aureus en las artroplastias totales de cadera y las artroplastias totales de rodilla, en cuanto a su capacidad de detección y descolonización, también la valoración de la incidencia de infección respecto a una cohorte histórica; y finalmente su viabilidad económica.
Material y métodosSe realiza un estudio de intervención comparativo con una cohorte histórica en los pacientes intervenidos de ATR y ATC en nuestro centro en 2019 y 2021. Se excluye el año 2020 por las disfunciones graves originadas en el centro hospitalario, servicio y circuitos por la pandemia COVID-19.
El estudio fue aprobado por el Comité de Ética de Investigación y Medicamentos (CEIM) de nuestro centro, con el código CEIC-2606.
Se cumple la «Declaración de la Iniciativa Strengthening the Reporting of Observational studies in Epidemiology (STROBE): directrices para la comunicación de estudios observacionales»19.
Los datos anonimizados y variables se recogen de forma prospectiva de una base de datos creada en el marco de un programa de recuperación mejorada «Enhanced Recovery After Surgery (ERAS)»20 implementado desde 2015, siendo una de las bases de dicho programa la recogida de datos para análisis y mejora continua. Las variables recogidas en el marco del programa son: demográficas, de estancia media, transfusiones, dolor y rescates analgésicos, cribado de S. aureus y complicaciones. El seguimiento se realiza mediante una revisión a 90 días en el marco del programa de vigilancia de la infección de Catalunya (VINCAT), que comporta el seguimiento mínimo de los 100 primeros procedimientos anuales; sin embargo, en nuestro centro se amplía la vigilancia activa de 90 días poscirugía a toda la cirugía de artroplastia.
Los pacientes elegibles fueron todos los pacientes intervenidos de ATR y ATC primaria en los años 2019 y 2021 por cualquier diagnóstico excepto fractura de fémur; también se excluyeron cirugías de revisión séptica o aséptica. Se estableció como grupo de intervención el de los pacientes intervenidos entre el 1 de enero y el 31 de diciembre de 2021, en los que se realizó el protocolo de cribado y descolonización para S. aureus; mientras que el grupo control fue el de los intervenidos entre el 1 y el 31 de diciembre de 2019, momento en el que no estaba implementado dicho protocolo.
El protocolo de cribado y descolonización consiste en lo siguiente: se incluye la petición de frotis nasal de S. aureus de forma rutinaria en el estudio preoperatorio de artroplastia que se solicita a todos los pacientes en la consulta de cirugía ortopédica y traumatología (la muestra se extrae en el centro de atención primaria mediante un frotis nasal en el mismo momento que la analítica preoperatoria, entre 4 a 6 semanas previas a la intervención). La revisión del resultado se realiza en la consulta preoperatoria de anestesiología: si el resultado es positivo para S. aureus (SASM o SARM), el anestesiólogo pauta el tratamiento de descolonización con mupirocina tópica cada 8h durante 5 días a iniciar 10 días antes de la intervención, a realizar en domicilio; de este modo, se cumple el plazo descrito en la literatura de realizar la cirugía máximo 3 semanas después de la descolonización11 y se da la oportunidad de entrar en el plazo si existe alguna reprogramación quirúrgica. El anestesiólogo solicita un frotis de control posterior al tratamiento de descolonización y previo a la cirugía, que también se realiza por atención primaria. La Unidad Territorial de Infección Nosocomial (UTIN) y política antibiótica es la encargada de revisar el resultado del frotis de control posterior al tratamiento. Si el cultivo de control posterior al tratamiento sigue siendo positivo por SARM el día de la intervención, la UFIN avisará al responsable quirúrgico y de anestesiología para tomar medidas desde el inicio del proceso: se requerirá realizar una profilaxis antibiótica con vancomicina 1g endovenosa en dosis única preoperatoria entre 120 y 60min antes de la incisión, medidas de contacto durante todo el proceso quirúrgico y un segundo tratamiento de 5-10 días para la descolonización con mupirocina o ácido fusídico.
El resto de las medidas de prevención de la infección fueron las mismas para las 2 cohortes. Entre las más destacadas se recomienda un baño con jabón neutro domiciliario el día previo a la cirugía, y se realiza una limpieza con jabón de clorhexidina de la zona a intervenir por parte del personal hospitalario al ingreso en el área quirúrgica. La profilaxis antibiótica por protocolo se realiza con cefazolina 2g endovenosa en dosis única preoperatoria, excepto en pacientes alérgicos a la penicilina en que se realiza con teicoplanina 600mg. El protocolo de asepsia quirúrgica, mantenimiento de la normotermia y normoglicemia también es el mismo para los 2 grupos.
Las variables de estudio recogidas para ambos grupos fueron: articulación intervenida, edad, lateralidad, sexo, ASA, infección del sitio quirúrgico a los 90 días de la cirugía, tipo de infección y germen causante.
En el grupo de intervención, además, se evaluó la realización del cultivo de detección para S. aureus, su resultado, y en caso de ser positivo, qué tipo (SARM o SASM); realización del tratamiento de descolonización, del cultivo posdescolonización y resultado de este; período de 3 semanas entre cultivo posdescolonización y cirugía.
Los datos se obtuvieron de tres fuentes diferentes. En primer lugar, la base de datos anonimizada del programa ERAS de donde se obtienen las variables demográficas y la realización de cultivo de detección de S. aureus y su resultado. En segundo lugar, la historia clínica electrónica de donde se obtienen la realización del tratamiento de descolonización, el resultado del cultivo posdescolonización y la fecha de realización. Y, por último, de la base de datos del programa VINCAT donde se recogen la presencia de infección a 90 días, el tipo de infección y el germen causante.
Las variables se describen como mediana (rango intercuartílico) o como porcentaje. Para la comparación entre los grupos, se utilizó la prueba de Mann-Whitney (no distribución normal según prueba Kolmogorov-Smirnov) para variables continuas y la prueba de Chi-cuadrado para las variables categóricas. Nivel de significación con p<0,05. Los cálculos se realizaron con el software SPSS®, versión 23.0 (SPSS, Chicago, Ill, EE. UU.).
En cuanto al análisis económico se asumen los siguientes costes directos: el precio de la realización del frotis nasal para detección de S. aureus es de 4,66€ según el precio tarifado del Instituto Catalán de la Salud (ICS), incluyendo escobillón, técnica de laboratorio y recursos humanos; el precio de la mupirocina 20mg/g en pomada 30g es de 7,51€.
Los posibles costes indirectos son despreciables ya que al realizar el análisis en el mismo centro de salud del paciente y en el mismo momento que la analítica peroperatoria no supone desplazamientos ni consumo de tiempo extra.
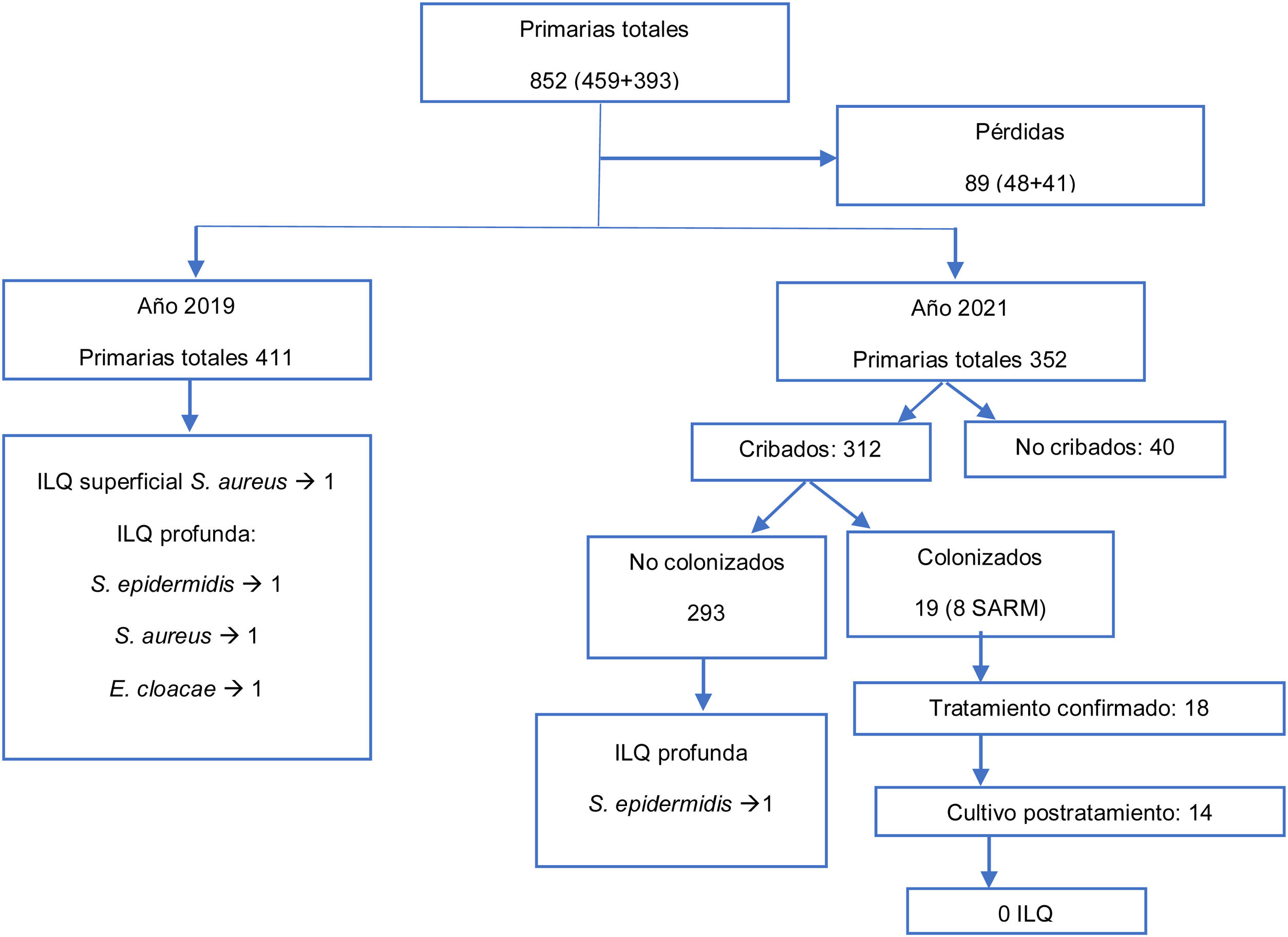
ResultadosLa población inicial elegible fue de 852 pacientes intervenidos de ATR o ATC en 2019 y 2021 (459 cohorte histórica de 2019 y 393 grupo intervención de 2021), se tuvieron unas pérdidas de 89 pacientes (48 y 41 respectivamente), debidas a problemas de identificación y registro en la base de datos. Por tanto, la muestra completa y analizada de 763 pacientes: 411 en la cohorte histórica y 352 en la cohorte de intervención (fig. 1).
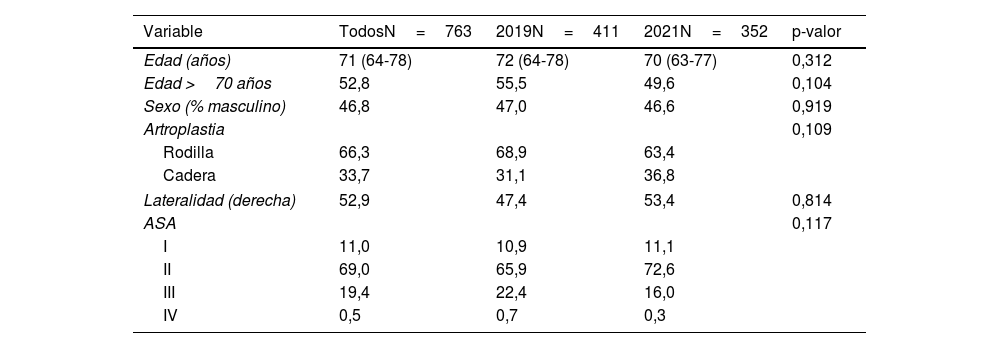
La muestra obtenida, presentó una mediana de edad de 71 años (64-78), con un 53,2% de mujeres y una lateralidad derecha en el 52,9% de los casos. El riesgo quirúrgico predominante fue ASA II. La intervención quirúrgica fue ATR en el 66,3% (68,9% en 2019 y 63,4% en 2021) o ATC en el 33,7% (31,1 y 36,8%, respectivamente). No se encontraron diferencias estadísticamente significativas en las características de los 2 grupos (tabla 1).
Características demográficas de los pacientes con sustitución protésica articular en los años 2019 y 2021 (n=763)
| Variable | TodosN=763 | 2019N=411 | 2021N=352 | p-valor |
|---|---|---|---|---|
| Edad (años) | 71 (64-78) | 72 (64-78) | 70 (63-77) | 0,312 |
| Edad >70 años | 52,8 | 55,5 | 49,6 | 0,104 |
| Sexo (% masculino) | 46,8 | 47,0 | 46,6 | 0,919 |
| Artroplastia | 0,109 | |||
| Rodilla | 66,3 | 68,9 | 63,4 | |
| Cadera | 33,7 | 31,1 | 36,8 | |
| Lateralidad (derecha) | 52,9 | 47,4 | 53,4 | 0,814 |
| ASA | 0,117 | |||
| I | 11,0 | 10,9 | 11,1 | |
| II | 69,0 | 65,9 | 72,6 | |
| III | 19,4 | 22,4 | 16,0 | |
| IV | 0,5 | 0,7 | 0,3 | |
ASA: clasificación según guías de la American Society of Anesthesiologists; p-valor: con el test de la Chi-cuadrado o el test de Mann-Whitney.
Valores expresados como porcentajes o mediana (rango intercuartil).
En pacientes alérgicos a penicilina se utilizó por protocolo teicoplanina, un glucopéptido, lo cual podría tener repercusión en la prevalencia de infección por S. aureus. El porcentaje de pacientes en que se administró teicoplanina en el grupo control fue del 7,79%, mientras que en el grupo intervención fue del 7,1%, sin diferencias significativas entre los 2 grupos (p=0,1573).
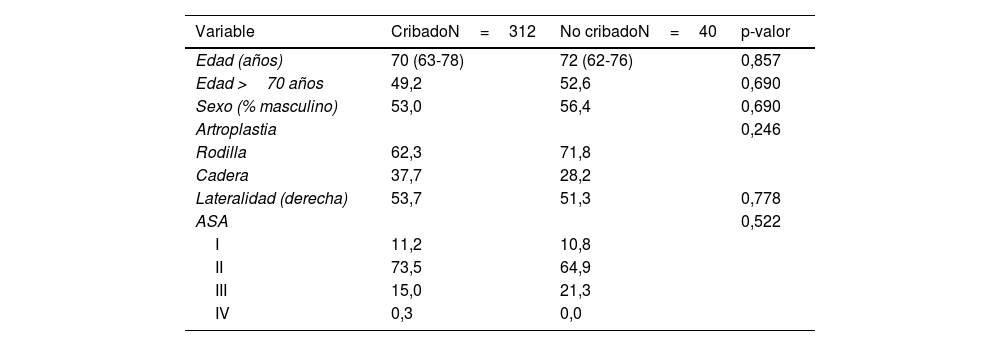
En el grupo de intervención: el cribado se realizó en el 89% de los casos, siendo positivo para S. aureus en 19 (8 SARM y 11 SASM). No se observaron diferencias en las características demográficas del grupo de cribados respecto al de no cribados (tabla 2).
Características demográficas de pacientes con sustitución protésica del año 2021. Según realización de cribado (n=352)
| Variable | CribadoN=312 | No cribadoN=40 | p-valor |
|---|---|---|---|
| Edad (años) | 70 (63-78) | 72 (62-76) | 0,857 |
| Edad >70 años | 49,2 | 52,6 | 0,690 |
| Sexo (% masculino) | 53,0 | 56,4 | 0,690 |
| Artroplastia | 0,246 | ||
| Rodilla | 62,3 | 71,8 | |
| Cadera | 37,7 | 28,2 | |
| Lateralidad (derecha) | 53,7 | 51,3 | 0,778 |
| ASA | 0,522 | ||
| I | 11,2 | 10,8 | |
| II | 73,5 | 64,9 | |
| III | 15,0 | 21,3 | |
| IV | 0,3 | 0,0 |
ASA: clasificación según guías de la American Society of Anesthesiologists; p-valor: con el test de la Chi-cuadrado o el test de Mann-Whitney.
Valores expresados como porcentajes o mediana (rango intercuartil).
De los pacientes con cultivo positivo, se confirmó el tratamiento en 18, realizándose el cultivo de control en el intervalo de 3 semanas antes de la cirugía en 14; todos ellos resultaron descolonizados, por lo que no requirieron medidas adicionales en el proceso quirúrgico. Ningún paciente con cultivo de detección positivo sufrió infección de sitio quirúrgico.
De los 5 pacientes restantes, en un caso no se pudo confirmar si el paciente había realizado el tratamiento con mupirocina de forma correcta; este caso era de colonización por SASM, por lo que se realizó profilaxis con cefazolina de forma habitual. En los 4 casos en que se confirmó el tratamiento, aunque no el cultivo post tratamiento, 3 resultaron colonizaciones por SASM en las que se realizó la profilaxis habitual, y otro, colonizado por SARM, fue tratado preoperatoriamente con vancomicina y aislado por contacto en la planta de hospitalización hasta obtener un frotis de control que fue negativo.
Un paciente con cultivo de detección negativo tuvo una infección de localización quirúrgica profunda por S. epidermidis tratado con desbridamiento, antibióticos y retención de implante con buen resultado.
En el grupo de cohorte histórica, 3 pacientes tuvieron una infección de localización quirúrgica profunda: uno por S. epidermidis, que requirió desbridamiento con retención del implante y antibioterapia; uno por E. cloacae, que se trató mediante recambio en 2 tiempos con recidiva de la infección y finalmente artrodesis; y, por último, uno por S. aureus SASM, que se resolvió con revisión en 2 tiempos. Otro caso de la cohorte histórica sufrió una dehiscencia de herida resuelta con desbridamiento, con cultivo positivo para S. aureus SASM, por lo que se catalogó como infección superficial. Estos hallazgos resultaron no tener significación estadística en una prueba de Chi-cuadrado.
Por lo que respecta al análisis económico, considerando que el cribado se ha realizado en 312 pacientes, que se han tratado 19 pacientes positivos, de los que se ha confirmado el tratamiento con mupirocina en 18, y se ha realizado el test posterior al tratamiento de descolonización en 14 pacientes antes de la cirugía, el coste del programa supone 1661,85€ (312×4,66€+19×7,51€+14×4,66€).
Por otro lado, el coste/efectividad de detectar un portador de S. aureus es de 76,5€ (312×4,66€/19).
Realizando una inferencia por intención de tratar, incluyendo no cribados y pérdidas, el coste del cribado en el grupo intervención habría sido de 1.831,38€ (393×4,66€) a lo que posteriormente se debería añadir el coste del tratamiento y cultivo de control.
DiscusiónEl programa de cribado y descolonización de S. aureus consiguió cribar el 89% de los pacientes. Se detectaron un 13% de pacientes colonizados por S. aureus, confirmando la descolonización en la mayoría. Ningún caso entre el grupo de pacientes cribados sufrió infección quirúrgica por S. aureus u otro germen. Comparando con una cohorte histórica las infecciones protésicas por cualquier germen se redujeron de 3 a una.
El presente estudio presenta limitaciones. La primera se refiere al diseño, ya que, en los estudios de cohortes históricas, los errores debidos a factores de confusión y a sesgos, como, por ejemplo, que la incidencia de infecciones pueda variar en determinados años, son más comunes que en estudios prospectivos. Las pérdidas de seguimiento fueron del 10,4%, sin llegar al límite del 20% definido en la literatura como alta perdida; además, las causas de pérdidas de seguimiento fueron iguales en los dos grupos21. El seguimiento realizado es a 90 días que, si bien es utilizado en determinadas publicaciones22,23 para valorar infección, es un criterio también usado para determinar los reingresos, y podría ser adecuado ampliar el seguimiento a uno o 2 años en una revisión posterior. Por último, se comparó la cohorte de 2021 con la de 2019 por el gran impacto de la pandemia por SARS-CoV-19 en el sistema de salud en 2020, haciendo imposible ese año la implementación de protocolos de seguimiento o recogida de datos respecto a la colonización por S. aureus y otros factores.
Los programas de cribado y descolonización de S. aureus están recomendados en diversos protocolos, pero habitualmente de forma opcional24–27. Las razones son la falta de evidencia científica de nivel elevado al respecto y las dificultades logísticas de implementación.
Nuestro centro está situado en una provincia y área de salud mayoritariamente rural, por lo que tiene el reto de cubrir una zona sanitaria extensa, pero con baja densidad de población, prestando servicio a 5 comarcas con poblaciones alejadas del centro hospitalario hasta en unos 65km. Así pues, con un protocolo basado en la obtención de muestras en múltiples centros de salud de atención primaria se consiguió cribar el 89% de los pacientes, porcentaje que se encuentra entre los valores reportados en otros estudios, donde consiguen cribar el 796 o hasta el 91,8%28.
La prevalencia de portadores de S. aureus en el grupo de intervención fue del 13%, inferior al 30% de otras series7,8 y al 20-30% de la población general10. En cuanto a la resistencia a meticilina se reportan 8 SARM siendo el 42,1% y 11 SASM el 57,9%, una tasa de resistencia diferente a series como la de Sousa et al.6, que reportan 96,5% SASM y 3,5% SARM.
Se trató a los pacientes colonizados con mupirocina nasal según la pauta indicada. Este es un tratamiento con mínimos efectos secundarios y de larga experiencia de uso, además al asociarlo a un cribado previo, se realiza un tratamiento selectivo disminuyendo los efectos secundarios y posibles resistencias antibióticas28. Existen otras estrategias de descolonización como el tratamiento de rutina con mupirocina a todos los pacientes7,22 que podría tener repercusiones negativas en cuanto a costes y resistencias antibióticas o la descolonización rutinaria con antisépticos farmacéuticos que pueden tener desventajas como la dificultad de acceso y preparación en todos los centros29.
Posterior al tratamiento, es importante confirmar la descolonización con cultivo de control en las 3 semanas pre-cirugía11, en nuestro estudio se consiguió en el 74% (14/19); no obteniéndose cultivo de control en el resto. Este dato es inferior al reportado en otros estudios como el de Kalmeijer et al.7 donde se reporta un 83,5% de confirmación de descolonización.
La prevalencia de infección protésica en el grupo de intervención fue del 0,28 y del 0,72% en la cohorte histórica; inferior a los resultados reportados por la literatura1,6. Además, S. epidermidis fue el microorganismo causante de la única infección en el grupo de intervención, diferente al S. aureus descrito en la literatura hasta en el 60% de las ocasiones6,8 y en el 33% en nuestra cohorte histórica. La baja tasa de infección protésica reportada y mayoritariamente de infección por S. aureus, incluso en la cohorte histórica, hace que el número pacientes necesario para encontrar diferencias significativas en cuanto a reducción de infección tras la aplicación del programa de descolonización deba ser muy elevado.
Por tanto, a pesar de no tener significación estadística en una prueba de Chi-cuadrado, la erradicación del estado de portador de S. aureus mediante el tratamiento condujo a una menor incidencia de infección de localización de sitio quirúrgico tanto por S. aureus como por otros gérmenes, respecto a una cohorte histórica de características basales estadísticamente comparables. Según la literatura, la implementación de programas de descolonización de S. aureus puede disminuir las infecciones protésicas por todo tipo de gérmenes11,23.
Con las variables empleadas, no se encuentran los factores que pudieran identificar a los posibles portadores, por lo tanto, parece indicada una detección generalizada de todos los pacientes candidatos a la realización de cirugía protésica.
Cabe reflexionar si se podrían recomendar de forma generalizada estos programas o sería necesario un estudio sobre la incidencia de infección por S. aureus en cada centro de manera individual, antes de la aplicación de los protocolos de descolonización; en aras de identificar tasas de infección que justifiquen los posibles beneficios que se obtendrían de su aplicación. En el caso de centros con baja tasa de infección protésica en general y por S. aureus, puede discutirse si el esfuerzo multidisciplinar y la dificultad de aplicación de este tipo de protocolos justifica su aplicación. De todas formas, los autores consideran que un protocolo bien establecido e integrado en la vía clínica habitual del paciente, como el que se presenta, no implica costes logísticos y económicos elevados y sí beneficios.
Existe discusión respecto a las implicaciones económicas de este tipo de programas8,22,23,29,30. Los costes directos son fácilmente imputables, aunque hay que tener en cuenta los costes indirectos que podrían existir en forma de: el tiempo dedicado por los facultativos y el equipo multidisciplinar al diseño e implementación del protocolo, el tiempo dedicado por anestesia a la revisión de los pacientes e identificación de los positivos para su tratamiento y el tiempo del equipo de prevención en la revisión de los positivos tratados y comprobar su descolonización. En nuestro caso se han considerado mínimos ya que el tiempo de diseño de protocolos no ha disminuido la actividad asistencial por parte del equipo, la identificación de portadores se realiza en la misma consulta preanestésica donde se realizan otras actividades y el equipo de prevención hace el seguimiento dentro de sus atribuciones laborales habituales.
A tenor de los costes calculados, se deduce que este programa es económicamente viable al tener unos costes directos reducidos 1.661,85€. Aunque la reducción de infección no cuente con significación estadística cabe considerar que dichos costes son muy inferiores a los que supone una revisión quirúrgica tanto en artroplastia total de rodilla (en un tiempo 24.027$ o en 2 tiempos 38.109$)3 como en artroplastia total de cadera (en un tiempo 31.133±9.733€ o en 2 tiempos 54.098±12.700€)4.
ConclusionesLa implementación de un programa de cribado y descolonización de S. aureus en cirugía protésica primaria de cadera y rodilla es útil para detectar y descolonizar los pacientes colonizados por S. aureus, con unos costes reducidos y la ventaja de una selectividad al dirigir el tratamiento. La implementación de estos programas en el contexto de un protocolo para la prevención de la infección quirúrgica puede disminuir la incidencia de infección de localización quirúrgica por S. aureus u otros gérmenes, ahorrando su impacto en calidad de vida y a nivel económico que estas suponen.
Nivel de evidenciaNivel de evidencia II.
FinanciaciónEl presente trabajo ha sido financiado por el Servicio de COT del Hospital Universitario de Santa Maria a través del Institut de Recerca Biomèdica de Lleida, Fundació privada Dr. Pifarré.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Comité de éticaAprobado por Comitè d’Ètica d’Investigació amb Medicaments, Hospital Universitari Arnau de Vilanova Lleida Número de registro: CEIC-2606.
Los autores desean agradecer su colaboración a los siguientes profesionales: Dra. Maria Fernanda Ramírez Hidalgo, por su colaboración en la revisión del protocolo; Dra. Laura Prats, por su colaboración en la revisión del manuscrito final; Sra. Inés Ortíz Catalan, enfermera de hospitalización, Sra. Alba Guitard Quer, enfermera de UTIN y Sra. Cristina Cortijo Lecina, enfermera de recepción del paciente quirúrgico, por su colaboración en la recogida de datos.