Se llevó a cabo un estudio longitudinal para analizar la viabilidad, la seguridad y los efectos de la práctica de mindfulness, relajación y estimulación cognitiva en la evolución clínica de la enfermedad de Alzheimer (EA) con el objetivo de analizar la equivalencia de estos tratamientos.
Material y métodosEn el estudio participaron 168 personas con EA probable en tratamiento con donepezilo. En este artículo se muestra a los 21 participantes en estadio grave que completaron el seguimiento de 24 meses. Se agrupó a los sujetos en 3 grupos experimentales (estimulación cognitiva, relajación y mindfulness) y uno control. Cada grupo desarrolló 3 sesiones semanales con medidas semestrales de seguimiento (cognición: CAMCOG y MMSE; funcionalidad: RDRS-2; psicopatología: NPI). Se realizaron análisis no paramétricos.
ResultadosLas puntuaciones de la función cognitiva y la funcionalidad indicaron que no existían diferencias significativas entre los diferentes grupos. No obstante, los grupos de mindfulness y estimulación cognitiva no perdieron puntuación en la capacidad cognitiva en el análisis intragrupo. En el NPI se produjeron diferencias entre el grupo de mindfulness y el control al final del estudio (p<0,017).
ConclusiónLos datos muestran que el tratamiento de donepezilo con mindfulness o estimulación cognitiva presenta una mejor evolución clínica que el tratamiento farmacológico solo o combinado con relajación. Estos datos indican que se debe seguir trabajando en nuevas alternativas terapéuticas para la EA avanzada y que los tratamientos no farmacológicos deben ser recomendados en la práctica clínica para el control evolutivo de la enfermedad a largo plazo. Ensayos con un mayor número de participantes son necesarios para confirmar los resultados informados en este estudio.
A longitudinal study was conducted in order to analyze the feasibility, safety, and effects of the practice of mindfulness, relaxation and cognitive stimulation on the evolution of Alzheimer's disease, with the aim of testing the equivalence of these interventions.
Material and methodsThere were a total of 168 participants with probable Alzheimer's disease (AD) treated with donepezil. In the present article, the 21 participants with advanced AD who completed a follow-up period of 24 months are presented. The participants were grouped into three experimental groups (mindfulness, relaxation, and cognitive stimulation) and one control group. Each group carried out three weekly sessions with bi-annual follow-up measurements (cognition: CAMCOG and MMSE; functionality: RDRS; psychopathology: NPI). Non-parametric analyses were performed.
ResultsThe cognitive function and functionality scores showed no significant differences between the groups. However, the scores in cognitive function of the mindfulness group and the cognitive stimulation group did not decrease in an intra-group analysis. In NPI, there were significant differences between the mindfulness group and the control group by the end of the study (P<.017).
ConclusionThe data showed that the treatment with donepezil in combination with mindfulness or cognitive stimulation presented a better clinical evolution than the pharmacological treatment alone or combined with relaxation. These data suggest that these therapeutic alternatives should be investigated further, and that the non-pharmacological treatments should be recommended in clinical practice in order to control the evolution of AD in the long term. In order to confirm these findings, a larger study is necessary.
La enfermedad de Alzheimer (EA) sigue siendo una de las mayores preocupaciones sanitarias por la falta de un tratamiento óptimo en el curso evolutivo de la enfermedad, especialmente en la etapa avanzada. El Estudio Longitudinal Canarias sobre tratamientos no farmacológicos en la EA (ELCA-TNF) ha mostrado como la práctica de mindfulness en el estadio leve-moderado mantiene la capacidad cognitiva, funcional y previene la psicopatología en al menos 2 años1. ¿Se puede afirmar lo mismo en la etapa avanzada?
Mindfulness es ser consciente de lo que está ocurriendo en el momento presente sin juzgar y con afecto. Actualmente, existen suficientes datos que avalan la posibilidad de utilizar mindfulness como tratamiento no farmacológico (TNF)2. Diferentes estudios han mostrado cómo esta práctica produce efectos positivos sobre el control de la psicopatología en la demencia avanzada3,4. Sin embargo, no existen datos que muestren la eficacia de mindfulness sobre la cognición y la funcionalidad en esta etapa. Este aspecto, unido a la falta de eficacia de los tratamientos en esta fase5, supone un estímulo para buscar nuevas formas de intervención.
A continuación, se muestran los efectos que presenta el entrenamiento neuropsicológico basado en mindfulness en personas mayores con EA avanzada. Este estudio muestra los datos obtenidos en el ELCA-TNF1 en esta fase de la enfermedad. El principal objetivo ha sido explorar si el entrenamiento en mindfulness, teniendo en cuenta el paradigma de la atención conjunta6, es eficaz para frenar el deterioro cognitivo, funcional y psicopatológico en la EA avanzada. En segundo lugar, se ha comparado mindfulness con otros TNF, estimulación cognitiva y relajación, para contrastar si el beneficio que aporta mejora el de estas técnicas. El tercer objetivo ha sido analizar si los TNF producen un beneficio adicional y acumulativo al tratamiento farmacológico.
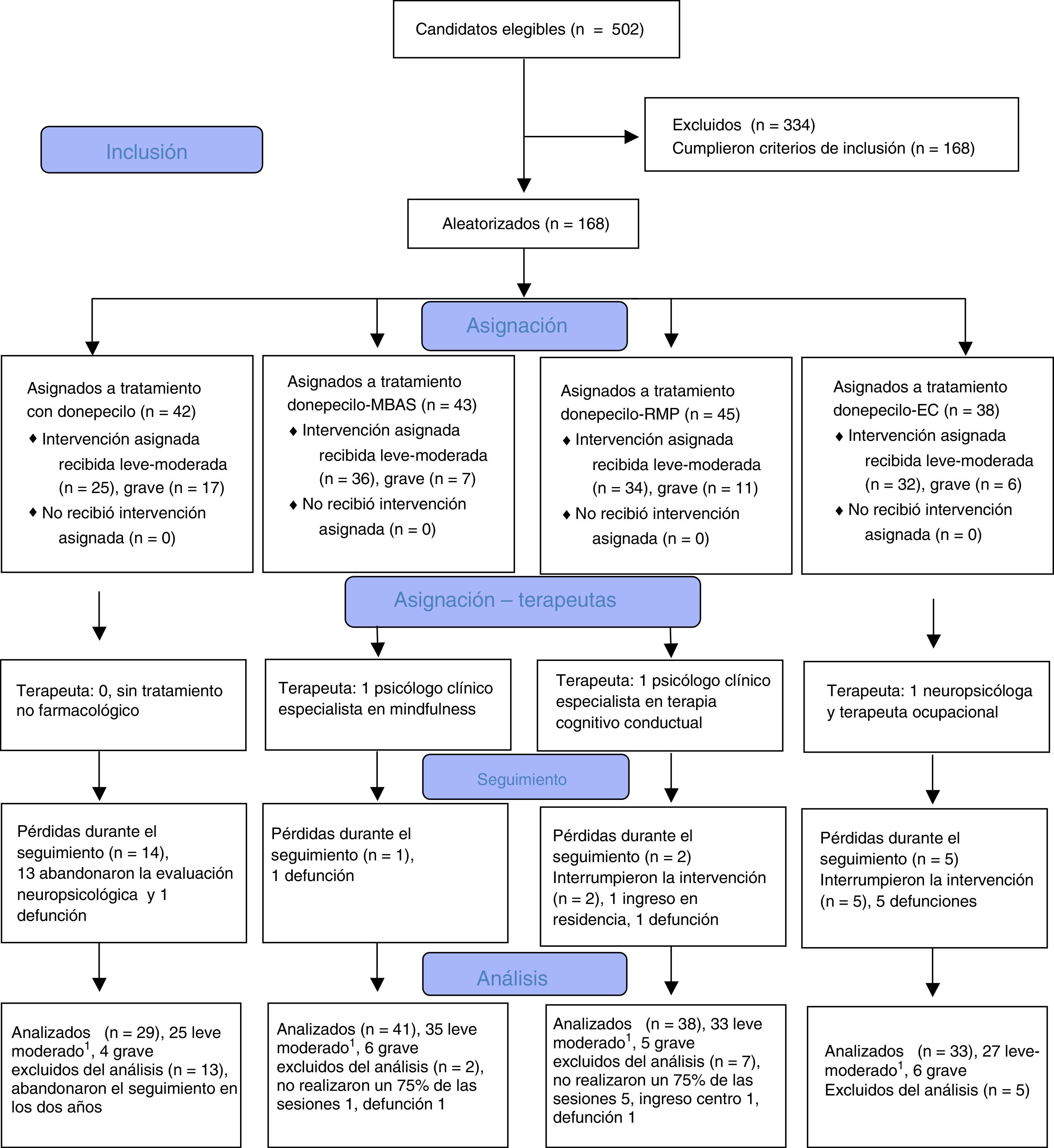
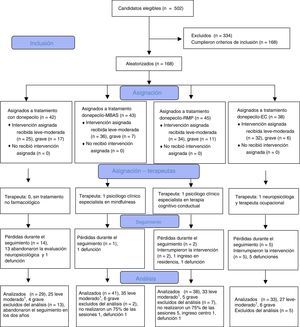
Material y métodoDiseño y participantesSe desarrolló un ensayo clínico longitudinal aleatorizado (1, 1, 1, 1) de medidas repetidas con 168 enfermos con «EA probable» según los criterios de la NINCDS-ARDA7. En este estudio se muestra a los 21 enfermos en fase avanzada, con una puntuación inicial en el Mini Examen del Estado Mental (MMSE) entre 15 y 17 puntos8 correspondiente a un estadio de deterioro global (GDS) 5 de Reisberg et al.9, que completaron el seguimiento. Se excluyó a los enfermos con psicopatología grave comórbida al inicio del estudio. En la figura 1 se puede observar la inclusión, la aleatorización y los criterios de análisis de los participantes en el ensayo clínico según Boutron et al.10.
Diagrama de flujo del Estudio Longitudinal Canarias de tratamientos no farmacológicos en la enfermedad de Alzheimer.Fuente: Boutron et al.10.
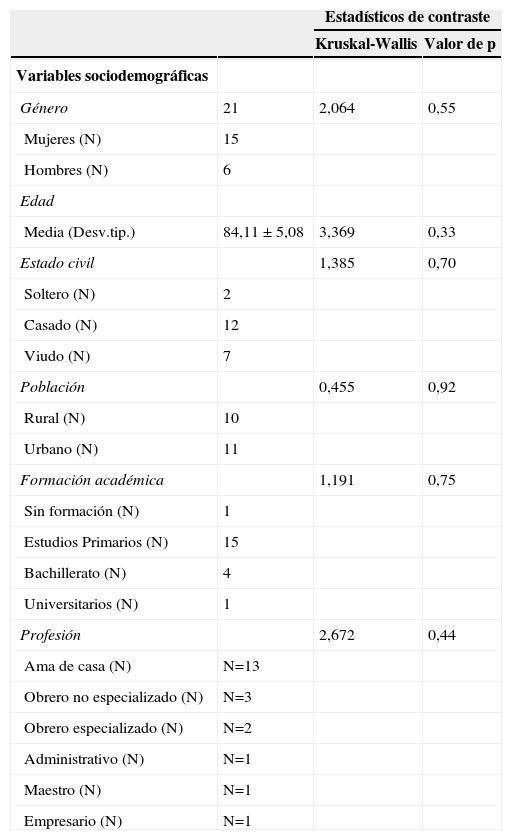
Se controlaron los factores de riesgo psicosociales y biológicos asociados a la demencia, como se muestra en la tabla 1. También se indica en la misma la ausencia de diferencias significativas en la evaluación neuropsicológica en la línea base.
Características sociodemográficas y clínicas de la muestra previas al estudio
| Estadísticos de contraste | |||
|---|---|---|---|
| Kruskal-Wallis | Valor de p | ||
| Variables sociodemográficas | |||
| Género | 21 | 2,064 | 0,55 |
| Mujeres (N) | 15 | ||
| Hombres (N) | 6 | ||
| Edad | |||
| Media (Desv.tip.) | 84,11±5,08 | 3,369 | 0,33 |
| Estado civil | 1,385 | 0,70 | |
| Soltero (N) | 2 | ||
| Casado (N) | 12 | ||
| Viudo (N) | 7 | ||
| Población | 0,455 | 0,92 | |
| Rural (N) | 10 | ||
| Urbano (N) | 11 | ||
| Formación académica | 1,191 | 0,75 | |
| Sin formación (N) | 1 | ||
| Estudios Primarios (N) | 15 | ||
| Bachillerato (N) | 4 | ||
| Universitarios (N) | 1 | ||
| Profesión | 2,672 | 0,44 | |
| Ama de casa (N) | N=13 | ||
| Obrero no especializado (N) | N=3 | ||
| Obrero especializado (N) | N=2 | ||
| Administrativo (N) | N=1 | ||
| Maestro (N) | N=1 | ||
| Empresario (N) | N=1 | ||
| % de enfermos | N | Kruskal-Wallis | Valor de p | |
|---|---|---|---|---|
| Factores de riesgo clínicos | ||||
| HTA | 50 | 6,182 | 0,10 | |
| DM 1 | 4,5 | 1,750 | 0,62 | |
| DM 2 | 13,6 | 1,557 | 0,66 | |
| TSH | 12 | 0,000 | 1,00 | |
| Dislipidemias | 27,3 | 0,089 | 0,99 | |
| Psicopatología | 40,9 | 4,006 | 0,26 | |
| Consumo antidepresivos | 31,8 | 2,064 | 0,55 | |
| Consumo ansiolíticos | 36,3 | 2,064 | 0,55 | |
| Consumo antipsicóticos | 4,5 | 1,750 | 0,62 | |
| Biomarcador APOE-E | 3,353 | 0,34 | ||
| 3/3 | 3 | |||
| 3/4 | 9 | |||
| 4/3 | 4 | |||
| 4/4 | 5 | |||
| Variables clínicas | ||||
| Cognitivas | ||||
| MMSE | 3,966 | 0,265 | ||
| CAMCOG | 7,089 | 0,069 | ||
| Funcionales | ||||
| RDRS-2 | 0,347 | 0,951 | ||
| Psicopatológica | ||||
| NPI | 3,738 | 0,291 | ||
CAMCOG: Examen cognitivo de Cambridge; MMSE: Mini Examen del Estado Mental; NPI: Inventario neuropsiquiátrico de Cummings; RDRS-2: escala de evaluación rápida de la discapacidad.
* p<0,05.
Se evaluó la cognición con las escalas cognitivas incluidas en el CAMDEX-R: el MMSE y el Examen cognitivo de Cambridge (CAMCOG) adaptadas a la población española y con un alfa de Cronbach para la versión británica de 0,8911. La funcionalidad se evaluó con la escala de evaluación rápida de la discapacidad (RDRS-2), con un alfa de Cronbach de 0,9112, y la psicopatología con el Inventario neuropsiquiátrico de Cummings (NPI), con un alfa de Cronbach de 0,8513.
IntervenciónLos grupos experimentales realizaron 288 sesiones semanales de 90 min durante 2 años. La intervención del grupo de estimulación cognitiva ha seguido las directrices del programa Integral de Psicoestimulación14. El grupo de relajación ha seguido un programa estándar de relajación muscular progresiva15 y el grupo de mindfulness desarrolló el programa de intervención neuropsicológica basada en mindfulness1.
Análisis estadísticoSe han desarrollado análisis estadísticos no paramétricos intragrupo (pruebas de Friedman y Wilcoxon) e intergrupos (pruebas de Kruskal-Wallis y Mann-Whitney). Se analizó a los sujetos experimentales que realizaron un 70% de las sesiones de tratamiento como mínimo.
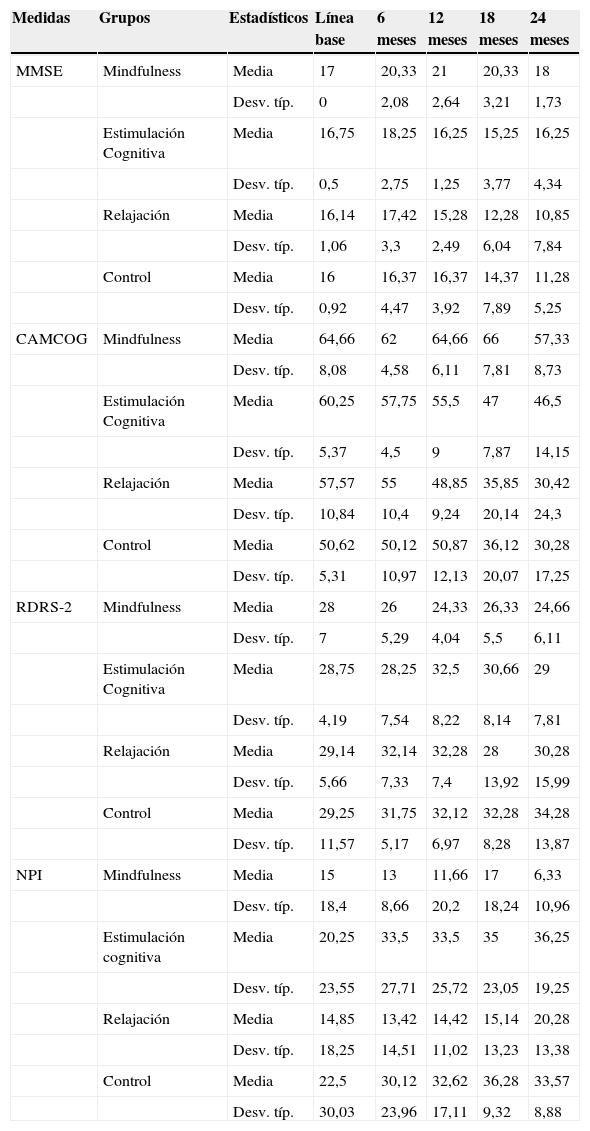
ResultadosEn la tabla 2 se pueden observar la evolución de los estadísticos descriptivos de todas las áreas clínicas a lo largo del estudio. A continuación, se expone el seguimiento de las áreas clínicas.
Evolución de estadísticos descriptivos en la fase avanzada (ELCA-TNF)
| Medidas | Grupos | Estadísticos | Línea base | 6 meses | 12 meses | 18 meses | 24 meses |
|---|---|---|---|---|---|---|---|
| MMSE | Mindfulness | Media | 17 | 20,33 | 21 | 20,33 | 18 |
| Desv. típ. | 0 | 2,08 | 2,64 | 3,21 | 1,73 | ||
| Estimulación Cognitiva | Media | 16,75 | 18,25 | 16,25 | 15,25 | 16,25 | |
| Desv. típ. | 0,5 | 2,75 | 1,25 | 3,77 | 4,34 | ||
| Relajación | Media | 16,14 | 17,42 | 15,28 | 12,28 | 10,85 | |
| Desv. típ. | 1,06 | 3,3 | 2,49 | 6,04 | 7,84 | ||
| Control | Media | 16 | 16,37 | 16,37 | 14,37 | 11,28 | |
| Desv. típ. | 0,92 | 4,47 | 3,92 | 7,89 | 5,25 | ||
| CAMCOG | Mindfulness | Media | 64,66 | 62 | 64,66 | 66 | 57,33 |
| Desv. típ. | 8,08 | 4,58 | 6,11 | 7,81 | 8,73 | ||
| Estimulación Cognitiva | Media | 60,25 | 57,75 | 55,5 | 47 | 46,5 | |
| Desv. típ. | 5,37 | 4,5 | 9 | 7,87 | 14,15 | ||
| Relajación | Media | 57,57 | 55 | 48,85 | 35,85 | 30,42 | |
| Desv. típ. | 10,84 | 10,4 | 9,24 | 20,14 | 24,3 | ||
| Control | Media | 50,62 | 50,12 | 50,87 | 36,12 | 30,28 | |
| Desv. típ. | 5,31 | 10,97 | 12,13 | 20,07 | 17,25 | ||
| RDRS-2 | Mindfulness | Media | 28 | 26 | 24,33 | 26,33 | 24,66 |
| Desv. típ. | 7 | 5,29 | 4,04 | 5,5 | 6,11 | ||
| Estimulación Cognitiva | Media | 28,75 | 28,25 | 32,5 | 30,66 | 29 | |
| Desv. típ. | 4,19 | 7,54 | 8,22 | 8,14 | 7,81 | ||
| Relajación | Media | 29,14 | 32,14 | 32,28 | 28 | 30,28 | |
| Desv. típ. | 5,66 | 7,33 | 7,4 | 13,92 | 15,99 | ||
| Control | Media | 29,25 | 31,75 | 32,12 | 32,28 | 34,28 | |
| Desv. típ. | 11,57 | 5,17 | 6,97 | 8,28 | 13,87 | ||
| NPI | Mindfulness | Media | 15 | 13 | 11,66 | 17 | 6,33 |
| Desv. típ. | 18,4 | 8,66 | 20,2 | 18,24 | 10,96 | ||
| Estimulación cognitiva | Media | 20,25 | 33,5 | 33,5 | 35 | 36,25 | |
| Desv. típ. | 23,55 | 27,71 | 25,72 | 23,05 | 19,25 | ||
| Relajación | Media | 14,85 | 13,42 | 14,42 | 15,14 | 20,28 | |
| Desv. típ. | 18,25 | 14,51 | 11,02 | 13,23 | 13,38 | ||
| Control | Media | 22,5 | 30,12 | 32,62 | 36,28 | 33,57 | |
| Desv. típ. | 30,03 | 23,96 | 17,11 | 9,32 | 8,88 |
CAMCOG: Examen cognitivo de Cambridge; MMSE: Mini Examen del Estado Mental; NPI: Inventario neuropsiquiátrico de Cummings; RDRS-2: escala de evaluación rápida de la discapacidad.
Los resultados intragrupo mostraron cómo el grupo de mindfulness y estimulación cognitiva han mantenido la puntuación estable a lo largo de los 2 años de seguimiento, sin que se produzca una pérdida significativa. Sin embargo, el grupo de relajación pierde capacidad desde los 18 meses (CAMCOG: Z=–2,366; p=0,018) y el control a los 24 meses (MMSE Z=–2,023; p=0,043; CAMCOG: Z=–2,371; p=0,018).
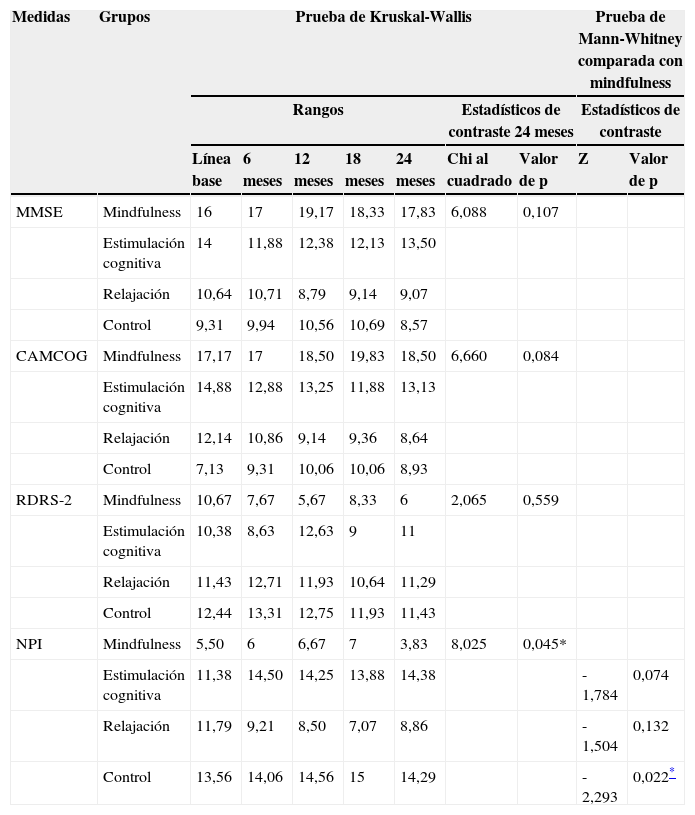
El análisis de las diferencias intergrupos mostró que no se produjeron diferencias significativas entre los diferentes grupos experimentales y el control, como se puede observar en la tabla 3. No obstante, la tendencia lineal que se observa en la puntuación media muestra cómo el grupo de mindfulness presenta un incremento de la puntuación en el MMSE y CAMCOG hasta los 18 meses, mientras que el resto de grupos presentan un deterioro progresivo desde los 12 meses, como se observa en la tabla 2.
Análisis no paramétricos intergrupos en la fase avanzada de la EA (ELCA-TNF)
| Medidas | Grupos | Prueba de Kruskal-Wallis | Prueba de Mann-Whitney comparada con mindfulness | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Rangos | Estadísticos de contraste 24 meses | Estadísticos de contraste | ||||||||
| Línea base | 6 meses | 12 meses | 18 meses | 24 meses | Chi al cuadrado | Valor de p | Z | Valor de p | ||
| MMSE | Mindfulness | 16 | 17 | 19,17 | 18,33 | 17,83 | 6,088 | 0,107 | ||
| Estimulación cognitiva | 14 | 11,88 | 12,38 | 12,13 | 13,50 | |||||
| Relajación | 10,64 | 10,71 | 8,79 | 9,14 | 9,07 | |||||
| Control | 9,31 | 9,94 | 10,56 | 10,69 | 8,57 | |||||
| CAMCOG | Mindfulness | 17,17 | 17 | 18,50 | 19,83 | 18,50 | 6,660 | 0,084 | ||
| Estimulación cognitiva | 14,88 | 12,88 | 13,25 | 11,88 | 13,13 | |||||
| Relajación | 12,14 | 10,86 | 9,14 | 9,36 | 8,64 | |||||
| Control | 7,13 | 9,31 | 10,06 | 10,06 | 8,93 | |||||
| RDRS-2 | Mindfulness | 10,67 | 7,67 | 5,67 | 8,33 | 6 | 2,065 | 0,559 | ||
| Estimulación cognitiva | 10,38 | 8,63 | 12,63 | 9 | 11 | |||||
| Relajación | 11,43 | 12,71 | 11,93 | 10,64 | 11,29 | |||||
| Control | 12,44 | 13,31 | 12,75 | 11,93 | 11,43 | |||||
| NPI | Mindfulness | 5,50 | 6 | 6,67 | 7 | 3,83 | 8,025 | 0,045* | ||
| Estimulación cognitiva | 11,38 | 14,50 | 14,25 | 13,88 | 14,38 | -1,784 | 0,074 | |||
| Relajación | 11,79 | 9,21 | 8,50 | 7,07 | 8,86 | -1,504 | 0,132 | |||
| Control | 13,56 | 14,06 | 14,56 | 15 | 14,29 | -2,293 | 0,022* | |||
CAMCOG: Examen cognitivo de Cambridge; MMSE: Mini Examen del Estado Mental; NPI: Inventario neuropsiquiátrico de Cummings; RDRS-2: escala de evaluación rápida de la discapacidad.
Los resultados intragrupos e intergrupos mostraron que no se produjeron diferencias significativas. En la tabla 3 se exponen los datos del análisis intergrupo.
Alteraciones psicopatológicasEl análisis intragrupo mostró que tampoco se producen diferencias significativas en esta variable. Sin embargo, el análisis intergrupo muestra que se producen diferencias significativas favorables para el grupo de mindfulness en comparación con el grupo control a los 24 meses, como se expone en la tabla 3.
DiscusiónEste estudio es el primer intento que trata de mostrar que mindfulness es útil como TNF para personas mayores con EA de forma longitudinal. Para ello ha sido necesario analizar su eficacia clínica en comparación con otros tratamientos combinados habituales o el uso aislado de la medicación con los cuidados básicos en el domicilio. Por tanto, el objetivo principal ha sido evaluar si la combinación basada en mindfulness y donepezilo en la fase avanzada de la enfermedad mostraba el mismo beneficio global encontrado en la fase leve-moderada1.
Los resultados generales indican que el tratamiento farmacológico es tan eficaz como el tratamiento combinado (farmacológico y no farmacológico) a lo largo del estudio. Los datos muestran una tendencia positiva sobre el área cognitiva de los grupos de mindfulness y estimulación cognitiva. Además, el grupo de mindfulness muestra diferencias significativas con el control al final del estudio en la evaluación psicopatológica.
Estos datos sobre la eficacia de los TNF están directamente relacionados con un segundo aspecto abordado en este estudio piloto, la elección del tratamiento más adecuado para la EA avanzada. Esta preocupación deriva de la controversia sobre la existencia de un efecto beneficioso sobre la evolución clínica en la fase avanzada. Existen diversos estudios que utilizando algún modelo de estimulación cognitiva han apuntado que no existe un beneficio clínico5. Sin embargo, otros estudios muestran que al menos en 12 meses produce un mantenimiento significativo de la capacidad cognitiva y funcional14. En este estudio, el dato más relevante es que no se produzca un deterioro significativo de la capacidad cognitiva en los grupos que practican mindfulness o estimulación cognitiva durante 2 años.
Un segundo aspecto que se debe destacar en este estudio, que es la principal novedad que aporta, ha sido la aplicación de mindfulness de forma conjunta con los cuidadores en el desarrollo de las actividades de la vida diaria teniendo en cuenta el paradigma de la atención conjunta6. La atención conjunta es la situación esencial sobre la que se construye la comunicación y el desarrollo cognitivo y, si se aplica mindfulness, se elimina la crítica en la interacción. Este aspecto es importante, pues el enfermo no se siente juzgado por no responder a una tarea con un resultado determinado de forma externa. Las tareas de mindfulness compartidas suponen el desarrollo de diferentes capacidades cognitivas que permite que se consolide un vínculo afectivo con el cuidador.
En resumen, los resultados de este estudio apoyan la eficacia comparada del mindfulness en la EA avanzada. Es importante destacar que muestran la misma tendencia que la encontrada en la fase leve-moderada de la enfermedad1. Estudios anteriores aplicando el programa de mindfulness para la reducción del estrés (MBSR)3,4 han mostrado resultados similares en el área psicopatológica. Sin embargo, estos estudios no se desarrollaron longitudinalmente ni compararon los resultados con otros tratamientos no farmacológicos tradicionales para mostrar el valor diferencial que aporta. A pesar de las tendencias mostradas en este estudio, se debe ser prudente sobre la eficacia de mindfulness en la EA avanzada, pues es necesario realizar un ensayo clínico controlado aleatorizado mayor que incluya marcadores biológicos.
LimitacionesLa limitación más importante de este estudio ha sido el escaso número de sujetos experimentales en los diferentes grupos, especialmente en la fase avanzada de la enfermedad. También es importante destacar que durante el proceso de aleatorización se produjo un sesgo en la secuencia de la misma, pues el grupo control quedó constituido con un mayor número de sujetos en fase avanzada. A pesar de ello, el dato más relevante del ELCA-TNF es que casi todos los sujetos que recibieron el tratamiento combinado finalizaron el estudio. También es relevante que no se produjeran diferencias significativas en la línea base entre los diferentes grupos experimentales y el control.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.