Mujer de 90 años de edad con antecedentes de hipertensión arterial, insuficiencia cardíaca crónica por disfunción diastólica e hipertensión pulmonar moderada con fracción de eyección del ventrículo izquierdo preservada, fibrilación auricular paroxística, bronquitis asmática reagudizadora y dislipemia.
Tratamiento habitual con furosemida 80 mg, hidroclorotiazida 25 mg, pravastatina 20 mg, bromuro de tiotropio 18 μg, formoterol/budesonida 320/9 μg, lorazepam 0,5 mg, enoxaparina 80 mg y oxigenoterapia crónica 24 horas.
Basalmente presenta deterioro funcional severo (fractura cadera previa, disnea y deterioro cognitivo). Dependiente para todas las actividades básicas de la vida diaria. IB 0/100. Inmovilizada desde antecedente traumático. Funcional Assessment Classification 0/5. Fallos mnésicos globales y desorientación temporo-espacial sin especificar tiempo de evolución, compatible con demencia severa (GDS 6) neurodegenerativa.
Ingresa por clínica de siete días con tos productiva, disnea y aumento progresivo de edemas, compatible con infección respiratoria e insuficiencia cardíaca. Asocia hipotensión arterial (TA 90/55 mmHg), taquicardia (110 lpm) y estabilidad respiratoria. Afebril. Signos de congestión sistémica con ingurgitación venosa yugular y anasarca.
Analíticamente, elevación de reactantes de fase aguda, leucocitosis (30.400 103 /μL), neutrofilia (95,4%) y Proteína C Reactiva (10,8 mg/dL). Procalcitonina negativa. Creatinina 4,95 mg/dL con filtrado glomerular estimado de creatinina inferior a 15 mL/min (función renal previa preservada). Orina de 24 horas con proteinuria en rango nefrótico (6 g). Urocultivo estéril. Marcadores tumorales negativos. Proteinograma e inmunoglobulinas normales. Estudio mieloma negativo. Autoinmunidad (ANA, ANCA, factor reumatoide, anticuerpos antipéptido cíclico citrulinado y antimembrana basal glomerular) y estudio microbiológico (virus hepatotropos, respiratorios, VIH y quantiferon) normales.
Radiografía de tórax con derrame pleural bilateral. Ecocardiograma transtorácico con disfunción diastólica con FEVI preservada. Ecografía renal normal.
A pesar del tratamiento médico activo con diuréticos, antibioterapia (meropenem) y corticoterapia, la evolución clínica de la paciente fue insatisfactoria. Presentó empeoramiento progresivo de función renal (creatinina 6,10 mg/dL con FGeCr inferior a 15 mL/min), oligo-anuria y desarrollo de varias complicaciones como anemización severa multifactorial y bacteriemia por Campylobacter fetus de probable etiología digestiva, contribuyendo al deterioro hemodinámico y clínico de la paciente. Considerando su situación basal y clínica presentada con mal pronóstico, se optó por manejo conservador sin progresar en la investigación etiológica, la paciente falleció tras nueve días de ingreso.
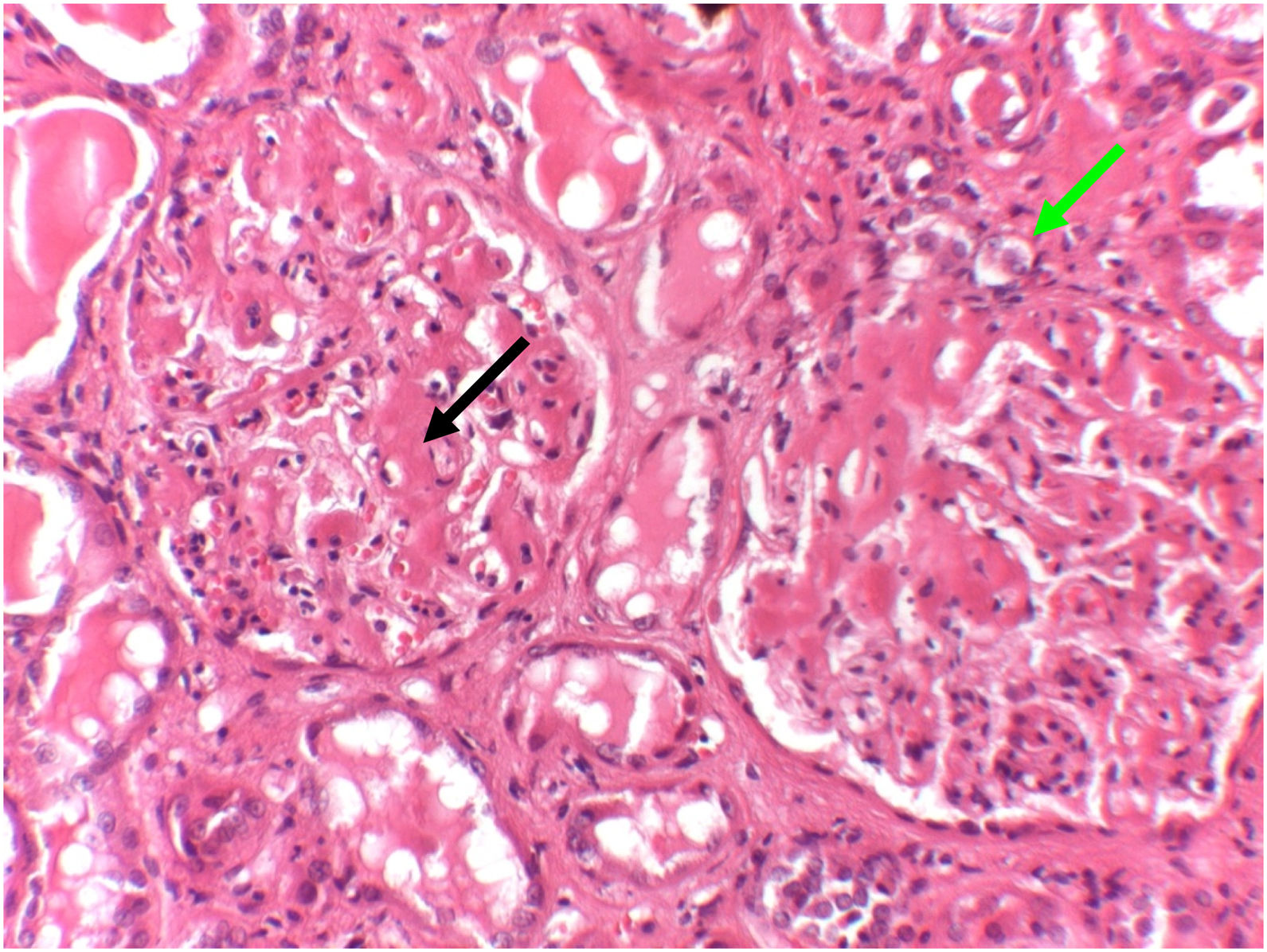
Debido a la ausencia de etiología clara y curso clínico presentado, se realizó necropsia que evidenció la existencia de infiltrados eosinofílicos (rojo Congo/tioflavina/AA positivos) en ambos riñones, difusos a lo largo del mesangio glomerular y capilares glomerulares, compatible con amiloidosis tipo AA (fig. 1). Presentó afectación moderada de glándulas suprarrenales, bazo, hígado y corazón, con depósito de amiloide en la pared de los vasos de pequeño calibre.
Tinción hematoxilina-eosina. Microscopía óptica (x20). Se observan dos glomérulos renales con extenso material amiloidótico depositado. La flecha negra señala el extenso infiltrado amiloidótico distribuido a lo largo del mesangio glomerular. La flecha verde señala el depósito de amiloide alrededor de los capilares glomerulares.
La amiloidosis sistémica AA provoca un depósito proteico extracelular (proteína SAA) ante estímulos inflamatorios severos y persistentes. Existe deterioro multisistémico con afectación preferentemente renal, desarrollo de síndrome nefrótico y fracaso renal1,2, contribuyendo a la morbimortalidad del cuadro. Las principales enfermedades implicadas son aquellas con sustrato inflamatorio crónico moderado-severo, como algunos procesos reumatológicos, neoplasias e infecciones3,4.
Prevalencia variable, entre 10-30% de los pacientes con afectación reumatológica crónica la desarrollan5. Prevalencia alta en ancianos con riesgo incrementado de curso complicado, la sospecha inicial del proceso es esencial para su diagnóstico y óptimo manejo. Tras la nefropatía diabética y membranosa, constituye la tercera causa de proteinuria en rango nefrótico en ancianos.
De curso clínico progresivo con aparición de síndrome nefrótico y deterioro de función renal de perfil subagudo-crónico6. Nuestra paciente debutó con un fracaso renal agudo severo con síndrome nefrótico con función renal previa normal, destacando por su curso agudo y rápidamente progresivo.
La investigación etiológica fue limitada debido a la situación clínica de la paciente sin lograr establecer la causa primaria del proceso. Una hipótesis probable, sin poder ser demostrada fehacientemente, fue el desarrollo de un estado proinflamatorio crónico (bronquitis asmática con perfil reagudizador), el cual, ante una nueva reagudización propició una intensa respuesta inflamatoria con activación masiva del proceso amiloidótico.
La necropsia permitió el diagnóstico, el cual no hubiera sido posible de otra forma7,8. Debemos plantearla en el anciano como una herramienta esencial para aquellos casos en los que la causa del fallecimiento no sea clara, ya que nos va a permitir investigar y estudiar la historia natural del proceso, así como identificar y abordar más eficientemente casos futuros.
La edad avanzada, múltiples comorbilidades y dependencia severa fueron los factores que contribuyeron decisivamente a una ominosa evolución clínica, a pesar de los esfuerzos terapéuticos. Una alta sospecha inicial de la enfermedad permite un estudio etiológico exhaustivo y un adecuado diagnóstico diferencial, individualizado para identificar la causa primaria del proceso. Un control precoz y estricto del proceso inflamatorio subyacente, permitirá controlar la enfermedad y prevenir el desarrollo de complicaciones.