Obtener una cohorte de sujetos con edad igual o mayor a 70 años, representativa de una población urbana española, para estimar la prevalencia de fragilidad y seguirla en el tiempo para analizar factores asociados.
Material y métodosEstudio de cohortes concurrente de base poblacional. Sobre un universo de 18.137 ancianos, se realizó un muestreo aleatorio estratificado para obtener una muestra representativa de 1.172. Aceptaron participar 993 personas (84,7%). Se recogieron variables sociodemográficas, de comorbilidad, funcionales (n=825), cognitivas, afectivas y de calidad de vida. A los sujetos que aceptaron se les determinó la composición corporal por bioimpedanciometría (n=557), el gasto energético basal por calorimetría indirecta (n=450) y se obtuvo muestra de sangre para la determinación de biomarcadores (n=859). La fragilidad se definió por la presencia de 3 o más de los criterios Fried: pérdida de peso no intencionada, baja fuerza, cansancio, lentitud al caminar y baja actividad física. La cohorte será seguida en el tiempo hasta el fallecimiento de los sujetos.
ResultadosEdad media±desviación estándar 79,4±6,4 años, con 601 (60,5%) mujeres. Institucionalizados el 21,3%. Fueron frágiles el 16,9%, prefrágiles 48,5%, no frágiles 21,8%, y no se dispuso de 3 criterios para poder determinar su estado en el 12,8%, de los cuales el 9,5% tenía una discapacidad moderada-severa, por lo que la prevalencia de fragilidad podría aumentar hasta el 26,4%.
ConclusionesSe ha construido la cohorte FRADEA, representativa de los mayores de una población urbana de España. La prevalencia de fragilidad en la cohorte fue del 16,9%.
To obtain a cohort of subjects of equal to or greater than 70 years, representative of a Spanish urban population, to estimate the prevalence of frailty and follow it up over time to analyse associated factors.
Material and methodsA prospective, population-based cohort study. From a population of 18,137 elderly persons, a representative sample of 1172 was randomly stratified, of which 993 (84.7%) agreed to take part. The variables collected were; sociodemographic, comorbidity, functional (n=825), cognitive, affective and quality of life. On the patients who agreed, body composition was determined by bioimpedance analysis (n=557), basal metabolic rate by indirect calorimetry (n=450) and a blood sample was obtained for biomarkers (n=859). Frailty was defined by the presence of 3 or more Fried criteria: unintentional weight loss, low energy, exhaustion, slow walking, and low physical activity. The cohort will be followed up over time until the death of the subjects.
ResultsMean age 79.4 (SD 6.4) years, with 601 (60.5%) women. A total of 21.3% were institutionalised; 16.9% were frail, 48.5% pre-frail, 21.3% non-frail, and 12.8% did not have the 3 criteria to be able to determine their state, of which 9.5% had moderate-severe incapacity, which would increase the prevalence of frailty to 26.4%.
ConclusionsA FRADEA cohort has been constructed, representative of an urban population in Spain. The prevalence of frailty in the cohort was 16.9%.
La fragilidad se define como un «síndrome biológico de disminución de la reserva funcional y resistencia a los estresores, debido al declive acumulado de múltiples sistemas fisiológicos que originan pérdida de la capacidad homeostática y vulnerabilidad a eventos adversos»1-3 y es considerada como «el mandato especial del geriatra»4. La probabilidad de ser frágil aumenta de manera no lineal con el número de sistemas fisiológicos alterados5. Diferentes autores han caracterizado este síndrome en la práctica clínica diaria a través de criterios, constructos y escalas6-16. Los más utilizados, y que definen el fenotipo de fragilidad, son los descritos por L.P. Fried en 20016, y que comprenden la pérdida de peso no intencionada, la debilidad, el cansancio, la lentitud de marcha y el bajo nivel de actividad física. Estos criterios han demostrado buena validez de criterio y constructo en diferentes cohortes de ancianos17.
La fragilidad es un síndrome frecuente en personas ancianas y que aumenta su prevalencia de manera exponencial a medida que se envejece, desde un 3,2% a los 65 años, un 16,3% en los mayores de 80 años y un 23,1% a los 90 años6. Diferentes estudios de cohortes han encontrado prevalencias entre el 4 y el 16,3% en diferentes ámbitos y países6,18-20, siendo más prevalente en mujeres y afroamericanos6, y con una incidencia a los 7,5 años del 9% en mujeres no frágiles21.
La principal relevancia de este síndrome es que funciona como un importante predictor de eventos adversos graves en ancianos como mortalidad (hasta el 45% a un año en los frágiles), institucionalización, caídas, deterioro de la movilidad, aumento de la dependencia en actividades básicas de la vida diaria (ABVD), en actividades instrumentales de la vida diaria (AIVD) y hospitalización17,22. Además, los sujetos con estado intermedio de fragilidad o prefragilidad (1 o 2 criterios) mostraron un riesgo aumentado de convertirse en frágiles a los 3 años.
A pesar de la relevancia de este síndrome, quedan aún muchas preguntas por contestar desde el punto de vista clínico y biológico23. ¿Es similar la prevalencia en todos los países y ámbitos? ¿Funcionan los criterios de Fried de igual manera para todos los ancianos del mundo, o los criterios y puntos de corte pueden variar? ¿Se puede mejorar el constructo añadiendo o suprimiendo criterios? ¿Podríamos disponer de alguna herramienta sencilla que ayudara a identificar y cuantificar de manera fiable a estos sujetos? ¿Cuáles son sus bases biológicas? Para dar respuesta a estas preguntas, diseñamos el estudio de cohortes FRADEA (Fragilidad y Dependencia en Albacete) del que se presentan el razonamiento, la metodología y algunos resultados parciales.
ObjetivosEl objetivo principal del proyecto FRADEA es determinar la proporción de ancianos frágiles en el área Sanitaria de Albacete capital.
Los objetivos secundarios son: establecer el valor pronóstico de los criterios de fragilidad de Fried en la aparición de eventos adversos en ancianos (comorbilidad, situación funcional, discapacidad, dependencia, caídas, hospitalización, institucionalización y muerte) durante un periodo de seguimiento de 2 años. Validar en español el instrumento Late Life Function and Disability Instrument abreviado (SF-LLFDI) para evaluar función y discapacidad en mayores de 70 años. Comprobar si mediante el instrumento SF-LLFDI es posible identificar fragilidad en mayores de 70 años, determinando su validez respecto a los criterios de Fried. Determinar si la inclusión de la tasa metabólica basal medida con el calorímetro indirecto FitMate® en lugar del consumo calórico, mejora el poder predictivo de los criterios de Fried sobre eventos adversos en ancianos. Analizar la prevalencia de sarcopenia en ancianos autónomos de la comunidad mediante el impedanciómetro Tanita®.
Material y métodosDiseñoEstudio de cohortes concurrente de base poblacional.
Participantes y criterios de selecciónPara obtener la muestra final se seleccionó mediante un muestreo aleatorio estratificado por edad y sexo, una muestra representativa de personas de 70 o más años residentes en la ciudad de Albacete (España) durante al menos 3 meses al año. El municipio de Albacete es una ciudad capital de provincia, que tenía a fecha 1 de enero de 2008, según el Instituto Nacional de Estadística (INE), 166.909 habitantes, de los cuales 16.959 (10,2%) tenían una edad igual o mayor a 70 años, 6.895 (40,7%) eran varones y 10.064 (59,3%) mujeres24.
La selección aleatoria se realizó a partir de la base de datos de tarjeta sanitaria. En esta base de datos, aparecían 18.137 personas con edad igual o mayor a 70 años, mientras que en los datos del INE eran 16.959, como se ha comentado. Esta discordancia puede deberse a cambios de domicilio o muertes no reflejadas, o a población itinerante. Se realizó un muestreo estratificado para reducir la variación debida a éste y obtener estimaciones más precisas. De esta forma, se obtuvo una muestra aleatoria de personas mayores en cada uno de los siguientes 4 estratos: varones y mujeres con edades inferiores o superiores a 80 años, a partir de 70, manteniendo las proporciones de la población de referencia.
Como único criterio de exclusión se consideró la negativa a la participación en el estudio o a firmar el consentimiento informado por escrito.
Tamaño muestral y potencia estadísticaEl tamaño muestral se calculó para detectar una tasa de eventos adversos un 20% mayor en ancianos de la comunidad frágiles que en no frágiles (el 30 frente al 10%) a los 2 años de seguimiento, con una α<0,05 y una β=0,10. Calculando un porcentaje de frágiles del 10% en este grupo poblacional, fueron necesarios 82 frágiles y 738 no frágiles en la comunidad, 820 en total. Si añadimos un 15% de ancianos institucionalizados, el número total sería de 943, y si añadimos un 25% de pérdidas (15% de negativas a participar y 10% de pérdidas durante el seguimiento), la muestra final debería tener 1.178 sujetos. Finalmente, se seleccionaron 1.172 por muestreo aleatorio.
Variables de estudioSe recogieron datos sociodemográficos (edad, sexo, nivel educacional, lugar de residencia y convivencia y ocupación habitual). El nivel educacional se clasificó en 5 categorías: analfabetos, estudios primarios incompletos, primarios completos, educación secundaria y estudios universitarios. La convivencia se clasificó en 4 grupos, según el participante viviera solo, con su cónyuge, con hijos u otro familiar, o en residencia. La ocupación habitual se clasificó en 7 grupos siguiendo la propuesta de un indicador de clase social basado en la ocupación25: grupo I, compuesto por directivos de la administración y de las empresas (excepto los incluidos en 2), altos funcionarios, profesionales liberales y técnicos superiores; grupo II, compuesto por directivos y propietarios-gerentes del comercio y de los servicios personales, otros técnicos (no superiores), artistas y deportistas; grupo III, compuesto por cuadros y mandos intermedios, administrativos y funcionarios, en general, personal de los servicios de protección y seguridad; grupo IVa, compuesto por trabajadores manuales cualificados de la industria, comercio, servicios y del sector primario; grupo IVb, con trabajadores manuales semicualificados de la industria, comercio, servicios y del sector primario; grupo V, con trabajadores no cualificados, y grupo VI, compuesto por otros casos como miembros del clero y de las fuerzas armadas, profesiones mal especificadas, o cuando no consta.
Se recogieron el consumo de fármacos habituales y los hábitos tóxicos. Para el hábito tabáquico se determinó el número de años que el participante había fumado, así como el número de cigarrillos/día durante ese periodo para hacer el cálculo de paquetes/año. Para el hábito enólico se calculó el número de unidades de bebida estándar26 por semana mediante el cuestionario interrogatorio sistemático del consumo de alcohol27.
El riesgo social en los participantes no institucionalizados se calculó mediante la escala sociofamiliar de Gijón abreviada y modificada, que evalúa 3 dominios (situación familiar, relaciones y contactos sociales y apoyos de la red social), cada uno de ellos puntuando entre 1 y 5. Esta versión de Barcelona ha sido validada para la predicción del retorno al domicilio y del riesgo de institucionalización, con una puntuación máxima de 15 y mínima de 5. Menos de 8 puntos sugieren una situación social buena, con bajo riesgo de institucionalización; entre 8 y 9 puntos, una situación intermedia, y más de 10 puntos, un deterioro social severo con alto riesgo de institucionalización)28. También se recogió el tipo de prestaciones sociales que recibían los participantes (ayuda en el hogar, comida en hogar, teleasistencia u otras).
La discapacidad se determinó mediante cuestionarios como el índice de Barthel para las ABVD29,30, el índice de Lawton para las AIVD31,32 y el instrumento SF-LLFDI para la medición de discapacidad y función33. Se consideró discapacidad para realizar alguna ABVD cuando los sujetos puntuaron por debajo del máximo en alguna de las siguientes 5 obtenidas del índice de Barthel: baño, aseo, alimentación, uso del retrete, vestido o transferencias.
El SF-LLFDI es una versión abreviada del Late Life Function and Disability Instrument original34,35 y está compuesto por 3 subescalas, 1 de función y 2 de discapacidad. La subescala de función consta de 15 preguntas. Cada una puntúa desde 5 (no le cuesta nada) hasta 1 (no puede realizarlo). El rango oscila entre 75 (no existe limitación funcional) hasta 15 (máxima limitación funcional). Las subescalas de discapacidad (frecuencia y dificultad) están compuestas cada una por las mismas 8 preguntas. La puntuación a cada pregunta presenta un rango de 5 (muy a menudo) a 1 (nunca). La puntuación que se puede obtener en cada subescala oscila entre 40 (ninguna discapacidad) hasta 8 (gran discapacidad). El rango de puntuación global final oscila entre 31 como peor funcionalidad posible y 155 como la mejor posible.
La dependencia se valoró aplicando los criterios del baremo de la Ley de la Autonomía Personal y Atención a la Dependencia de 21 de abril de 2006, en sus artículos 26 y 27, que la clasifican en 3 grandes grados: grado I o dependencia moderada, cuando la persona necesita ayuda para realizar varias ABVD al menos una vez al día; grado II o dependencia severa, cuando la persona necesita ayuda para realizar varias ABVD 2 o 3 veces al día, pero no requiere la presencia permanente de un cuidador, y grado III o gran dependencia, cuando la persona necesita ayuda para realizar varias ABVD varias veces al día y, por su pérdida total de autonomía física, mental, intelectual o sensorial necesita la presencia indispensable y continua de otra persona36.
La deambulación se valoró mediante la escala Functional Ambulation Classification37 y además se recogió la necesidad de ayuda técnica (andador, bastón o silla de ruedas). El equilibrio y la marcha se evaluaron mediante la velocidad de marcha a ritmo normal en 4 m, en m/s, el timed up and go (TUG) (tiempo que tardó el sujeto en levantarse de una silla sin reposabrazos, caminar 3 m, girar y volver a sentarse)38, el tiempo de equilibrio unipodal y la Short Physical Performance Battery (SPPB) (batería compuesta por 3 pruebas de observación directa que son la velocidad de marcha, el equilibrio y el tiempo en levantarse 5 veces de una silla)39.
La fuerza de tren superior se calculó mediante la determinación de la fuerza prensora de mano dominante con dinamómetro digital de JAMAR y la fuerza flexora de codo con dinamómetro hidráulico de JAMAR. La fuerza de tren inferior se calculó indirectamente mediante el 5 sit-to-stand chair test (tiempo en levantarse y sentarse 5 veces de una silla sin reposabrazos con los brazos en cruz)39.
El estado cognitivo se evaluó mediante el Minimental State Examination de Folstein40,41 y el estado afectivo mediante la escala de depresión geriátrica de Yesavage42,43, ambos validados en español.
La identificación de las enfermedades crónicas presentadas, así como los tratamientos habituales, se realizó a partir del historial médico del paciente. Las enfermedades se codificaron según la clasificación CIE-10, y posteriormente fueron agrupadas en grandes grupos homogéneos para su posterior análisis. Los fármacos consumidos también se clasificaron según grandes grupos terapéuticos. Para el análisis de la comorbilidad se calculó el índice de Charlson44. Se consideró que los sujetos tenían alta comorbilidad cuando la puntuación en el índice de Charlson fue igual o mayor a 3 puntos44. El estado auditivo se valoró mediante la escala de actividades diarias dependientes de la audición45. Esta escala tiene un rango de puntuación entre 0 (nulo impacto de la audición en la realización de las actividades de la vida diaria) y 24 (impacto máximo). Una puntuación igual o inferior a 20 puntos fue indicativa de alteración de la audición, con una sensibilidad del 80,0% y una especificidad del 70,2%.
Como variables antropométricas se recogieron el peso en kilogramos, la talla en centímetros y el perímetro abdominal en centímetros, y se calculó el índice de masa corporal (IMC) en kg/m2. Se efectuó una medición de la presión arterial sistólica y diastólica en reposo con aparato automático modelo OMRON®.
Como cribado nutricional se empleó el Mini Nutritional Assessment Short Form46.
La actividad física habitual se determinó mediante la herramienta Calcumed®47. Este instrumento recoge, durante una semana habitual, las horas diarias de sueño, las de actividad física muy ligera (sentarse y permanecer de pie, conducir automóvil o camión, trabajo de laboratorio, escribir a máquina, tocar instrumentos musicales, coser o planchar), las de actividad física ligera (caminar en terreno plano 4 a 5km/h, trabajos de sastrería, reparaciones caseras, tareas eléctricas, trabajo de cocina, carpintería, lavar ropa a mano, ir de compras y traer poca mercancía, golf, navegación a vela, tenis de mesa o voleibol), las de actividad física moderada (caminar entre 5,5 y 6,5km/h, trabajos de albañilería, deshierbar, cargar y apilar fardos, fregar pisos, comprar y cargar muchas cosas, pasear en bicicleta, esquiar, jugar al tenis o bailar) y las de actividad física severa (trepar con carga, talar árboles, trabajar con pico y pala, baloncesto, natación, alpinismo o fútbol) y mediante algoritmo matemático calcula las kilocalorías de actividad física diaria habituales.
La calidad de vida se determinó mediante el cuestionario SF-12 adaptado y validado en español48.
La composición corporal se determinó mediante bioimpedanciometría (BIA) con el instrumento Tanita® (Biológica SL), que calcula la masa grasa y masa libre de grasa en valor absoluto y en porcentaje, totales y por segmentos (tronco, miembro superior derecho e izquierdo y miembros inferior derecho e izquierdo). La masa muscular (SM) se calculará mediante la ecuación de Janssen: SM (kg)=(0,401 x [altura2/resistencia]+[3,825 x género] – [0,071 x edad)+5,102), donde la altura se mide en cm, la resistencia en ohmios, para el género los varones puntúan 1 y las mujeres 0, y la edad se contabiliza en años49. La SM absoluta se convertirá en el índice musculoesquelético (SMI), dividiéndola por la altura en metros al cuadrado (kg/m2). Se definió sarcopenia como un SMI igual o menor a 2 desviaciones estándar de la media de la población joven ajustada por sexo50.
La tasa metabólica basal se calculó mediante el instrumento FitMate® (COSMED SRL) de calorimetría indirecta. Se invitó a los participantes a acudir al hospital de día a las 9 de la mañana en ayunas. Tras 15min en reposo sentados en un sillón a temperatura estable de 22°C, respiraron durante 10min a través de una mascarilla específica del instrumento FitMate, para determinar la tasa metabólica basal, el consumo de oxígeno (VO2) y la frecuencia respiratoria51. La función respiratoria se calculó mediante peak-flow meter, tomando el mejor de tres intentos.
Se evaluaron los eventos adversos acontecidos en los últimos 6 meses, incluidas caídas, fracturas, necesidad de hospitalización y visitas a servicios de urgencias.
Criterios de fragilidadSe aplicaron los criterios de fragilidad de Fried6, con alguna pequeña modificación. Pérdida de peso no intencionada igual o mayor a 4,600kg o igual o mayor al 5% del peso corporal en el último año. Debilidad identificada por baja fuerza prensora, menor al percentil 20, ajustada por sexo e IMC, según valores originales de Fried. Baja energía y resistencia, cansancio autorreferido identificado por dos preguntas de la escala CES-D, según original de Fried. Lentitud, mediante velocidad para caminar 4 m, inferior al percentil 20 y ajustado para sexo y altura, según valores originales de Fried. Nivel de actividad física bajo, identificado mediante el cálculo de kilocalorías consumidas semanalmente, según información dada por el paciente mediante el instrumento Calcumed®, en el quintil inferior ajustado por sexo, con puntos de corte originales de Fried. Para que se pudiera construir la variable de fragilidad, fue necesario que los participantes tuvieran valores en al menos 3 de los 5 criterios. Se consideró que los sujetos eran frágiles cuando aparecían 3 o más de ellos, y prefrágiles cuando presentaban 1 o 2.
Variables de resultadoLa principal variable de resultado durante el periodo de seguimiento será la mortalidad por cualquier causa, aunque posteriormente se analizará según su causa. Se considerarán también variables de resultado el cambio de estado desde no frágil a prefrágil o a frágil, la aparición de una nueva discapacidad en la realización de ABVD, o AIVD, o en la movilidad, la hospitalización, las visitas a urgencias, la presencia de caídas y fracturas, la institucionalización o el cambio de domicilio debido a la aparición de discapacidad.
Fuentes de informaciónLa información se recogió mediante entrevista directa única con el participante en las consultas externas de geriatría del Complejo Hospitalario Universitario de Albacete, por parte de cuatro enfermeras entrenadas. Cuando el participante no podía desplazarse, las enfermeras acudieron a su domicilio para obtener la información. La información fue facilitada por el propio participante o por el cuidador principal cuando el primero no podía. Las pruebas de ejecución para evaluar la limitación funcional y la BIA fueron realizadas el mismo día de la entrevista por médicos geriatras, en el hospital de día de geriatría del hospital. La calorimetría indirecta se realizó en el hospital de día de geriatría en un día diferente al de la entrevista, puesto que los participantes debían estar en ayunas, y debía realizarse a la misma hora en condiciones basales. La información clínica de las enfermedades crónicas se obtuvo del historial médico de los sujetos. A todos los participantes que dieron su consentimiento se les realizó una extracción sanguínea para la realización de analítica de rutina que incluía hemograma, perfil bioquímico completo, hormonas tiroideas, hemoglobina glucosilada, velocidad de sedimentación globular y proteína C reactiva. Se congelaron alícuotas de plasma, suero y sangre completa a –80°C para la posterior determinación de biomarcadores.
Aspectos éticosLa investigación ha cumplido con la normativa de Helsinki52 referente al estudio con humanos. El estudio fue aprobado por el comité ético de investigación clínica del Área Sanitaria de Albacete y la comisión de investigación clínica del Complejo Hospitalario Universitario de Albacete. Todos los participantes firmaron consentimiento informado previo a su inclusión en el estudio.
Análisis estadísticoLos resultados que se presentan en este trabajo son la descripción del primer corte efectuado a la cohorte completa. En primer lugar, se realizó un análisis descriptivo de las características de los sujetos de la muestra mediante proporciones, medidas de tendencia central y medidas de dispersión, según la naturaleza de las variables. Se construyó el índice de fragilidad según criterios de Fried6 y se analizará su asociación con discapacidad y comorbilidad.
Se describió la prevalencia de los estratos de fragilidad en la cohorte y posteriormente se aplicará a la población de referencia con su intervalo de confianza del 95%. Para la estimación de los datos en la población de referencia, éstos se ponderarán asignando a cada individuo de la muestra un peso especifico (W), cuyo valor será W=N1/N: n1/n (N es el número total de individuos de la población, N1 es el número de individuos de cada estrato en la población, n es el número total de individuos de la muestra que aceptó participar y n1 es el número de individuos de la muestra que aceptó participar en ese estrato).
Posteriormente, se realizará un análisis bivariante mediante las pruebas de la chi cuadrado, de la t de Student o ANOVA cuando convenga entre las diferentes variables de control y el estado de fragilidad. Se efectuará un análisis con pruebas no paramétricas cuando las variables no cumplan criterios de normalidad. Se realizará un análisis multivariante empleando técnicas de regresión lineal o logística para ajustar las asociaciones por las variables de confusión.
Para la consecución del resto de objetivos, en un futuro se realizarán los siguientes análisis estadísticos.
Para la validación del instrumento SF-LLFDI al español, en primer lugar se analizará la validez de constructo mediante análisis factorial, empleando la metodología de componentes principales basada en el análisis de correlaciones. La idoneidad se probará mediante la prueba de esfericidad de Bartlett y la prueba de adecuación de Kaiser-Meyer-Olkin, se determinarán los componentes principales, así como el porcentaje de la varianza explicada. El modelo se comprobará mediante el análisis de rotación con la metodología Varimax. El supuesto de coherencia interna de las respuestas se evaluará mediante el estadístico alfa de Cronbach. La validez de contenido, se comprobará analizando que las preguntas del SF-LLFDI contienen información sobre aspectos directamente relacionados con la discapacidad y la función. Para la validez convergente, se utilizarán como criterios de referencia el índice de Barthel, el índice de Lawton y 4 pruebas de ejecución, como son la fuerza prensora de la mano dominante, velocidad de la marcha, TUG y SPPB. El grado de correlación entre las puntuaciones obtenidas en el SF-LLFDI y el resto de pruebas funcionales se determinará mediante el coeficiente rho de Spearman. El rendimiento global del SF-LLFDI se calculará a partir de las curvas ROC construidas frente a los principales puntos de corte de las variables de control analizadas y se determinará el mejor punto de corte para cada una, así como los valores de sensibilidad y especificidad. La fiabilidad inter e intraobservadores se examinará mediante el coeficiente de correlación intraclase. Para determinar el efecto techo y suelo del SF-LLFDI, se calculará el porcentaje de sujetos que obtuvieron las puntuaciones máximas y mínimas en cada una de ellas.
Por último, cuando la cohorte tenga un seguimiento mínimo de 3 años, se determinará el riesgo que supone el estado de fragilidad sobre las diferentes variables de resultado mediante análisis de riesgos proporcionales de Cox. Se sustituirá el gasto calórico determinado mediante el instrumento Calcumed por la tasa metabólica basal medida con el calorímetro indirecto, para comprobar si el modelo mejora su poder predictivo. Todos los datos serán almacenados y analizados mediante el programa SPSS 17.0.
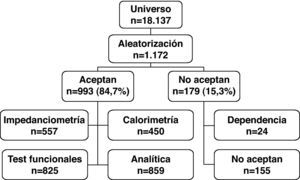
ResultadosLa figura 1 presenta el cronograma del estudio. Sobre un universo de 18.137 personas con edad igual o mayor a 70 años del Censo de Tarjeta Sanitaria de Albacete, se seleccionaron aleatoriamente 1.172. Aceptaron participar 993 (84,7%) y rechazaron participar 179 (15,3%). Los motivos del rechazo fueron una situación de dependencia severa, sin que existiera cuidador principal que firmara el consentimiento informado en 24 casos, mientras que 155 rechazaron su participación de manera activa. De los 993 participantes, se pudieron realizar las pruebas funcionales en 825, se pudo realizar impedanciometría en 557, calorimetría indirecta en 450 y se obtuvo analítica sanguínea en 859.
De los 993 participantes, en 911 (91,7%) se dispuso del dato del criterio de fragilidad de Fried cansancio, en 860 (86,6%) del criterio baja actividad física, en 819 (82,5%) del criterio lentitud, en 935 (94,2%) del criterio pérdida de peso y en 801 (80,7%) del criterio baja fuerza. Los participantes que cumplían cada uno de los criterios de fragilidad fueron 223 (22,5%) para el criterio cansancio, 178 (17,9%) baja actividad física, 302 (30,4%) lentitud, 135 (13,6%) pérdida de peso y 446 (44,9%) baja fuerza.
En 866 (87,2%) participantes se dispuso de 3 o más criterios válidos para determinar el número de sujetos frágiles, prefrágiles y no frágiles. Así, de los 993 participantes, 168 (16,9%) cumplían criterios de fragilidad, 482 (48,5%) fueron prefrágiles, 216 (21,8%) no cumplían ningún criterio de fragilidad y en 127 (12,8%) no se dispuso de 3 criterios para poder determinar su estado. De estos 127 participantes sin datos, 94 tenían un índice de Barthel igual o menor a 60 puntos, por lo que podría presuponerse que son frágiles, aumentando entonces la prevalencia de fragilidad hasta el 26,4%.
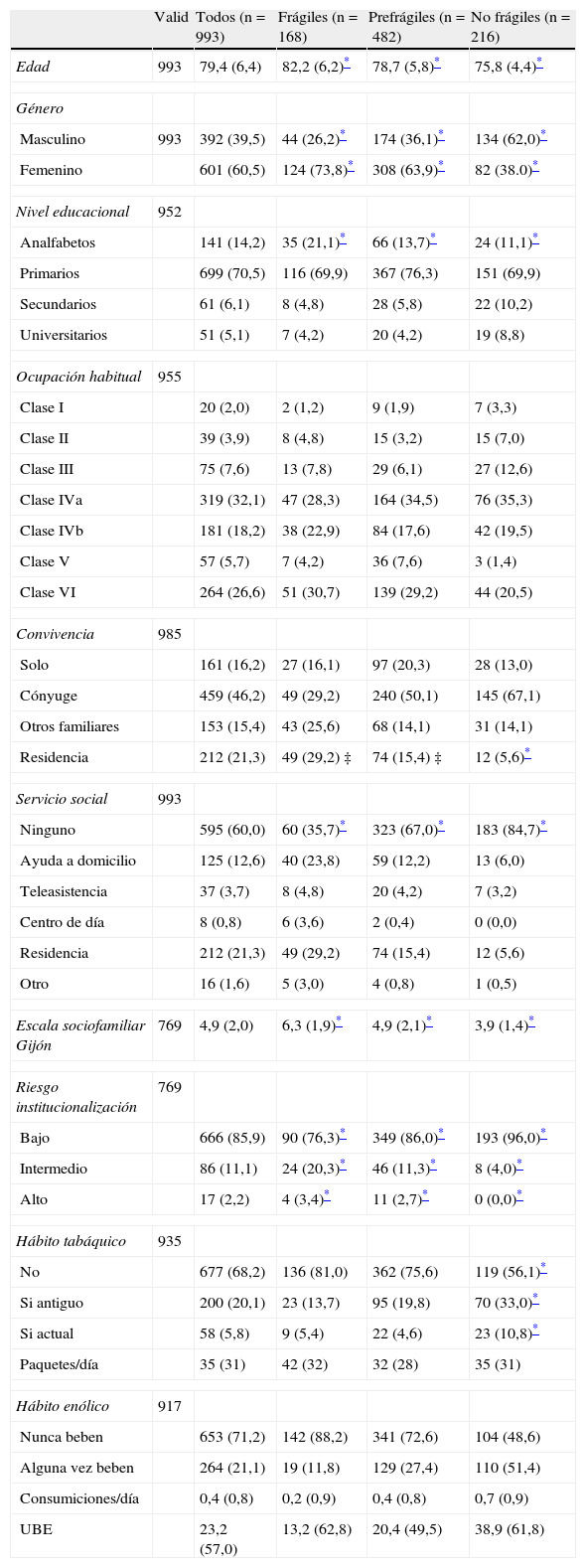
La tabla 1 muestra las características sociodemográficas basales de la muestra global y de los participantes frágiles, prefrágiles y no frágiles. El estado de fragilidad se asoció a mayor edad, género femenino, bajo nivel educacional, institucionalización actual, mayor riesgo de institucionalización y necesidad de ayuda social. No se apreciaron claras diferencias en los hábitos tóxicos ni en la ocupación habitual.
Características sociodemográficas de la muestra
| Valid | Todos (n=993) | Frágiles (n=168) | Prefrágiles (n=482) | No frágiles (n=216) | |
| Edad | 993 | 79,4 (6,4) | 82,2 (6,2)* | 78,7 (5,8)* | 75,8 (4,4)* |
| Género | |||||
| Masculino | 993 | 392 (39,5) | 44 (26,2)* | 174 (36,1)* | 134 (62,0)* |
| Femenino | 601 (60,5) | 124 (73,8)* | 308 (63,9)* | 82 (38.0)* | |
| Nivel educacional | 952 | ||||
| Analfabetos | 141 (14,2) | 35 (21,1)* | 66 (13,7)* | 24 (11,1)* | |
| Primarios | 699 (70,5) | 116 (69,9) | 367 (76,3) | 151 (69,9) | |
| Secundarios | 61 (6,1) | 8 (4,8) | 28 (5,8) | 22 (10,2) | |
| Universitarios | 51 (5,1) | 7 (4,2) | 20 (4,2) | 19 (8,8) | |
| Ocupación habitual | 955 | ||||
| Clase I | 20 (2,0) | 2 (1,2) | 9 (1,9) | 7 (3,3) | |
| Clase II | 39 (3,9) | 8 (4,8) | 15 (3,2) | 15 (7,0) | |
| Clase III | 75 (7,6) | 13 (7,8) | 29 (6,1) | 27 (12,6) | |
| Clase IVa | 319 (32,1) | 47 (28,3) | 164 (34,5) | 76 (35,3) | |
| Clase IVb | 181 (18,2) | 38 (22,9) | 84 (17,6) | 42 (19,5) | |
| Clase V | 57 (5,7) | 7 (4,2) | 36 (7,6) | 3 (1,4) | |
| Clase VI | 264 (26,6) | 51 (30,7) | 139 (29,2) | 44 (20,5) | |
| Convivencia | 985 | ||||
| Solo | 161 (16,2) | 27 (16,1) | 97 (20,3) | 28 (13,0) | |
| Cónyuge | 459 (46,2) | 49 (29,2) | 240 (50,1) | 145 (67,1) | |
| Otros familiares | 153 (15,4) | 43 (25,6) | 68 (14,1) | 31 (14,1) | |
| Residencia | 212 (21,3) | 49 (29,2) ‡ | 74 (15,4) ‡ | 12 (5,6)* | |
| Servicio social | 993 | ||||
| Ninguno | 595 (60,0) | 60 (35,7)* | 323 (67,0)* | 183 (84,7)* | |
| Ayuda a domicilio | 125 (12,6) | 40 (23,8) | 59 (12,2) | 13 (6,0) | |
| Teleasistencia | 37 (3,7) | 8 (4,8) | 20 (4,2) | 7 (3,2) | |
| Centro de día | 8 (0,8) | 6 (3,6) | 2 (0,4) | 0 (0,0) | |
| Residencia | 212 (21,3) | 49 (29,2) | 74 (15,4) | 12 (5,6) | |
| Otro | 16 (1,6) | 5 (3,0) | 4 (0,8) | 1 (0,5) | |
| Escala sociofamiliar Gijón | 769 | 4,9 (2,0) | 6,3 (1,9)* | 4,9 (2,1)* | 3,9 (1,4)* |
| Riesgo institucionalización | 769 | ||||
| Bajo | 666 (85,9) | 90 (76,3)* | 349 (86,0)* | 193 (96,0)* | |
| Intermedio | 86 (11,1) | 24 (20,3)* | 46 (11,3)* | 8 (4,0)* | |
| Alto | 17 (2,2) | 4 (3,4)* | 11 (2,7)* | 0 (0,0)* | |
| Hábito tabáquico | 935 | ||||
| No | 677 (68,2) | 136 (81,0) | 362 (75,6) | 119 (56,1)* | |
| Si antiguo | 200 (20,1) | 23 (13,7) | 95 (19,8) | 70 (33,0)* | |
| Si actual | 58 (5,8) | 9 (5,4) | 22 (4,6) | 23 (10,8)* | |
| Paquetes/día | 35 (31) | 42 (32) | 32 (28) | 35 (31) | |
| Hábito enólico | 917 | ||||
| Nunca beben | 653 (71,2) | 142 (88,2) | 341 (72,6) | 104 (48,6) | |
| Alguna vez beben | 264 (21,1) | 19 (11,8) | 129 (27,4) | 110 (51,4) | |
| Consumiciones/día | 0,4 (0,8) | 0,2 (0,9) | 0,4 (0,8) | 0,7 (0,9) | |
| UBE | 23,2 (57,0) | 13,2 (62,8) | 20,4 (49,5) | 38,9 (61,8) | |
Todos los datos se ‘presentan como media con la desviación estándar entre paréntesis o el número de sujetos con los porcentajes entre paréntesis.
UBE: unidades de bebida estándar; Valid: número de participantes con datos válidos para cada variable.
En este trabajo presentamos el razonamiento, diseño y metodología de la cohorte FRADEA. Las mejoras socioeconómicas, sanitarias y culturales de nuestro país y de los países desarrollados en los últimos 60 años están produciendo un cambio en la tipología de los mayores, con una disminución en la prevalencia de discapacidad53 y una necesidad de permanecer autónomo hasta edades muy avanzadas, con cambios en los estilos de vida y aficiones. Es por ello que la prevención primaria de la discapacidad es una prioridad54,55, que debe abordarse desde la identificación de sujetos en riesgo o en estadios precoces de la misma según el esquema de Verbrugge56 y a través de una metodología de valoración geriátrica avanzada57.
Aunque el término anciano frágil está presente en la literatura especializada desde hace años1-3, es desde 2001 con la publicación del fenotipo de Fried6 cuando la identificación de este estado se hace clínicamente posible. Estudios posteriores identifican al anciano frágil como aquél que es todavía independiente, pero que tiene una vulnerabilidad especial y, por consiguiente, un riesgo aumentado de discapacidad y otros eventos adversos17.
Aunque los criterios de fragilidad han sido aplicados en cohortes norteamericanas6,17, australianas58 o francesas19, hay pocos trabajos en nuestro país que los hayan estudiado. La cohorte de Peñagrande20 en Madrid y la cohorte de Toledo son los dos principales estudios en nuestro medio, cada una con sus objetivos, diseños y conclusiones complementarios. Sin embargo, creemos que el tópico ante el que nos encontramos es de tal relevancia y está llamado a marcar el futuro de la geriatría que merece la pena el diseño de nuevas cohortes que permitan profundizar en aspectos epidemiológicos, diagnósticos o terapéuticos con estos sujetos. Bajo esta premisa, diseñamos la cohorte FRADEA para intentar responder a preguntas como cuál es la prevalencia de la fragilidad en nuestro medio, qué nuevas herramientas nos pueden ayudar a la identificación de estas personas y si el estado de fragilidad se asocia a eventos adversos graves en nuestro medio al igual que lo ha hecho en otros.
La principal fortaleza de nuestro estudio es que la cohorte es de base poblacional, seleccionada mediante muestreo aleatorio estratificado, lo que confiere mucho poder a las conclusiones. La tasa de participación fue muy elevada, del 84,7%, probablemente debida al medio urbano en que nos encontramos, una capital de provincia mediana con mayoritaria afiliación a la seguridad social y fácil acceso a los dispositivos asistenciales sanitarios. El hecho de que el estudio fuera diseñado y conducido desde un servicio de geriatría con una larga tradición de atención a los ancianos de la ciudad, puede también haber facilitado la elevada tasa de participación, así como el modelo de citación, puesto que tras enviar una carta informativa, se contactó telefónicamente con todos los sujetos seleccionados para informarles del estudio y concertar la primera cita. Otra fortaleza es la inclusión por primera vez en nuestro país de ancianos institucionalizados, lo que permitirá identificar la prevalencia y las características de los ancianos frágiles en este medio. Todo el proceso de recogida de datos fue realizado por las mismas cuatro enfermeras entrenadas en la aplicación de cuestionarios, por las dos enfermeras de hospital de día que realizaron la calorimetría y extrajeron las analíticas y por residentes de geriatría que realizaron las pruebas funcionales de observación directa y la impedanciometría, bajo la monitorización del investigador principal que garantizó la exactitud y rigor en este proceso.
Por el contrario, la principal debilidad del estudio radica en que los datos de nuestra población podrían no ser aplicables a los de otras poblaciones españolas. La contestación a esta pregunta podrá derivarse de futuras comparaciones con otras cohortes como la de Peñagrande o Toledo. La cohorte se diseñó para incluir sujetos con edad igual o mayor a 70 años, y no 65 como en otras, porque el cambio fenotípico de los ancianos españoles hace que a los 65 años se sea todavía «joven», y realmente el riesgo de discapacidad aumente exponencialmente a partir de los 70 años actualmente.
La construcción de la cohorte contó con financiación de la Fundación FISCAM, pero dicha financiación sólo garantiza el seguimiento de la cohorte durante 2 años. Sin embargo, el servicio de geriatría buscará nuevas vías de financiación para garantizar el seguimiento de la misma hasta su extinción, o en su defecto usará sus propios recursos humanos para garantizarlo.
Los primeros datos del estudio que se presentan en el trabajo actual ofrecen una prevalencia de fragilidad más elevada que en otras cohortes6,19,20. Ello puede deberse a que nuestra cohorte fue de base poblacional, a que se incluyeron personas institucionalizadas, a que el criterio de edad de entrada fue mayor o a que los puntos de corte de los criterios de Fried no son válidos en nuestro medio y deben adaptarse.
Otro aspecto relevante de nuestros primeros datos es la elevada prevalencia de ancianos institucionalizados en la cohorte, superior al 20%, cuando para este estrato de edad y en nuestra ciudad, se calcula un porcentaje de institucionalización del 10%, ya que casi todas las residencias de la provincia se encuentran en la capital. Pensamos que el sesgo puede haberse derivado de los numerosos errores encontrados durante la aleatorización de los sujetos en el censo de tarjeta sanitaria, y que puede haber penalizado a las personas claramente identificadas en instituciones frente a aquellas no institucionalizadas que podían haber cambiado de domicilio y/o teléfono, o bien a que en las residencias se encuentran mayoritariamente ancianos afiliados a la seguridad social, y menos de otro tipo de compañías sanitarias que no fueron incluidos en nuestra cohorte. Este sesgo nos obligará a hacer un análisis de los datos en dos estratos, aquellos en residencias y aquellos que viven en la comunidad.
No basta con ser excelentes clínicos. Es un mandato que los geriatras nos impliquemos en la investigación básica, epidemiológica y clínica en el campo de la fragilidad, así como en otros aspectos relacionados con la salud de los mayores, para ser auténticos líderes de opinión en el ámbito que nos compete, la atención sanitaria al anciano. Si no lo hacemos nosotros, otros lo harán en nuestro lugar. En concreto en el campo de la fragilidad, son necesarios más trabajos que aporten luz sobre los numerosos interrogantes que quedan por resolver.
FinanciaciónEste trabajo ha sido financiado a través de una ayuda de la fundación FISCAM n.° PI2006/42.
Declaración de conflicto de interesesNo existe conflicto de interés para ninguno de los autores.
Agradecemos a todos los mayores de Albacete que han participado en el estudio FRADEA su desinteresada colaboración.