Mujer de 85 años con antecedentes de hipertensión arterial, dislipemia, demencia de perfil mixto estadio avanzado (Global Deterioration Scale 6, Functional Assessment Staging E), trastorno de ánimo adaptativo y osteoporosis. En tratamiento habitual con colecalciferol, denosumab, memantina y macrogol. Funcionalmente no es capaz de caminar, y es dependiente para todas las actividades básicas de la vida diaria (índice de Barthel 0/100, Functional Assessment Category 0). Está institucionalizada.
Acude a urgencias por dolor abdominal, estable hemodinámicamente y afebril. En la exploración física destaca el abdomen levemente distendido y timpánico, con ruidos conservados, molestias a la palpación difusa, así como edemas en tercio inferior de extremidades.
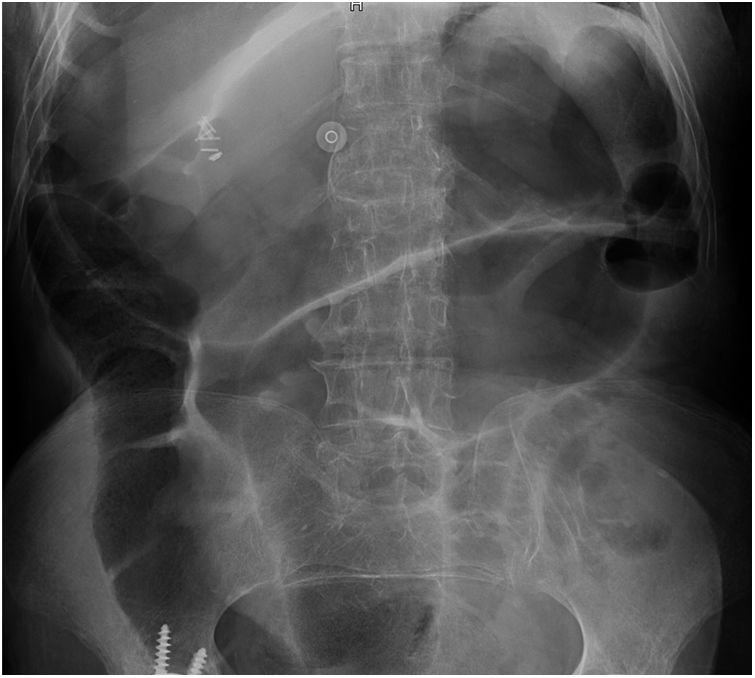
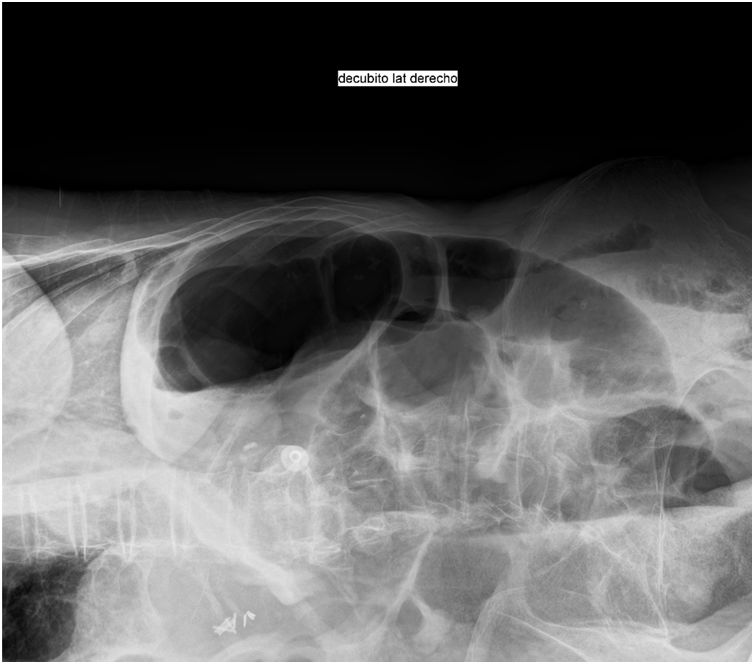
En la analítica de sangre presenta acidosis metabólica moderada con hiperlactatemia severa con cifras de lactato de 9,32mmol/l, patrón de citolisis y elevación de reactantes de fase aguda. En la radiografía de abdomen destaca una imagen sugestiva de vólvulo intestinal (figs. 1 y 2). Se realiza una TAC abdominal objetivándose engrosamiento circunferencial de las paredes de la ampolla rectal sugerente de cambios inflamatorios/isquémicos secundarios a cuadro de seudoobstrucción. Es valorada por los servicios de cirugía general y de medicina digestiva optando por un tratamiento conservador.
Tras el diagnóstico de seudoobstrucción intestinal aguda y probable proceso isquémico secundario se inició tratamiento con enemas 3 veces al día y cobertura antibiótica con ceftriaxona y metronidazol con mejoría clínica y analítica, pudiendo ser dada de alta a los 9 días tras no aparecer incidencias al iniciar tolerancia oral.
En la revisión de la historia clínica previa de la paciente, se objetivaron 3 episodios de seudoobstrucción intestinal en los últimos 5 meses. Una vez descartadas las causas primarias en las pruebas de imagen, se realizó el estudio no invasivo de posibles causas secundarias. Se solicitaron las serologías de citomegalovirus (CMV), virus de Epstein-Bar (VEB) y virus herpes simple (VHS). La IgM fue positiva para CMV y la carga viral fue mayor a 1.000 copias, iniciándose tratamiento con valaciclovir 1.000mg/cada 12h/durante 15 días. Cinco meses más tarde la paciente continúa clínicamente estable y sin nuevos episodios de seudoobstrucción.
El síndrome de Ogilvie o seudoobstrucción intestinal aguda, se caracteriza por una dilatación aguda del colon en ausencia de una obstrucción mecánica asociada1–4. El mecanismo fisiopatológico exacto por el que se produce continúa siendo desconocido, pero la evidencia actual sugiere una alteración en la regulación del sistema nervioso autónomo del colon2–6.
Suele ocurrir en pacientes hospitalizados o institucionalizados en el contexto de un evento agudo. Entre las principales causas se encuentran las farmacológicas (opioides, anticolinérgicos, antipsicóticos...), las alteraciones hidroelectrolíticas y las cirugías abdominales, traumatológicas y ginecológicas2,4. Entre las causas menos comunes destacan las enfermedades neurológicas (enfermedad de Parkinson), las autoinmunes (esclerodermia, lupus eritematoso...), su manifestación como síndrome paraneoplásico (carcinoma microcítico de pulmón, timoma...) y las causas infecciosas (CMV, VEB, VHS, virus herpes zóster [VHZ], virus JC)3,5,6.
Se han descrito pocos casos en la literatura de síndrome de Ogilvie secundarios a infección por CMV, y la mayoría en pacientes inmunodeprimidos4. Su relación con infecciones virales agudas fue establecida en primer lugar con el VHZ y posteriormente con el virus de la varicela7,8.
El mecanismo de acción de dichos virus en la génesis de la seudoobstrucción intestinal no está claro4,7–9. Existen 2 hipótesis específicamente con la infección por VHZ: en primer lugar a través de la infección de las neuronas motoras de la región anterior de la médula espinal o del plexo celíaco afectando al sistema nervioso autónomo extrínseco8,9. El segundo a través de un desequilibrio en la inervación autónoma intrínseca del colon, ya sea directamente a través de la infección del plexo mientérico o indirectamente a través de inflamación contigua, lo que podría aumentar el impulso simpático favoreciendo así el cuadro obstructivo8–10.
El diagnóstico se realiza a través de la biopsia de las lesiones mediante colonoscopia. En nuestro caso no se realizó colonoscopia dada la situación basal de la paciente. Sin embargo, su diagnóstico se apoya por la presencia de IgM CMV en sangre con carga viral elevada y por la ausencia de nuevos episodios de seudoobstrucción tras el tratamiento con ganciclovir.
La etiología infecciosa en la seudoobstrucción intestinal no es frecuente, pero es una causa reversible con tratamiento médico adecuado, por lo que debe plantearse en el diagnóstico diferencial ante episodios recurrentes.