En el grupo estudiado fue frecuente el uso de sedantes y la presencia de sedación profunda, el midazolam y el fentanilo fueron los fármacos más usados. El uso de BNM podría asociarse de forma independiente a una mayor mortalidad.
First of all, and as an introduction, this review of scientific literature offers information on therapeutic education for the person with diabetes and his/her family members, as well as the concept of nutritional dietary education. Secondly, it reviews the current approach to treating diabetes mellitus type 1 either with therapy with multiple doses of insulin (MDI) or with continuous subcutaneous insulin infusion (CSII), their relation with the most liberalized food plan since they allow the dosage of pre-prandial insulin to be better adapted to the intake of carbohydrates (CH), and also offering aspects related with adhesion to dietetic monitoring. Lastly, in the third place, the bases and characteristics of the CSII therapy and specific learning that people with diabetes and their family members have to do basically focusing on the differential aspects in relation with the food plan with respect to the MDIs are explained. CSII therapy can offer more dietary flexibility than any other form of treatment, although in order to optimize the infusers benefits, the patient not only has to learn to estimate the amount of CHs, but also other nutrients like the amount of fat or fibre that can interfere in their absorption.Introducción: la educación terapéutica en la diabetes
La diabetes es una enfermedad crónica que requiere atención médica continuada y educación terapéutica para poder prevenir las complicaciones agudas y reducir el riesgo de complicaciones crónicas1.
La educación terapéutica2,3 es una atención centrada en la persona con diabetes que parte de sus necesidades, recursos, valores y estrategias. Permite a los pacientes mejorar sus conocimientos, habilidades y actitudes. Pretende mejorar la calidad de vida y la adherencia al tratamiento con una reducción de las complicaciones agudas y crónicas relacionadas con la diabetes. La parte más compleja de la educación terapéutica se produce quizá cuando los pacientes deben cambiar su comportamiento.
Centrados en el tema de la alimentación como parte fundamental del tratamiento de la diabetes, la educación dietético-nutricional4 es el conjunto de intervenciones dirigidas a modificar los conocimientos, habilidades, actitudes y comportamientos, tanto individuales como de grupos y poblaciones, en vista a mejorar y racionalizar sus hábitos alimentarios.
Las dificultades para modificar los comportamientos alimentarios son de orden social, cultural y familiar, aspectos que se han de considerar al pactar un plan de alimentación a una persona con diabetes.
Enfoque actual del tratamiento de la diabetes mellitus tipo 1
El enfoque actual del tratamiento de la diabetes mellitus tipo 1 (DM1) está basado principalmente en el estudio DCCT (Diabetes Control and Complications Trial)5 diseñado para valorar el efecto del control metabólico en la aparición y la gravedad de las complicaciones microvasculares. Este estudio demostró claramente que el tratamiento intensivo de la diabetes, sea con múltiples dosis de insulina, 3 o más inyecciones diarias (MDI) o con la infusión de insulina continua subcutánea (ISCI), es esencial para poder mejorar el control metabólico de las personas con DM1. En el momento del estudio se utilizaba insulina humana de acción rápida y lenta. A pesar de los importantes resultados del estudio DCCT en la reducción de complicaciones microvasculares, la terapia intensiva de insulina conllevó un aumento notable de la hipoglucemia grave (62 episodios/100 pacientes-año de tratamiento). En la actualidad se han desarrollado nuevas insulinas: análogos de insulina rápida y lenta6,7 que se han diseñado para que la administración de la insulina sea más "fisiológica" en su farmacocinética y farmacodinamia; la administración de esta insulina se relaciona con la aparición de una menor cantidad de hipoglucemias a igualdad de control metabólico. Actualmente se recomienda en la terapia de la DM1 las siguientes premisas: a) uso de múltiples inyecciones de insulina con MDI (3-4 inyecciones diarias de insulina preprandial y basal) o terapia ISCI, y b) la adecuación de la insulina preprandial según la ingesta de hidratos de carbono (HC), el control glucémico y la previsión de actividad física. La terapia intensiva y la incorporación de dichos análogos de insulina tienen implicaciones dietéticas importantes ya que permiten una mayor flexibilidad y libertad dietética8-11.
Aunque muchos estudios han intentado identificar la mejor distribución de macronutrientes para la alimentación de la persona con diabetes, no hay evidencias de que una distribución sea mejor que otra12. La recomendación de nutrientes para las personas que padecen diabetes es la alimentación saludable, al igual que para cualquier otra persona adulta sin diabetes: el 45-60% del total de la energía para mantener un peso adecuado en forma de HC; el 30-35% en forma de grasa, y el 10-20% en forma de proteínas.
Sin embargo, existen algunos aspectos diferenciales en la diabetes:
- La ingesta de ácidos grasos saturados debe ser inferior al 7% del total de calorías, y la de ácidos grasos trans debe reducirse al mínimo. Asimismo, debe limitarse la ingesta de colesterol dietético a menos de 200 mg/día. Además, se recomienda asegurar dos o más porciones de pescado por semana (con la excepción de los filetes de pescado frito comercial) para proporcionar ácidos grasos poliinsaturados omega-3.
- En referencia a la ingesta de HC, la American Dietetic Association1,12 recomienda con un nivel de evidencia A (máxima evidencia) que en los tratamientos con MDI o ISCI el control de los HC (sea por recuento de carbohidratos, intercambios por raciones o mediante experiencia basada en la estimación) sigue siendo una estrategia clave para lograr un mejor control glucémico. Un aprendizaje básico, por lo tanto, debe ser que los pacientes aprendan a ajustar la dosis de insulina preprandial según el contenido de HC de la comida o suplemento que realiza.
- El uso de índice glucémico y carga glucémica puede proporcionar un modesto beneficio adicional para el control glucémico, más que el observado cuando sólo se controla el total de HC (nivel de evidencia B). En la práctica habitual este aspecto es difícil de seguir durante el tratamiento con MDI; sin embargo, la terapia ISCI podría considerarlo de una forma más práctica mediante diferentes tipos de suministro de insulina preprandial (véase el apartado específico de la terapia ISCI del presente artículo).
- Si el paciente realiza ejercicio físico planificado, es necesario reducir la dosis de insulina para evitar hipoglucemias. Para ejercicios no planificados la ingesta de alimentos ricos en HC puede ser necesaria. Aunque el aporte depende de varias variables, como el control previo de glucemia, la insulina activa, la duración y la intensidad del ejercicio, una aproximación inicial puede ser para una persona de 70 kg, que debe tomar entre 15 y 20 g de HC por hora durante una actividad moderada.
- Si el paciente puede tomar alcohol, el consumo ha de ser moderado. La recomendación de ingesta máxima de alcohol diaria es de 1 bebida para las mujeres (equivalente a 250 ml de cerveza, 125 ml de vino o 40 ml de alcoholes destilados) y 2 bebidas para los varones. Si se toma alcohol, para reducir el riesgo de hipoglucemia nocturna el paciente debería hacerlo durante las comidas, y si lo toma en ayunas, debería acompañarlo de alguna fuente de HC, valorando además la posibilidad de hacer cambios en la actividad física. Es especialmente importante trabajar este aspecto en personas jóvenes en las salidas nocturnas.
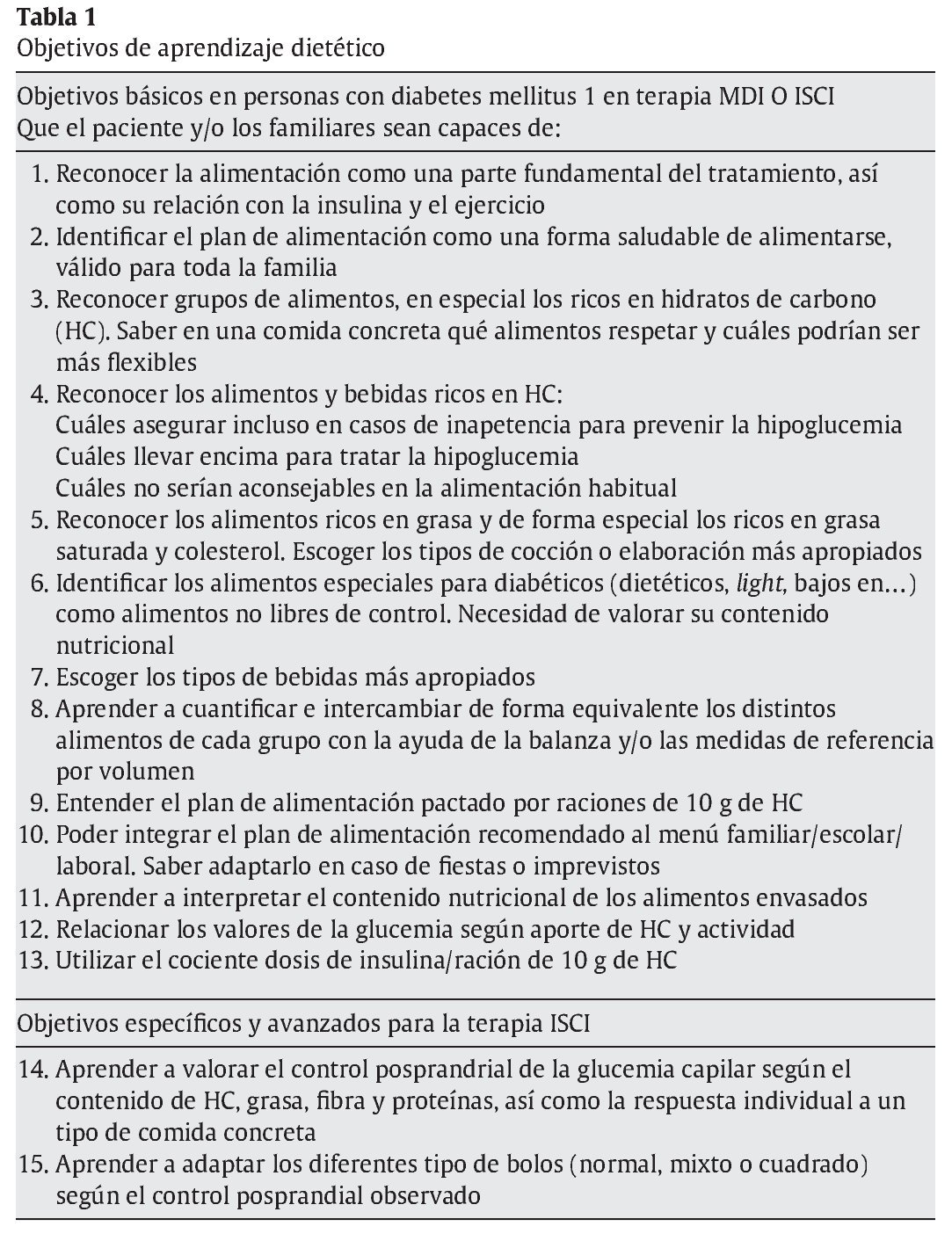
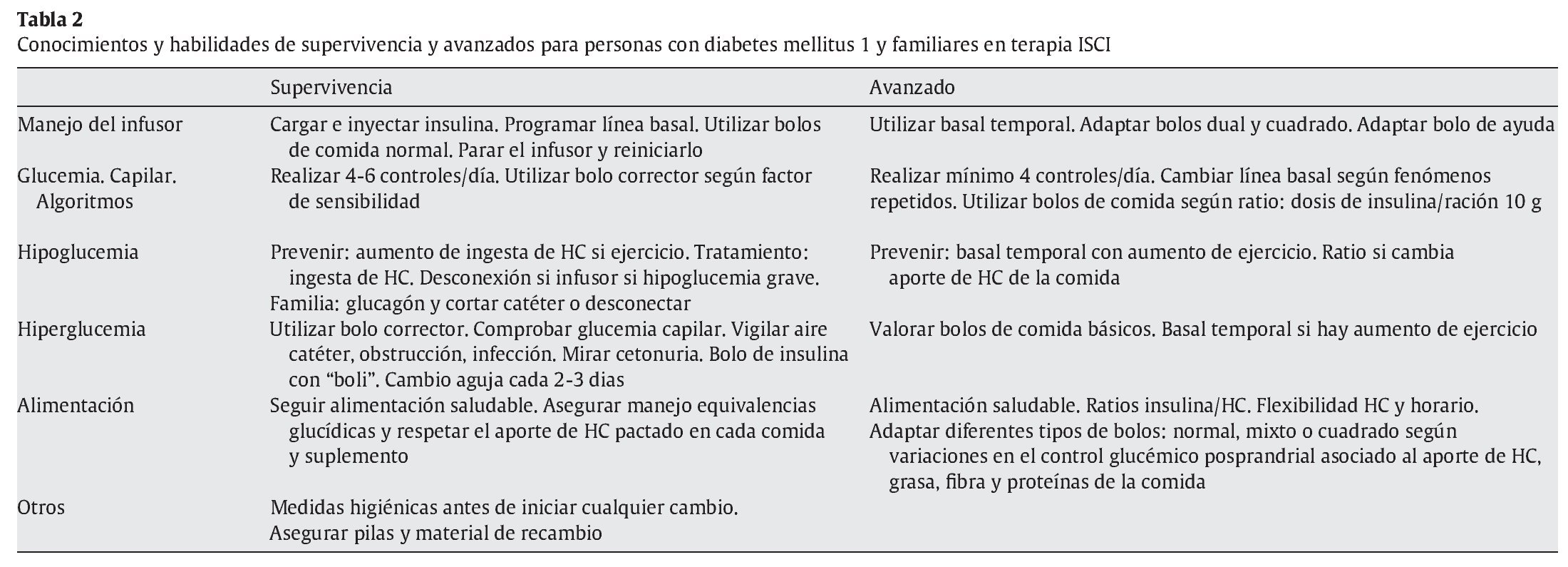
El enfoque actual del tratamiento de la DM1 se centra en liberalizar el aporte y la distribución de HC mediante educación terapéutica, lo que permite una mejor calidad de vida de la persona con diabetes. Este aspecto plantea un reto tanto para el paciente y su familia como para el equipo de salud que lo atiende. Para realizar esta tarea se debe dominar muy bien el autocontrol de la terapia intensiva, la estimación del consumo de HC y el ajuste de dosis en cada ingesta. Los programas educativos estructurados que integren la alimentación en el contexto educativo total del paciente y su familia13-19 es, por lo tanto, una necesidad. Dichos programas deben facilitar de manera especial los conocimientos y habilidades sobre las bases de la terapia intensiva en la diabetes, la alimentación (consejos de alimentación saludable, sistemas de cuantificación de HC, etc.), el concepto de ratio individual insulina/hidratos de carbono (I/HC) y los ajustes de la dosis de insulina según la glucemia capilar, el aporte de HC y la previsión de actividad física. En la tabla 1 pueden observarse los objetivos de aprendizaje dietético básicos y comunes en personas en terapia con MDI o ISCI, así como aquellos específicos y de nivel avanzado para la terapia ISCI. En la figura 1 se observa el soporte fotográfico para estimar el aporte de HC y las equivalencias glucídicas.
Figura 1. Equivalencias de alimentos ricos en hidratos de carbono. Equivalencia de aproximadamente 10 g de hidratos de carbono por ración.
El estudio DAFNE20 (Dose Adjustment for Normal Eating) es un ejemplo de programa educativo estructurado. Este programa demostró que los pacientes pueden aprender a utilizar la glucemia capilar para ajustar mejor la insulina a la ingesta de HC, y poder así liberalizar su ingesta. La estrategia de liberalizar la dieta demostró que, además de ser útil para mejorar el control de la glucohemoglobina (HbA1c) sin aumentar el riesgo de hipoglucemias graves, puede mejorar la percepción de calidad de vida, la satisfacción con el tratamiento y el bienestar psicológico, a pesar del mayor número de inyecciones de insulina y mediciones de la glucemia capilar. Asimismo, el estudio demostró que los pacientes se adherían mejor al seguimiento dietético.
La adherencia al tratamiento de la diabetes21 resulta crucial y es una variable de medida de las intervenciones en la educación terapéutica, de ahí el interés para todos los educadores en diabetes. La Organización Mundial de la Salud (OMS), como muy bien defiende, indica que la adherencia al tratamiento no es una responsabilidad exclusiva del paciente22, sino que es un fenómeno multidimensional determinado por la acción recíproca de un conjunto de factores relacionados con el paciente (los tratamientos, las enfermedades), los factores sociodemográficos y el sistema de salud. En relación con el sistema de salud, el acceso al medicamento y la asistencia, la comunicación al paciente o el profesional y la educación terapéutica estructurada son factores determinantes en dicho proceso. Por lo tanto, es importante evaluar la adherencia a los diferentes componentes del tratamiento23 de forma independiente: la glucemia capilar, la administración de insulina, la alimentación, la actividad física, el autoanálisis, autocontrol, revisiones, etc. En este sentido, hay que tener en cuenta que una persona puede adherirse bien a la administración de insulina, pero parcialmente a los controles glucémicos y no adherirse al seguimiento dietético, hecho que demuestra que la adherencia no es unidimensional. Por lo tanto, hay que considerar la adherencia a la diabetes según diferentes aspectos del tratamiento, tanto farmacológico como no farmacológico, así como a las técnicas de autoanálisis y autocontrol. Además, hay que valorar si la falta de adherencia es intencional o no intencional ya que las estrategias de mejora pueden ser diferentes.
La adherencia al seguimiento dietético es muy variable según el programa seguido, tal y como se desmuestra en distintos estudios publicados: en el estudio DAWN23, realizado en 13 países, se demostró una adherencia general a la dieta de un 39%, en el estudio de Carvajal et al24, realizado en Cuba, fue de un 25%; en Estados Unidos, Wing et al25 hallaron una adherencia de un 30%, mientras que Toljamo et al26, en Finlandia, demostraron una adherencia del 70%, y Christensen et al27, un 60% de adherencia al número de comidas y horarios y un 10% de falta de adherencia a los intercambios equivalentes. Cabe decir que algunos de dichos resultados no están en el contexto del enfoque actual del tratamiento de la DM1, el cual permite una mayor flexibilidad dietética favoreciendo la adherencia20.
Otro aspecto a valorar en el seguimiento dietético es la conducta alimentaria y la manipulación de las dosis de insulina para controlar el peso corporal. Polonsky et al28 demostraron que el 31% de las mujeres admitieron omitir de forma intencionada las dosis de insulina; en el 9% como estrategia para no ganar peso. Brayden et al29 hallaron también datos parecidos, concluyendo que el 30% de las adolescentes (ningún jóven varón en la muestra) admitieron disminuir las dosis de insulina para controlar el peso corporal. En este sentido, cabe destacar que en 2008 Takii et al30 demostraron que la falta de adherencia a la insulina y la duración de la omisión de dosis en pacientes con trastornos de la conducta alimentaria es el factor más firmemente ligado a la aparición de retinopatía y neuropatía, y Giménez et al31 demostraron en 2008 que la conducta alimentaria anómala en jóvenes trasladados de centros pediátricos se asociaba con un peor control metabólico.
Cuando la adherencia al seguimiento dietético no es correcta, es necesario valorar si dicha falta de adherencia es intencional o no. Si no es intencional, puede deberse a falta de individualización del plan de alimentación, falta de educación terapéutica y/o problemática sociofamiliar o motivacional32. Si es intencional y se acompaña de omisión de dosis, hay que descartar trastornos de la conducta alimentaria, especialmente en mujeres jóvenes.
Aspectos diferenciales de la terapia con infusión continua subcutánea de insulina
Como se ha descrito en el apartado anterior, la terapia ISCI se utilizó en el estudio DCCT en los años ochenta-noventa, pero no fue hasta el año 2000 que se empezó a utilizar de manera general en España debido, básicamente, a la mejora técnica de los infusores y al sistema público de financiación.
¿Qué perfil de pacientes es candidato para la terapia con ISCI?
Las agencias reguladoras recomiendan este tipo de terapia sólo para los pacientes con DM1 que no consiguen un buen control metabólico de la diabetes a pesar de las MDI y un buen manejo del autocontrol diario.
A título de ejemplo se exponen las indicaciones contempladas por la Conselleria de Salut de la Generalitat de Catalunya33, una de las primeras comunidades autónomas que empezó a financiar la terapia ISCI en el año 2000:
1. Deficiente control metabólico con tratamiento con MDI y valores de HbA1c > 7,5%.
2. Embarazo o su planificación.
3. Hipoglucemias graves muy frecuentes o asintomáticas.
4. Horarios de comida variables o imprevisibles.
5. Dificultad de control glucémico durante el periodo nocturno (fenómeno del alba).
6. Complicaciones crónicas de evolución acelerada.
7. Alergia o lipodistrofia secundaria a la inyección de insulina.
8. Requerimientos bajos de la dosis de insulina.
Para que un centro sanitario pueda ser acreditado para realizar este tipo de terapia, se necesita una serie de requisitos: atención de un equipo interdisciplinario, acceso durante las 24 horas para posibles emergencias y una adecuada atención en educación terapéutica para que el paciente y su familia puedan adquirir los conocimientos, las habilidades y el soporte necesario para llevar a cabo el nuevo autocontrol del tratamiento. Diversos estudios han demostrado que la terapia ISCI puede mejorar el control metabólico y la calidad de vida de las personas con DM133,34.
¿Cómo funcionan los infusores de insulina?
Los infusores de insulina35,36 son unos instrumentos del tamaño de un buscapersonas que permiten la infusión continua de insulina vía subcutánea. Pueden administrar insulina rápida (Actrapid®) o, bien, análogos de insulina rápida aspártica (NovoRapid®), lispro (Humalog Lispro®) o glulisina (Apidra®). No existen cargas de insulina para estos instrumentos, sino que es el propio paciente quien debe rellenar las cargas del infusor con insulina mediante un vial o boli de insulina. El catéter que se inserta vía subcutánea hay que cambiarlo cada 3 días. Actualmente en el mercado español hay tres modelos de infusores (fig. 2). El suministro de insulina se puede realizar de dos formas:
Figura 2. Modelos de infusores de insulina disponibles en España (2009). ACCU-CHEC Spirit (Roche), Animas 2020 (Animas) y Paradigm (Minimed).
1. Línea basal o cantidad de insulina que se programa y se administra de manera continua con el infusor, así se cubren las necesidades basales de insulina y se controla su producción endógena. La dosis de esta línea basal puede ser diferente cada hora, así se puede configurar y programar una línea basal continua según las necesidades individuales de cada paciente en particular. Esta línea basal puede admistrar entre 0,05 y 2 unidades de insulina por hora. Un mismo infusor puede tener varias líneas basales programadas (días festivos, turnos de trabajo distintos, etc.).
2. Bolo de comida o unidades de insulina que el paciente se administra antes de cada comida y/o suplemento en función de las raciones de HC que desee comer intentando controlar las glucemias posprandiales. Por lo tanto, es muy importante que el paciente aprenda a estimar la cantidad de HC que ingerirá para adaptar su bolo. Es muy importante que estos pacientes dominen bien el sistema de intercambio de raciones de 10 g de HC o cualquier otro sistema de recuento de HC. Hay varios sistemas para ajustar los bolos de comida iniciales:
- Regla del 500. Este sistema nos indica los gramos de HC que cubre 1 unidad de insulina. Se calcula dividiendo el sumatorio (å) de insulina de 24 horas entre el sumatorio (å) de raciones de HC 24 horas. Este sistema se utiliza poco en la práctica diaria.
- Ratio insulina/HC. Indica la cantidad de insulina para cubrir 1 ración de 10 g de HC. Para personalizar este ratio habría que tener en cuenta básicamente tres factores: la cantidad de análogo de insulina rápida que se utiliza antes de las comidas; el aporte de HC que se hace en una comida determinada, y el valor de glucemia capilar preprandial y posprandial. Para empezar, se parte de la dosis de insulina que cada persona utiliza en cada desayuno, comida y cena, asegurando que se ha entendido: número de raciones de 10 g de HC programado en cada toma. Para comprobrar que se ha personalizado correctamente la ratio, es necesario comprobar el valor de glucemia capilar antes y después (2 h) de cada ingesta durante varios días. Si se comprueba en varias ocasiones que una persona en el desayuno necesita 10 unidades de insulina y 5 raciones de HC, su ratio en el desayuno será de 2 unidades por cada ración. Si una vez adaptada la ratio, el paciente varía el aporte de HC, deberá variar la insulina acorde con esta ratio. Es necesario individualizar las ratios para el desayuno, la comida y la cena. En la mayoría de las personas la ratio del desayuno es superior a la de la comida o la cena.
3. Bolo corrector o unidades de insulina extra que el paciente puntualmente puede administrarse según el control glucémico y el factor de sensibilidad a la insulina (mg/dl de glucemia que disminuye una unidad extra de insulina). Este factor de sensibilidad a la insulina se calcula para cada paciente en función de la dosis total requerida en 24 horas. La fórmula para su cálculo es: 1.800 dividido entre el sumatorio (å) de la dosis total de insulina en 24 horas.
4. Basal temporal, que es la cantidad de insulina que el paciente puede aumentar o disminuir de forma temporal sobre su línea basal programada. Esta función es especialmente útil frente a cambios en la actividad física.
5. Bolo ayuda. Algunos modelos de infusores tienen esta función integrada dentro del mecanismo del propio infusor, mientras que en otros es externo. Es una prestación de ayuda a la decisión que permite grabar la información individual del paciente sobre:
- El factor de sensibilidad a la insulina, es decir, los miligramos de glucosa que descienden con una unidad extra de insulina.
- La ratio: dosis de insulina/10 g de HC que el paciente requiere; se pueden gravar distintas ratios para el desayuno, la comida y la cena si fuera necesario.
- La insulina activa. La función de bolo de ayuda tiene en cuenta la insulina que pudiera estar activa desde el último bolo inyectado (estimación de 4 h de duración).
Ejemplo práctico del funcionamiento del bolo de ayuda: con tres datos arriba mencionados, si el paciente añade el valor de glucemia, el bolo de ayuda le pregunta si quiere o no comer y cuántas raciones desea ingerir. La máquina puede indicar una dosis de insulina correctora en función de la concentración de glucosa en sangre y la dosis correspondiente de HC que se pretende ingerir, teniendo en cuenta en el cálculo de la dosis final la insulina que todavía pudiera estar activa si el paciente hace menos de 4 h que se ha inyectado el último bolo. El bolo de ayuda, como su nombre indica, es sólo una propuesta de ayuda a la decisión, aunque es el propio paciente quien decide si acepta o no la propuesta de bolo a inyectar. Se han publicado estudios sobre la efectividad en la utilización de este tipo de bolo37.
6. Diferentes líneas basales programadas. Poder tener varias líneas basales programadas es especialmente útil para los pacientes con turnos de trabajo diferentes, o cambios importantes de actividad entre fines de semana y laborables o, por ejemplo, mujeres que experimentan diferentes perfiles glucémicos durante el periodo u ovulación, etc.
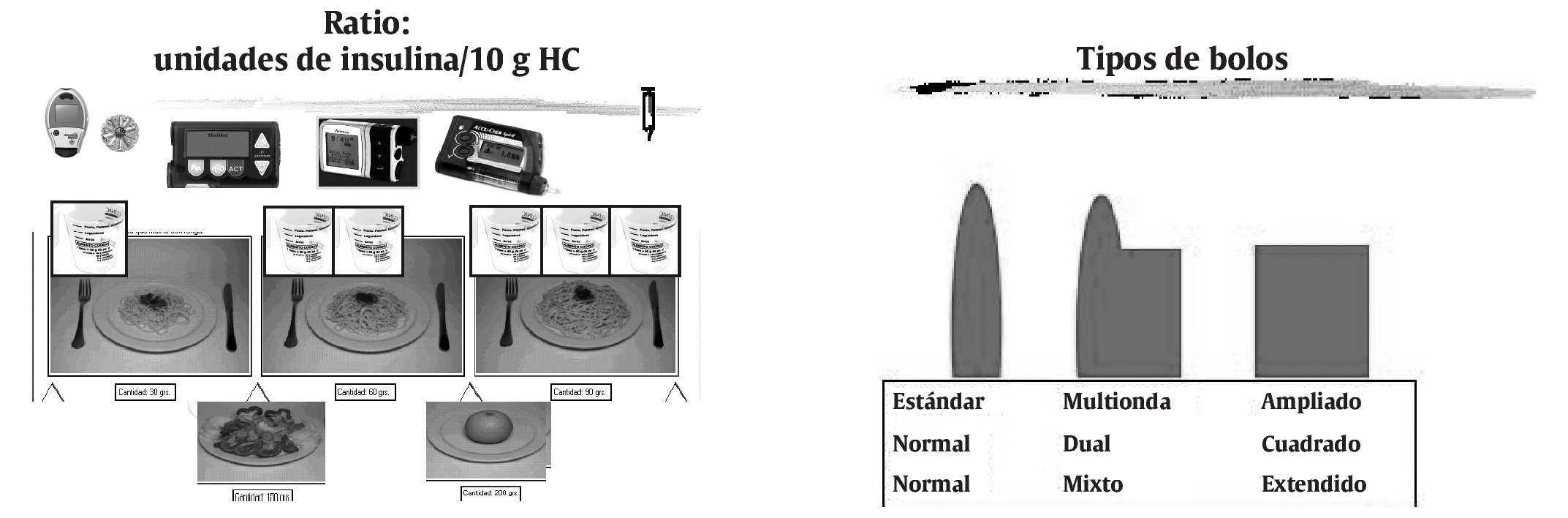
7. Diferentes formas de administar los bolos (fig. 3). Los infusores pueden administrar los bolos de tres formas diferentes:
Figura 3. Flexibilidad dietética con la utilización de la ratio y distintos tipos de bolos.
- Bolo "normal", denominado también "estándar", que tiene una cinética de acción insulínica idéntica a la administrada con una jeringa convencional y/o bolígrafo de insulina. Este bolo está indicado en comidas con alto contenido en HC y poca grasa o proteínas. Por ejemplo: patatas al horno, bocadillo, etc.
- Bolo de forma "cuadrada" o denominado también "expandida" o "ampliada". El paciente puede decidir que la insulina del bolo de una comida se suministre más lentamente (por ejemplo, durante 3 o 4 h). Este tipo de suministro está especialmente indicado en comidas largas y con alto contenido en grasa y proteínas que pueden retrasar la absorción de los HC como, por ejemplo, un cocido de lentejas con verduras. También está indicado en personas con digestiones muy lentas, como es el caso de los pacientes que sufren gastroparesias.
- Bolo "dual", denominado también "mixto" o "multionda". Se suministra una parte de la insulina del bolo de forma normal y otra parte de forma cuadrada. Está especialmente indicado en comidas con alto porcentaje de HC, proteínas y grasa como, por ejemplo, paella o pizza.
Se puede observar que las personas con diabetes que inician terapia ISCI necesitan aprender nuevos conceptos, habilidades y actitudes para poder integrar la nueva terapia a su vida cotidiana. El aprendizaje debe permitir:
- Conocer las bases del tratamiento ISCI.
- Adquirir habilidad en preparar el infusor e inyectar el catéter de insulina, y prevenir infecciones cutáneas.
- Seguir una alimentación saludable; adaptar el plan de alimentación mediante la ratio y establecer el tipo de bolo y la forma de infusión.
- Utilizar algoritmos de modificación de pauta: línea basal y bolo.
- Mejorar el control metabólico, y prevenir factores de riesgo vascular.
- Integrar el nuevo tratamiento a la vida cotidiana.
- Mejorar la percepción de calidad de vida.
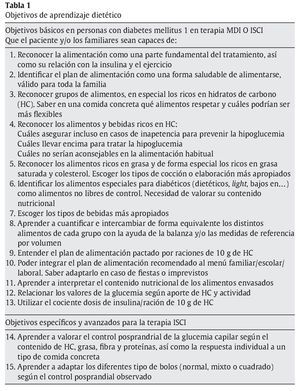
Los pacientes que inician terapia ISCI deberán realizar programas educativos estructurados que les ayuden a adquirir estos nuevos conocimientos38,39. En este sentido, es primordial diferenciar los objetivos educativos que son imprescindibles para el inicio de la terapia de aquellos que se pueden ir adquiriendo para optimizar sus resultados (tabla 2).
Adaptación dietética en la terapia ISCI
La flexibilidad dietética que nos proporciona la terapia ISCI es considerable; sin embargo, para realizarla correctamente se tiene que valorar inicialmente si el paciente ha adquirido los objetivos 1-11 de aprendizaje básico común de toda persona que tiene diabetes tipo 1 o 2 tratada con MDI (tabla 1). Las premisas para introducir el nuevo aprendizaje son tener un manejo básico de las equivalencias de 10 g de HC, seguir un plan de alimentación saludable, estar motivado, tener habilidad para el cálculo y tener habilidad para interpretar las etiquetas nutricionales de los alimentos envasados. El nuevo aprendizaje se basa en reforzar los objetivos 1-12 según se detallan en la tabla 1 y recalcular el objetivo 13. Una vez adaptadas las ratios desayuno-comida-cena (habitualmente se tarda 1 o 2 meses), se deberán introducir los objetivos 14 y 15 que son los avanzados y específicos de la terapia ISCI (tabla 1).
Aprender a valorar el control posprandial de la glucemia capilar según el contenido de HC, así como el contenido de grasa, fibra y proteínas y la respuesta individual de cada comida, y aprender a adaptar los diferentes tipo de bolos (normal, mixto o cuadrado), según el control posprandial, son dos aspectos fundamentales a tener en cuenta durante la educación de estos pacientes40.
Conclusiones
La terapia intensiva en la DM1, sea con MDI o ISCI, tiene implicaciones dietéticas importantes ya que permite una mayor flexibilidad y libertad dietética.
En referencia a la ingesta de HC, la American Diabetes Association (ADA)1,12 recomienda, con un nivel de evidencia A (máxima evidencia), que en los tratamientos con MDI o ISCI el control de los HC (sea por recuento de carbohidratos, intercambios por raciones o mediante experiencia basada en la estimación) sigue siendo una estrategia clave para lograr un mejor control glucémico. Por lo tanto, un aprendizaje básico debe ser que los pacientes aprendan a ajustar la dosis de insulina preprandial según el contenido de HC de la comida o suplemento que realiza.
La (ADA)1 considera, con un nivel de evidencia B, que el uso del índice glucémico y la carga glucémica para todas las personas con diabetes puede proporcionar un modesto beneficio adicional para el control glucémico, en comparación con el observado cuando sólo se tiene en cuenta la cantidad total de hidratos de carbono por sí solo. En la práctica habitual este aspecto es difícil de seguir durante el tratamiento con MDI; sin embargo, la terapia ISCI podría considerarlo de una forma más práctica, ya que utiliza diferentes tipos de suministro de insulina preprandial (bolo normal, mixto o expandido). Un aprendizaje básico, por lo tanto, debe ser que los pacientes aprendan a ajustar la dosis de insulina preprandial y el tipo de bolo según el contenido de HC, el índice glucémico o la cantidad de grasa y proteínas de la comida o suplemento que realiza.
Las nuevas tecnologías aplicadas a la diabetes, como los sensores de lectura continua de glucosa, nos aportan información para determinar ciertos patrones de comportamiento posprandial en función del tipo de alimento y el condimento ingerido. Un ejemplo es el estudio de Jones et al41 en el cual se comprueba que en la ingesta de pizza la mejor forma de administrar el bolo es la mixta con la fase extendida durante 8 h. De esta forma, se aporta un menor pico hiperglucémico posprandial sin aumentar el riesgo de hipoglucemia. Otro ejemplo es el de O'Connell et al42, que han publicado recientemente un estudio en niños con DM1 cuyo bolo mixto fue el más indicado en comidas con un índice glucémico bajo para optimizar el control posprandial. Probablemente los nuevos sistemas de medir la glucosa de manera continua nos aportarán estrategias de mejora del control posprandial individual y harán variar algunas de las recomendaciones aceptadas actualmente.
Promover la flexibilidad dietética en personas con DM1 en tratamiento con MDI o ISCI, con la utilización de las ratios (dosis de insulina/ración de 10 g de HC), requiere una educación terapéutica específica del paciente y su familia. Esto implica que los profesionales del equipo de diabetes deben estar en continua actualización y deben adherirse a las guías clínicas actuales, las cuales promueven la flexibilidad dietética en el contexto de una alimentación equilibrada.
Agradecimientos
Quisieramos agradecer a las personas con diabetes tipo 1 en terapia con MDI o ISCI que siguen tratamiento en el Hospital Clínic, así como a los diferentes miembros del equipo de diabetes, de manera especial a: Dr. Ignacio Conget, Dr. Enric Esmatjes, Dra. Marga Giménez y las enfermeras Gemma Yago, Pilar Ara, Anna Alonso y Mercè Lara, su labor educativa en alimentación saludable y en ayudar a que los pacientes adapten la pauta insulínica a sus hábitos dietéticos.
* Autor para correspondencia.
Correo electrónico:mjansa@clinic.ub.es (M. Jansà).
INFORMACIÓN DEL ARTÍCULO
Historia del artículo:
Recibido el 17 de julio de 2009
Aceptado el 4 de agosto de 2009