INTRODUCCIÓN
Definimos la disfunción eréctil (DE) como la incapacidad persistente o recurrente para conseguir o mantener la suficiente rigidez del pene que permita una relación sexual satisfactoria1. La DE es un problema de salud de alta prevalencia, y se estima que alrededor del 50% de los varones mayores de 40 años presentan algún grado de DE2. Un estudio epidemiológico multicéntrico realizado en 8 países situó la prevalencia de la DE en un 16%. Los valores de prevalencia más elevados fueron hallados en Estados Unidos (22%) y los inferiores en España (10%)3.
Para poder determinar la necesidad de intervención terapéutica para la DE, resulta indispensable evaluar tanto la calidad de vida del paciente afectado como la de su pareja4. Los trabajos publicados hasta el momento muestran que la DE tiene una gran implicación en la calidad de vida de los varones afectados y en la de sus parejas, y afecta áreas como la estabilidad emocional o la felicidad y las relaciones sociales5,6. El estudio multicéntrico ESTIMA, realizado en España, constató que la DE tiene un marcado impacto en la autoconfianza y la autoestima de los varones que la presentan7.
Actualmente, para la evaluación de la calidad de vida de los pacientes que presentan DE se han utilizado escalas de calidad de vida general, como LISAT-8 (Life-satisfaction Check List)8 o EQ-5d (Euro-QoL)9, herramientas potentes, pero no específicas para la DE. Se han desarrollado unos cuestionarios de calidad de vida específicos para la DE, como la ED-EQoL (Erectile Dysfunction-Effect on Quality of Life)10, una escala de 15 ítems que aún no se ha validado psicométricamente y que se centra únicamente en la evaluación de la calidad de vida del paciente afectado. El QOL-MED (Quality of Life specific to Male Erection Difficulties)11 es otra escala desarrollada para la evaluación de la calidad de vida del paciente con DE; está validada psicométricamente, aunque no permite evaluar la satisfacción de vida de la pareja del paciente con DE. A la hora de evaluar la satisfacción de la vida sexual de las parejas de pacientes con DE, se ha utilizado el cuestionario ISL (Index of Sexual Life), un instrumento de 11 ítems validado psicométricamente, aunque orientado exclusivamente a la calidad de vida de las parejas de pacientes con DE y no de los propios pacientes12,13.
La escala SLQQ (Sexual Life Quality Questionnaire)14, es la única herramienta disponible en la actualidad que permite la evaluación de la calidad de vida sexual de los pacientes con DE y la de sus parejas. Es necesario evaluar ambas partes, ya que los 2 miembros de la pareja presentan las consecuencias del trastorno eréctil4. La escala SLQQ está compuesta por 16 ítems, 10 de los cuales hacen referencia a la calidad de vida sexual y los 6 restantes a su satisfacción con el tratamiento. El cuestionario SLQQ se presenta como una herramienta potente, con una gran consistencia interna (a de Cronbach = 0,97; 0,97 para pacientes y 0,98 para sus parejas), capaz de detectar cambios en la calidad de vida sexual, tanto del paciente como de su pareja, de fácil manejo por el clínico, por tratarse de un cuestionario autoadministrado, y específico para la DE14.
Hasta la fecha, no existía una traducción validada en español del SLQQ, así como tampoco se había validado psicométricamente, ni baremado poblacionalmente. En consecuencia, el objetivo del presente estudio es validar, primero lingüísticamente y después psicométricamente, la versión castellana del cuestionario SLQQ en España, todo ello de acuerdo con los siguientes pasos:
Desarrollar la versión española del cuestionario y realizar la validación lingüística y cultural de ésta.
Evaluar la factibilidad, establecer la validez de constructo, la consistencia interna, la fiabilidad test-retest, la validez concurrente, la validez discriminante y la sensibilidad al cambio del cuestionario.
Comparar las propiedades psicométricas de la versión española respecto al instrumento original.
SELECCIÓN DE LOS SUJETOS
Para realizar la validación psicométrica del cuestionario se incluyeron 2 grupos de sujetos:
1. Grupo de pacientes con DE y sus parejas.
2. Grupo control de voluntarios y sus parejas.
En el grupo de pacientes con DE, los sujetos que se incluían en el estudio no debían haber recibido tratamiento alguno para la DE durante las últimas 4 semanas y no haber recibido ningún tratamiento para la DE entre las primeras 2 mediciones del cuestionario SLQQ en las visitas primera (basal) y segunda (2 semanas después), con la finalidad de evaluar la estabilidad test-retest de la escala. Tras la segunda visita, estos mismos pacientes recibieron un tratamiento oral para la DE a criterio de cada investigador, y fueron citados de nuevo para una visita final, 4 semanas más tarde. La comparación de las mediciones de la segunda visita y la final permitiría evaluar la sensibilidad al cambio del cuestionario SLQQ.
Los criterios de inclusión para la población con DE fueron:
1. Que presentasen DE, según la definición de los NIH (incapacidad para lograr o mantener una erección del pene el tiempo necesario para una relación sexual satisfactoria)1.
2. Relación heterosexual estable (misma pareja durante el estudio).
3. Edad comprendida entre los 18 y los 75 años.
4. No haber recibido ningún tratamiento para la DE durante las últimas 4 semanas.
5. Obtención del consentimiento informado por escrito del paciente y de su pareja.
Los criterios de exclusión para la población con DE fueron:
1. Cualquier proceso médico o psiquiátrico inestable o abuso de sustancias que, en opinión del investigador, pudieran afectar a la capacidad del paciente para completar el estudio o impidiesen su participación en éste.
2. Pacientes analfabetos o incapaces de comprender el lenguaje en que se presentan los cuestionarios o que no estén dispuestos a cumplimentar los cuestionarios del estudio.
3. En el grupo de pacientes que reciban un tratamiento para la DE a lo largo del estudio deberá verificarse que no cumplan ninguno de los criterios de exclusión relacionados con la ficha técnica del tratamiento prescrito.
El grupo control debió estar formado por voluntarios sanos. Varones que no presentaran enfermedad alguna relacionada con la función sexual y de características similares a los pacientes, apareados por edad ± 5 años, y sus parejas. Además, el sujeto control y su pareja debieron firmar el consentimiento informado.
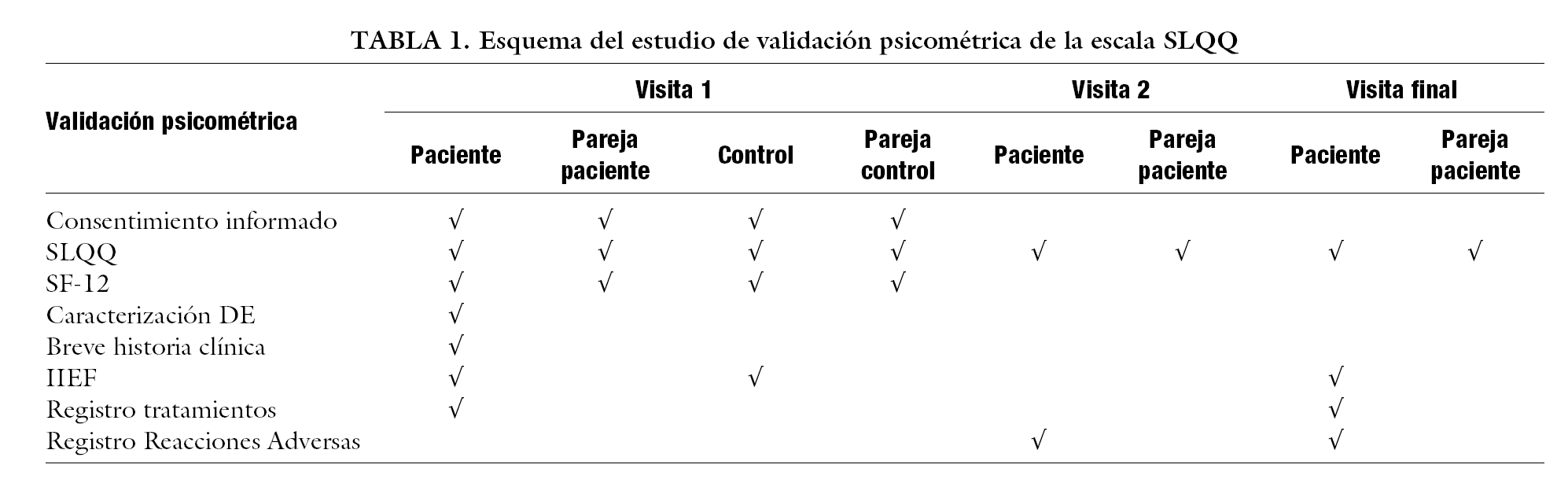
En la tabla 1 se expone un resumen esquematizado del procedimiento.
MÉTODO
Validación lingüística
Como se ha comentado anteriormente, antes del inicio del estudio de validación psicométrica de la versión castellana del cuestionario SLQQ en España, se realizó la validación lingüística y cultural, llevada a cabo por la empresa Adelphi Targis15. Dicha validación lingüística y cultural del SLQQ comprendió los siguientes pasos:
Traducción del cuestionario al español (2 traducciones independientes).
Análisis y definición de la primera versión del cuestionario.
Retrotraducción al inglés de la primera versión (una retrotraducción independiente).
Análisis y definición de la segunda versión del cuestionario.
Debriefing cognitivo (evaluar la comprensibilidad y la factibilidad de la segunda versión del cuestionario con 5 pacientes con DE y 5 parejas de pacientes con DE).
Análisis y definición de la tercera versión del cuestionario.
Revisión por parte de un clínico de la tercera versión del cuestionario.
Análisis y definición de la cuarta versión del cuestionario.
Proof-reading (control de calidad final).
Versión final del cuestionario (véase un comparativo en la tabla 2).
Validación psicométrica
Al inicio de este estudio multicéntrico nacional, se entregó a cada investigador el Cuaderno de Recogida de Datos (CRD), con el formulario que contenía todos los datos que permitían validar psicométricamente el cuestionario SLQQ: caracterización de la DE, breve historia clínica, cuestionario IIEF, registro de tratamientos, escala SLQQ adaptada lingüística y culturalmente a la población española y la escala SF-1216,17, que se utilizaron como gold-standard para la valoración de la sensibilidad y la especificidad del SLQQ (tabla 1).
Todos los pacientes incluidos en el estudio en tratamiento para su DE fueron documentados adecuadamente en relación con las reacciones adversas graves (RAG). En caso de RAG se estaba obligado a notificarla inmediatamente a la unidad de farmacovigilancia de los titulares de autorizaciones de comercialización, tal y como indica el artículo 7 de Obligaciones de los Profesionales Sanitarios del Real Decreto 711/2002, de 19 de julio.
De acuerdo con las normas internacionales relativas a la realización de estudios epidemiológicos, recogidas en las International Guidelines for Ethical Review of Epidemiological Studies (Council for the International Organizations of Medical Sciences CIOMS, Ginebra, 1991)18 y las recomendaciones de la Sociedad Española de Epidemiología (SEE)19 acerca de la revisión de los aspectos éticos de la investigación epidemiológica, se recomienda que este tipo de estudios se sometan a revisión por un comité independiente. Por ello, el presente estudio fue sometido para su evaluación al Comité Ético de Investigación de la Universidad de La Laguna y aprobado por éste, el 2 de septiembre de 2005.
Para la estimación del tamaño de la muestra en este estudio de validación psicométrica se recomienda que el número de sujetos sea 10 veces superior al número de ítems de la escala que se desea validar20,21. Por ello, teniendo en cuenta que el cuestionario está compuesto de 16 ítems, se definió un tamaño de la muestra de 160 sujetos con DE, que garantizara contar con la muestra suficiente, aun en el caso de pérdidas de seguimiento o datos incompletos. Una pérdida de
seguimiento o datos incompletos del 30% seguiría proporcionando un tamaño muestral suficiente (112 sujetos) para validar psicométricamente el cuestionario.
Por otro lado, el tamaño del grupo control se ha estimado en 60 sujetos, con la finalidad de tener una muestra suficiente para evaluar la validez discriminante del cuestionario. Con esta muestra fue posible detectar diferencias de 30 puntos entre pacientes y controles, asumiendo una desviación estándar de 50 puntos, un error a del 5% y una potencia estadística del 80%, con la misma tasa de datos incompletos (30%).
El proceso de validación psicométrica comprendió los siguientes pasos:
Evaluación de la factibilidad para de la escala en estudio SLQQ, analizando y calculando el porcentaje de pacientes que no responden al cuestionario en su totalidad.
La fiabilidad en términos de consistencia interna de la escala SLQQ, mediante el coeficiente a de Cronbach, utilizando la puntuación obtenida en la visita basal. Se calcularon las correlaciones individuales de cada uno de los ítems del instrumento con la puntuación global obtenida y se calculó el coeficiente a de Cronbach sin el ítem incluido en la escala, con el fin de valorar la adecuación de la inclusión de cada uno de los ítems.
La evaluación de la fiabilidad test-retest del SLQQ se incluyó en el análisis únicamente en aquellos sujetos que mostraron estabilidad en la puntuación obtenida en la escala en la SF-12, y se procedió a aplicar el coeficiente de correlación intraclase (CCI).
La validez concurrente de la escala SLQQ se analizó mediante el estudio de la relación entre el resultado de la escala de calidad de vida SF-12. Los contrastes a posteriori se analizaron mediante la aplicación de la prueba de Scheffe. En caso de no cumplimiento de la homocedasticidad de los datos, se procedió a realizar un análisis no paramétrico mediante la prueba de Kruskal-Wallis. En caso de que la prueba indicase diferencias a escala global, se procedió a analizar los contrastes 2 a 2, aplicando la prueba de la U de Mann-Whitney.
La validez predictiva de la escala SLQQ se valoró mediante la aplicación del análisis discriminante.
RESULTADOS
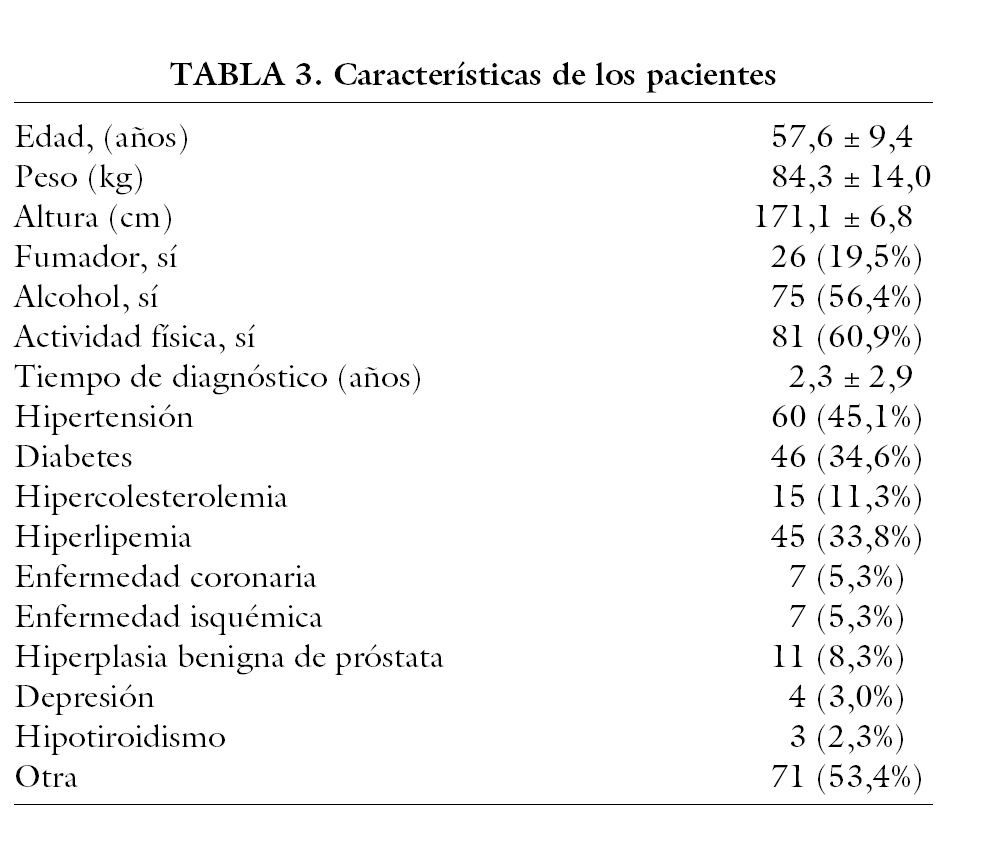
Los resultados preliminares de la validación psicométrica realizada con 133 pacientes afectados de DE (cuyos datos demográficos y de patología asociada se muestran en la tabla 3) y sus parejas, más 60 pacientes controles y sus parejas, muestran una factibilidad de prácticamente el 100%, lo que denota una comprensión alta del cuestionario. El cuestionario obtuvo una elevada consistencia interna (a de Cronbach = 0,894 pacientes; 0,892 parejas de pacientes; 0,97 para pacientes y 0,98 para parejas en el cuestionario original22). La estabilidad en el tiempo se calculó usando el ICC (ICC = 0,669). La validez concurrente se estableció correlacionando el cuestionario SLQQ con la puntuación de función eréctil del cuestionario IIEF (International Index of Erectil Function) (Pearson r = 0,678) y con la respuesta a la pregunta sobre la posibilidad de continuar con el tratamiento para la DE (Pearson r = 0,552, r = 0,54, en el cuestionario original).
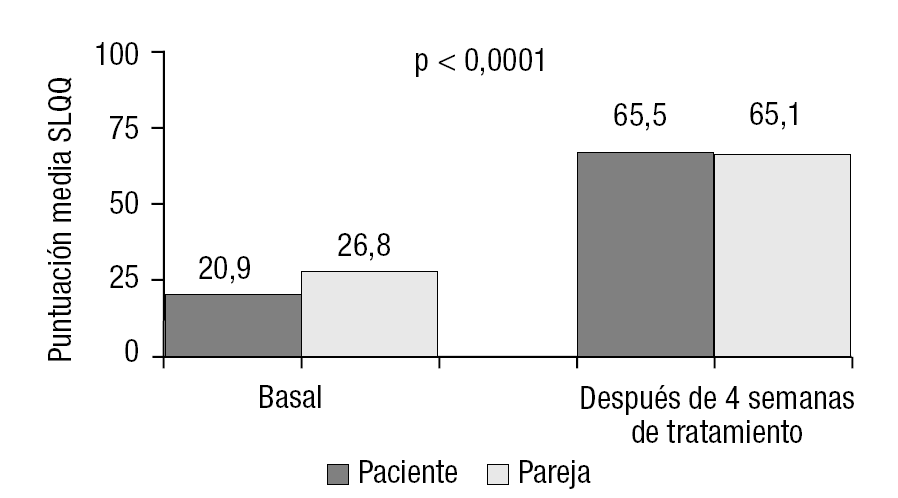
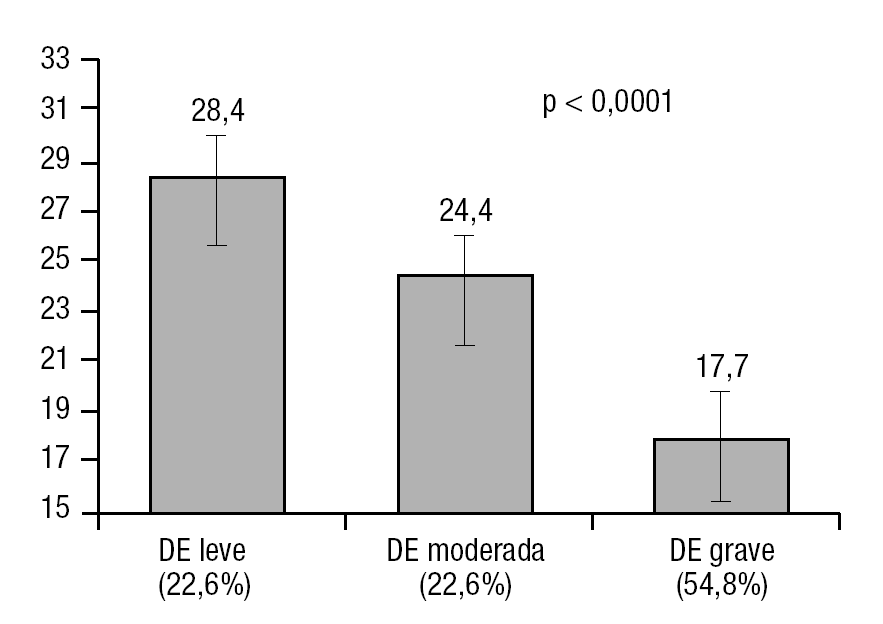
Las puntuaciones de la calidad de vida sexual tanto de los pacientes como de sus parejas fueron significativamente inferiores que en los controles y sus parejas (20,9 y 26,8 frente a 49,4 y 49,7; p < 0,0001 y < 0,0001, respectivamente, test de la t de Student); asimismo, se observó una correlación alta (Pearson r = 0,678; p < 0,0001) entre la puntuación de la calidad de vida y la gravedad de la DE, loo que sugiere, en ambos casos, una correcta validez discriminante. El cuestionario mostró una buena sensibilidad al cambio en los pacientes y sus parejas tras 4 semanas de tratamiento para la DE (pacientes: 20,9 frente a 65,5; p < 0,0001; parejas: 26,8 frente a 65,1; p < 0,0001, test de la t de Student para datos apareados) (fig. 1). Basalmente, se observaron diferencias significativas en la puntuación de la escala SLQQ en función de la gravedad de la DE calculada, utilizando el dominio de función eréctil (FE) del IIEF (fig. 2).
Figura 1. El cuestionario SLQQ detecta cambios de calidad de vida entre 2 momentos diferentes en el tiempo, después de haber empezado el tratamiento.
Figura 2. SLQQ según dominio FE-IIEF.
CONCLUSIONES
La validación psicométrica de la versión castellana del cuestionario SLQQ confirma que es una herramienta factible, fiable, válida y sensible al cambio para evaluar la calidad de vida sexual de los pacientes con DE y sus parejas en España. Presenta propiedades psicométricas comparables al cuestionario original.
AGRADECIMIENTOS
Los autores de este manuscrito desean expresar su agradecimiento al Servicio de Urología del Hospital Universitario de Canarias (Tenerife) y a la empresa Bayer Health Care (Barcelona), por la colaboración prestada, sin la cual hubiese resultado imposible la consecución de éste.
Correspondencia:
Dr. P.R. Gutiérrez Hernández.
Plaza de la Concepción, 15.
38202 San Cristóbal de La Laguna. Santa Cruz de Tenerife. España.
Correo electrónico: prguti@ull.es