Se revisan los trastornos más comunes del sistema endocrino que se detectan en la consulta no especializada. Se hace énfasis en: a) Trastornos tiroideos tales como hipo o hipertiroidismo, nódulos de la tiroides y la importancia de la enfermedad de la tiroides durante el embarazo, b) la enfermedad adrenal en la hipertensión y el enfoque de la incidentaloma suprarrenal c) hiperparatiroidismo primario y la deficiencia de vitamina D d) Trastornos gonadal y la importancia de la detección precoz de la enfermedad hormonal, tanto en la disfunción ovárica y testicular.
We review the most common disorders of the endocrine system that are detected in non-specialist consultation. Emphasis is placed on: a) thyroid disorders such as hypo-or hyperthyroidism, thyroid nodules and the importance of thyroid disease during pregnancy, b) adrenal disease in hypertension and the approach to the adrenal incidentaloma c) metabolic disorders such as primary hyperparathyroidism and vitamin D deficiency d) gonadal disorders and the importance of early detection of hormonal disease in both ovarian and testicular dysfunction.
La endocrinología es una rama especialmente amplia de la medicina interna. Las hormonas influyen en forma determinante en todas las etapas del ser humano desde su nacimiento hasta la vejez y muerte. La valoración del paciente endocrinológico exige dedicar algunos minutos en conocer al paciente, lo que permitirá establecer un marco apropiado para llegar al diagnóstico y tratamiento. El médico no especialista en endocrinología es generalmente la primera fuente de derivación al endocrinólogo, debido a alguna alteración en el laboratorio general como nivel de calcio y/o fósforo, o desviación de los niveles de TSH, en un estudio de rutina o simplemente una preocupación específica del paciente con antecedentes familiares. La ausencia de síntomas y signos puede ser una constante en estos pacientes, sin embargo es importante destacar el valor del diagnóstico precoz y la prevención de una mayor morbilidad. En medicina preventiva el objetivo es detectar a tiempo condiciones de riesgo o trastornos endocrinos en su etapa subclínica, con lo cual podremos establecer un plan de tratamiento o de estudio que finalmente se traducirá en un mejor pronóstico y en un tratamiento de menor complejidad.
A continuación revisaremos algunos de los aspectos más importantes en el diagnóstico precoz de diversos trastornos endocrinológicos.
Enfermedad tiroideaDiagnóstico y screening de la enfermedad tiroideaLos trastornos tiroideos presentan una alta prevalencia en la población general, que se grafica en parte por la elevada frecuencia de anticuerpos antitiroideos positivos, que varía entre 5 a 18 % (1). Estos aumentan especialmente en mujeres mayores y multíparas y pueden ser determinantes en el desarrollo de disfunción tiroidea como hipotiroidismo primario. El hipotiroidismo subclínico (TSH sobre 4uUI/ml) puede afectar hasta el 12% de la población (1, 2). En EE.UU. el estudio NHANES III encontró una prevalencia de hipotiroidismo clínico de 4,6 %, existiendo hipertiroidismo en un 1,3% de la población estudiada (2). En mujeres embarazadas se ha encontrado una prevalencia de hipotiroidismo subclínico entre un 2,5 hasta un 5%, lo que justifica una acción de carácter preventivo en la mujer tendiente a disminuir las complicaciones del hipotiroidismo durante el embarazo (3–4).
A continuación revisaremos las estrategias destinadas a detectar trastornos tiroideos en forma precoz en la consulta médica no endocrinológica, considerando que la sintomatología es de poca ayuda en aquellos pacientes con trastorno tiroideo subclínico. Por esto, es muy importante en el paciente asintomático recabar antecedentes de enfermedad tiroidea personal y familiar, es esencial realizar un examen físico general con especial énfasis en la región tiroidea.
Trastornos funcionalesCorresponden a hipo o hipertiroidismo, el examen de laboratorio de elección es la TSH. El estudio se puede complementar con la determinación de anticuerpos antitiroideos y ecografía de tiroides. Toda alteración en los niveles de TSH requiere de evaluación especializada antes de iniciar terapia específica. TSH sobre 4uUI/ml es compatible con hipotiroidismo, mientras que TSH bajo 0,3uUI/ml hace pensar en hipertiroidismo. Recomendamos que todo paciente con TSH sobre 2,5uUI/ml sea observado al menos una vez al año, especialmente aquellos con antecedentes familiares de enfermedad tiroidea. Aquellos con pruebas tiroideas normales, pero anticuerpos antitiroideos positivos o alteración ecográfica deben necesariamente ser evaluados por especialista.
Nódulos tiroideosTodos los pacientes con nódulos palpables deben realizarse al menos una TSH, idealmente acompañada con anticuerpos antitiroideos y necesariamente una ecografía de tiroides. La ecografía como screening no está validada en población general, sin embargo una vez que se ha detectado un incidentaloma tiroideo se debe establecer un estudio formal (5). El cintigrama tiroideo es un examen que debe reservarse para el endocrinólogo ya que su indicación actualmente se limita a la detección de bocio nodular autónomo y con TSH suprimida (6, 7). Por otro lado la punción tiroidea es un examen que también es de exclusiva indicación por el endocrinólogo y que escapa a los objetivos de este artículo. Por otro lado, es importante destacar que la tomografía computada de cuello, especialmente con medio de contraste, puede interferir con el tratamiento a futuro de un nódulo tiroideo, por lo tanto, no es un examen de primera línea en la evaluación tiroidea.
Enfermedad tiroidea y embarazoPor la alta prevalencia de trastornos tiroideos durante el embarazo, actualmente se considera que la búsqueda de hipotiroidismo subclínico en la embarazada es una estrategia costo-efectiva en un amplio rango de circunstancias (8–10). Los exámenes de elección son T4libre y TSH. Por otra parte, la TSH, que si bien disminuye durante el embarazo por efecto de la gonadotropina coriónica, sigue siendo un importante indicador de función tiroidea durante el embarazo. No son de utilidad las hormonas totales (T3 y T4) que están unidas a TBG la que aumenta por efecto de estrógenos y determina elevación ficticia de hormonas tiroideas (11). Por las implicancias del hipotiroidismo en el embrazo, aquellas pacientes con valores de T4libre menor de 1,0ng/dl o TSH sobre 2,5uUI/ml deben ser tratadas como hipotiroideas y deben ser derivadas al endocrinólogo (12–14). Ver Tabla 1.
Enfermedad tiroidea
| Examen de elección | Derivación a Endocrinólogo | Control en 6 meses | |
|---|---|---|---|
| Hipotiroidismo | TSH | > 4uUI/ml | TSH>2,5uUI/ml |
| Hipertiroidismo | TSH | < 0,3uUI/ml | TSH<0,5uUI/ml |
| Nódulo palpable | Ecografía Tiroidea | Todos | |
| Enfermedad tiroidea y Embarazo | TSH y T4 libre | TSH>2,5uUI/ml o<0,3uUI/ml o T4Libre<0,8ng/dl o>2,0ng/dl |
La corteza suprarrenal produce tres tipos de hormonas principales: glucocorticoides, mineralocorticoides y esteroides sexuales (especialmente andrógenos). El colesterol es el precursor de toda la esteroidogénesis suprarrenal (15). Los glucocorticoides son secretados en la zona fasciculada bajo el control de la ACTH, los mineralocorticoides se secretan en la zona glomural bajo el control del angiotensina 2. Los andrógenos (dehidroepiandrosterona o DHEA) son los esteroides más abundantes y no tienen un regulador especifico (15–17).
Los trastornos generados por exceso de glucocorticoides se manifiestan clínicamente por el clásico síndrome de Cushing el cual debe ser sospechado en todo paciente obeso con hipertricosis hipersecreción sebácea, atrofia muscular proximal, adiposidad central y en las mujeres, alteraciones del ciclo menstrual como amenorrea (18, 19), en los niños se puede presentar en forma atípica y debe considerarse especialmente en aquellos con obesidad mórbida. El estudio básico del paciente con sospecha de enfermedad de Cushing es la determinación de cortisol basal matinal y cortisol libre urinario en orina de 24 horas (19). Los estudios confirmatorios deben ser realizados por el endocrinólogo.
Corteza suprarrenal e hipertensión arterialSe ha propuesto que desde un 10% hasta un 15% de los pacientes con hipertensión arterial pueden presentar un trastorno a nivel de la corteza suprarrenal constituyendo un hiperaldoteronismo primario (20, 21). La presencia de hipopotasemia espontánea sugiere un trastorno de la secreción de aldosterona, sin embargo, se ha demostrado que la mayoría de los pacientes con hiperaldosteronismo tiene concentraciones séricas basales de potasio dentro de rangos normales. Por este motivo se hace recomendable solicitar exámenes más específicos especialmente en pacientes hipertensos resistentes al tratamiento, hipertensión arterial sistólica mayor de 160mmHg o diastólica mayor de 100, también debe estudiarse pacientes con hipertensión y masa suprarrenal o aquellos pacientes hipertensos jóvenes (21–23). Las pruebas necesarias son determinación de aldosterona (A) y actividad de renina plasmática (ARP). Esta prueba puede realizarse durante la mañana y sin necesidad de estimulación postural. Una relación A/ARP mayor a 20 es sugerente de hiperaldosteronismo primario, especialmente si se acompaña de A sobre 15ng/dl. Los antagonistas de la aldosterona como la espirolactona son los únicos fármacos contraindicados. Los inhibidores de la enzima convertidora de angiotensina elevan falsamente la ARP, de modo que el encontrarla suprimida en un paciente usuario de IECA puede ser indicador de hiperaldosteronismo (21–23).
Nódulo suprarrenal o incidentaloma suprarrenalSe define incidentaloma suprarrenal a toda masa mayor de 1cm de diámetro detectada a nivel suprarrenal en relación a un estudio imageneologico de abdomen como TAC o RNM. En todo incidentaloma se debe determinar su naturaleza, benigna o maligna y la capacidad funcional, es decir si se asocia a secreción hormonal (glucocorticoicodes, mineralocorticoides y/o andrógenos) (24) estos pacientes deben ser derivados inmediatamente al endocrinólogo. Ver Tabla 2.
Enfermedad suprarrenal. hipertensión arterial y sospecha de patología suprarrenal (21 – 23)
| Examen de elección | Derivación a Endocrinólogo | |
|---|---|---|
| Hipertensión Arterial | Aldosterona /ARP | Relación ARP/Aldosterona mayor a 20 y/o Aldosterona > 15ng/dl |
| Nódulo Suprarrenal | TAC | Todos |
La prevalencia de hiperparatiroidismo primario varía entre 0,1 a 0,4 %, y la incidencia aumenta con la edad alcanzando el peak entre los 50 y 60 años. La hipercalcemia asintomática es actualmente la presentación más frecuente (25). Este diagnóstico se debe sospechar en: todo paciente con hipercalcemia (Calcio sobre 10,5mg/dl) e hipoposfemia (fósforo menor a 2mg/dl), en pacientes con nefrolitiasis a repetición y en aquellos con desmineralización ósea especialmente a nivel de hueso cortical (25). Estos pacientes presentan un mayor riesgo de enfermedad cardiovascular, neoplasias y fracturas de caderas (25–27). El examen de elección es PTH intacta asociada a calcio y fósforo. La interpretación de estos valores debe ser realizada por el endocrinólogo.
Hipovitaminosis DEntre las estrategias de prevención de trastornos endocrinológicos, es de gran importancia para el médico no especialista tener presente la eventual deficiencia de vitamina D, cuyos niveles se pueden determinar a través de la medición de 25 OH vitamina D. La vitamina D es considerada evolutivamente como una de las hormonas más antiguas (28). Cómo cualquier hormona actúa a distancia, sobre diversos receptores, influye la homeostasis ósea, tropismo muscular, entre otros, es regulada por otras hormonas y requiere de síntesis endógena. Por otro lado la vitamina D tiene funciones de citoquina influyendo positivamente sobre la actividad del sistema inmune, siendo fabricada por macrófagos y actuando en la respuesta antimicrobiana (28–29). Su acción más conocida es permitir la absorción de calcio a nivel intestinal, cuando hay déficit de vitamina D se activa la secreción de PTH que determinará la activación del gen Cyp27b1 con el consiguiente aumento de 1–25 Vitamina D e incremento de la absorción de calcio intestinal. Valores menores de 31ng/ml generan estímulo de la secreción de PTH y constituyen estados de insuficiencia de Vitamina D, valores menores de 20ng/ml son denominados deficiencia de vitamina D. Durante los últimos años se ha producido un aumento significativo de la prevalencia del déficit de vitamina D, llegando a afectar hasta un 60%, de grupos de mujeres postmenopáusicas, incluso en latitudes con adecuada exposición solar (30–31). El déficit de vitamina D se ha asociado a miopatía de predominio proximal, neuropatía, alteración de la respuesta inmune y aumento del índice de masa corporal en niños, adolescentes y adultos, en individuos con rango de peso normal hasta obesidad extrema, en ambos géneros y en todas las razas (32). En este sentido, animales de experimentación con receptor vitamina D negativo presentan significativa disminución de la grasa visceral y son mucho más delgados que los animales con el gen nativo. Por otro lado animales bajo dieta restringida en vitamina D ganan peso. En esta hipótesis el bajo nivel de vitamina D generaría un aumento de la secreción de PTH e incremento del receptor de vitamina D que por un motivo aún no explicado determina aumento de la grasa corporal (33).
La disminución acelerada de Vitamina D en la población general se explica por disminución de síntesis cutánea de vitamina D, disminución de la ingesta de alimentos ricos en vitamina D, aumento de los depósitos de vitamina D a nivel del tejido adiposo asociado falla en movilización de vitamina D desde el tejido adiposo (34). Actualmente las recomendaciones internacionales apoyan la suplementación de vitamina D en población de mayor riesgo siendo esta alrededor de 1000 unidades diarias. Ver Tabla 3.
Enfermedad metabólica ósea
| Exámenes | Derivación a Endocrinólogo | |
|---|---|---|
| Hiperparatiroidismo primario | Calcio, Fósforo | Calcio sobre 10,5mg/dl con fósforo en rango bajo |
| Densitometría ósea | Nefrolitiasis a repetición | |
| Osteoporosis de predominio cortical (caderas) en paciente menor de 60 años y/o asociada Nefrolitiasis | ||
| Hipovitaminosis D | 25 OH Vitamina D En población de riesgo | Aquellos con valor menor a 20ng/ml* * valores 20 a 30ng/ml suplementar con 1000 U vitamina D diarias y controlar en 6 meses |
En la consulta no especializada especialmente frente a sospecha de trastorno gonadal tanto en la mujer como en el hombre, el médico no especialista debe tener presente que podría estar frente a un trastorno de origen endocrinológico.
Revisaremos las más importantes.
Disfunción ovárica Oligomenorrea:Se define como oligomenorrea a la ausencia de menstruación durante 3 ó más meses y su prevalencia es del 3 al 4% cuando se excluye embarazo, lactancia y menopausia (35, 36). Las causas endocrinológicas de oligomenorrea que deben ser investigadas en una primera evaluación son:
- 1.
Síndrome de ovario poliquístico (hiperandrogenismo ovárico funcional).
- 2.
Hiperandrogenismo de origen suprarrenal (hiperplasia suprarrenal congénita, síndrome de Cushing).
- 3.
Disfunción tiroidea.
- 4.
Neoplasia productora de andrógenos, HCG u otro.
- 5.
Hipogonadismo hipo o hipergonadotrópico.
- 6.
Disfunción hipotálamo – hipofisiaria (anorexia nerviosa, entrenamiento extremo, hiperprolactinemia).
- 7.
Menopausia.
Los exámenes a solicitar deben estar orientados según la historia y examen físico de la paciente, es decir, según la presencia de obesidad, bajo peso, acné, hirsutismo, galactorrea, cefalea, bocio, hábito y grado de desarrollo mamario y genital (36).
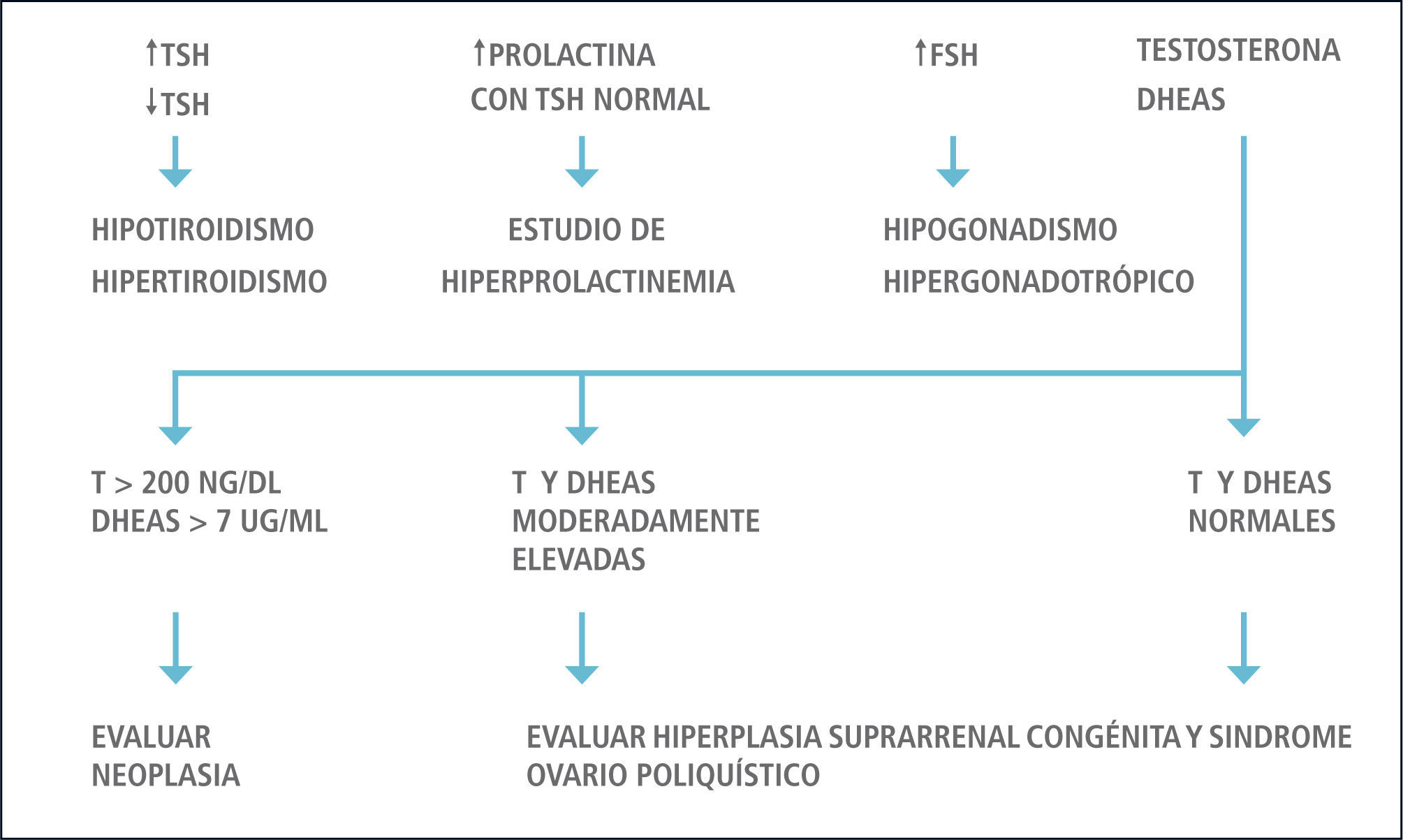
La historia, examen físico y la determinación de β-HCG, FSH, TSH, Prolactina, Testosterona Total más SHBG y cortisol matinal identificarán la mayoría de las causas de amenorrea de origen endocrinológico. Estas pacientes idealmente deben ser sometidas a una evaluación multidisciplinara compuesta por un equipo mixto endocrino-ginecológico. Ver Figura 1 y Tabla 4.
Disfunción testicularHipogonadismo masculino: es un síndrome clínico ocasionado por una disminución de la producción de testosterona por falla testicular, determinando deficiencia androgénica. Esta alteración puede ser ocasionada por una falla a cualquier nivel del eje hipotalámico-hipofisiario-testicular. La falla testicular se denomina primaria cuando la alteración se localiza solo a nivel testicular y se presenta con disminución de niveles de testosterona, alteración de la espermatogenesis y elevación de gonadotropinas (LH y FSH). La falla testicular secundaria se refiere a alteraciones a nivel de hipófisis y/o hipotálamo encontrando gonadotropinas en rango normal o bajo (37). En la consulta médica no endocrinológica se pueden presentar la sospecha de falla testicular en pacientes con disfunción sexual o con características sugerentes de hipoandrogenismo (disminución de vello corporal, ginecomastia, etc.). Frente a estas consultas es necesario considerar la declinación fisiológica de los niveles de testosterona a lo largo de la vida a partir de los 30 años, confirmado en varios estudios transversales y longitudinales siendo el promedio de declinación de los niveles de testosterona de 1 a 2% al año. Una fracción significativa de hombres mayores tienen niveles de testosterona bajo el límite inferior normal de un hombre joven sano (38).
Cuando se sospecha hipogonadismo masculino, es necesario solicitar niveles de testoterona total idealmente asociado a LH y FSH. En aquellos casos que estos niveles se encuentren alterados (valores menores a 250ng/dl) en la consulta no especializada no se recomienda la determinación de testosterona libre, ya que es una prueba de laboratorio que puede presentar variaciones significativas y de interpretación dificultosa para el médico no especialista. La indicación de terapia de sustitución con testosterona debe ser siempre dada por el endocrinólogo y requiere una evaluación urológica con el fin de descartar enfermedad prostática (39). No se recomienda iniciar tratamiento de sustitución con testosterona en pacientes que no han sido sometidos a una evaluación endocrinológica completa ya que se pueden enmascarar enfermedades a diferentes niveles hipotalamico-hipofisiario-testicular. Ver Tabla 5.
ConclusionesEn suma, los trastornos hormonales se caracterizan por producción hormonal excesiva o insuficiente, o tumores benignos o malignos de las glándulas endocrinas. En la consulta médica no especializada, es el primer contacto de pacientes con trastornos del ámbito endocrinológico. El médico no especialista debe tener presente que los trastornos hormonales más frecuentes se presentan en forma subclínica por lo cual es necesario dar especial relevancia a la anamnesis y el examen físico cuidadoso y en muchos casos complementar con estudios básicos, antes de la derivación. Se deben tener presente las patologías aquí presentadas y considerar la derivación al especialista cuando sea justificado después del estudio básico inicial. Como en otros campos de la medicina la prevención y el diagnóstico precoz optimizan el pronóstico del paciente endocrinológico.
Los autores declaran no tener conflictos de interés, en relación a este artículo.