La ketamina se ha utilizado en dosis sub-anestésicas en pacientes no obesos sugiriendo que su uso disminuye el consumo de morfina postoperatoria, sin embargo, la evidencia en la literatura es contradictoria.
ObjetivoDeterminar efecto de ketamina intraoperatoria en el consumo de morfina durante las primeras 24 horas postoperatorias de pacientes obesos operados de manga gástrica laparoscópica.
Material y métodoEnsayo Clínico Controlado, Aleatorizado, doble ciego de grupos paralelos unicéntrico realizado entre septiembre del 2015 y Enero de 2017. Se incluyeron pacientes entre 18 y 60 años de ambos sexos, obesos con indicación de quirúrgica de Manga Gástrica Laparoscópica, ASA II. Se aleatorizó la intervención a un grupo experimental (ketamina) y uno placebo (suero fisiológico). Se administró ketamina 0.5mg/kg 1 como dosis de carga después de la inducción anestésica y luego una infusión de 0.1mg/kg/h hasta el final de la cirugía. Al ingreso a la Unidad de Post Anestesia, en ambos grupos se inició una bomba de infusión de morfina programada con 1mg de bolo y con un bloqueo de tiempo de 10 minutos entre dosis, durante 24 horas.
ResultadosSe analizaron 63 pacientes. Treinta y dos pacientes en el grupo ketamina y 31 en el grupo placebo. La mediana de consumo de morfina del grupo ketamina fue de 20mg (ric 11mg/min:5-máx.:57 y 19mg (ric:11/min.:8-máx.:82) en el grupo placebo, diferencia estadísticamente no significativa (p=0.412). No se encontraron diferencias estadísticas entre los grupos en cuanto a efectos adversos a los opioides, sedación y deambulación.
ConclusiónLa administración de ketamina en cirugía laparoscópica de manga gástrica no disminuyó el consumo de morfina durante las primeras 24 horas postoperatorias, ni la proporción de efectos adversos a los opioides y no demoró la deambulación de los pacientes postoperados en este estudio.
Este estudio se realizó con fondos concursables de la Dirección Académica de Clínica Las Condes. Ninguno de los investigadores participantes en este estudio declaró conflictos de interés de ninguna clase.
Ketamine has been used in sub-anesthetic doses in non-obese patients suggesting that its use decreases postoperative morphine consumption. however, the evidence in the literature is contradictory.
ObjectiveTo determine the effect of intraoperative ketamine on postoperative morphine consumption during the first 24hours postoperatively in obese patients operated on laparoscopic gastric sleeve.
Material and methodControlled, randomized, double-blind, unicentric clinical trial, approved by the health research ethics committee of our institution. We included obese patients 18 to 60 years old of both sexes, obese with an indication of laparoscopic Gastric Sleeve, ASA II. The intervention was randomized to an experimental group (ketamine) and a placebo (saline).Ketamine 0.5mg/kg was administered as a loading dose after anesthetic induction and then an infusion of 0.1mg/kg/h until the end of surgery. On admission to the Post Anesthesia Unit, in both groups, a morphine infusion pump was started, programmed with 1mg of bolus and with a time block of 10minutes between doses, for 24hours.
Results63 patients were analyzed. Thirty-two patients in the ketamine group and 31 in the placebo group. The median morphine consumption of the ketamine group was 20mg (ric 11mg / min: 5-max .: 57 and 19mg (ric: 11 / min .: 8-max .: 82) in the placebo group, nonsignificant statistical difference (p=0.412). No statistical differences were found between the groups in terms of adverse effects to opioids, sedation and ambulation
ConclusionThe administration of ketamine in laparoscopic gastric sleeve surgery does not decrease morphine consumption during the first 24 postoperative hours, nor the proportion of adverse effects to opioids and does not delay the ambulation of postoperative patients in this studio. This study was carried out with funds from the Academic Department of Clinica Las Condes. None of the researchers participating in this study declared conflicts of interest of any kind.
La obesidad es una condición producida por el aumento de la grasa corporal en todos los tejidos del organismo, cuya causa es multifactorial e involucra tanto factores genéticos hereditarios como ambientales1. Debido al aumento de su prevalencia a nivel mundial es considerada actualmente una pandemia que incluso motivó a la Organización Mundial de la Salud (OMS) para desarrollar una estrategia global para su enfrentamiento2. Hasta hace 50 años atrás, el gran problema nutricional era la desnutrición, especialmente en la infancia, pero en la actualidad, es la obesidad la que ha pasado a ser la problemática más relevante ya que del 20% a 25% de los niños y adolescentes latinoamericanos tienen obesidad o sobrepeso, estimándose que, de no cambiar las condiciones actuales, un 81.9% de la población será obeso o tendrá sobrepeso para el año 20303. En la región, Argentina y Brasil se estima que presentan una prevalencia de sobrepeso cercana al 50%4, y la tendencia, lejos de ir disminuyendo, va en aumento en toda Latinoamérica, siendo México, Argentina, Chile y Brasil los países con mayor prevalencia de sobrepeso y obesidad5. En Chile la prevalencia de obesidad en la población general, según la Encuesta Nacional de Salud (ENS) 2009-2010, es de 25% y de obesidad mórbida de 2.3%. Con respecto a la obesidad infantil, esta ha aumentado también, llegando a estimarse una prevalencia de obesidad en un 9.9% de los niños menores de 6 años de nuestro país6. Debido a estas situaciones, el Ministerio de Salud de Chile reconoció, en el año 2008 al sobrepeso y la obesidad infantil como uno de los factores de riesgo de morbimortalidad más importantes en la población y definió una estrategia nacional de salud en la que entre sus metas se contempla la disminución de la prevalencia de la obesidad en un 10% durante el decenio 2010-20207. Una vez establecida, el tratamiento de la obesidad se basa en un enfoque multidisciplinario que incluye la modificación de los estilos de vida, diminución de la ingesta calórica, apoyo psicológico, farmacoterapia y cirugía8. La cirugía, como opción terapéutica, es la más efectiva en la mantención de la pérdida de peso en aquellos casos que no respondan a las terapias menos invasivas y que se asocien a un enfoque multidisciplinario9-11. El paciente obeso que va a ser sometido a una cirugía bariátrica tiene condiciones que se asocian a una mayor morbimortalidad como una alta prevalencia de Síndrome de Apnea Obstructiva del Sueño (71%)(SAOS)12, y mayor prevalencia de atelectasias pulmonares preoperatorias que los no obesos13,14. Por este motivo la movilización precoz de estos pacientes es fundamental para disminuir complicaciones como la enfermedad tromboembólica y el trombo embolismo pulmonar (TEP). El dolor se asocia a toda cirugía y en su manejo, el uso de morfina es la droga de elección16. Sin embargo, efectos como riesgo de depresión respiratoria, sedación, náuseas y vómitos se asocian a su uso. Esto ha llevado a buscar alternativas que permitan administrar una analgesia multimodal17-19 basado en el principio de “preventive” analgesia20,21. En este contexto, el uso de ketamina, un inductor anestésico conocido ampliamente22-23, se ha utilizado en dosis subanestésicas para potenciar la analgesia postoperatoria en distintos tipos de cirugías (abdominales, ginecológicas, etc.)24-34, lo que sugiere su utilidad en pacientes que se sometan a cirugías bariátricas. Es por ello, que el propósito de este estudio fue determinar el efecto del uso ketamina intraoperatoria sobre el consumo de morfina durante las primeras 24 horas postoperatorias de pacientes obesos operados de manga gástrica laparoscópica, sus efectos adversos en estas dosis y en la deambulacíon postoperatoria.
MATERIAL Y MÉTODOEnsayo Clínico Controlado, Aleatorizado, doble ciego de grupos paralelos unicéntrico realizado entre septiembre del 2015 y Enero de 2017 aprobado por el comité de ética de investigación de Clínica Las Condes. Fueron ingresados a este estudio aquellos pacientes adultos obesos que cumplieron con los criterios de inclusión y de exclusión y que aceptaron la invitación de participar luego de haber sido explicado, leído, entendido y firmado el consentimiento informado. Los criterios de inclusión fueron: tener entre 18 y 65 años, ASA II, IMC ≥30kg/mt2 y estar programado para una gastrectomía en manga por videolaparoscopía (MGL). Se excluyeron pacientes con antecedentes de trastornos psiquiátricos, trastorno psiquiátrico diagnosticado y en tratamiento actual, antecedentes de adicción o de abuso de sustancias, insuficiencia hepática, insuficiencia renal, alergia a ketamina, deterioro cognitivo que impida al paciente entender las implicancias del estudio y no hablar español. La asignación de la intervención fue aleatoria. El grupo experimental recibió ketamina y el grupo placebo recibió suero fisiológico. El día programado para la cirugía, un integrante del equipo le comunicó a farmacia central el ingreso de un caso desde donde se envió una jeringa de 50ml de una solución transparente con el nombre del paciente y un digito identificador. La secuencia de aleatorización fue creada por la investigadora del Departamento de Salud Pública de la Universidad Los Andes con el software STATA versión 12 (StataCorp, 4905 Lakeway, Dr. College Station, TX 77845, USA) en bloques de 4 para mantener balanceados los grupos y enviada a la jefa de farmacia de la clínica, quien asignó las intervenciones de manera secuencial según la lista recibida. Ninguno de los investigadores que realizó la intervención tuvo conocimiento de la lista y que se midió.
Se llenó la hoja de registro y se preparó una bomba de infusión Fresenius Pilot 2 (Fresenius Vial, Le Grand Chemin, 38590 Brezins, France) con la solución enviada desde farmacia. El paciente ingresó desde su domicilio y se preparó según el protocolo quirúrgico-anestésico diseñado para este tipo de cirugía. Ni el paciente, ni los cirujanos, ni los anestesiólogos conocían el contenido de la jeringa. Una vez en pabellón, luego de la inducción anestésica (con Fentanilo, Propofol y Rocuronio) e intubación orotraqueal, pero antes de la realización de la incisión en la piel, se administró una dosis de 0.5mg/kg de ketamina (basado en el peso real del paciente) en 10 minutos y luego se programó la bomba para administrar 0.1mg/kg/h hasta el final de la cirugía, cortándose la infusión y registrando el total de ketamina administrada, al momento en el que se sacaba el último trócar laparoscópico abdominal. Se asumió que la solución contenía ketamina en una concentración de 5mg/ml. La mantención de la anestesia se realizó con Desfluorano y se administraron dosis de Fentanil según el criterio del anestesiólogo tratante. Todos los pacientes recibieron un antiinflamatorio no esteroidal, paracetamol y morfina entre 80 a 100 ugr/kg antes de la incisión quirúrgica. Una vez terminada la cirugía, los pacientes fueron trasladados a la unidad de post anestesia en donde se ingresó al programa de dolor agudo del departamento de anestesiología del centro y se realizaron las siguientes evaluaciones: consumo de morfina, dolor (mediante el uso de la escala visual análoga (EVA)), presencia de nauseas y/o vómitos, retención urinaria, depresión respiratoria, presencia de agitación, movilización y nivel de sedación. Los momentos de las evaluaciones fueron: al ingreso a la unidad de cuidados post anestésicos, cada 1 hora las primeras 6 horas postoperatorias y cada 3 horas las siguientes 18 horas hasta completar 24 horas post operatorias. Las evaluaciones nocturnas fueron realizadas por personal de enfermería que estaba a cargo de los pacientes ingresados al estudio a quienes previamente se les invitó a participar y se les capacitó en el registro de los datos. Todos los evaluadores estaban ciegos a la asignación. En caso de dudas se les instruyó aclararlas con el residente de anestesiología quien conocía el caso y podía solucionar dudas metodológicas. Todos los datos generados por este estudio se manejaron en la más estricta confidencialidad y se guardó una copia de la base de datos con clave (Software Excel 2011 para Mac versión 14.0.0.). Ninguno de los investigadores declaró tener conflicto de intereses con este estudio ni con los medicamentos utilizados.
ANÁLISIS ESTADÍSTICOLa estimación del consumo promedio de morfina las primeras 24 horas post operatorias se basó en los registros de consumo de pacientes sometidos a MGL que ingresaron al Programa de Dolor Agudo (PDA) del Departamento de Anestesiología entre los años 2011-2014 y en estudios internacionales30. En base a lo anterior se estimó el consumo de morfina durante las primeras 24 horas postoperatorias en 27mg (DE ±11mg). Para el cálculo del tamaño muestral se definió como hipótesis alternativa, que la administración de ketamina disminuye el consumo de morfina a la mitad durante las primeras 24 horas post operatorias. Considerando una potencia (β) de 0.9 y un α=0.01, se obtuvo un cálculo de 20 pacientes por rama. Se decidió ingresar 10 pacientes más por rama, considerando las posibles pérdidas. Se realizó un análisis descriptivo de las variables en base al tipo y escala. Para evaluar la normalidad de las variables cuantitativas, se efectuó el test de Shapiro Wilks. Los resultados que distribuyeron normal se reportaron con media y desviación estandar. En el caso de aquellas que no, se describieron con mediana y valor minimo y máximo. Se utilizó el test de t-student para muestras independientes para comparar los grupos cuando la variable distribuyo normal. Si no fue así, se utilizó el test de U Mann-Whitney para su comparación. El nivel de significación utilizado fue de p< 0.05. Para los análisis estadísticos se utilizó el Software STATA versión 12 para Macintosh (StataCorp, 4905 Lakeway, Dr. College Station, TX 77845, USA).
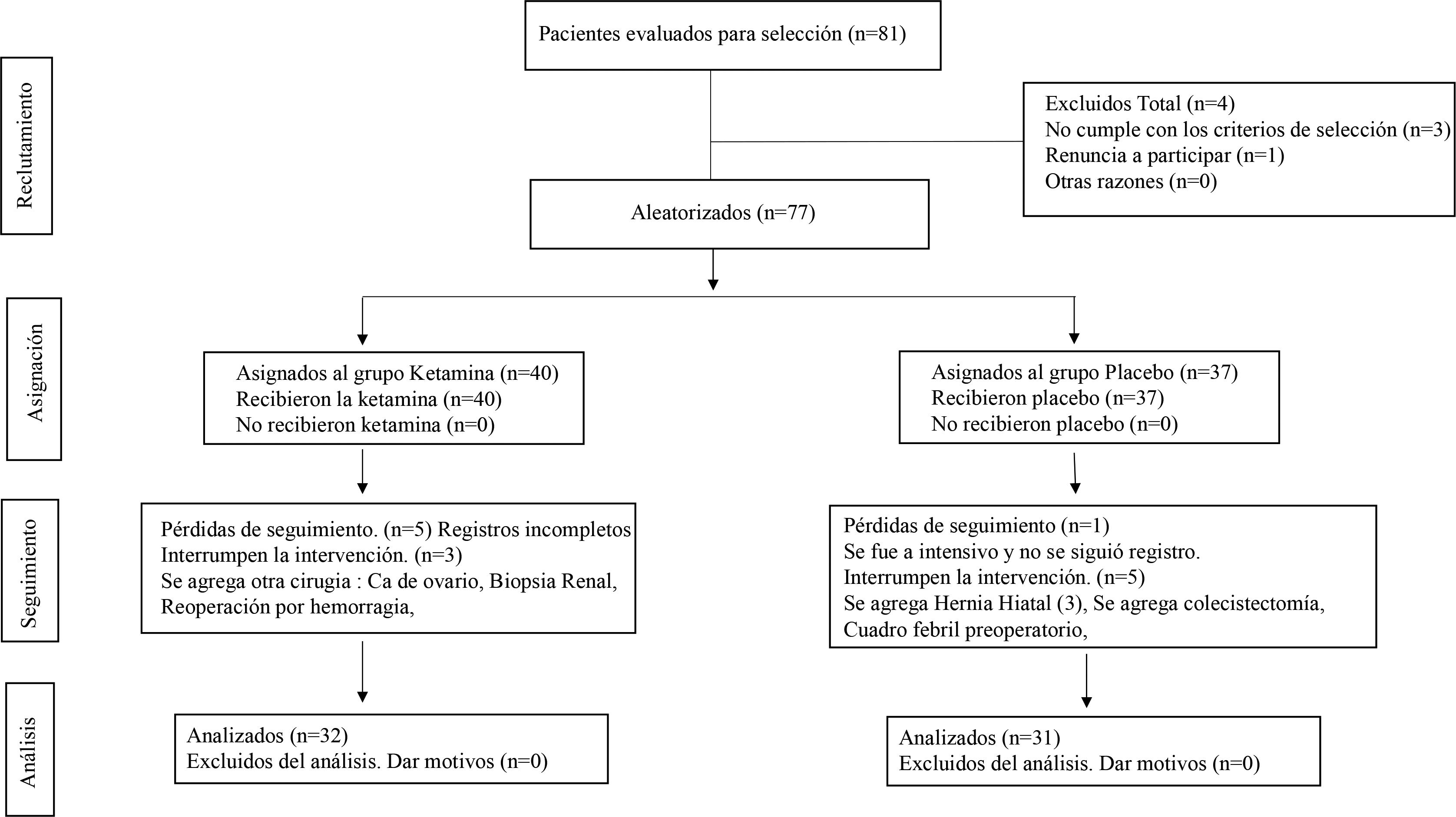
RESULTADOSIngresaron 63 pacientes al estudio. De ellos 32 fueron asignados al grupo ketamina (K) y 31 al grupo placebo(P). (Figura 1) Que es el diagrama de flujo de los pacientes y que debería ir aqui. Ambos grupos fueron comparables (Tabla 1). Las dosis medias de fentanyl utilizadas en el intraoperatorio fueron de 287.5 mcg (±79.31 mcg) en el grupo ketamina (K) versus 248.3 mcg (±48.21 mcg) utilizadas en el grupo placebo (P). Esta diferencia fue estadísticamente significativa (p=0.023). Con respecto a la dosis media de morfina administrada en el intraoperatorio fue de 6.5mg (±1.45mg) en el grupo K, versus 6.93mg (±1.69mg) en el grupo p. Esta diferencia no fue estadísticamente significativa (p=0.277).
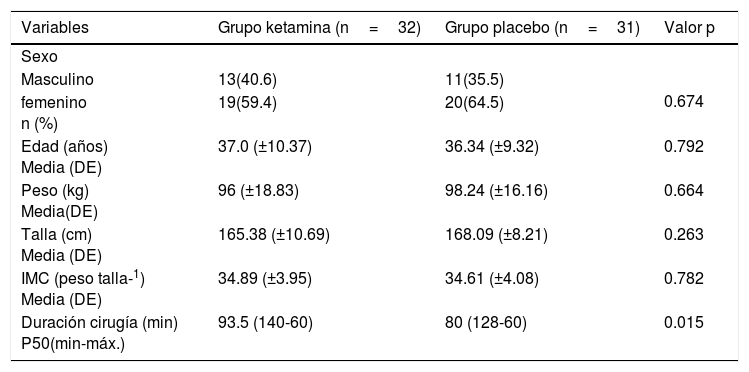
Características demográficas del grupo de estudio
| Variables | Grupo ketamina (n=32) | Grupo placebo (n=31) | Valor p |
|---|---|---|---|
| Sexo | |||
| Masculino | 13(40.6) | 11(35.5) | 0.674 |
| femenino n (%) | 19(59.4) | 20(64.5) | |
| Edad (años) Media (DE) | 37.0 (±10.37) | 36.34 (±9.32) | 0.792 |
| Peso (kg) Media(DE) | 96 (±18.83) | 98.24 (±16.16) | 0.664 |
| Talla (cm) Media (DE) | 165.38 (±10.69) | 168.09 (±8.21) | 0.263 |
| IMC (peso talla-1) Media (DE) | 34.89 (±3.95) | 34.61 (±4.08) | 0.782 |
| Duración cirugía (min) P50(min-máx.) | 93.5 (140-60) | 80 (128-60) | 0.015 |
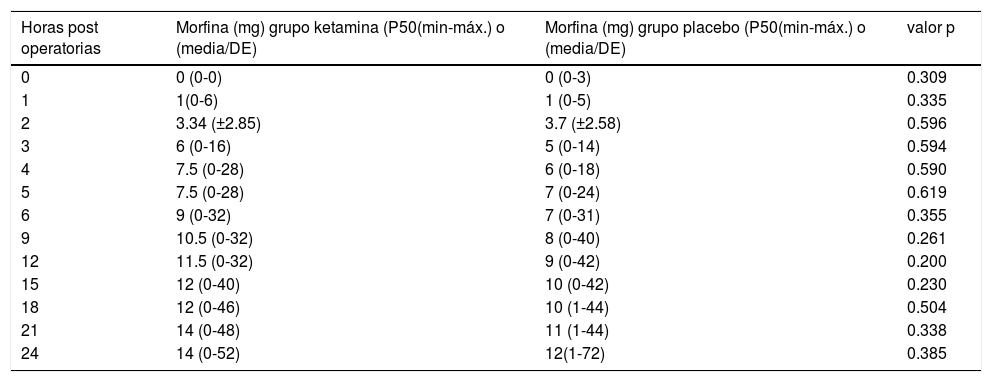
La dosis total promedio de ketamina administrada a los pacientes del grupo K fue de 64.5mg (± 18.4mg). El consumo acumulado de morfina las primeras 24 horas no mostró diferencias significativas entre ambos grupos (Tabla 2). La mediana de consumo total de morfina durante las 24 horas post operatorias (dosis intraoperatoria más la dosis total administrada durante el seguimiento) fue de 20mg (min:5 mg- ma: 57mg) en el grupo K y de 19mg (min: 8mg-max: 82mg) en el grupo P. Esta diferencia no fue significativa (p=0.412). Con respecto al dolor post operatorio no hubo diferencias entre los grupos excepto a las 15 horas en las que se encontró una diferencia que fue estadísticamente significativa (p=0.0454). No hubo diferencias significativas entre los grupos con respecto a las náuseas y vómitos post operatorios, episodios de retención de orina, depresión respiratoria, episodios de agitación psicomotora ni en el tiempo de primera deambulación.
Consumo acumulado medio de morfina las primeras 24 horas post operatorias por grupo
| Horas post operatorias | Morfina (mg) grupo ketamina (P50(min-máx.) o (media/DE) | Morfina (mg) grupo placebo (P50(min-máx.) o (media/DE) | valor p |
|---|---|---|---|
| 0 | 0 (0-0) | 0 (0-3) | 0.309 |
| 1 | 1(0-6) | 1 (0-5) | 0.335 |
| 2 | 3.34 (±2.85) | 3.7 (±2.58) | 0.596 |
| 3 | 6 (0-16) | 5 (0-14) | 0.594 |
| 4 | 7.5 (0-28) | 6 (0-18) | 0.590 |
| 5 | 7.5 (0-28) | 7 (0-24) | 0.619 |
| 6 | 9 (0-32) | 7 (0-31) | 0.355 |
| 9 | 10.5 (0-32) | 8 (0-40) | 0.261 |
| 12 | 11.5 (0-32) | 9 (0-42) | 0.200 |
| 15 | 12 (0-40) | 10 (0-42) | 0.230 |
| 18 | 12 (0-46) | 10 (1-44) | 0.504 |
| 21 | 14 (0-48) | 11 (1-44) | 0.338 |
| 24 | 14 (0-52) | 12(1-72) | 0.385 |
El uso de ketamina a bajas dosis como coadyuvante analgésico fue planteado hace más de 30 años24. Desde entonces, se ha tratado de demostrar su efecto en la disminución en el consumo de opioides post operatorios con diferentes modalidades de administración.
Fu et al. (1997)35 encontraron un beneficio al administrar ketamina 0.5mg/k antes de la incisión quirúrgica más una infusión mantenida durante el intraoperatorio de 10 ugr k-1 min-1 en un protocolo en el que ingresaron distintos tipos de cirugías abdominales. Sin embargo, debido al diseño del estudio, sus resultados no fueron lo suficientemente concluyentes para el beneficio del uso de ketamina. Mathisen et al. (1999) también estudiaron el uso de ketamina en pacientes operados de colecistectomía laparoscópica que fueron dados de alta a su domicilio 4 horas después de la cirugía con seguimiento telefónico. En ese estudio se utilizó R-ketamina, el isómero de la ketamina que tiene menor efecto analgésico que la ketamina racémica, pero también con menos efectos adversos. En el grupo que recibió ketamina al final de la cirugía, encontraron un retardo en el término de la anestesia (que fue estadísticamente significativo, pero clínicamente no) y un menor dolor medido por EVA a los 30 minutos del postoperatorio. El resto del tiempo de seguimiento no hubo diferencias entre los grupos estudiados (ni en las primeras 4 horas post cirugía ni en el seguimiento realizado en los 7 días posteriores). Mathisen explicó sus resultados como debidos al enfoque multimodal del tratamiento analgésico utilizado, lo que podría haber enmascarado el efecto de la ketamina36. Un año después, Dahl et al. (2000)37 compararon el uso de una dosis de 0.4mg/k de ketamina antes de la incisión quirúrgica en histerectomía abdominal versus una dosis al final de la cirugía sin encontrar un efecto de disminución de consumo de opioides post operatorio. Menigeaux et al. (2000) en cirugía de reparación artroscópica de ligamento cruzado anterior de rodilla bajo anestesia general, utilizaron dosis de 0.15mg/k antes de la incisión quirúrgica en un grupo y al final de la cirugía en otro. Encontraron que esta pequeña dosis disminuye el consumo de morfina post operatoria y mejora la movilización de sus pacientes al compararlo con placebo38.
Ante la aparición de múltiples trabajos en los que se exploraba el uso como analgésico de la ketamina, Rae et al. (2013) publicaron una revisión Cochrane cuyo principal objetivo fue evaluar la tolerancia y efectividad del uso de ketamina en dosis sub anestésicas en el manejo del dolor agudo post operatorio39. Esta revisión incluyó 2240 pacientes de 37 estudios. Aunque el resultado mostró una disminución del consumo de morfina, de las náuseas y de los vómitos en el post operatorio, la heterogeneidad de los estudios incluidos y las diferentes dosis de ketamina usadas, así como los momentos en los que fue administrada nos hicieron tener ciertas precauciones al momento de considerar definitivos sus conclusiones. Por otro lado, Nistal-Nuño et al. (2014) realizaron un estudio en el que compararon el uso de un bolo único preincisional de ketamina de 0.5mg/k en cirugías coloproctológicas (hemicolectomia izquierda, hemicolectomia derecha y resecciones abiertas) versus placebo, no encontrando diferencias estadísticamente significativas en el consumo de morfina postoperatorio40.
Este estudio fue diseñado para comparar el efecto de una dosis de carga de ketamina administrada antes de la incisión asociada a una infusión continua, a dosis sub anestésica, solamente durante el periodo intraoperatorio. De esta manera se pretendía tener un efecto en el receptor NMDA antes de la agresión quirúrgica y mantener este efecto durante todo el proceso operatorio al continuar la administración y lograr una concentración estimada de 100 ng/ml de ketamina durante la cirugía, tal como fue planteado por Suzuki (2009, 2014)41,42. Sin embargo, no se observaron diferencias significativas en el consumo post operatorio de morfina entre los grupos. Van Elstraete et al. (2004) plantearon que para lograr un efecto con la administración de ketamina preoperatoria es necesario que el receptor NMDA se active con el estímulo nociceptivo y de esta manera el uso de un antagonista no competitivo podría tener un efecto en la disminución de la transmisión de los impulsos en las vías nociceptivas y disminuir así el dolor. En nuestro centro se utiliza un protocolo de analgesia multimodal estandarizado en la cirugía de MGL. Doce horas previas a la cirugía se les administra 150mg de pregabalina vía oral y en el intraoperatorio se administran un AINE, paracetamol y una dosis entre 80 a 100 ug de morfina antes de la incisión una vez que se ha iniciado la anestesia y antes de la incisión quirúrgica. El uso de estos distintos medicamentos que actúan a distintos niveles de las vías del dolor podría haber ayudado a explicar, al menos en parte, nuestros resultados ya que el nivel analgésico pudo haber sido adecuado antes de la administración de ketamina y por lo tanto la activación central no haber ocurrido43. En este contexto, el efecto de la ketamina administrada no se reflejaría en un menor consumo de opiáceos.
Con respecto a la evaluación del dolor, las evaluaciones medidas fueron mayores a 4 las primeras 4 horas post operatorias y luego se mantuvieron bajo esa graduación. No se evidenciaron alzas mayores luego de ese periodo. Ambos grupos no mostraron diferencias significativas, lo que confirma el manejo adecuado del dolor.
El uso de fentanyl se mantuvo entre 2-3 ug/kg en ambos grupos. Sin embargo, en el grupo que no recibió ketamina se utilizó una dosis mayor. Esta situación fue debida a que la dosis de Fentanyl a utilizar, se dejó a decisión del anestesiólogo tratante. La diferencia fue estadísticamente significativa, pero clínicamente no lo fue.
Con respecto a los efectos adversos de la ketamina, a estas dosis no se presentaron efectos psicomiméticos o nistagmus en los pacientes que recibieron ketamina lo que confirma lo encontrado en otros estudios en los que se ha usado ketamina a dosis sub anestésicas.
Tampoco se encontraron diferencias entre los grupos respecto a la presencia de nauseas y/o vómitos. En ambos grupos el 9.6% de los pacientes presentó esta situación durante las 24 horas de seguimiento. La gastrectomía en manga, por tratarse de una cirugía laparoscópica y por lo tanto, con mayor riesgo de presentar nauseas y/o vómitos post operatorios, es una cirugía en la que se realiza prevención de esta complicación de manera activa, tal como se sugiere en las publicaciones internacionales44, lo que podría explicar este resultado. Sin embargo, esta prevalencia fue menor a la de estudios previos no publicados realizados en nuestra institución.
La deambulación de los pacientes en ambos grupos no presentó diferencias significativas por lo que no se alteró el plan de movilización precoz de los pacientes obesos en el periodo post operatorio.
El nivel de sedación en todo el periodo de estudio tampoco presentó diferencias significativas entre ambos grupos durante el periodo estudiado, pero el diseño del estudio tampoco fue hecho para encontrarlas.
Este estudio tiene limitaciones. Los pacientes obesos que fueron ingresados tuvieron un IMC menor de 40kg/m2 en su mayoría y el seguimiento fue solamente de 24 horas. Otra de sus limitaciones podría ser que la diferencia que se esperaba encontrar fue grande (una disminución de un 50% en el consumo de morfina al utilizar ketamina) y que bajo estas condiciones, diferencias menores, pero significativas, podrían haber quedado encubiertas. Sin embargo, las diferencias encontradas son clínicamente no relevantes y no significativas por lo que es poco probable que aumentar el número de participantes para intentar encontrar diferencias menores sea una medida útil.
CONCLUSIÓNEl uso de ketamina en dosis sub anestésicas en cirugía de manga laparoscópica no mostro una disminución del consumo de morfina en las primeras 24 horas post operatorias. El uso de ketamina no produjo un efecto de “preventive” analgesia en estas condiciones ni de disminución de la hiperalgesia post operatoria encontrado en otros estudios45-49.
Declaración de interésFinanciamiento:
Este estudio de realizó con fondos de investigación de la Dirección Académica de Clínica Las Condes (DACLC). La DACLC no intervino en el diseño del estudio, análisis ni en la interpretación de los resultados, así como tampoco en la revisión y preparación del manuscrito. Ninguno de los investigadores participantes en este estudio declaró conflictos de interés de ninguna clase.
Referencias no citadas