La Enfermedad de Crohn es una enfermedad crónica progresiva que afecta el tubo digestivo. El objetivo de tratamiento es un control adecuado de la enfermedad para evitar progresión y deterioro de la calidad de vida, pudiendo con una terapia personalizada lograr un buen pronóstico. En este artículo se proponen algoritmos de tratamiento y de seguimiento de los escenarios más frecuentes que presentan los pacientes con Enfermedad de Crohn.
Crohn's disease is a chronic and progressive disease that affects the gut. Currently treatment should be based on treat to target concept to prevent progression and deterioration of the quality of life. With a personalized therapy it could be possible to achieve a good prognosis. In this article we propose algorithms for treatment and follow-up of the most frequent scenarios presented by patients with Crohn's disease.
La Enfermedad de Crohn (EC) forma parte de la Enfermedad Inflamatoria Intestinal (EII) y se caracteriza por una inflamación crónica, de etiología desconocida del tubo digestivo, donde existe una desregulación del sistema inmune en el reconocimiento de ciertos antígenos bacterianos en el lumen intestinal que gatilla una respuesta inflamatoria. El proceso inflamatorio a su vez, produce un daño progresivo que avanza en el tiempo y genera alteraciones que pueden afectar severamente la calidad de vida de los pacientes1.
Las estrategias terapéuticas para la EC deben apuntar a modificar el curso clínico, logrando remisión de la enfermedad, evitando de este modo progresión a fenotipos penetrantes o fibroestenóticos que podrían requerir mayor necesidad de hospitalizaciones, cirugías y que pueden finalmente inhabilitar a los pacientes para las actividades de la vida diaria2.
En el contexto de un equipo multidisciplinario dedicado a tratar pacientes con EII, hemos elaborado algoritmos de tratamiento para aquellas situaciones clínicas que con mayor frecuencia presentan pacientes con EC. La meta es entregar una medicina personalizada, donde a cada paciente se le deben plantear y discutir los objetivos terapéuticos, que deben acordarse en conjunto, explicándoles las opciones de tratamiento y los potenciales riesgos y beneficios de estas estrategias. Una vez realizada la evaluación inicial, donde eventualmente y según sea necesario, participan profesionales de la psicología, nutrición, kinesiología y otras especialidades médicas como reumatólogos, dermatólogos, infectólogos, obstetras, entre otras, se deben considerar las medidas de cuidado general y de prevención de complicaciones asociadas a la enfermedad y/o al tratamiento.
En los algoritmos que se presentan a continuación se deben considerar siempre los siguientes elementos:
- 1.
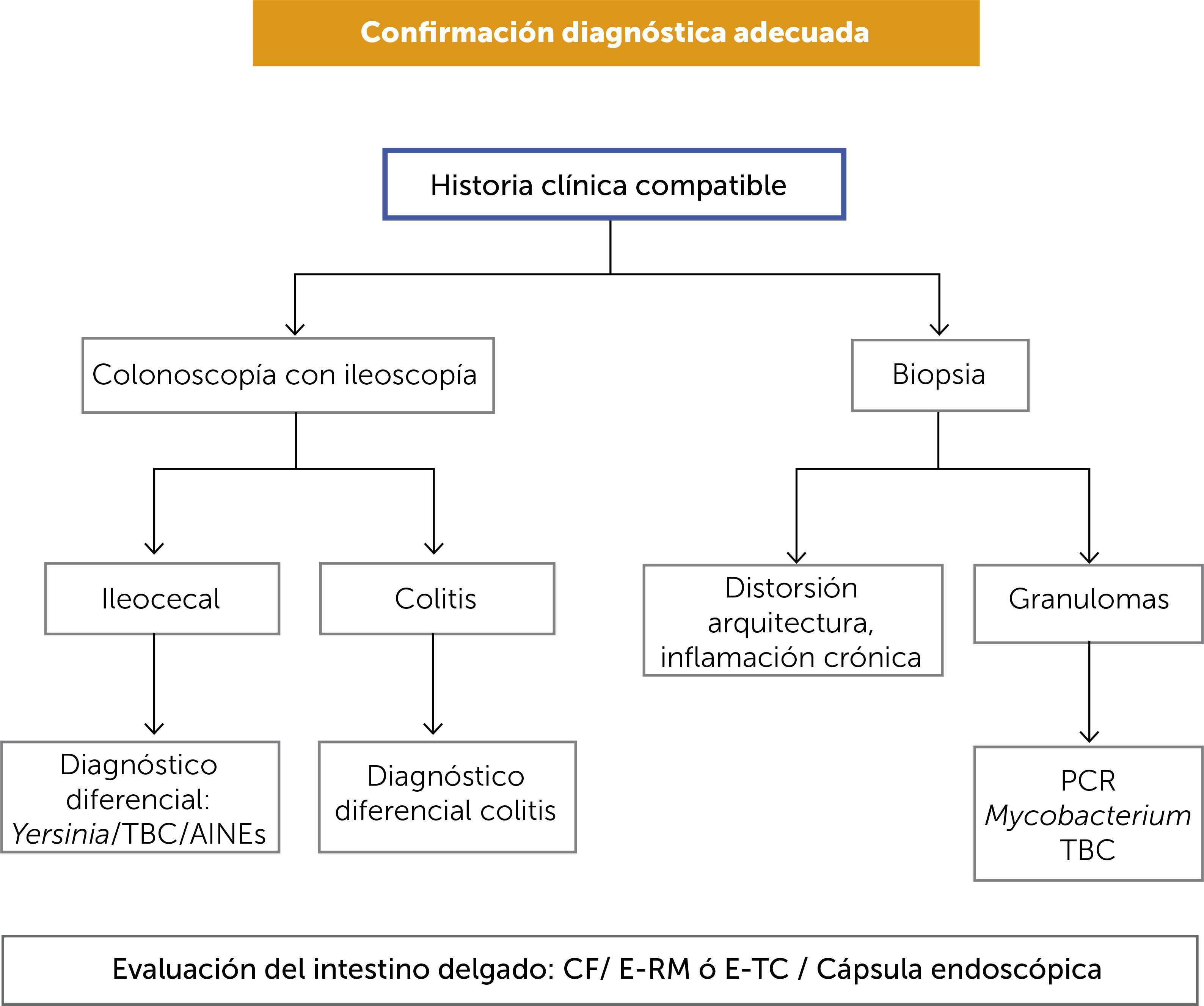
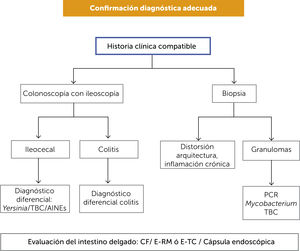
Confirmación diagnóstica adecuada (Figura 1).
- 2.
Establecer al comienzo del diagnóstico, la extensión y severidad de la enfermedad3,4.
- 3.
Identificar factores de mal pronóstico que permitan elegir estrategias que eviten complicaciones de la enfermedad.
- 4.
Una vez iniciada una estrategia de tratamiento, considerar plazos para evaluar la eficacia de ésta y realizar ajustes o cambios en la estrategia si no se han logrado los objetivos terapéuticos.
- 5.
Optimización de terapia: se debe optimizar el tratamiento, en el caso de no alcanzar los objetivos terapéuticos. Idealmente posterior a la evaluación de los niveles plasmáticos de los medicamentos anti-factor de necrosis tumoral alfa (anti-TNF) y sus anticuerpos. Actualmente en Chile hay acceso a infliximab, adalimumab y certolizumab para EC. En el caso de que el paciente se encuentre con tiopurínicos, se recomienda medir los niveles de sus metabolitos en sangre, con el objetivo de ajustar dosis según el resultado. Si se considera que ha fracasado la terapia, evaluar cambiar a otra familia de biológico según disponibilidad y experiencia local5,6.
- 6.
Tener un adecuado monitoreo; además del monitoreo clínico y de los exámenes generales, los pacientes con EII y por lo tanto, aquellos con EC, requieren elementos objetivos para determinar la actividad de la enfermedad, como calprotectina fecal (CF), estudios endoscópicos, biopsia y/o imágenes según la localización y condición de severidad establecida al diagnóstico7,8.
- 7.
En pacientes que se controlen con estudios de imágenes, preferir el ultrasonido o Entero-Resonancia Magnética (E-RM) por sobre Entero-Tomografía Computada (E-TC) con el fin de reducir exposición a radiación9. La evaluación imagenológica debe ser realizada por un radiólogo con experiencia en EII.
- 8.
Debido a la influencia en el pronóstico y eficacia de los tratamientos, en un paciente con EC que fume, siempre se debe considerar no sólo el consejo de suspensión del hábito tabáquico, sino que se le deben ofrecer terapias de apoyo para lograrlo10.
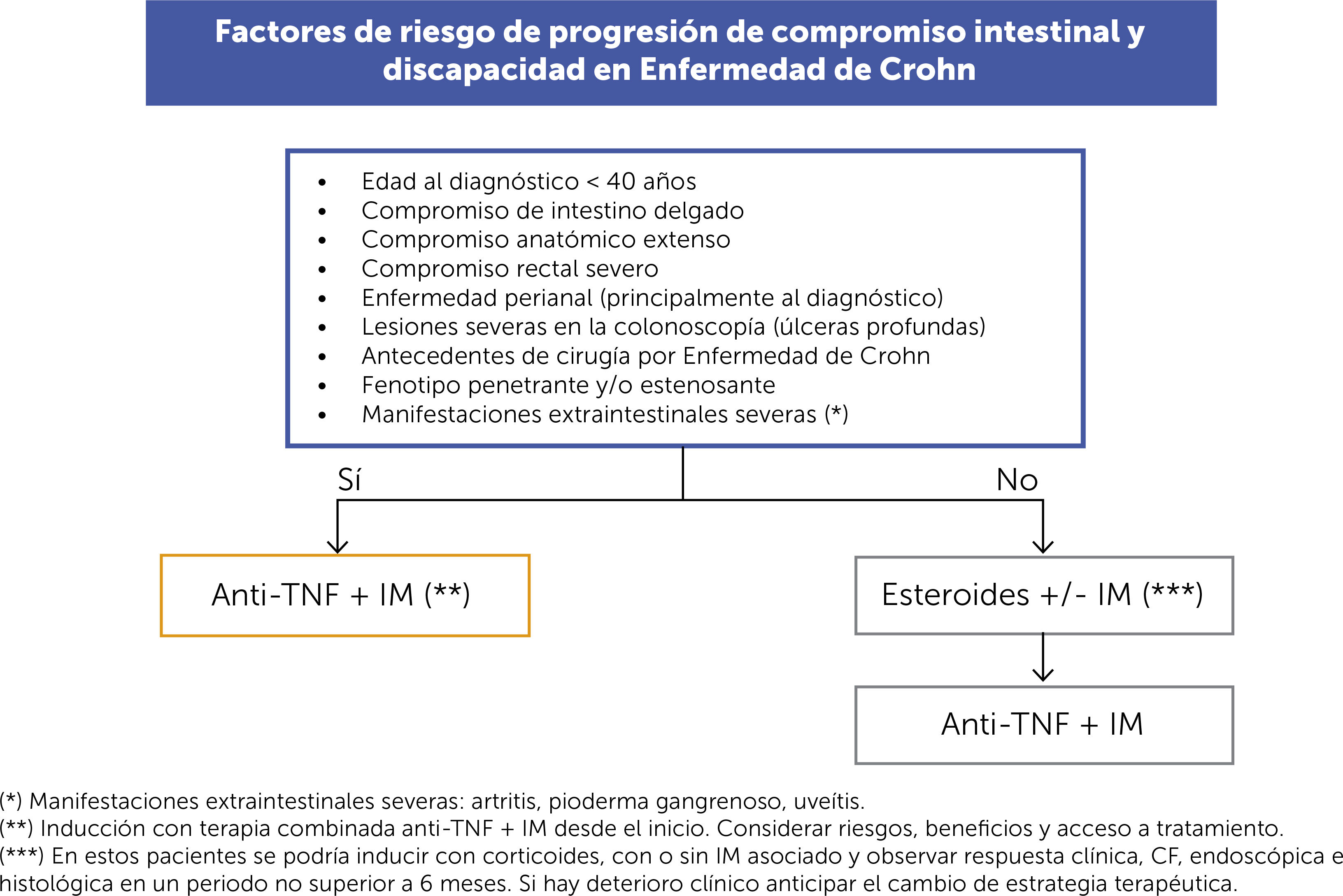
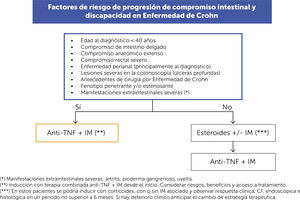
En los pacientes con EC existen numerosos factores que se han asociado a un mal pronóstico y se enuncian en la Figura 2. Debemos mencionar que hemos incluido junto a los otros elementos clínicos, las manifestaciones extraintestinales más severas como artritis, pioderma gangrenoso y uveítis como factores a considerar al momento de decidir el inicio de la terapia Anti-TNF, idealmente combinado con inmunomoduladores (IM) (azatioprina o metotrexato). El compromiso extraintestinal representa un nivel de inflamación de otros órganos o tejidos los cuales inhabilitan severamente a los pacientes con EII. La decisión de utilizar terapia combinada con IM depende de factores como el tipo de Anti-TNF (existiendo mayor evidencia de su impacto positivo en la eficacia para infliximab (IFX) en comparación a adalimumab (ADA) o certolizumab (CTZ)), los potenciales riesgos (ej. en hombres jóvenes de preferencia evitar azatioprina o en mujeres en edad fértil evitar metotrexato) y la tolerancia del paciente11,12.
En aquellos pacientes que no presenten estos factores de mal pronóstico, se podría inducir con corticoides, con o sin IM y observar respuesta clínica, CF, endoscópica e histológica en un período no superior a 6 meses.
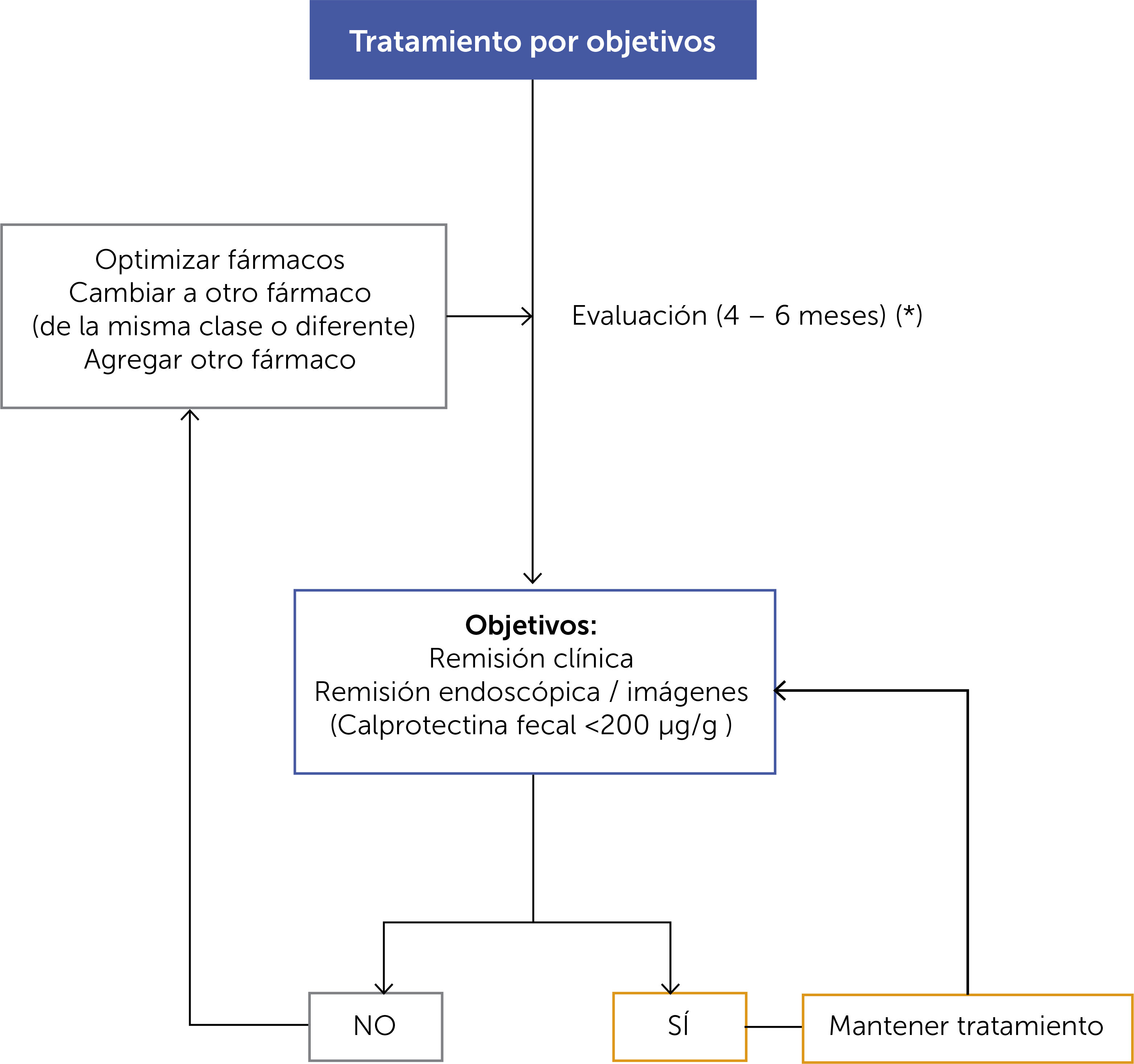
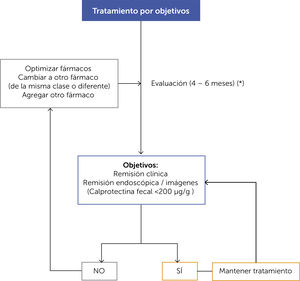
EVALUACIÓN DE TRATAMIENTO EN RELACIÓN A OBJETIVOS (FIGURA 3)Una vez iniciada la estrategia terapéutica, se debe considerar los plazos adecuados para evaluar la eficacia, considerando en general que la respuesta clínica dependiendo el tipo de fármaco a usar, se observa en unas 2 a 4 semanas para los 5-ASA derivados y anti-TNF y de 12-16 semanas para los agentes inmunomoduladores. Independiente de la respuesta clínica, es necesario el uso de parámetros objetivos como biomarcadores (calprotectina), endoscópicos y/o imágenes y en función de la clínica y estos parámetros definir ajustes o cambios en la estrategia de tratamiento si no hubieran sido alcanzados los objetivos.
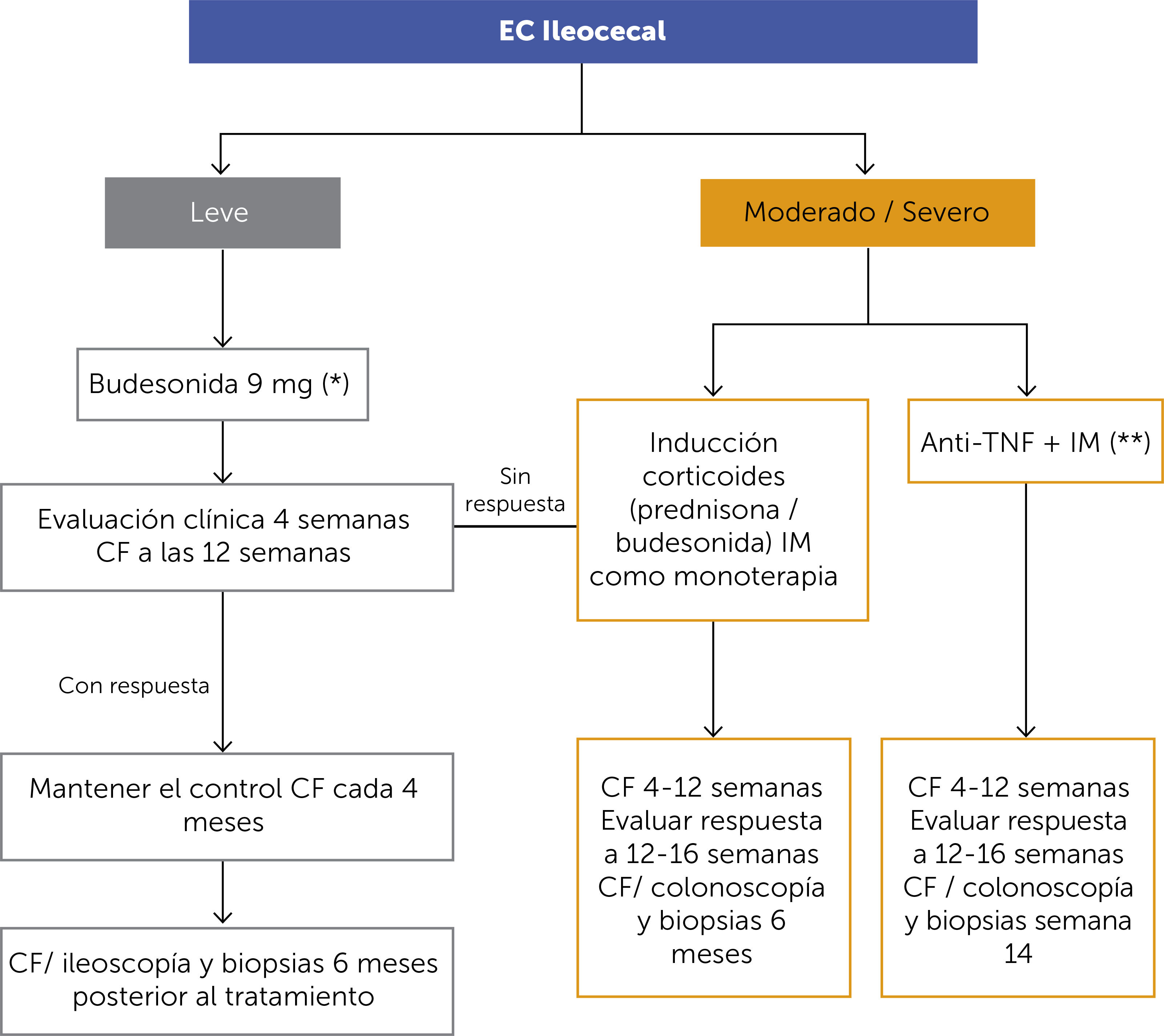
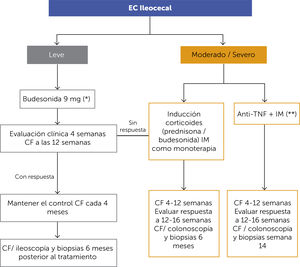
ALGORITMO DE TRATAMIENTO DE ENFERMEDAD DE CROHN ILEOCECAL (FIGURA 4)En los pacientes con EC ileal o ileocecal leve, se recomienda el uso de budesonida por 3 meses (9mg/día por un mes, reducir a 6mg/día el 2° mes y luego 3mg/día el último mes y suspender). Si el paciente responde adecuadamente y los controles de CF son adecuados (<200μg/g), se recomienda el seguimiento clínico y con CF cada 4 meses. De no haber respuesta se debe considerar inducción con corticoides e IM para la mantención.
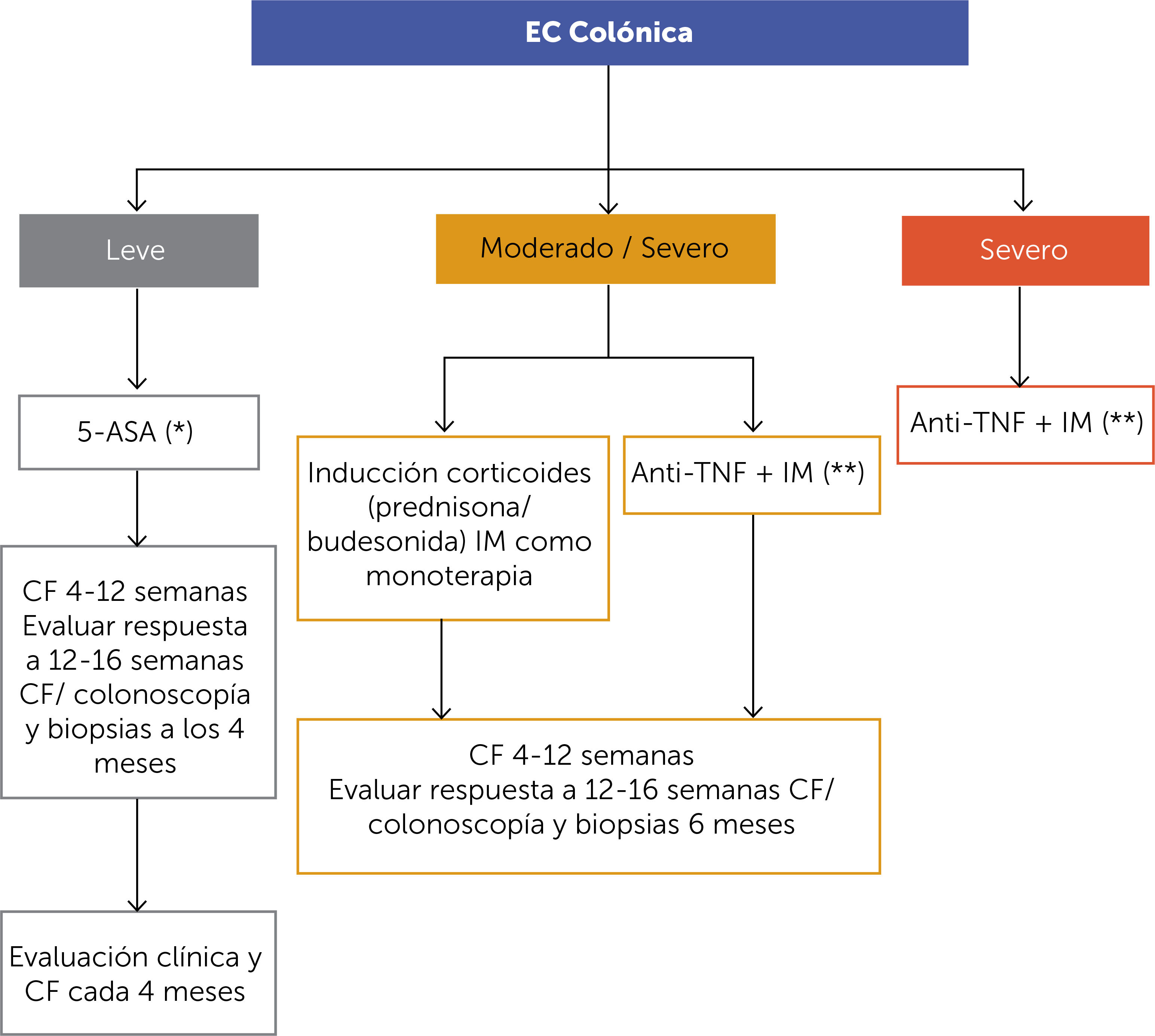
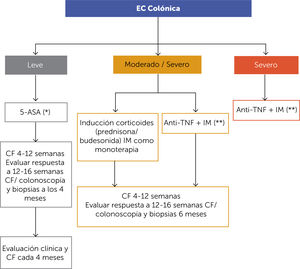
ALGORITMO DE TRATAMIENTO DE ENFERMEDAD DE CROHN COLÓNICA (FIGURA 5)Si bien la evidencia es negativa para el uso de 5-aminosalicilatos (5-ASA) derivados en la EC y su uso no está recomendado, la excepción podrían ser pacientes con EC con compromiso leve y de ubicación exclusivamente colónica. De optarse por esta estrategia de tratamiento, consideramos absolutamente imprescindible un monitoreo estricto, seguimiento con CF y colonoscopía con biopsias a los 6 meses de iniciado el tratamiento. De lograrse la remisión de la enfermedad el seguimiento debe ser con CF cada 4 meses. En caso de elevar CF >200μg/g de manera repetida (1 mes entre ambas determinaciones en paciente asintomático), se recomienda reevaluar el colon con colonoscopía y de resultar normal, considerar estudio de intestino delgado por cápsula o E-RM.
En los pacientes con EC de colon moderado a severo, el tipo de tratamiento dependerá de la presencia o no de factores de riesgo de progresión, como se indica en el algoritmo.
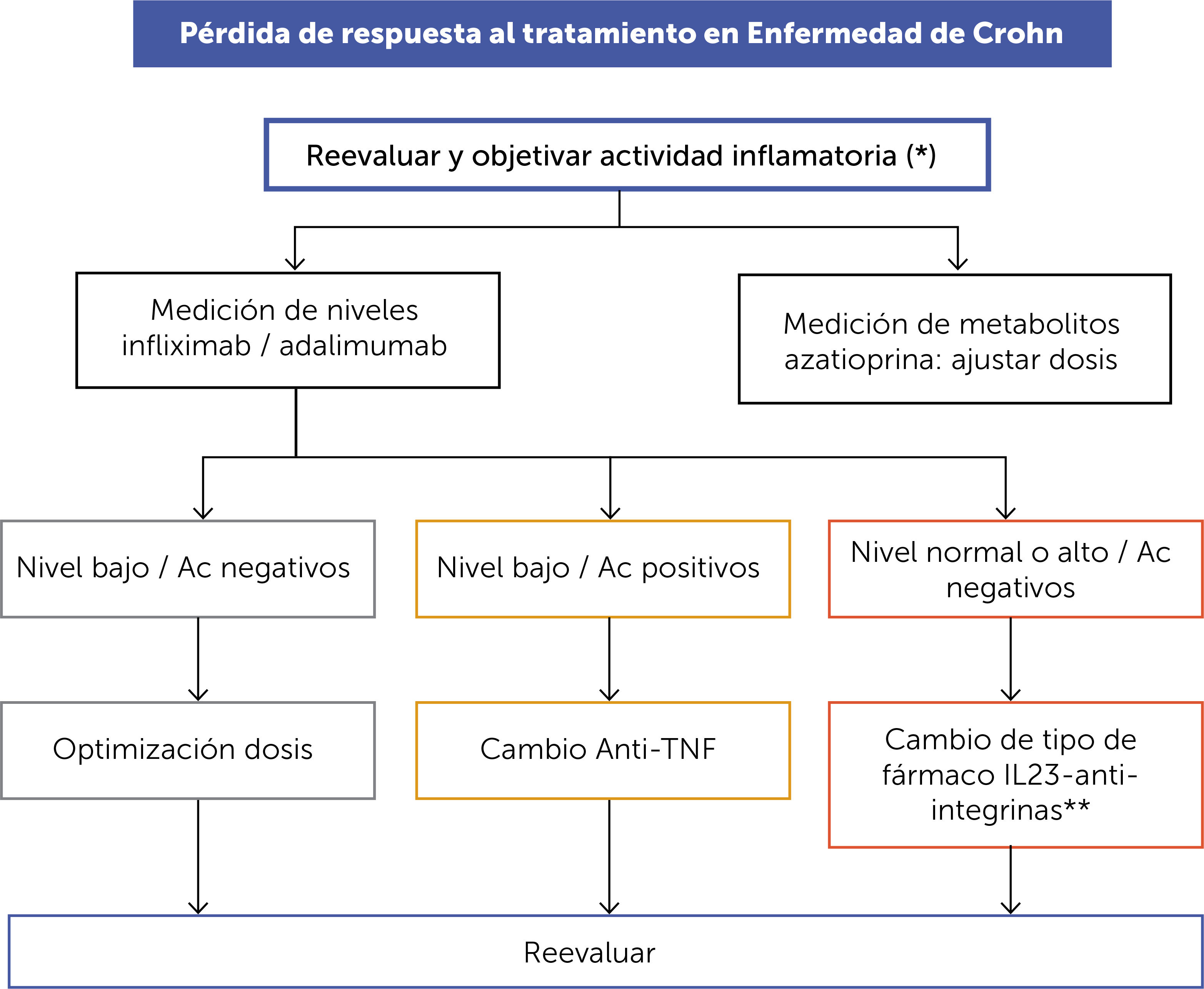
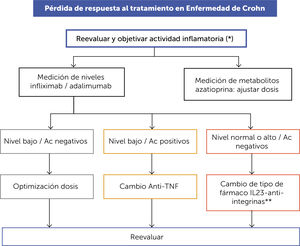
ALGORITMO DE TRATAMIENTO DE PÉRDIDA DE RESPUESTA AL TRATAMIENTO EN ENFERMEDAD DE CROHN (FIGURA 6)En los pacientes con EC inflamatorio que se encontraban en remisión e inician síntomas gastrointestinales, se debe considerar como una posibilidad la pérdida de respuesta al tratamiento una vez que se han descartado otras condiciones como falta de adherencia (suspensión o interrupción del tratamiento), infecciones intercurrentes donde siempre se debe descartar Clostridium difficile por PCR y citomegalovirus (inmunohistoquímica ó PCR, ambas en biopsia). Se debe objetivar la actividad inflamatoria con CF, colonoscopía con ileoscopía, biopsias y de ser necesario estudio de imágenes (idealmente ultrasonido o E-RM). Es importante la objetivación de la actividad inflamatoria, pues la sola presencia de síntomas podría no deberse a la EC, sino a otras entidades patológicas como síndrome de intestino irritable, sobrecrecimiento bacteriano intestinal, intolerancia a la lactosa, enfermedad celiaca, diarrea por sales biliares, entre otras.
Una vez confirmada la pérdida de respuesta, que puede ocurrir hasta en un 40% de los pacientes, el algoritmo plantea la medición de niveles de fármacos (metabolitos de azatioprina, niveles de IFX y ADA) y anticuerpos antidrogas biológicas para definir los ajustes necesarios. Es importante destacar que, en una publicación reciente, la presencia de anticuerpos anti-TNF pudo ser evitada con el incremento de dosis y acortando el intervalo de administración del fármaco6.
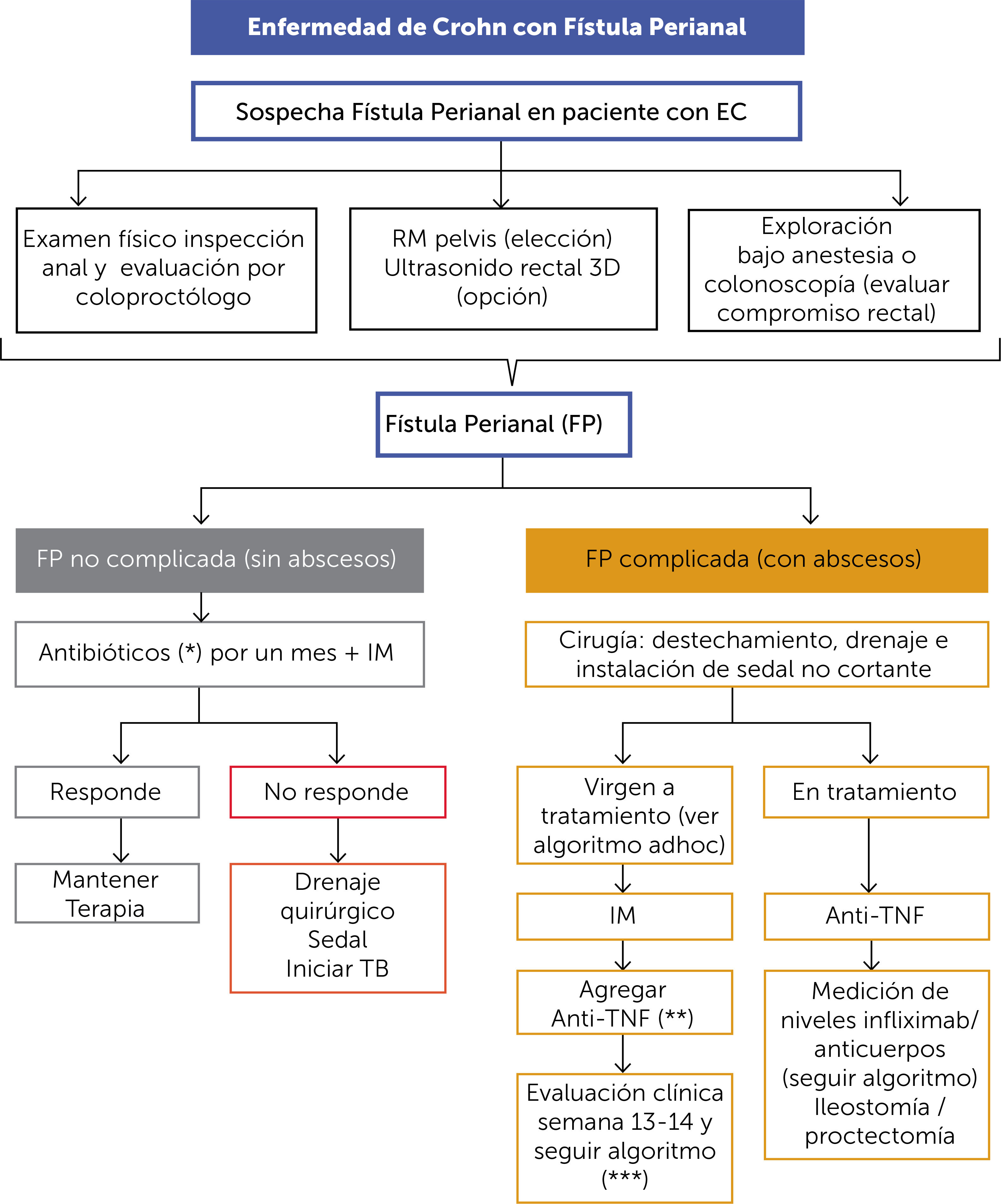
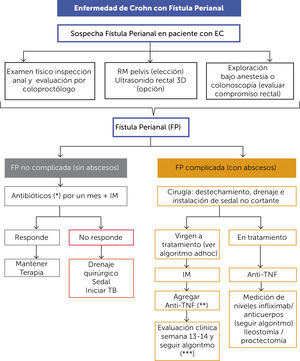
ALGORITMO DE TRATAMIENTO DE LA ENFERMEDAD DE CROHN CON FÍSTULA PERIANAL (FIGURAS 7 Y 8)La evaluación a través de la historia y el examen físico sobre la búsqueda de Enfermedad de Crohn con fístula perianal (ECp) debe hacerse de manera sistemática en todos los pacientes con EC conocida o recién diagnosticada, pues puede llegar a afectar hasta un 20% de los pacientes y tiene implicancias en el tratamiento y pronóstico.
Frente a la sospecha de ECp, se debe contactar al coloproctológo para un examen físico de la región ano-rectal acucioso, estudiar con RM pelvis y definir la necesidad de exploración bajo anestesia para la confirmación del diagnóstico (Figura 7).
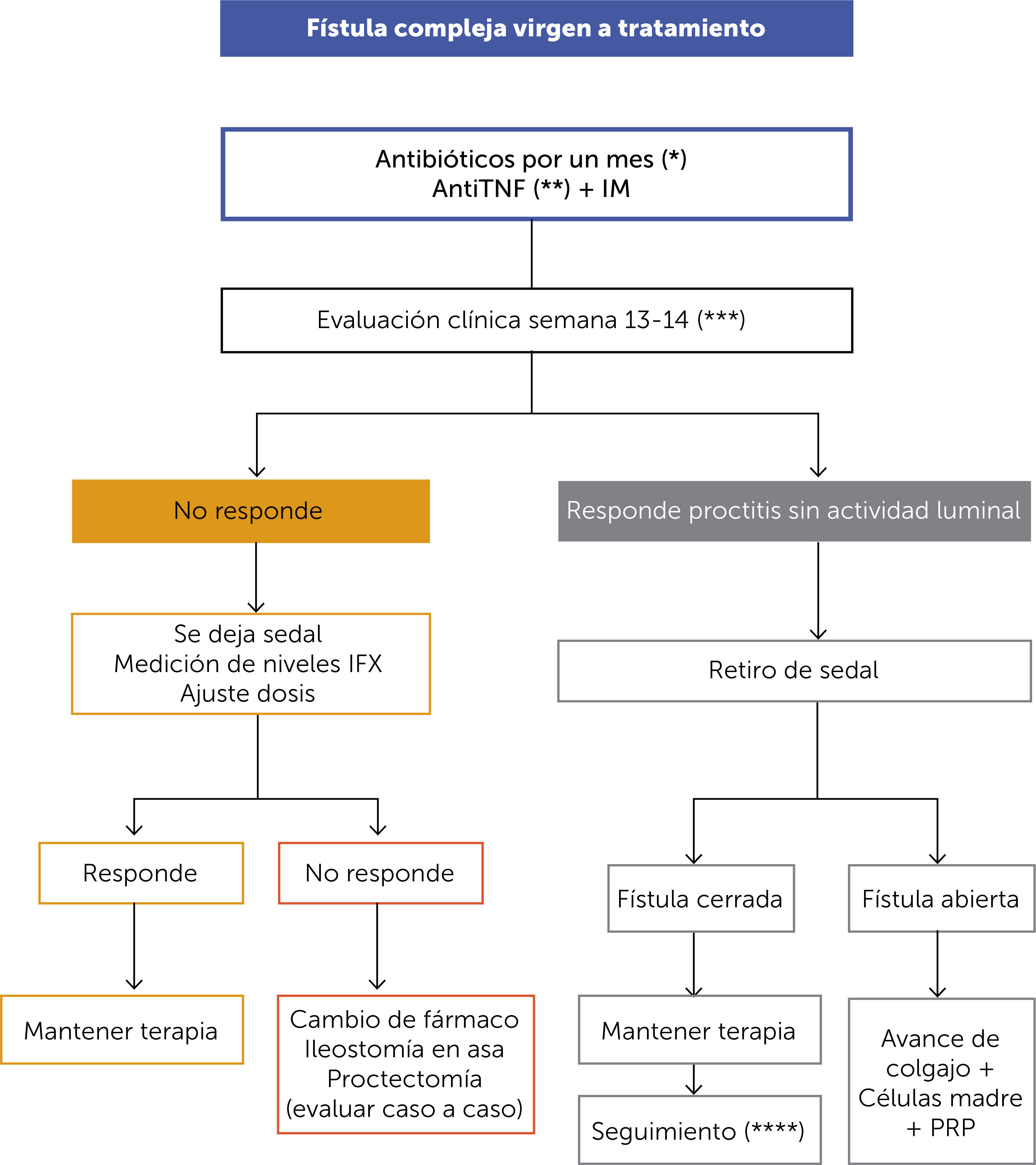
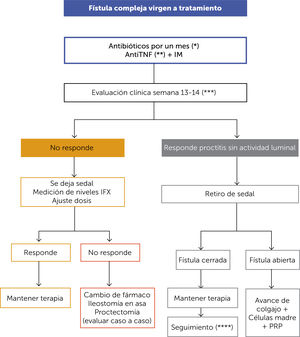
En el caso de fístulas complicadas con abscesos, el manejo considera el tratamiento quirúrgico urgente con destechamiento, drenaje e instalación de sedal(es) antes de cualquier tratamiento farmacológico. Una vez realizado el manejo quirúrgico de la fístula, el tratamiento médico en pacientes vírgenes a tratamiento (Figura 8) debe incluir el uso de antibióticos (ciprofloxacino 500mg cada 12hrs. + metronidazol 500mg cada 8hrs. por 1 mes)13 más terapia combinada de IM y anti-TNF. En este escenario se prefiere el uso de IFX por sobre ADA como primera línea de anti-TNF en dosis de inducción de 5 a 10mg/kg a las 0-2-6 semanas, buscando niveles séricos más elevados de IFX que en pacientes con EC de fenotipo inflamatorio. La evaluación de la respuesta se realiza a la semana 13-14 (antes de la primera dosis de mantención de IFX) con colonoscopía y biopsias. Si se observa una respuesta favorable con ausencia de proctitis, se puede proceder a retirar los sedales y observar la evolución. En caso de que la fístula no cierre en esas condiciones, se considerará tratamiento quirúrgico con avance de colgajo endorrectal, inyección de células madre (CM) y plasma rico en plaquetas (PRP), o la combinación de ambos en centros especializados14.
En caso de que no haya respuesta adecuada al tratamiento inicial con IM + IFX, se dejan los sedales in situ y se procede a optimizar tratamiento según metabolitos de tiopurínicos y niveles/anticuerpos para IFX. Hay que considerar que para el tratamiento de ECp, niveles elevados de IFX pueden ser favorables para el cierre de las fístulas.
En el caso de que el paciente ya esté bajo tratamiento previo al diagnóstico de la fístula (Figura 7), la modificación del tratamiento depende del esquema terapéutico en curso. En pacientes en tratamiento con IM se optimiza la terapia según metabolitos y se agrega terapia biológica con IFX; en pacientes que desarrollan la fístula bajo tratamiento con IM + terapia biológica, se requiere optimización del tratamiento con metabolitos y niveles/anticuerpos como se señala en el “Algoritmo de pérdida de respuesta al tratamiento en enfermedad de Crohn” (Figura 6). En casos de difícil manejo, una desfuncionalización mediante ostomía temporaria puede ser útil para apoyar el cambio de tratamiento, y en casos refractarios a toda terapia, una proctectomía con ileostomía definitiva puede ser necesaria para brindarle al paciente una mejor calidad de vida.
Si en la evaluación inicial no hay presencia de absceso (fístula no complicada) (Figura 7), la fístula se puede manejar inicialmente con antibióticos (ciprofloxacino 500mg cada 12hrs.+metronidazol 500mg cada 8hrs. por 1 mes) más IM. Si no hay respuesta en ese plazo, se debe considerar la exploración bajo anestesia, drenaje de la fístula con instalación de sedal y el inicio de terapia biológica.
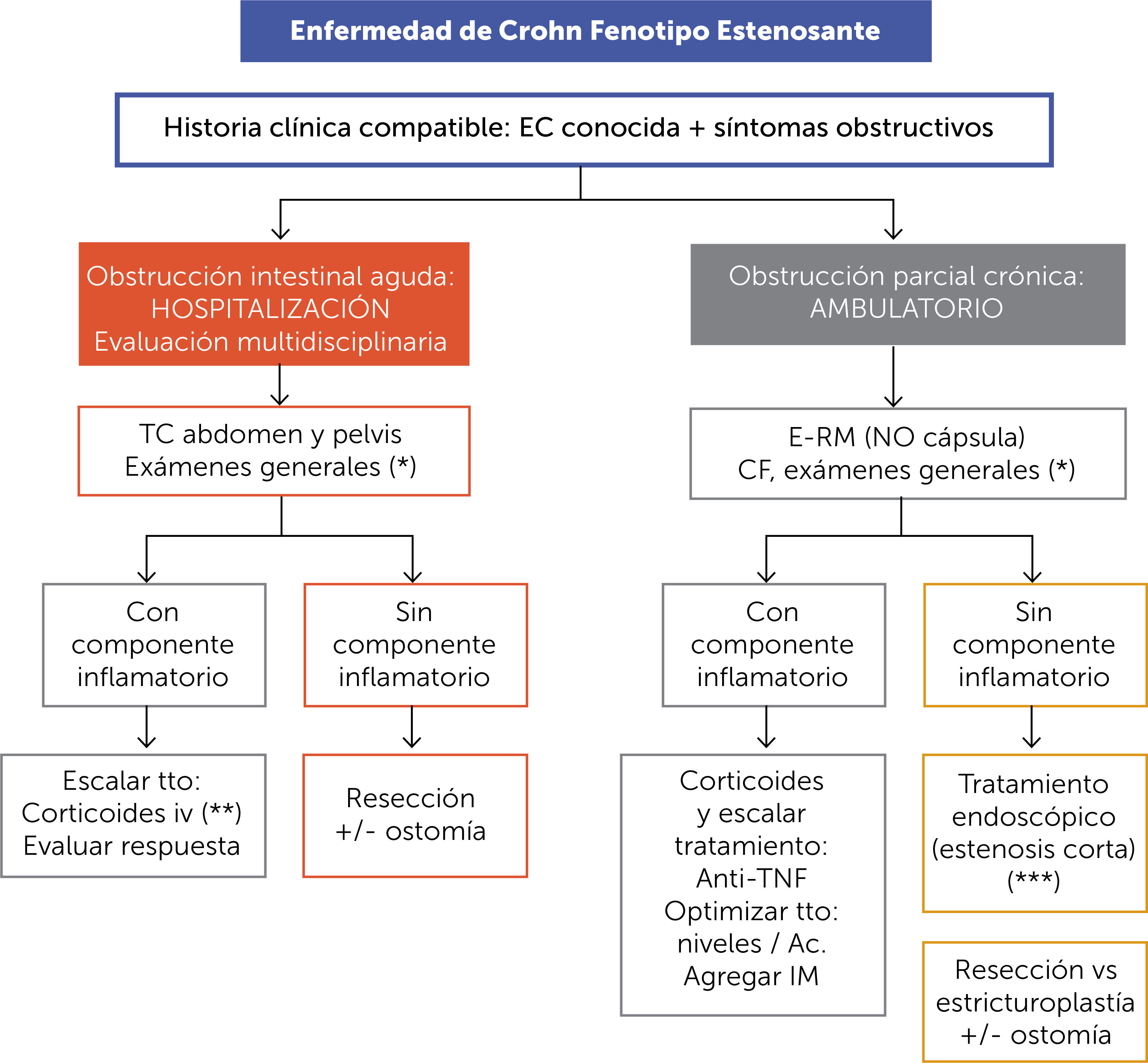
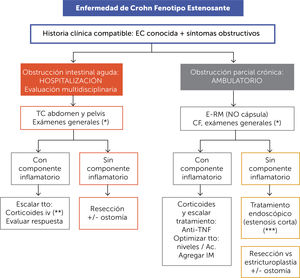
ALGORITMO DE TRATAMIENTO DE ENFERMEDAD DE CROHN FENOTIPO ESTENOSANTE (FIGURA 9)En este algoritmo, se distingue la situación clínica de la obstrucción intestinal aguda, que habitualmente hace consultar al paciente en el servicio de urgencia, donde el examen de elección es la tomografía computada (TC) de abdomen y pelvis que confirma el diagnóstico y de encontrarse elementos inflamatorios, la terapia de elección será el uso de corticoides por vía parenteral (hidrocortisona en nuestro centro) y se observará su respuesta clínica. Si no hay elementos inflamatorios en los exámenes de imagen se optará por la cirugía.
Es importante considerar que independiente del curso de acción, se requiere un manejo multidisciplinario con la participación del coloproctológo y nutriólogo desde el ingreso.
En aquellos pacientes que presenten un curso clínico más prolongado con síntomas sub-agudos de obstrucción (distensión abdominal, dolor abdominal post-pandrial, náuseas y baja de peso), la sospecha de obstrucción parcial crónica debe estudiarse por E-RM (evitar cápsula por el riesgo de retención) y de haber componente inflamatorio por sobre el fibro-estenótico se debe preferir optimizar la terapia médica. En caso de predominio del factor estenótico se puede optar por tratamiento endoscópico si la estenosis es inferior a 5cm, mientras que se plantea la opción quirúrgica con o sin ostomía en caso de ser superior a 5cm o fracaso en el intento endoscópico.
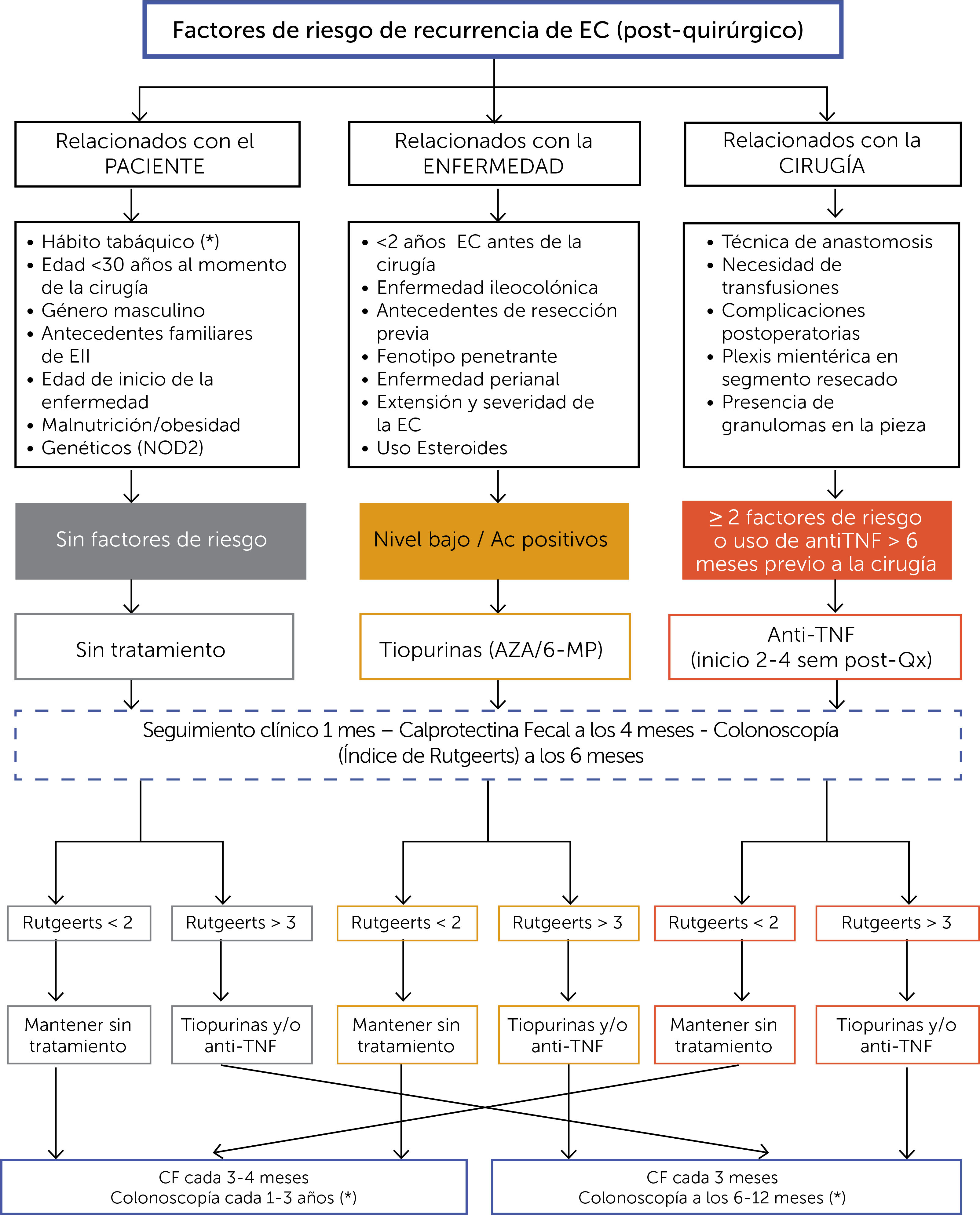
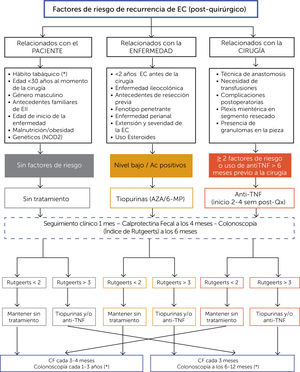
ALGORITMO DE TRATAMIENTO DEL PACIENTE CON ENFERMEDAD DE CROHN POST-QUIRÚRGICO (FIGURA 10)La cirugía en la EC no cura la enfermedad, ya que la historia natural de la misma señala que reaparece endoscópica y/o clínicamente en la mayoría de los pacientes. Se han identificado factores que se asocian a un mayor riesgo de recurrencia entre los que destacan el tabaquismo, la edad menor a 30 años al momento de la cirugía, fístula perianal e historia de cirugía previa. Estos factores son importantes al momento de definir la mejor estrategia terapéutica para prevenir la recurrencia post-quirúrgica.
A los 6 meses post cirugía debe realizarse una colonoscopía para evaluar la actividad endoscópica en el íleon de acuerdo al índice descrito por Rutgeerts3. Según los hallazgos, la decisión terapéutica deberá determinarse de acuerdo a lo descrito en el algoritmo.
El seguimiento posterior a la colonoscopía dependerá del riesgo de recurrencia determinado por el índice de Rutgeerts; score <2, CF cada 4 meses y colonoscopía cada 1 a 3 años, score >3, CF cada 3 meses y colonoscopía cada 6 a 12 meses.
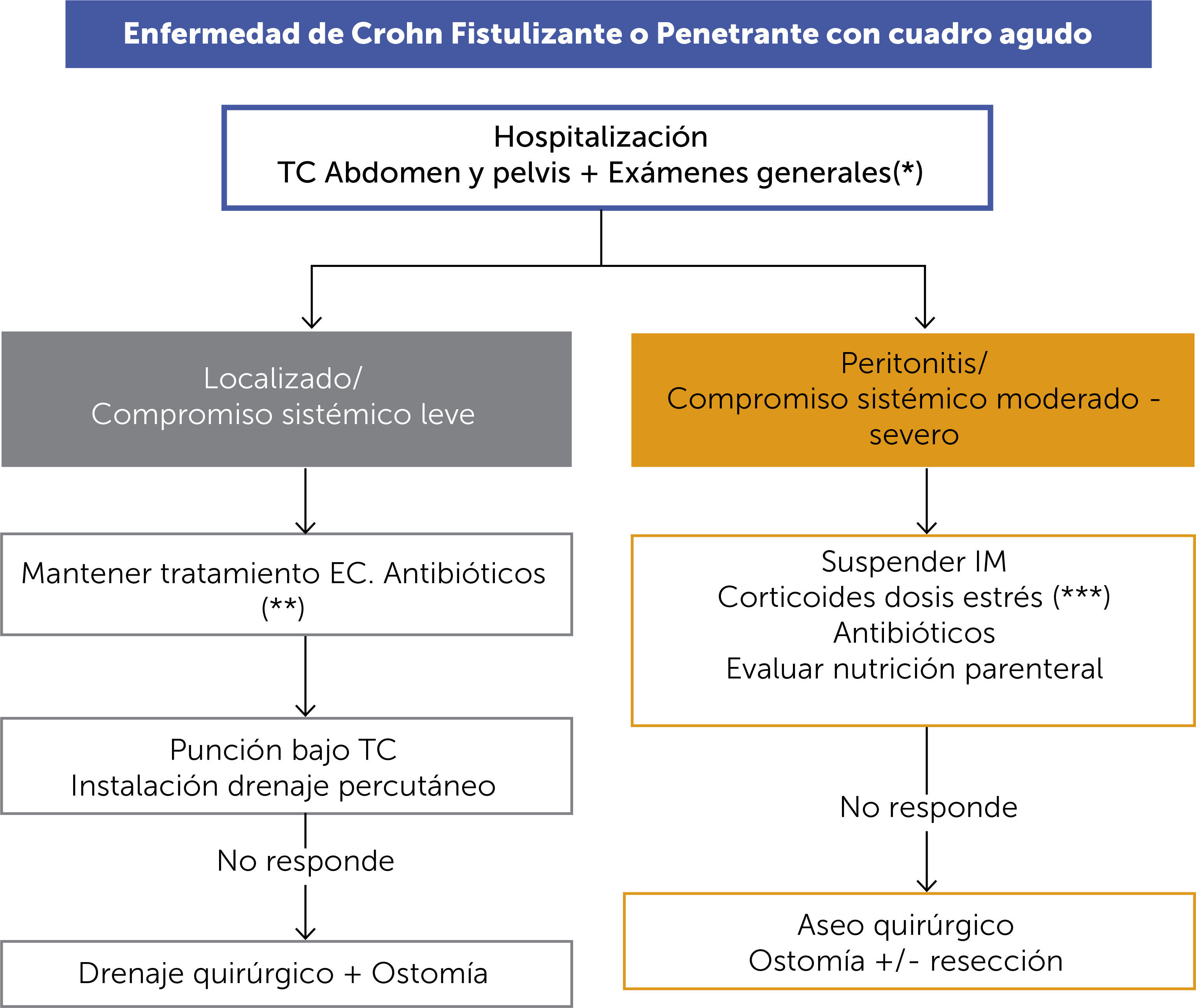
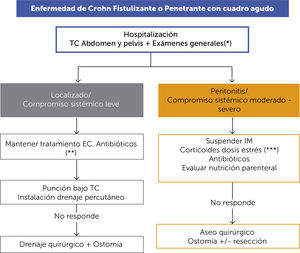
ALGORITMO DE TRATAMIENTO DE LA ENFERMEDAD DE CROHN FISTULIZANTE O PENETRANTE CON CUADRO AGUDO (FIGURA 11)Los pacientes con EC con fenotipo fistulizante se pueden presentar con un cuadro agudo con dolor abdominal y la clínica propia de un absceso con una respuesta inflamatoria sistémica. En este escenario se requiere del manejo multidisciplinario desde el primer momento. Para aquellos con compromiso sistémico leve se debe mantener el tratamiento para la EC, agregar antibióticos y de acuerdo a los hallazgos de la TC de abdomen y pelvis, definir punción y drenaje percutáneo versus el drenaje quirúrgico con o sin la necesidad de una ostomía.
Para aquellos con peritonitis y/o compromiso sistémico moderado a severo, se recomienda suspender el tratamiento IM, suplementar corticoides en dosis de estrés si estaba bajo terapia con corticoides, uso de antibióticos y el apoyo con nutrición parenteral y aseo quirúrgico con ostomía con o sin resección.
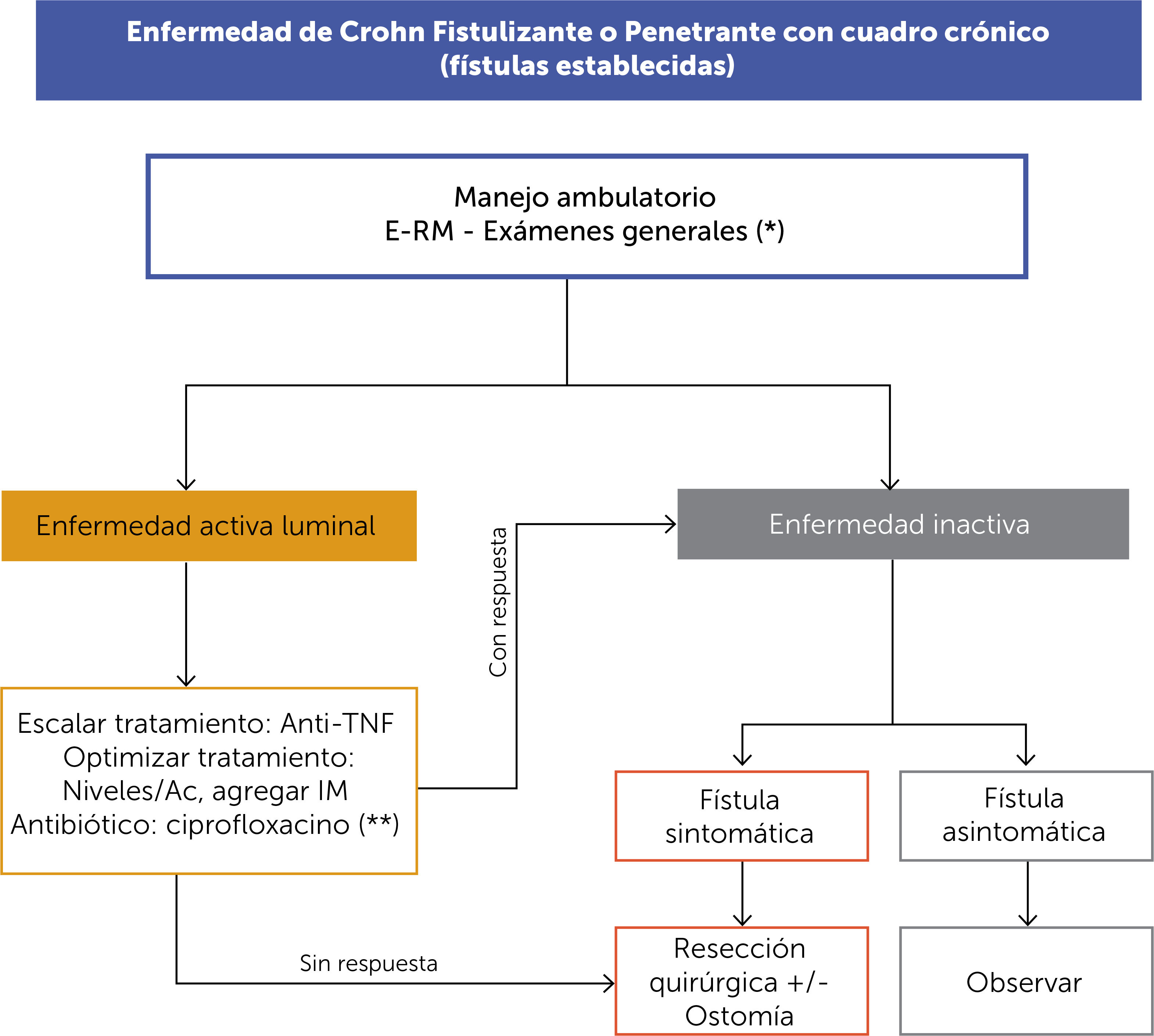
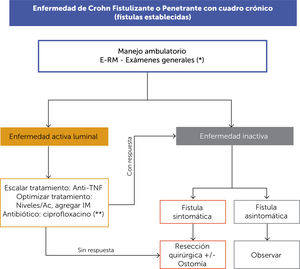
ALGORITMO DE TRATAMIENTO DE LA ENFERMEDAD DE CROHN FISTULIZANTE O PENETRANTE CON CUADRO CRÓNICO (FÍSTULAS ESTABLECIDAS) (FIGURA 12)En los pacientes con fístulas intraabdominal se debe distinguir si es un hallazgo en un paciente que se encuentra con una EC inactiva, asintomático, en cuyo caso sólo se recomienda observar. En pacientes con síntomas secundarios a la fístula, sin actividad inflamatoria luminal, la recomendación es el tratamiento quirúrgico (que considera la resección quirúrgica que puede o no requerir de una ostomía).
En pacientes con EC activa, se puede considerar optimizar el tratamiento médico con anti-TNF más IM y el uso de ciprofloxacino o considerar de manera primaria la cirugía para inducir remisión de la enfermedad.
COMENTARIO FINALLos algoritmos aquí expuestos, representan la visión de manejo práctico de la EC por el equipo del Programa de Enfermedad Inflamatoria Intestinal de Clínica Las Condes donde participan gastroenterólogos, coloproctológos y enfermeras, quienes incorporan los conceptos de tratamiento en función de objetivos (treat to target) de monitoreo moderno de la EII y de medicina personalizada, los cuales no pretenden ser una guía clínica ni pauta general de la EC.
Estos algoritmos se revisarán de manera periódica realizando las modificaciones en función de nuevas evidencias científicas y de la aparición de nuevas estrategias terapéuticas. Es necesario considerar que el objetivo final de toda estrategia terapéutica debe ser mejorar la calidad de vida del paciente, por lo tanto, las decisiones en estos escenarios y en otros menos frecuentes pueden variar en función de factores como efectividad, disponibilidad, costos y riesgo de cada uno de ellos.
Declaración de interésPI: Abbvie speaker y financiamiento de asistencia a un congreso. Janseen speaker. Biotoscana speaker
JL: Abbvie speaker
GP: Abbvie y Ferring speaker
LF: Abbvie speaker
CF, RQ, UK y DS declaran no tener conflictos de interés.