La fragilidad es un estado multidimensional caracterizado por la disminución de las reservas fisiológicas y de la resistencia a factores estresantes. Su dimensión física es altamente reconocida y genera vulnerabilidad para desarrollar mayor dependencia y/o muerte. Los pacientes con enfermedades respiratorias crónicas tienen un mayor riesgo de fragilidad y dentro de los factores de riesgo se encuentran las comorbilidades, tabaquismo, bajos niveles de actividad física, exacerbación sobre patología de base, hospitalizaciones recurrentes, mal nutrición y polifarmacia. La fragilidad es un proceso dinámico y modificable. Dentro de los distintos tratamientos, se encuentra la derivación oportuna a programas de rehabilitación respiratoria. El presente artículo describe la fragilidad asociada a pacientes con enfermedades respiratorias crónicas y brinda herramientas para evaluarla y modificarla.
Frailty is a multidimensional state characterized by a decrease in physiological reserves and resistance to stressors. Its physical dimension is highly recognized and increases vulnerability for developing greater dependency and/or death. Patients with chronic respiratory diseases have a higher risk of developing frailty and among the risk factors are comorbidities, smoking, low levels of physical activity, exacerbations of their underlying pathology, recurrent hospitalizations, poor nutrition and polypharmacy. Frailty is a dynamic and modifiable process. Timely referral to pulmonary rehabilitation programs is one of the different treatments available. The present article describes fragility in chronic respiratory disease patients, and offers tools to evaluate and modify it.
Las enfermedades respiratorias crónicas (ERC), representan un importante problema de salud a nivel mundial y están consideradas entre las principales causas de discapacidad severa1,2. A pesar de no ser curables, existen diferentes tratamientos que permiten controlar los síntomas y mejorar la calidad de vida de los pacientes que las padecen1–3. Dentro de las más comunes, se encuentran el asma, la enfermedad pulmonar obstructiva crónica (EPOC), las enfermedades pulmonares intersticiales difusas (EPID) y la hipertensión pulmonar. El consumo de tabaco, la contaminación del aire, los productos químicos en el trabajo, la exposición al polvo y otros contaminantes ambientales, son los principales factores de riesgo1–4.
La principal alteración de las ERC es sobre la función pulmonar, siendo su principal síntoma la disnea, la cual tiene como consecuencia sensación permanente de fatiga y disminución a la tolerancia al ejercicio físico. Por otra parte, la ansiedad, depresión y miedo son síntomas que aparecen durante la progresión de la enfermedad y que deben ser considerados en todo momento5–7.
Además de la alteración en la función pulmonar, la disfunción músculo esquelética es una de las principales manifestaciones de las ERC e incluyen debilidad de cuádriceps, atrofia muscular y cambio en el tipo de fibra muscular. Por otra parte, existen alteraciones asociadas al envejecimiento que contribuyen a la disfunción músculo esquelética, dentro de ellos la sarcopenia8, y la fragilidad1,8. Hoy en día la fragilidad es considerada como un síndrome, el cual es modificable con la derivación oportuna a programas de rehabilitación respiratoria9. El presente artículo tiene como objetivo describir la fragilidad en pacientes con enfermedades respiratorias crónicas, dando a conocer las distintas escalas para su evaluación y las opciones de tratamiento a través de los programas de rehabilitación respiratoria.
Concepto de fragilidadEl concepto de fragilidad es un término ampliamente usado en geriatría en donde se define como “un síndrome médico, con múltiples causas y contribuyentes que se caracteriza por disminución de la fuerza, resistencia y reducción de la función fisiológica que aumenta la vulnerabilidad de un individuo de desarrollar una mayor dependencia y/o muerte”10.
En el campo de la geriatría, está asociado a la pérdida del funcionamiento físico y cognitivo necesario para mantener un estilo de vida independiente. Por otra parte, identifica pacientes con mayor riesgo de caídas, hospitalización e institucionalización10. La prevalencia de fragilidad aumenta con la edad y está presente en el 10% de los mayores de 65 años y en una cuarta parte de los mayores de 85 años, siendo más común en hombres que en mujeres8.
La fragilidad se manifiesta por las deficiencias en la capacidad física, como debilidad muscular, disminución en la velocidad de la marcha, reducción de la destreza y alteraciones en el equilibrio, llevando a un incremento en el sedentarismo, fatigabilidad y pérdida de peso involuntario. Si bien el deterioro físico es la principal característica, la fragilidad considera otras dimensiones, como el estado cognitivo y el bienestar psicológico9–11.
Fisiopatología de la fragilidadLos mecanismos que producen fragilidad son múltiples y reflejan la complejidad del proceso de envejecimiento.
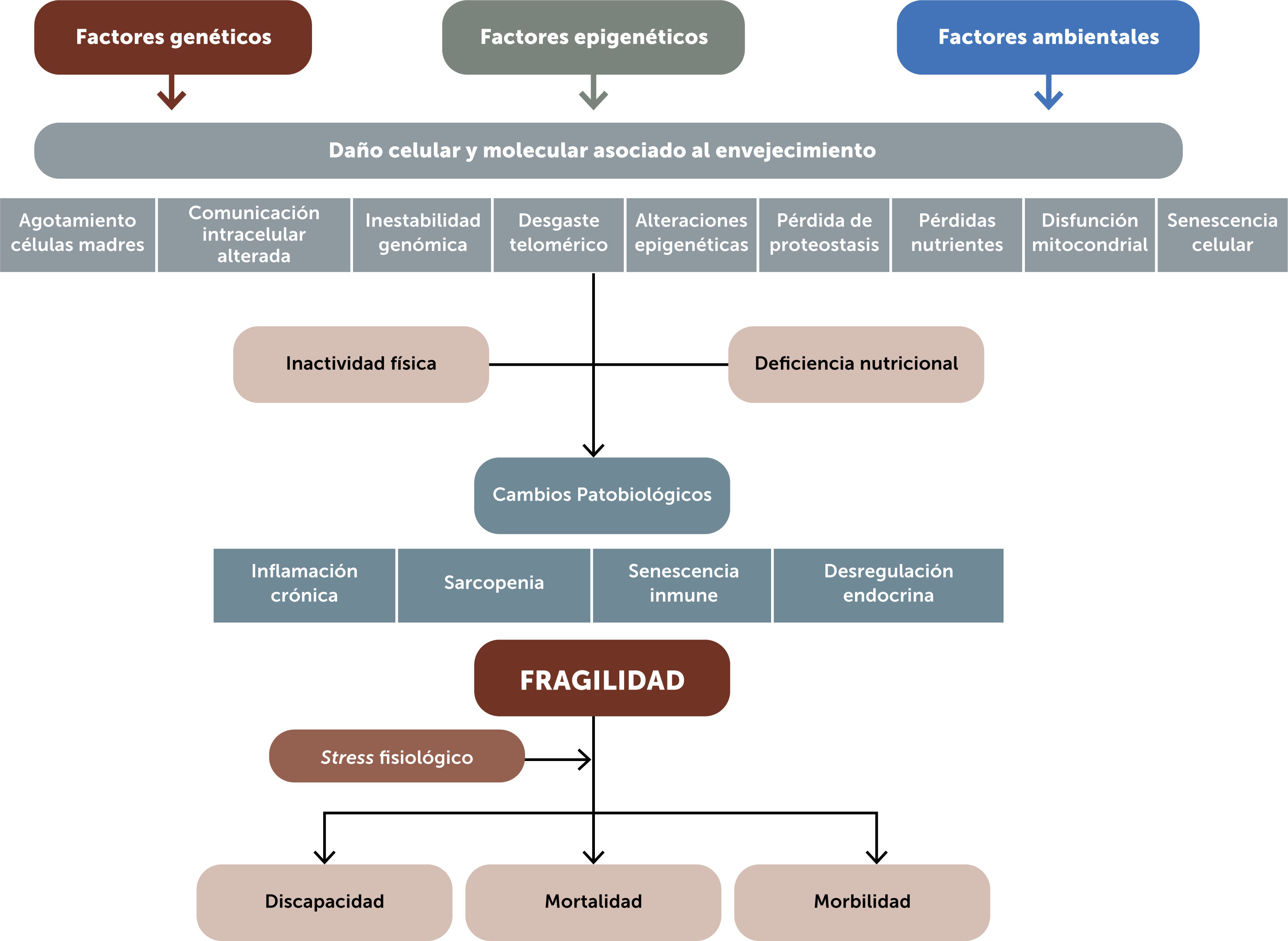
En la figura 1, López-Otis et al. proponen nueve características moleculares y celulares de envejecimiento que, a su vez, se ven afectadas por la genética, epigenética y factores ambientales12. Además de estas nueve características, se incluyen la inactividad física, desnutrición y otras enfermedades relacionadas con la edad como, por ejemplo, demencia y osteoporosis. Ya sea individualmente o en combinación, se cree que estos factores dan como resultado alteraciones patobiológicas como inflamación crónica, senescencia inmune, desregulación endocrina y sarcopenia13.
La sarcopenia, se desarrolla por la deficiencia de proteínas, inflamación crónica, desregulación endocrina y atrofia por desuso, los cuales también están asociados con la fragilidad14,15
Una vez desarrollada la fragilidad, un nuevo factor de estrés pudiese exceder la reserva fisiológica disponible, resultando en discapacidad, morbilidad y muerte1.
Fragilidad en pacientes con enfermedades respiratorias crónicasEl envejecimiento conlleva una disminución de las reservas biológicas y fisiológicas que dependen del tiempo, lo que resulta en una vulnerabilidad cada vez mayor. Con el tiempo, las células, los tejidos y los órganos pierden su resiliencia y capacidad de adaptarse a factores estresantes. Los pacientes con ERC presentan con frecuencia un envejecimiento biológico más acelerado de lo normal y progresivo, en donde sus síntomas (principalmente disnea y tos) y la mala función pulmonar, reducen el rendimiento físico, generan mala calidad de vida y producen mayor riesgo de mortalidad temprana1,9.
En comparación con adultos mayores sin enfermedad pulmonar crónica, el riesgo de desarrollar fragilidad aumenta en aquellos que sí la tienen3. El reciente meta-análisis de Wang et al., reporta que al menos el 19% de pacientes que padecen de EPOC estable presentan fragilidad3. Muchos factores contribuyen al mayor riesgo de generar fragilidad en esta población, incluidas las comorbilidades, tabaquismo, bajos niveles de actividad física, exacerbaciones recurrentes, readmisión hospitalaria, malnutrición y polifarmacia. Por lo tanto, la fragilidad no está limitada a personas de mayor edad, si no que puede presentarse en el contexto de una limitación crónica al flujo aéreo3.
En consecuencia, detectar fragilidad en etapas tempranas, predice de forma independiente muchos resultados adversos relacionados con la salud, incluido el reingreso hospitalario, mayor estancia hospitalaria y mortalidad. Por otra parte, la fragilidad también se asocia con aumento de las exacerbaciones, síntomas y dependencia en las actividades de la vida diaria1,16–18.
La fragilidad es un proceso dinámico y modificable19. Dentro de los tratamientos, se incluyen la actividad física, el ejercicio y soporte nutricional. Los pacientes con ERC deben ser derivados a programas de rehabilitación respiratoria (RR)5.
Evaluación de la fragilidadExisten dos grandes modelos para la evaluación de la fragilidad. El primero de ellos, considera la fragilidad como un síndrome biológico, identificable como un fenotipo de fragilidad física. Este modelo, desarrollado por Fried et al.11 es ampliamente usado y cuantifica la fragilidad por la presencia de 3 o más de las siguientes características: pérdida de peso involuntaria, debilidad, fatiga, enlentecimiento y baja actividad física9. El segundo modelo, expresa la fragilidad como la proporción de déficit de salud (síntomas, signos, condiciones clínicas, deterioros funcionales y alteraciones de laboratorio) que presenta un individuo al final de una evaluación integral9.
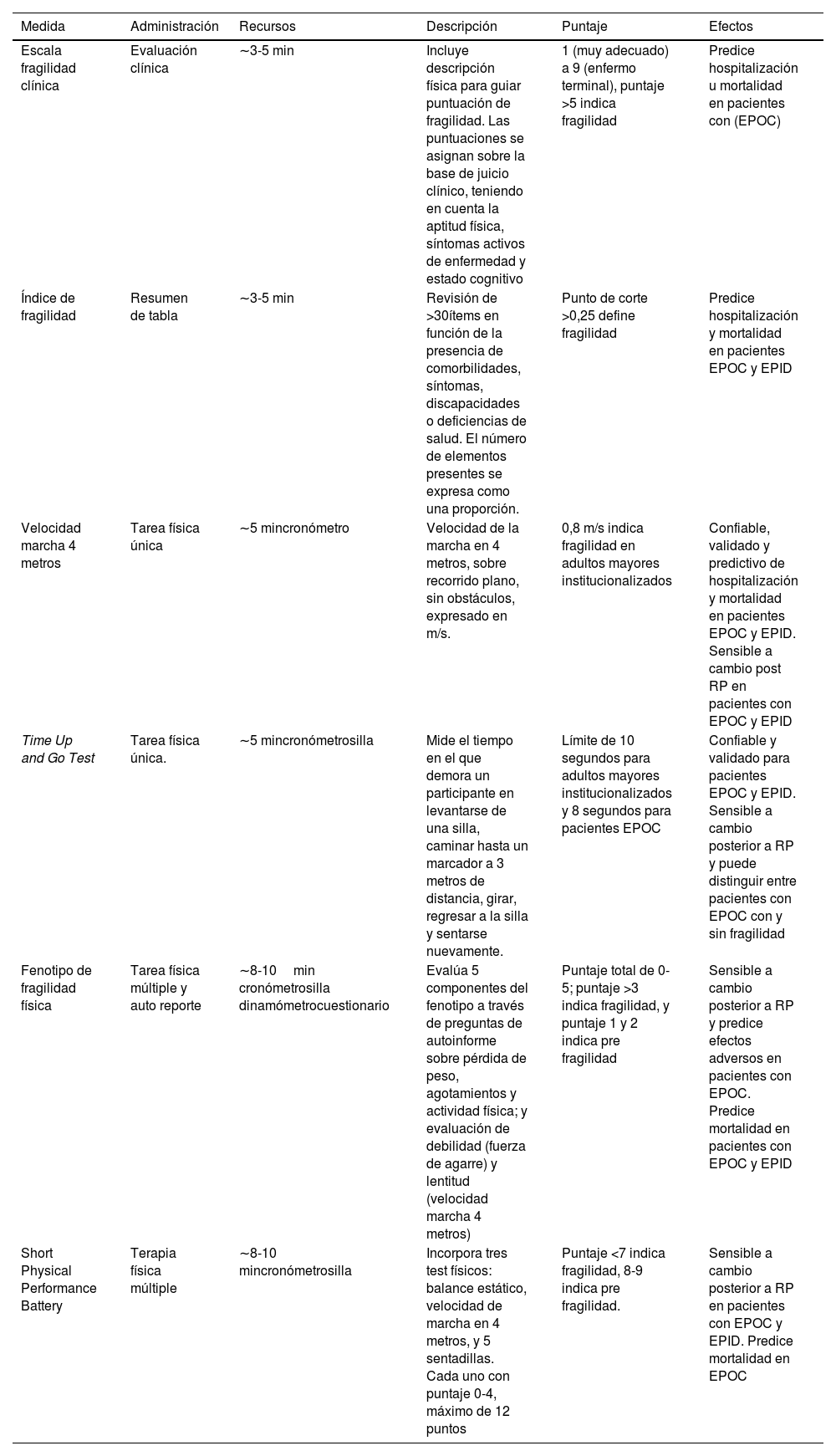
De estos dos modelos, surgen una variedad de instrumentos para cuantificar o medir la fragilidad. En pacientes con ERC, los más estudiados y utilizados son: Fenotipo de Fragilidad Física16,20, Short Physical Performance Battery (SPPB)21, Time Up and Go22, Velocidad de la Marcha en 4 metros23, Escala de Fragilidad Clínica24 y el Índice de Fragilidad25. En la tabla 1, se describen las diferentes escalas de medición de fragilidad y su implicancia en enfermedades respiratorias crónicas.
Ejemplos de escalas validadas para evaluar fragilidad en contexto de enfermedades respiratorias
| Medida | Administración | Recursos | Descripción | Puntaje | Efectos |
|---|---|---|---|---|---|
| Escala fragilidad clínica | Evaluación clínica | ∼3-5 min | Incluye descripción física para guiar puntuación de fragilidad. Las puntuaciones se asignan sobre la base de juicio clínico, teniendo en cuenta la aptitud física, síntomas activos de enfermedad y estado cognitivo | 1 (muy adecuado) a 9 (enfermo terminal), puntaje >5 indica fragilidad | Predice hospitalización u mortalidad en pacientes con (EPOC) |
| Índice de fragilidad | Resumen de tabla | ∼3-5 min | Revisión de >30ítems en función de la presencia de comorbilidades, síntomas, discapacidades o deficiencias de salud. El número de elementos presentes se expresa como una proporción. | Punto de corte >0,25 define fragilidad | Predice hospitalización y mortalidad en pacientes EPOC y EPID |
| Velocidad marcha 4 metros | Tarea física única | ∼5 mincronómetro | Velocidad de la marcha en 4 metros, sobre recorrido plano, sin obstáculos, expresado en m/s. | 0,8 m/s indica fragilidad en adultos mayores institucionalizados | Confiable, validado y predictivo de hospitalización y mortalidad en pacientes EPOC y EPID. Sensible a cambio post RP en pacientes con EPOC y EPID |
| Time Up and Go Test | Tarea física única. | ∼5 mincronómetrosilla | Mide el tiempo en el que demora un participante en levantarse de una silla, caminar hasta un marcador a 3 metros de distancia, girar, regresar a la silla y sentarse nuevamente. | Límite de 10 segundos para adultos mayores institucionalizados y 8 segundos para pacientes EPOC | Confiable y validado para pacientes EPOC y EPID. Sensible a cambio posterior a RP y puede distinguir entre pacientes con EPOC con y sin fragilidad |
| Fenotipo de fragilidad física | Tarea física múltiple y auto reporte | ∼8-10min cronómetrosilla dinamómetrocuestionario | Evalúa 5 componentes del fenotipo a través de preguntas de autoinforme sobre pérdida de peso, agotamientos y actividad física; y evaluación de debilidad (fuerza de agarre) y lentitud (velocidad marcha 4 metros) | Puntaje total de 0-5; puntaje >3 indica fragilidad, y puntaje 1 y 2 indica pre fragilidad | Sensible a cambio posterior a RP y predice efectos adversos en pacientes con EPOC. Predice mortalidad en pacientes con EPOC y EPID |
| Short Physical Performance Battery | Terapia física múltiple | ∼8-10 mincronómetrosilla | Incorpora tres test físicos: balance estático, velocidad de marcha en 4 metros, y 5 sentadillas. Cada uno con puntaje 0-4, máximo de 12 puntos | Puntaje <7 indica fragilidad, 8-9 indica pre fragilidad. | Sensible a cambio posterior a RP en pacientes con EPOC y EPID. Predice mortalidad en EPOC |
Abreviaciones: EPOC: enfermedad pulmonar obstructiva crónica; EPID: enfermedad pulmonar intersticial difusa; RP: rehabilitación pulmonar.
La rehabilitación respiratoria se define como “una intervención integral, basada en la evaluación exhaustiva del paciente, seguida de terapias adaptadas, que incluyen, entre otros, entrenamiento físico, educación y cambio de hábito, diseñados para mejorar el estado físico y sicológico de paciente en ERC”7.
Hoy en día, la RR es un elemento esencial en el tratamiento de pacientes con ERC. Dentro de los componentes centrales se incluye la evaluación personalizada; entrenamiento estructurado y progresivo y medidas de educación y autocuidado; las cuales son impartidos por el equipo multidisciplinario de profesionales de la salud7.
Los principios fundamentales para la prescripción del ejercicio (es decir, prescripción personalizada, intensidad, duración y frecuencia) no son diferentes para esta población. Sin embargo, se deben considerar los síntomas y comorbilidades de cada individuo7. Muchos de los pacientes con enfermedades respiratorias crónicas que presentan fragilidad no toleran el ejercicio de manera continua ya que se encuentran limitados por la disnea y fatiga. Es por esto, que existen diferentes modalidades de entrenamiento que permiten una mejor tolerancia a la intensidad y duración del ejercicio. Dentro de ellas, se puede encontrar el entrenamiento a intervalos26, aporte de oxigenoterapia adicional, uso de ventilación mecánica no invasiva27,28 y estimulación eléctrica neuromuscular29,30 los cuales reducen la carga sobre los síntomas respiratorios y mejoran la tolerancia al ejercicio.
La alteración del equilibrio y la reducción en la velocidad de la marcha, son los principales componentes de fragilidad física, además de ser un fuerte predictor de caídas. Por lo tanto, deben ser consideradas al momento de planificar el entrenamiento. La disminución de la actividad física y la debilidad muscular, condicionan estas alteraciones, sin embargo, factores psicosociales como ansiedad y desorientación también contribuyen a esta condición7,9,12.
La participación en programas de RR reduce la disnea; incrementa la capacidad de ejercicio; mejora la calidad de vida relacionada a la salud y función emocional; brinda apoyo emocional; y, para pacientes que padecen de EPOC reduce la admisión hospitalaria y riesgo de mortalidad posterior a exacerbación7,31–35.
Los pacientes con fragilidad tienen más probabilidades de deteriorase entre el momento de la evaluación y el inicio de un programa de rehabilitación, por lo tanto, debe ser prioridad comenzar con la actividad física7,9,33.
Existen diferentes modelos de rehabilitación pulmonar, que van desde programas hospitalarios, centros ambulatorios e incluso mediante telerehabilitación. La elección dependerá de cada paciente y debe ser de mutuo acuerdo con el equipo de rehabilitación, considerando siempre la evaluación, prescripción individualizada y educación35.
ConclusionesLa fragilidad es un síndrome altamente estudiado y se encuentra relacionado a pacientes con enfermedades respiratorias crónicas. Por otra parte, la rehabilitación pulmonar aborda y reduce la fragilidad, por lo tanto, la presencia de ella no debería limitar el acceso a programas de ejercicio.
La prescripción del ejercicio debe considerar la presencia de síntomas, así también como las comorbilidades. La integración de un equipo multidisciplinario es fundamental para mejorar la participación y los resultados de los pacientes, principalmente en términos de calidad de vida.
Conflicto de interésLa autora no declara conflicto de intereses.