La necesidad de ajustar la inmunosupresión en forma individualizada ha estimulado la emergencia de técnicas que permiten predecir eventos clínicos como rechazo agudo o tolerancia. Esta revisión analiza, considerando principalmente el trasplante renal, las limitantes actuales de la inmunosupresión para concluir que una terapia individualizada permitiría mejorar la sobrevida de pacientes y órganos trasplantados en el largo plazo. En segundo lugar describe los métodos diagnósticos que en forma más consistente han demostrado tener valor predictivo con importancia clínica. Entre ellos se cuentan ensayos funcionales, determinación de anticuerpos específicos y linfocitos reactivos contra el donante, así como el análisis de marcadores a nivel de proteínas o genómicos. Los avances logrados auguran el comienzo de una nueva era en trasplantes.
Organ transplantation is often related to higher survival and lower morbidity than conservative treatments. Nevertheless, survival and morbidity could be optimized tailoring the immunosupression to the particular needs of each individual patient. The requirement to optimize immunosupression makes necessary to improve the immunologic assessment and therefore has promoted the development of new immunological diagnostic tools.
This review addresses first the need to tailor immunosupression, and then focuses in the value of anti HLA antibodies, alloreactive T cells, phenotypic analysis of lymphocytes and cytokines, repertoire analysis and genetic approaches, as well as in vivo studies.
Further validation and standardization of these tests are needed in order to enter the routine clinical practice. Accomplishment of these goals would signal the beginning of a new era in transplantation.
El trasplante renal se ha convertido en una terapia muy exitosa en el sentido que se relaciona tanto con una mayor sobrevida como con una mejor calidad de vida. A pesar de ello el trasplante renal tiene limitaciones, como la falta de órganos y la pérdida de injertos en el largo plazo.
A pesar de la elevada sobrevida de injertos y pacientes en el corto plazo, la sobrevida en el largo plazo no ha mejorado en la misma medida. La pérdida de injertos en el largo plazo contribuye a aumentar la brecha entre oferta y demanda, aumentando la demanda por segundos o terceros trasplantes. Esta revisión tiene por objeto entregar una visión de las principales causas de pérdida de trasplantes renales en el largo plazo y de cómo el mejor monitoreo inmunológico puede contribuir a mejorar los resultados. Es oportuno destacar que los trasplantes de diversos órganos tienen características comunes y características que son específicas para cada órgano. De ello se deduce que los marcadores con valor diagnóstico pueden variar dependiendo del órgano trasplantado. Una revisión más detallada en referencia a marcadores de tolerancia para los diversos órganos se encuentra en el trabajo de Turka LA y Lechler RI (1).
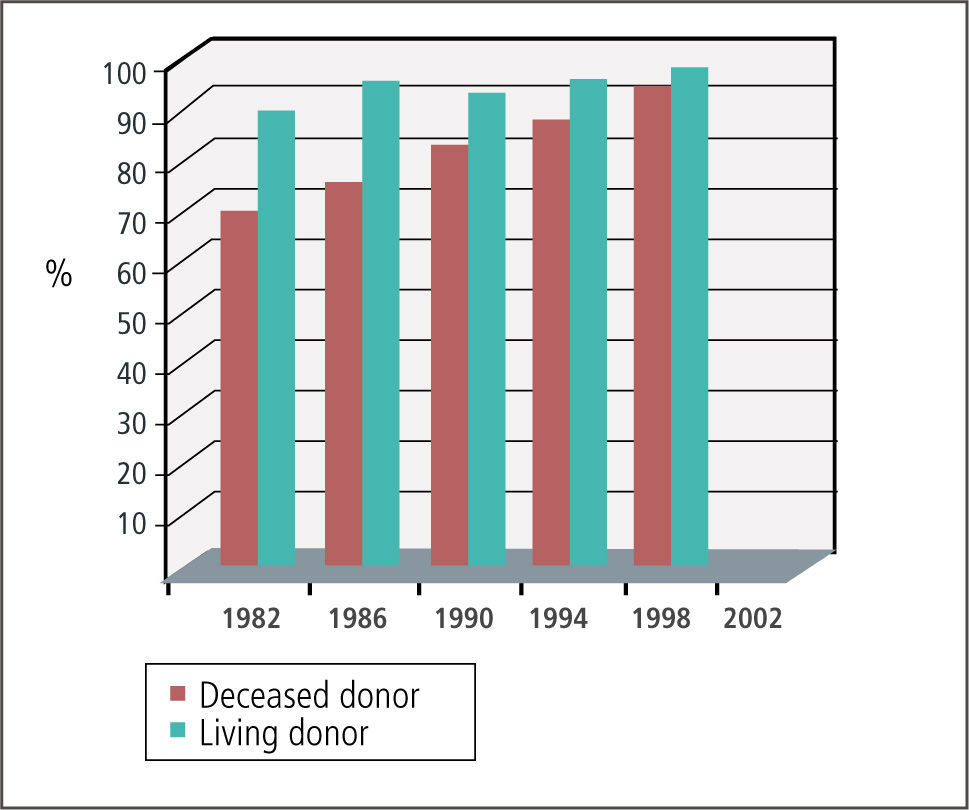
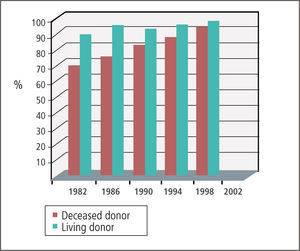
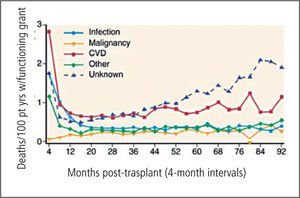
Sobrevida de injertos a corto y largo plazoDiversos factores han contribuido a mejorar sustantivamente el pronóstico del trasplante renal. En la década de 1980 fue la introducción de la ciclosporina, en la década de 1990 la introducción de nuevos antivirales y antifúngicos y desde los finales de esa misma década la introducción de la rapamicina, el alemtuzumab y el rituximab. Ello se ha traducido en una sobrevida de órganos y pacientes superior al 90% en el primer año de trasplante (Figura 1).
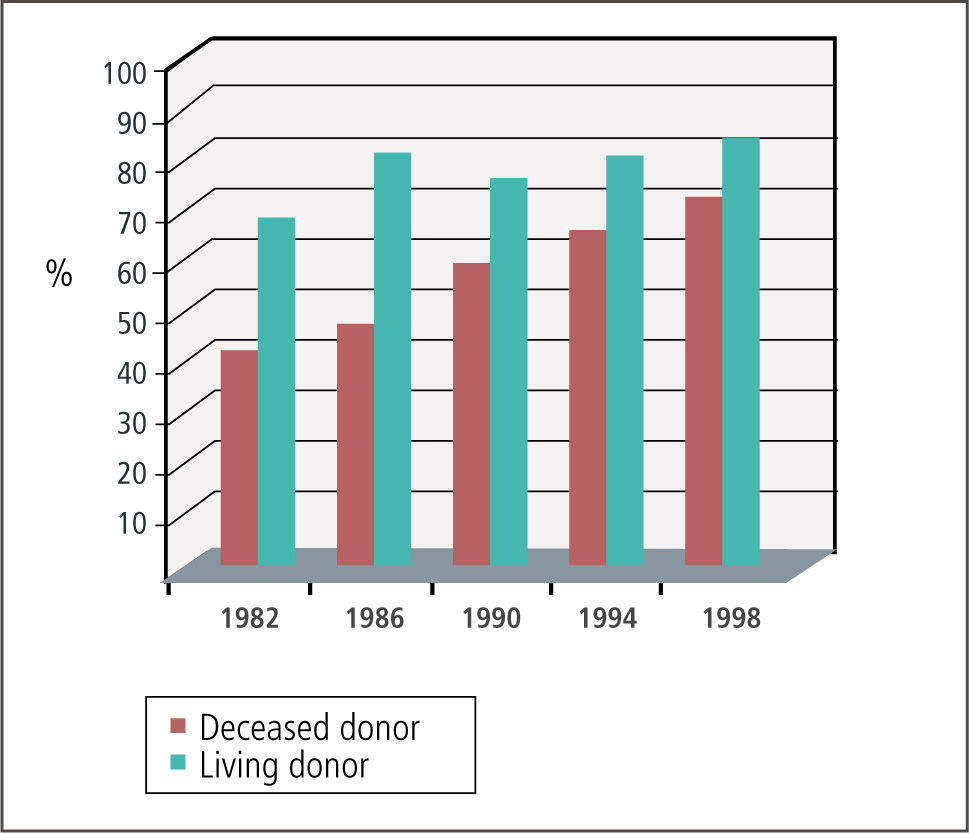
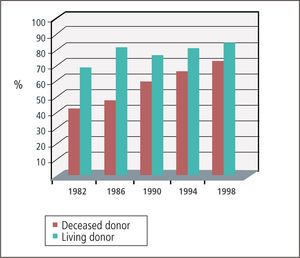
En el mediano y largo plazo el pronóstico registra también una mejoría. Sin embargo, esta mejoría no alcanza la misma proporción que en el corto plazo (Figura 2) y contribuye substancialmente a la lista de espera (2). Este fenómeno tiene dos componentes. Por un lado, la mortalidad de pacientes con injerto funcionando y por otro lado la pérdida de función del riñón trasplantado.
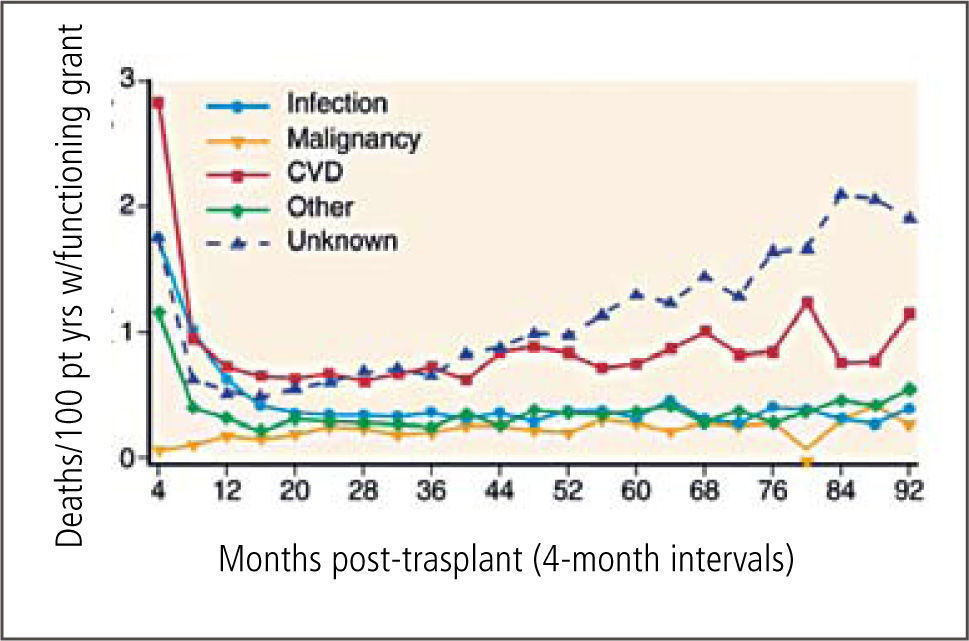
La principal causa de mortalidad es enfermedad cardiovascular, seguido de enfermedades infecciosas y neoplasias (Figura 3) lo que guarda relación con efectos colaterales del tratamiento inmunosupresor.
Los medicamentos anticalcineurínicos (ciclosporina, tacrolimus) han significado un enorme progreso en la reducción de los episodios de rechazo agudo. Sin embargo también se relacionan con una mayor incidencia de enfermedad cardiovascular, neoplasias, infecciones y disfunción del injerto en el largo plazo (3). Los esteroides se utilizan actualmente en dosis muy bajas o se suspenden del todo por su perfil de efectos colaterales. Los inhibidores de la proliferación (azatioprina, micofenolato mofetil o sódico) y los inhibidores mTOR (rapamicina o sirolimus y everolimus) tienen también efectos colaterales significativos que pueden limitar tanto la esperanza de vida como la vida media del trasplante. Por lo tanto, el óptimo sería tener elementos de laboratorio que permitan modular la inmunosupresión en forma individual para evitar tanto fenómenos de rechazo inmunológico como sus efectos colaterales.
Las causas específicas de pérdida del injerto se señalan en la Tabla 1. Entre ellas, la más frecuente es la “nefropatía crónica del injerto”. Esta corresponde al cuadro histológico de atrofia tubular, fibrosis intersticial y obsolescencia glomerular. Sus causas son complejas y no se encuentran plenamente esclarecidas (4). Juegan un rol muy importante la edad del donante y del receptor, la causa del fallecimiento, la isquemia fría, la compatibilidad, la ocurrencia de rechazo agudo, la intensidad de características de la inmunosupresión. También juegan un rol importante otros fenómenos como la posible existencia de hipertensión arterial, dislipidemia y, diabetes mellitus. Cualquiera sean las causas, cuando la nefropatía crónica del injerto es detectada por elementos clínicos, ya es irreversible. De allí emanan los esfuerzos dirigidos a prevenir la nefropatía crónica del injerto y a encontrar elementos clínicos y de laboratorio que permitan predecir su aparición en el futuro.
Diagnóstico Diferencial De La Disfunción Del Riñón Trasplantado
| 1- Nefrotóxicos |
2- Nefropatía crónica del injerto
|
3- Rechazo agudo tardío y recurrente
|
4- Infecciones:
|
| 5- Glomerulonefritis: recurrencia y de novo |
| 6- Obstrucción del flujo urinario |
| 7- Estenosis de arteria renal |
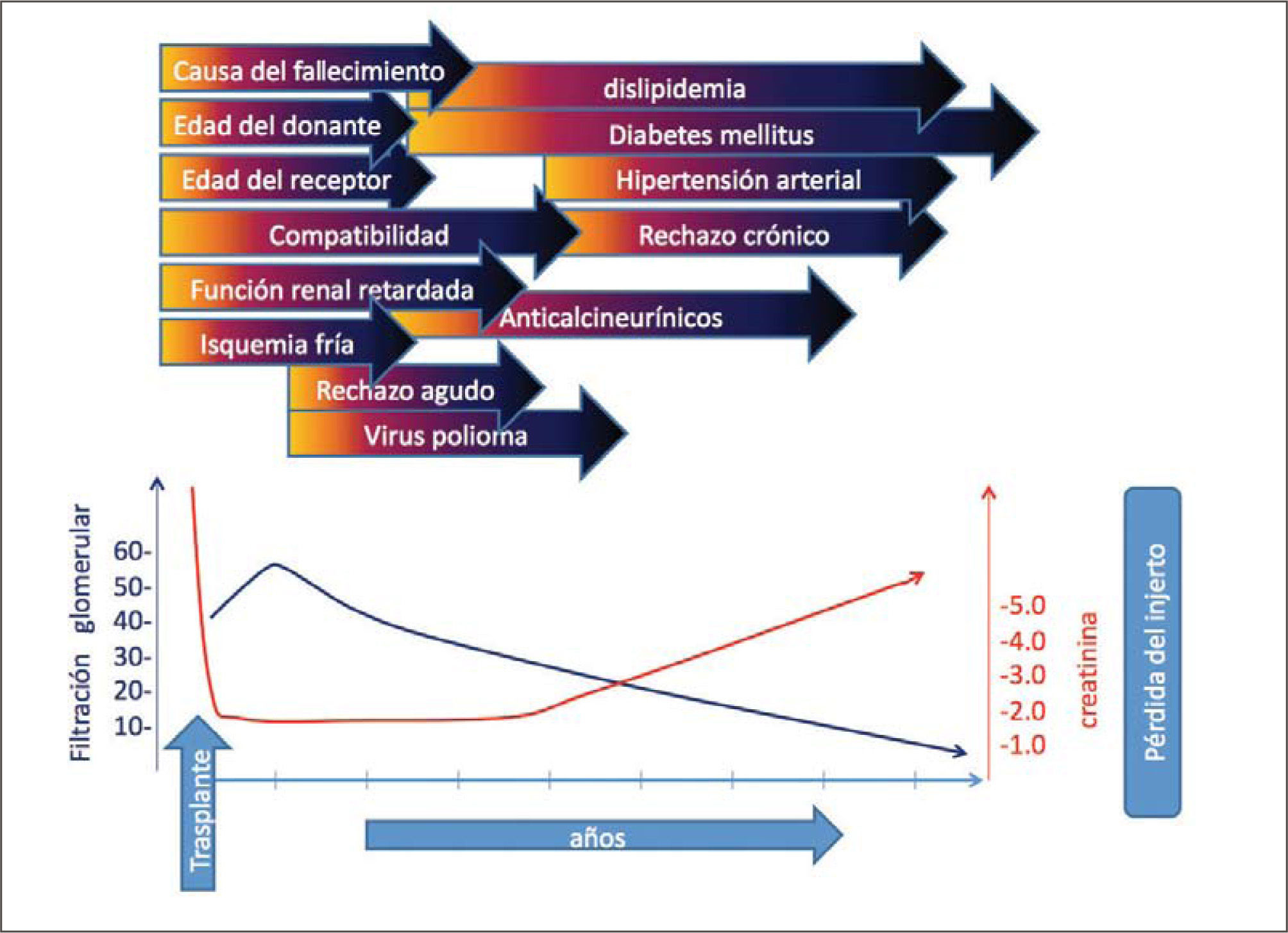
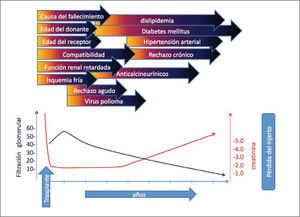
Los instrumentos tradicionales no invasivos como la creatinina o la medición de la filtración glomerular son claramente elementos tardíos, que solamente reflejan el daño ya producido. Los estudios de correlación entre biopsias realizadas regularmente en un protocolo de estudio y la filtración glomerular medida por la creatinina plasmática y métodos cintigráficos ilustran claramente esta afirmación. En el estudio del grupo de Sydney (5) la filtración glomerular alcanza su mejor nivel a los 6 meses con 60ml/min. Luego, esta hiperfiltración inicial inicia un descenso en paralelo con alteraciones histológicas. Estas consisten en fibrosis intersticial, atrofia tubular, hialinosis arteriolar. Si existe rechazo subclínico este sólo puede observarse en biopsias de protocolo. En este estudio la creatinina sólo registra un alza clínicamente evidente cuando la filtración glomerular alcanza valores de 30ml/min. (Figura 4). En ese momento en la histología ya se observan alteraciones avanzadas, que incluyen la obsolescencia glomerular. Desde ese momento en adelante, la progresión hacia la insuficiencia renal es una realidad inevitable.
En la parte superior se señalan los principales factores incidentes en la disfunción crónica del trasplante renal graficados en función de su tiempo de aparición. En la parte inferior se observa que el alza de creatinina es un marcador tardío en relación a la disminución de la filtración glomerular Información extraída de los trabajos de Chapman JR, Nankivell BJ et al.
La ecotomografía doppler del riñón trasplantado puede prestar cierta ayuda en el monitoreo. Por un lado es útil para diagnosticar colecciones y obstrucción del flujo urinario. Por otro lado se ha visto que índices de resistencia mayores a 0.8 se correlacionan con un pronóstico más limitado (6). Ello permite identificar pacientes con riesgo muy elevado de pérdida del injerto. Sin embargo, el examen carece de la sensibilidad necesaria para detectar una nefropatía inicial, leve o moderada.
La biopsia renal constituye actualmente el método de referencia para monitorizar la evolución del trasplante. La utilización de agujas automáticas más finas y el apoyo in situ de la ecotomografía han permitido bajar la frecuencia de complicaciones mayores (transfusiones de sangre o intervenciones) en pacientes trasplantados a menos del 1% (7, 8). Por esa razón la biopsia renal se ha convertido en un método prácticamente de rutina en el seguimiento de los pacientes trasplantados. Se trata sin embargo de un método invasivo que tiene morbilidad y costos relacionados. Por último, a pesar de ser el mejor método disponible todavía está lejos de ser perfecto. Entre sus limitantes se cuenta el requerimiento de alta especialización para la interpretación correcta de los resultados. Por otro lado aún cuando la información morfológica es bastante detallada, la información referida a la funcionalidad es limitada.
De lo señalado se desprende la necesidad de disponer de métodos de seguimiento de naturaleza no invasiva que permitan evaluar funcionalmente los diversos aspectos de la respuesta biológica del riñón trasplantado, incluyendo la capacidad de predecir ciertas patologías, antes que ocurran cambios histológicos irreversibles. Estos métodos deben ser capaces de indagar en la condición del sistema inmune previo al trasplante, así como en la interacción del donante y el receptor en forma de ensayos funcionales (9).
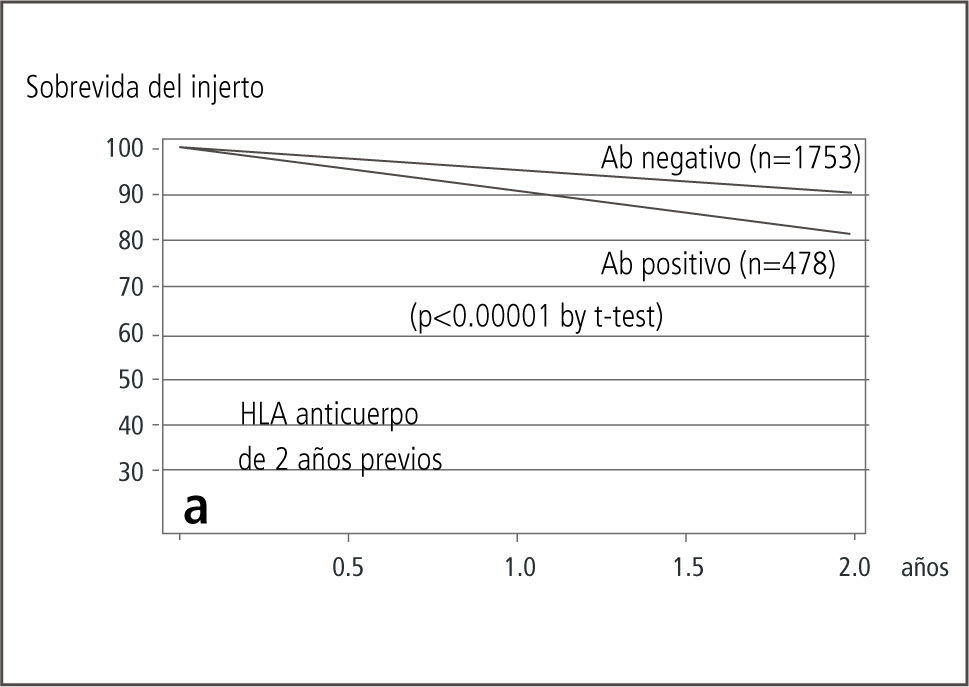
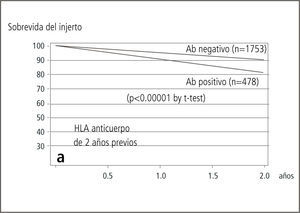
Determinación de anticuerpos anti HLAPeter Morris describió la formación de anticuerpos en pacientes trasplantados en el año 1969 (10). Paul Terasaki fue el primero (11) en estudiar el problema en forma dirigida al realizar mediciones seriadas de anticuerpos durante ocho años en la evolución de 139 pacientes trasplantados renales. 29 de esos pacientes evolucionaron hacia un “rechazo crónico” en ese período. En todos estos pacientes se demostró la formación de anticuerpos anti HLA ya sea preexistentes o de novo. Cuando se analizan los datos en forma retrospectiva en todos los pacientes que perdieron el injerto (n=14) se detectó la aparición de anticuerpos previo a la pérdida. Un estudio prospectivo, multicéntrico en 2.231 pacientes (12) ha venido luego a confirmar el valor predictivo de la detección de anticuerpos en la evolución post trasplante (Figura 5).
Los pacientes que desarrollan anticuerpos anti HLA tienen una menor sobrevida. Las diferencias se acentúan en función del tiempo transcurrido desde el trasplante. Terasaki PI, Ozawa M.
Valor predictivo de Ac HLa y creatinina sérica en rechazo crónico: resultados de estudio prospectivo de 2 años.
En pacientes hipersensibilizados (es decir aquellos que presentan anticuerpos anti donante antes del trasplante) se ha estudiado la relación entre la presencia de anticuerpos anti HLA y la incidencia de rechazo agudo (13). El estudio realizado en 70 pacientes permite extraer las siguientes conclusiones. Por una parte, la presencia niveles elevados de anticuerpos donante-específicos se correlaciona con una mayor incidencia de rechazo humoral agudo. Por otra parte los niveles permanecen bajos en los pacientes que no hacen rechazo humoral agudo, mientras que cuando suben (alrededor del día 10 post trasplante) se observa una elevada incidencia de rechazo humoral (92%).
Sin embargo la evaluación de anticuerpos anti HLA tiene limitaciones. Se ha visto que en algunos pacientes los anticuerpos anti HLA pueden persistir por años sin deterioro aparente de la función renal y que pueden estar presentes en pacientes que cursan con tolerancia operacional (14). Una segunda limitante es la gran variabilidad de las técnicas y falta de estandarización entre los diferentes laboratorios. Las técnicas principales de determinación de anticuerpos anti donante son el crossmatch por linfocitotoxicidad y el cross-match por citometría de flujo. Las principales técnicas de determinación de anticuerpos anti HLA específicos son el ELISA, la citometría de flujo y el sistema xMAP-Luminex. Recientemente la técnica xMAP-Luminex ha sido adaptada también para la realización de crossmatch.
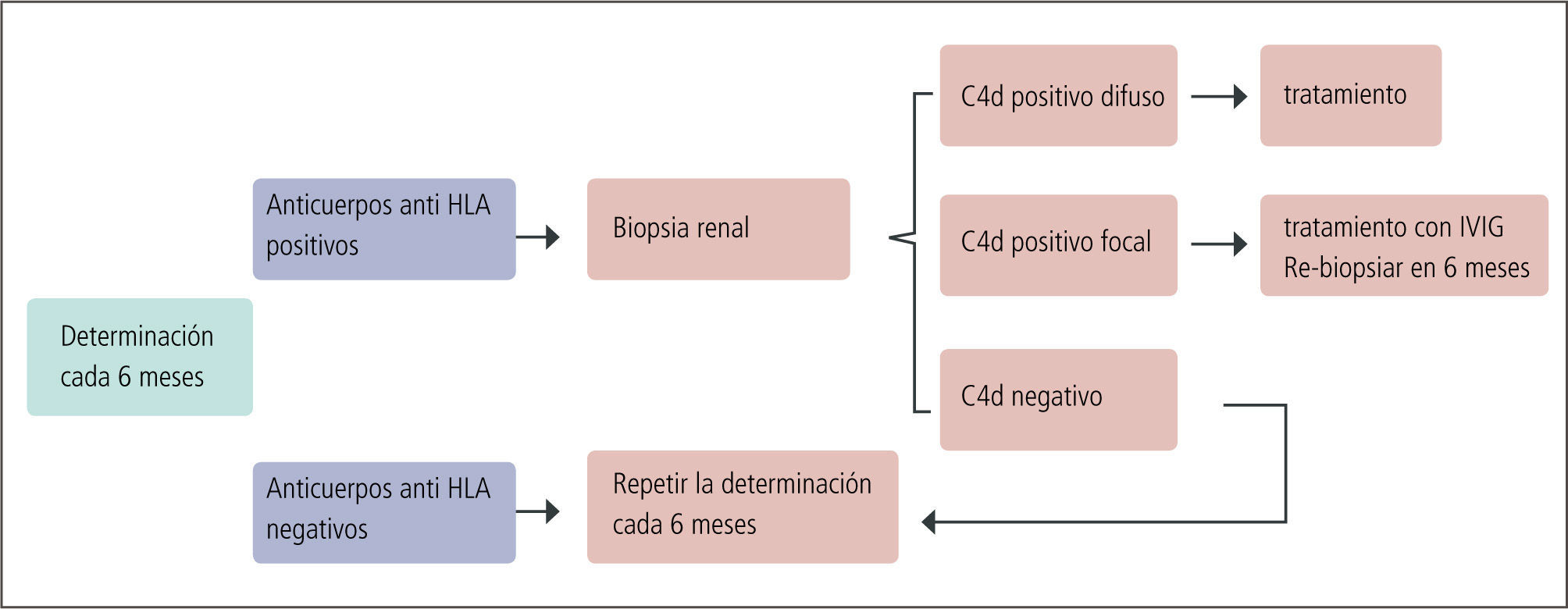
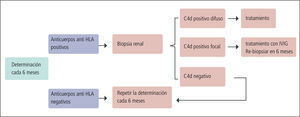
En la práctica, la determinación de anticuerpos anti HLA es un instrumento que permite identificar -tanto antes del trasplante como durante su evolución- aquellos pacientes de mayor riesgo inmunológico, lo que tiene consecuencias terapéuticas. Entre estas no disminuir la inmuno-supresión, motivar un estudio histopatológico y eventualmente realizar un tratamiento destinado a disminuir la formación de anticuerpos. Por esa razón se propone realizar esta determinación en forma rutinaria en períodos regulares (Figura 6).
Algoritmo Para La Determinación De Anticuerpos Anti Hla y Sus Conductas Derivadas En Pacientes Con Función Renal Estable
Durante el primer año de evolución o si la función renal es fluctuante la determinación debería ser hecha en forma mas frecuente. Clínica Las Condes 2009 (Mayo). IVIG: Inmunoglobinas intravenosas en dósis de 2 grs por kilo de peso, dosis máxima 140 grs.
El sistema inmune adaptable reconoce antígenos presentados en el marco del MHC propio. En ese contexto la detección de antígenos presentados por MHC extraño constituye una excepción a la regla y una paradoja en el funcionamiento del sistema inmune. Se estima que la frecuencia de linfocitos T periféricos que reconocen antígenos del donante varía entre el 1 y el 10% dependiendo de los métodos utilizados. Utilizando diversas técnicas se ha comprobado que la cantidad de estos linfocitos “aloreactivos” se correlaciona con la presencia de rechazo en la evolución post trasplante (15) y que las terapias de inducción con anticuerpos benefician especialmente a los pacientes con una frecuencia elevada de LT aloreactivos. Las técnicas más comúnmente empleadas con esta finalidad son las siguientes:
El cultivo mixto linfocitario, en su forma más tradicional pone en contacto células del donante irradiadas con células del receptor midien do la proliferación celular por medio de la incorporación de timidina marcada radioactivamente. Este ensayo creó inicialmente grandes expectativas, sin embargo tiene limitaciones, como el hecho que permite observar sólo la presentación directa y no la presentación indirecta, que en el concepto actual constituye el principal mecanismo de pérdida de injertos en el largo plazo.
El análisis de dilución limitante estima la frecuencia de precursores aloreactivos por medio de diluciones seriadas de células respondedoras en contacto con células del donante. El ensayo se mide en términos de producción de citoquinas, de proliferación o citotoxicidad. Utilizando esta metodología se ha observado que un aumento en el número de precursores de LT citotóxicos anticipa un episodio de rechazo agudo durante el primer año de evolución (16). Sus principales limitantes son su laboriosidad y dificultades en la reproducibilidad de los resultados.
La técnica de ELISPOT (Enzyme-Linked Immunosorbent Spot) en su forma más clásica, consiste en poner en contacto células presentadoras del donante (generalmente irradiadas) con respondedoras del receptor en una placa que permite la captura y detección de citoquinas en el lugar en que es secretada. Ello permite la detección a nivel de células individuales, lo que le da una extraordinaria sensibilidad. Esta técnica se utilizó primero para evaluar la presentación directa (17) y luego la presentación indirecta (18). Estudios prospectivos demostraron que la detección de LT productores de interferon gama antes del trasplante constituye un factor de riesgo de rechazo en los primeros meses de evolución (19) que se correlaciona a su vez con la función renal en el corto (20) y largo plazo (21). Por las razones señaladas se ha propuesto su utilización como un análogo del crossmatch para evaluar la reactividad celular antes del trasplante (22). Especialmente interesante podría ser la monitorización de la reactividad de subpoblaciones linfocitarias. Se ha evaluado la respuesta de PBMC comparando antes y después de depletar LT reguladores (CD4+, CD25high), observando en algunos pacientes que la presencia de esta subpoblación disminuye la producción de interferón gama por LT efectores expuestos a presentación indirecta. Esta reacción fue observada en 40 % de los pacientes que no habían experimentado nunca un episodio de rechazo (23).
Experimentos en modelo animal sugieren que la activación seguida de agotamiento y deleción de linfocitos T CD8+ aloreactivos constituye un predictor de aceptabilidad y tolerancia (24). Especialmente, LT reactivos en presentación indirecta podrían tener gran importancia en la evolución del trasplante (25).
El Análisis del repertorio de los receptores de linfocitos T (TCR)Se basa en la demostración que pacientes que han perdido el injerto renal por rechazo crónico tienen linfocitos infiltrantes cuyo TCR tiene un repertorio fuertemente alterado (26), sugiriendo que un número limitado de determinantes antigénicas son críticas para estimular el sistema inmune del receptor y provocar una disfunción crónica y pérdida del injerto.
Un fenómeno similar de alteración en el repertorio de TCR, junto a una falta de producción de ciertas citoquinas se observa en pacientes tolerantes al injerto (27).
No existen aún pruebas consistentes que el estudio del repertorio de TCR en forma aislada (por tipificación espectral) constituya un buen instrumento para predecir eventos clínicos. Sin embargo, la utilización de esta técnica puede ser útil en el marco de estudios genómicos complejos. Utilizando estos instrumentos la empresa TcLand, localizada en Nantes ha desarrollado un “Kidney Score” de aceptación o rechazo y ofrece este servicio a pacientes trasplantados (http://www.tcland-biotech.com/).
CD30 soluble (tumor necrosis factor receptor superfamily, member 8)CD30 es una molécula de superficie perteneciente a la familia de receptores del Factor de Necrosis Tumoral TNF que se sobre expresa y libera a la circulación luego de la activación de LT. Tanto LT activados de memoria como efectores contribuyen a su concentración circulante (28). Se ha observado una buena correlación entre los niveles de CD30 soluble pre trasplante con la posibilidad de rechazo o pérdida de injerto (29, 30), sin embargo existen también reportes en contrario (31, 32). Existe información en el sentido que su elevación podría ser predictiva de bronquiolitis obliterante en trasplante pulmonar (33). Por tratarse de un marcador inespecífico cuya elevación es característica de infecciones (34) y otros fenómenos como el embarazo (35), es posible que otras variables oscurezcan su valor.
Cuantificación de citoquinas circulantesLa concentración plasmática de ciertas citoquinas así como la detección de sus mensajeros (36) han sido evaluadas con resultados contradictorios respecto de su posible valor predictivo de disfunción del injerto en trasplante renal o hepático. Se han publicado estudios que asignan un valor predictivo positivo para rechazo a los valores elevados de IL-6 (37) o al balance de TGF beta y PDGF-BB (38). Otros estudios entregan resultados distintos (39). Seguramente su corta vida media, su influencia potencial por múltiples factores no relacionados al trasplante, su distancia al sitio del injerto y sus funciones reverberantes hacen que sus valores sean demasiado fluctuantes y complejos para revelar las interacciones estables entre el huésped y el órgano trasplantado. Una estrategia alternativa es el seguimiento de ciertas citoquinas en los productos del órgano trasplantado. Así por ejemplo, la expresión del mRNA de IL23 e IL17 se encuentra elevada en células de secreción bronquial en pacientes trasplantados de pulmón que cursan con bronquiolitis obliterante (40).
El Análisis De Subpoblaciones Linfocitarias constituye un nuevo recurso para monitorizar el sistema inmune del paciente trasplantado. Gracias al conocimiento de marcadores característicos de los diversos grupos celulares su análisis puede realizarse en sangre por medio de citometría de flujo y en tejido por inmunohistoquímica. La subpoblación de linfocitos T reguladores que expresan el factor de transcripción Foxp3 es fácilmente identifiable y su análisis ha permitido la introducción de nuevos conceptos en la inmunología del trasplante. En especial, su presencia se encuentra relacionada tanto a tolerancia (41) como a rechazo (42) hacia el órgano trasplantado. En ese sentido existe experiencia publicada que evalúa la presencia de linfocitos T reguladores en relación a LT totales (43), así como LT efectores y de memoria (44).
La detección de diversos tipos de células dendríticas puede constituir también un elemento valioso de monitoreo inmunológico. Se ha observado que aquellos pacientes tolerantes que no tienen inmunosupresión o tienen inmunosupresión mínima tienen una mayor proporción de células dendríticas plasmocitoides (45). Más tarde, el mismo grupo ha demostrado que la razón de PD-L1 (programmed death ligand-1)/CD86 se relaciona con LT reguladores Foxp3+ (46). Un fenómeno que apunta en la misma dirección se observa en pacientes trasplantados de pulmón. En estos pacientes se ha observado que la presencia de bronquiolitis obliterante se asocia a la presencia de células dendríticas más maduras, a una menor cantidad de LT reguladores y a una mayor expresión de CTLA-4 en los LT. Para interpretar adecuadamente la información referida a LT reguladores, debe considerarse que estas células también pueden aumentar en el órgano trasplantado durante los fenómenos de rechazo (47).
La determinación de LT de memoria central y efectores también tiene el potencial para correlacionarse con eventos clínicos como se ha observado en casos aislados tratados con alemtuzumab (48). En otra serie clínica más extensa se ha observado que la incidencia de rechazo agudo al retirar los anticalcineurínicos se correlaciona con una mayor proporción de LT de memoria versus LT reguladores antes de la suspensión (49).
El Análisis De Expresión Génica incluye diversas técnicas para identificar secuencias específicas del DNA o RNA que a su vez se correlacionan con ciertas funciones del sistema inmune. Para ello utiliza las técnicas de microarray, PCR (Reacción de Polimerasa en Cadena) en tiempo real y recientemente se ha agregado el complejo sistema DASL (DNA-mediated Annealing, Selection, extension and Ligation) (50). El microarray permite el análisis simultáneo de hasta miles de genes en forma no sesgada, mientras que el análisis y cuantificación dirigida de algunos de ellos es dominio del PCR. El sistema DASL permite el análisis de expresión de ciertos genes en tejido fijado en formalina. Para ello “reconstruye”el mRNA alterado y parcialmente degradado (http://www.illumina.com/downloads/WGDASLAssay_Datasheet.pdf).
La principal ventaja del microarray es el análisis simultáneo de gran cantidad de genes, incluso aquellos aparentemente no relacionados con los procesos inmunológicos. Ello equivale a identificar el RNA mensajero de proteínas que no han sido buscadas en forma dirigida. Luego es posible identificarlas y cuantificarlas con la ayuda de PCR, lo que se puede realizar tanto en sangre como en tejido. Ambas técnicas tienen una correlación adecuada (51).
El trasplante hepático ha permitido identificar pacientes en los que la inmunosupresión ha sido suspendida sin efectos negativos para el órgano trasplantado. En esos pacientes se han identificado en sangre periférica los RNA mensajeros de proteínas cuya expresión se manifiesta en forma de patrones característicos (52).
En trasplante renal esa búsqueda se ha iniciado exitosamente tanto en modelos murinos (53) como humanos (54). Recientemente se ha identificado en forma consistente en sangre periférica un set de 343 genes que permite clasificar correctamente a > 80 % de los pacientes (55, 56).
Al restringir el análisis a ciertos grupos celulares se pueden observar fenómenos específicos como la sobreexpresión de transcriptos de linfocitos B, células plasmáticas e inmunoglobulinas a lo largo del tiempo (57) o los transcriptomas de LT efectores de memoria y citotóxicos (58).
La misma metodología ha permitido evaluar la expresión génica en relación a rechazo en orina o secreción bronquial, lo que constituye un examen no invasivo y por lo tanto exento de riesgos (59). Ello es especialmente valioso cuando se requiere un monitoreo continuo, como es el diagnóstico de rechazo agudo durante un episodio de necrosis tubular (60).
QuimerismoEl estudio de la presencia de células del donante en el receptor constituye un tema central en el trasplante de médula ósea. En trasplante de órganos sólidos se ha detectado la presencia de quimerismo en un número substancial de los pacientes (61, 62). El valor clínico de la presencia de quimerismo ha sido extensamente discutido en la literatura. Existen reportes que plantean que la presencia de quimerismo se correlaciona y sobre todo favorece la inducción de tolerancia (63), sin embargo ello no es sinónimo de un buen predictor del curso clínico del trasplante. Mientras algunos reportes informan su detección como un buen indicador de aceptación del órgano trasplantado (64) otros observan resultados variables (65), faltos de valor predictivo (66) o dependientes del órgano trasplantado (67). Actualmente no se considera la detección de microquimerismo un instrumento útil en el seguimiento de pacientes trasplantados bajo inmunosupresión estándar y su valor podría estar más bien relacionado a los mecanismos posibles de inducción de tolerancia.
La reacción de HIPERSENSIBILIDAD RETARDADA TRANSVIVO representa otro posible predictor de rechazo o aceptación del injerto. Este tipo de análisis se realiza rutinariamente para evaluar la respuesta inmune frente a antígenos como la tuberculosis. En el caso de pacientes trasplantados se utilizan células de sangre periférica del receptor junto a antígenos del donante obtenidos por sonicación celular y la reacción se observa utilizando ratones portadores de inmunodeficiencia combinada severa (SCID) (68). El estudio por lo tanto constituye un ensayo funcional en el que participan todos los tipos celulares de la sangre periférica del receptor, las proteínas sonicadas del donante y un medio (oreja o pie del animal) con capacidad para secretar citoquinas, reclutar células accesorias y aumentar la permeabilidad vascular. Ello le confiere características que lo distinguen de las reacciones de cultivo mixto linfocitario y le agrega similitud a la situación del trasplante. En contraposición su evaluación es subjetiva y sujeta a factores incontrolables como la variación interindividual de los ratones. Los estudios publicados permiten identificar pacientes hiporespondedores en los cuales se ha retirado la inmunosupresión (69, 70). Sin embargo, en estudios clínicos más amplios no se ha podido demostrar el valor predictivo de este examen (71). Su importancia principal es que ha permitido observar detalladamente fenómenos relacionados a la patogenia de la aceptación y rechazo (72).
La REACTIVIDAD DE LT LUEGO DE ACTIVACIÓN POLICLONAL medida por la producción de ATP es un ensayo funcional que entrega una medida de la inmunoreactividad inespecífica y por esa vía un estimado del nivel global de inmunosupresión. La activación de LT puede realizarse con PHA y su activación puede ser medida por la expresión de marcadores de superficie como CD69 (73) o la concentración de ATP. La última técnica, con el nombre de ImmuKnow ha alcanzado cierto desarrollo luego de su aprobación por la FDA (http://www.cylex.net/products.html).
En principio, sangre entera es incubada con PHA por 15–18hrs. Se separan LT CD4+ por método inmunomagnético, se lisan las células y se mide el ATP liberado utilizando luciferasa como trazador. La lectura se realiza en un luminómetro comercial. Un estudio multicéntrico ha permitido establecer valores normales así como valores predictivos de infección o de rechazo (74). Existe información reciente en el sentido que sus resultados se correlacionan con la aparición de rechazo agudo precoz (75).
ConclusionesLos métodos tradicionales de vigilancia de la función del trasplante renal no permiten la detección temprana de una respuesta inmune de rechazo, especialmente crónico. Los niveles de creatinina se elevan tardíamente, en general cuando existen alteraciones histológicas irreversibles. Ello hace necesario la incorporación de nuevas tecnologías que permitan monitorizar tanto la respuesta inmune como los efectos biológicos de la terapia inmunosupresora.
Los últimos dos años han registrado avances importantes para monitorizar en mejor forma la respuesta inmune en pacientes trasplantados. Especialmente la detección de anticuerpos anti HLA se está introduciendo rápidamente en la práctica clínica. Otros métodos todavía experimentales permiten tener información más detallada tanto de la respuesta inmune celular como humoral. Para ello hacen uso tanto de modelos funcionales como de detección de proteínas o expresión génica de ciertos marcadores. La tarea del momento se centra en la necesidad de validar los mejores marcadores. La utilización de estas nuevas herramientas pavimenta el camino para una medicación ajustada a las necesidades individuales de cada paciente. De esa forma las nuevas formas de monitoreo representan el inicio de una nueva era en trasplantes.
El autor declara no tener conflictos de interés, en relación a este artículo.