La muerte fetal es un evento poco frecuente pero de gran repercusión afectiva para los padres involucrados y su entorno. En el presente artículo revisaremos la epidemiología, las causas, orientaremos a los médicos en los pasos a seguir para realizar adecuadamente el estudio, la resolución del embarazo y el manejo del embarazo siguiente junto con las estrategias para prevenirlo.
Stillbirth is not frequent but is a strong emotional event for parents and their families. In this article, we will review epidemiology, etiology, we will guide physicians to follow the right steps to make the appropriate study, delivery and the best management for the next pregnancy.
Uno de los eventos más dramáticos que debe enfrentar el médico que atiende a una embarazada, es encontrarse con la muerte del feto en gestación. Algunas veces es parte de un proceso diagnosticado con antelación, lo que permite de alguna forma, preparar a los padres para ese momento. En la mayoría de las ocasiones sin embargo, se trata de un hallazgo y por lo tanto, de un evento no previsto. Esto generará un golpe de tal magnitud que muchas veces dificultará la toma de decisiones para esa pareja y su entorno. Por eso, el médico debe estar preparado para afrontar este momento y dar luces a esos padres de los pasos a seguir, programar la evacuación uterina, estudiar la etiología del caso y dar directrices para una siguiente gestación.
EpidemiologíaEn Chile se ha definido históricamente como óbito fetal (del latín obitus, fallecimiento de una persona) la ocurrencia de muerte fetal in utero durante la gestación desde las 22 semanas de edad gestacional o desde que el feto tenga un peso de 500 gramos hasta el momento del parto.
Desde 2005, el Ministerio de Salud de Chile, incluye dentro de las estadísticas de muerte fetal todo producto de la concepción nacido fallecido, es decir, no considera límite inferior de peso ni edad gestacional, ni consideración de viabilidad extrauterina (1).
La frecuencia de este problema es variable, estando claramente asociado al nivel de desarrollo del país. La tasa de mortinatalidad mundial según cifras obtenidas en 2004, fue de 23.9 por 1.000 nacidos vivos, variando, desde un punto de vista socio-económico, desde 5.3 en los países desarrollados a 25.5 por mil nacidos vivos en aquellos subdesarrollados. Desde un punto de vista geográfico, desde 32 por 1.000 en África Subsahariana y el sur asiático; a 13 por 1.000 nacidos vivos en América Latina (2).
En los países desarrollados la tasa de mortinatalidad disminuyó fuertemente a contar de mediados del siglo pasado, en gran parte debido a la mejoría en condiciones sanitarias, el acceso a control de embarazo y la atención profesional del parto; además de avances tecnológicos y logísticos vinculados a la monitorización fetal anteparto e intraparto y a la capacidad e implementación de protocolos para actuar de emergencia frente a situaciones de urgencia.
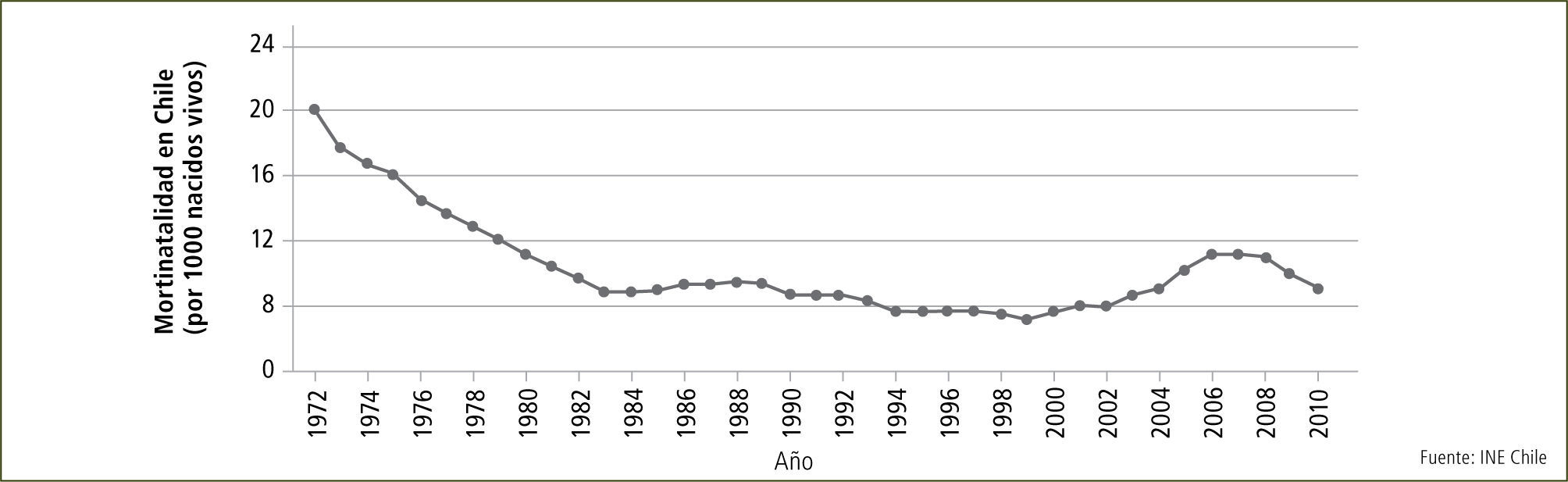
En los últimos 40 años en Chile, las cifras de mortinatalidad han mostrado un considerable descenso, especialmente a partir de la década de los 70, pasando de 19 por 1.000 RN vivos a inicio de los 70 a 7.7 por 1.000 RN vivos 10 años después. Desde entonces, la declinación ha sido de menor cuantía, desde 5.9 por 1.000 y 4.9 por 1.000 RN vivos a inicio de los 90 y a inicios de este siglo, respectivamente. Sin embargo, la última década ha mostrado una tendencia al alza en las cifras, subiendo progresivamente a 5.7 por 1.000 en 2003; 7.6 por 1.000 en 2005; y 8.6 por 1.000 en 2010 (figura 1).
Mortinatalidad en Chile 1972–2010
Evolución de la tasa de muerte fetal en Chile en los últimos 40 años. En la década de los 70 se evidencia una notoria caída desde 20 por mil hasta alrededor de 10 por mil en los ochenta. La declinación es menos evidente pero persiste la tendencia a la baja en los 90 llegando a su mínimo a comienzos de siglo. Los años siguientes se observa un alza leve, pero desde 2006 se nota un aumento más notorio explicado por la extensión de certificado de defunción a cualquier aborto independiente del peso o edad gestacional del feto o embrión.
Cabe considerar que los últimos años, aproximadamente el 40% de los casos corresponde a fetos menores de 500 gramos. Por lo tanto, el aumento en las tasas de mortinatalidad más que una causa epidemiológica corresponde más bien al cambio en el nivel de corte inferior.
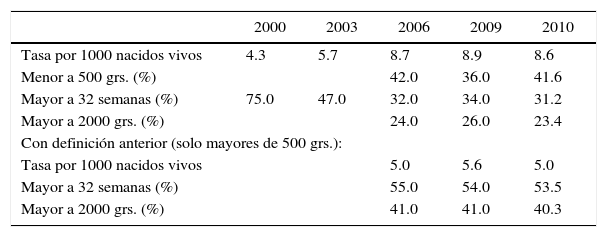
Para comprender la importancia de este problema en nuestro país, hay que considerar que, de la tasa de 8,6 por 1.000 nacidos vivos el año 2010, el 31% correspondió a fetos mayores de 32 semanas y el 23% a fetos mayores de 2.000 gramos, es decir, fetos viables, que de nacer tenían amplias probabilidades de sobrevivir fuera del útero. Además, si se considera la definición más usada, es decir, sólo los fetos mayores a 500 gramos, la situación es aún más notoria, ya que el 54% de los fetos que murieron in utero tenían más de 32 semanas y el 40% más de 2.000 gramos (tabla 1) (1).
Muerte fetal en chile entre los años 2000 y 2010 ¿un aumento real en la prevalencia?
| 2000 | 2003 | 2006 | 2009 | 2010 | |
|---|---|---|---|---|---|
| Tasa por 1000 nacidos vivos | 4.3 | 5.7 | 8.7 | 8.9 | 8.6 |
| Menor a 500 grs. (%) | 42.0 | 36.0 | 41.6 | ||
| Mayor a 32 semanas (%) | 75.0 | 47.0 | 32.0 | 34.0 | 31.2 |
| Mayor a 2000 grs. (%) | 24.0 | 26.0 | 23.4 | ||
| Con definición anterior (solo mayores de 500 grs.): | |||||
| Tasa por 1000 nacidos vivos | 5.0 | 5.6 | 5.0 | ||
| Mayor a 32 semanas (%) | 55.0 | 54.0 | 53.5 | ||
| Mayor a 2000 grs. (%) | 41.0 | 41.0 | 40.3 | ||
Desde 2006 en Chile se extiende certificado de defunción y se contabiliza las muertes fetales independiente de peso o edad gestacional. Esto ha influido en un aumento en la tasa de mortinatalidad. Sin embargo si excluimos los fetos menores a 500 grs se observan tasas estables de alrededor de 5 por 1000, comparable a los países desarrollados.
La muerte fetal es un evento que puede ser recurrente. Históricamente se consideraba que la ocurrencia aumentaba el riesgo en embarazos siguientes hasta en 10 veces. Hoy se sabe que el riesgo no alcanza esa magnitud. Recientemente datos de una gran cohorte en Escocia, que tuvieron su primer hijo entre 1980 y 2000 (2.677 pacientes con muerte fetal) mostraron que el riesgo de recurrencia de muerte fetal (ajustado para variables confundentes) en un segundo embarazo (luego de un embarazo con esta complicación) es de 1.94 [1.29–2.92] (3).
Factores de riesgoEn los países desarrollados la disminución en las tasas de muerte fetal ha sido mínima en las últimas dos décadas. La estrategia propuesta para disminuir la mortinatalidad en estos países, pasa por identificar y tratar los factores de riesgo. Para determinar los más importantes, una revisión australiana de la literatura publicada en Lancet en 2011, seleccionó 96 estudios poblacionales que analizaron los principales factores de riesgo en pacientes con muerte fetal. Desde el punto de vista de impacto poblacional, éstos son: obesidad, edad materna y tabaquismo.
La edad materna aumenta el riesgo progresivamente a partir de los 35 años, así, comparado con una madre menor a esta edad, la paciente tendrá un riesgo de 1,5 veces mayor entre 35 y 40 años; 2 veces mayor entre 40 y 45 años; y 3 veces más alto sobre los 45 años.
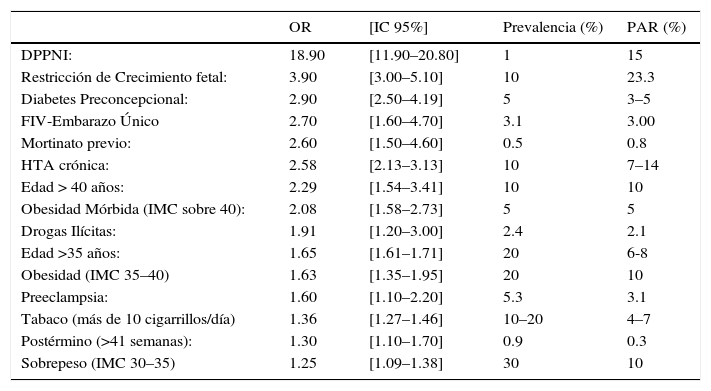
De los factores de riesgo modificables los de mayor importancia son el uso de tabaco, que aumenta el riesgo 1,5 a 3 veces; y la obesidad que incrementa el riesgo 2 veces. La ausencia de control prenatal tiene una Razón de Oportunidad (OR) de 3,3. El uso de drogas ilícitas, de 1,9. El bajo nivel socioeconómico y el bajo nivel educacional tienen OR de 1,2 y 1,7 respectivamente. Otros factores de riesgo importantes son patologías crónicas maternas como la hipertensión, diabetes mellitus, insuficiencia renal, patología tiroidea, enfermedades del mesénquima y reumatológicas (tabla 2) (4).
Factores de riesgo maternos y riesgo estimado de mortinato.
| OR | [IC 95%] | Prevalencia (%) | PAR (%) | |
|---|---|---|---|---|
| DPPNI: | 18.90 | [11.90–20.80] | 1 | 15 |
| Restricción de Crecimiento fetal: | 3.90 | [3.00–5.10] | 10 | 23.3 |
| Diabetes Preconcepcional: | 2.90 | [2.50–4.19] | 5 | 3–5 |
| FIV-Embarazo Único | 2.70 | [1.60–4.70] | 3.1 | 3.00 |
| Mortinato previo: | 2.60 | [1.50–4.60] | 0.5 | 0.8 |
| HTA crónica: | 2.58 | [2.13–3.13] | 10 | 7–14 |
| Edad > 40 años: | 2.29 | [1.54–3.41] | 10 | 10 |
| Obesidad Mórbida (IMC sobre 40): | 2.08 | [1.58–2.73] | 5 | 5 |
| Drogas Ilícitas: | 1.91 | [1.20–3.00] | 2.4 | 2.1 |
| Edad >35 años: | 1.65 | [1.61–1.71] | 20 | 6-8 |
| Obesidad (IMC 35–40) | 1.63 | [1.35–1.95] | 20 | 10 |
| Preeclampsia: | 1.60 | [1.10–2.20] | 5.3 | 3.1 |
| Tabaco (más de 10 cigarrillos/día) | 1.36 | [1.27–1.46] | 10–20 | 4–7 |
| Postérmino (>41 semanas): | 1.30 | [1.10–1.70] | 0.9 | 0.3 |
| Sobrepeso (IMC 30–35) | 1.25 | [1.09–1.38] | 30 | 10 |
PAR: Población atribuible al riesgo
RO: Razon de Oportunidad
HTA: Hipertensión Arterial
DPPNI: Desprendimiento Placentario
IC: Intervalo de Confianza
Modificado de Lancet 2011;377:1331-1340
La aproximación a este problema, es vital para poder entregar una explicación al evento actual; e indispensable para una ordenada elaboración de un duelo por los padres. Permitirá también el diseño de una estrategia preventiva acorde para la siguiente gestación. Lamentablemente no existe un estudio completo que permita responder todas estas interrogantes en forma rápida, eficiente y económica.
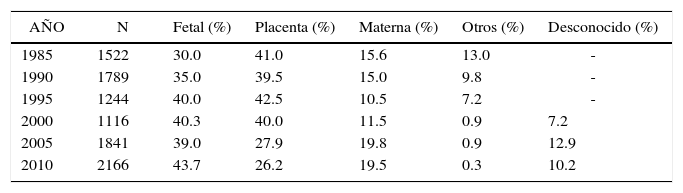
En Chile durante los últimos 30 años, el mayor porcentaje lo comparten las causas placentarias y fetales, con un 30 a 40% cada uno. Las muertes fetales atribuidas a enfermedades maternas corresponden a un 10-15%, las cuales han aumentado en la última década a casi un 20%. Otro 10% es considerado desconocido o no informado. Estos grupos se han mantenido relativamente estables sin embargo, cuando aumentan las causas desconocidas disminuyen en la misma proporción las placentarias. Aparentemente la consignación de hallazgos funiculares o placentarios como causa de muerte sin otros elementos histopatológicos, explica estas variaciones (tabla 3). Las causas fetales son lideradas por asfixia (desde 2003 se les denomina hipoxia) la que se puede observar entre un 50 y 60%, seguido por malformaciones congénitas y cromosomopatías, entre 25 y 30%. De manera menos frecuente aparecen la restricción de crecimiento fetal y las infecciones. Los datos de una reciente revisión sobre muerte fetal al término, muestran un 25% de causas fetales, 25–30% de causas placentarias, 10% enfermedades maternas y entre un 15–40% de los casos no se logra identificar la causa. Las estadísticas nacionales son bastante similares (tabla 4). En la experiencia nacional de centros únicos, un estudio retrospectivo descriptivo, a partir de los datos consignados en la ficha clínica, analizó los casos de muerte fetal en el hospital Padre Hurtado entre 1999 y 2006. Se registró un total de 277 casos de muerte fetal intrauterina, lo que implica una incidencia levemente mayor que la nacional. De estos, un 34% eran embarazos de término y un 60% embarazos de 32 semanas o más. La etiología fue liderada por el origen placentario con un 40%, seguidas por el origen fetal, con un 26%. El origen materno explicó un 12% y un 20% se consideró inexplicada. La tendencia de los últimos años ha sido la reducción de los casos en embarazos de término y en el número de casos en que no se encuentra una causa de muerte. Sin embargo, estas aproximaciones están influenciadas por los aspectos antes mencionados respecto de la fidelidad y precisión de la información (1).
Muerte fetal en chile 1985-2010. caracterización clínica.
| AÑO | N | Fetal (%) | Placenta (%) | Materna (%) | Otros (%) | Desconocido (%) |
|---|---|---|---|---|---|---|
| 1985 | 1522 | 30.0 | 41.0 | 15.6 | 13.0 | - |
| 1990 | 1789 | 35.0 | 39.5 | 15.0 | 9.8 | - |
| 1995 | 1244 | 40.0 | 42.5 | 10.5 | 7.2 | - |
| 2000 | 1116 | 40.3 | 40.0 | 11.5 | 0.9 | 7.2 |
| 2005 | 1841 | 39.0 | 27.9 | 19.8 | 0.9 | 12.9 |
| 2010 | 2166 | 43.7 | 26.2 | 19.5 | 0.3 | 10.2 |
Las categorías de muerte fetal han estado lideradas por las causas fetales y placentarias. Interesantemente a lo largo de los años estudiados se observa un aumento de las causas fetales y disminución proporcional de las placentarias. Al mismo tiempo en los últimos 10 años las patologías maternas adquieren mayor relevancia, llegando a casi el 20% de los casos.
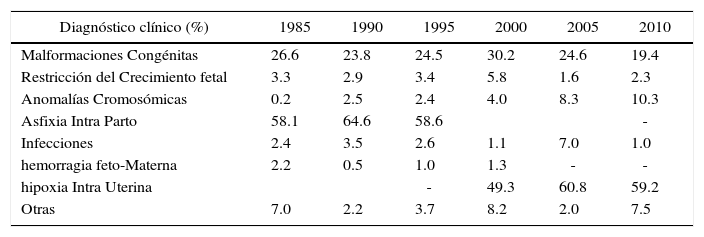
Mortalidad fetal: causas fetales chile 1985–2010.
| Diagnóstico clínico (%) | 1985 | 1990 | 1995 | 2000 | 2005 | 2010 |
|---|---|---|---|---|---|---|
| Malformaciones Congénitas | 26.6 | 23.8 | 24.5 | 30.2 | 24.6 | 19.4 |
| Restricción del Crecimiento fetal | 3.3 | 2.9 | 3.4 | 5.8 | 1.6 | 2.3 |
| Anomalías Cromosómicas | 0.2 | 2.5 | 2.4 | 4.0 | 8.3 | 10.3 |
| Asfixia Intra Parto | 58.1 | 64.6 | 58.6 | - | ||
| Infecciones | 2.4 | 3.5 | 2.6 | 1.1 | 7.0 | 1.0 |
| hemorragia feto-Materna | 2.2 | 0.5 | 1.0 | 1.3 | - | - |
| hipoxia Intra Uterina | - | 49.3 | 60.8 | 59.2 | ||
| Otras | 7.0 | 2.2 | 3.7 | 8.2 | 2.0 | 7.5 |
La principal causa de muerte fetal son los fenómenos hipóxicos que hasta 1998 estaban clasificados como asfixia. Desde entonces se prefiere hipoxia intrauterina. Ambas categorías son meramente descriptivas del evento final, aunque pueden deberse a distintas etiologías. Siguen las malformaciones y cromosomopatías. Estas últimas en aumento, probablemente por mejor diagnóstico. Llama la atención la ausencia de hemorragia feto materna en los últimos años, aunque es probable que se deba a un diagnóstico insuficiente.
Es importante estandarizar tanto los pasos a seguir como los especialistas involucrados en la evaluación, con el objetivo de alcanzar una interpretación precisa de los resultados. Una vez realizado esto, el siguiente paso es asignar causalidad a un conjunto de hallazgos determinados.
Estudio etiológicoLa aproximación etiológica debe incluir estudio materno, del feto y de la placenta, tanto clínico como de laboratorio. El análisis patológico de la placenta y feto junto con el cariograma son fundamentales. Los exámenes de laboratorio adicionales deben ser realizados de acuerdo a la situación clínica y fuertemente basados en la historia personal, familiar, examen clínico al ingreso y resultados de los estudios antes mencionados. Debe considerarse guardar muestras de líquido amniótico, plasma materno y fetal junto con tejidos placentarios para realizar exámenes una vez que el estudio inicial esté completo. Un aspecto fundamental en la realización de estas evaluaciones es la obtención de los consentimientos para la evaluación fetal, que incluye la realización de una amniocentesis anteparto y de un estudio postparto del feto y de la placenta. Estos exámenes otorgarán casi un 70% de las veces una respuesta sobre de la causa del problema. Además son importantes para determinar el riesgo de recurrencia y establecer el manejo clínico en el siguiente embarazo (5).
Estudio materno: Se debe realizar una anamnesis personal, familiar y laboral detallada, que debe incluir la historia personal y familiar del cónyuge. El examen físico debe ser completo y riguroso. Una vez obtenidos los consentimientos es importante realizar una amniocentesis (en ocasiones este examen no es factible de realizar) para poder tener un análisis citogenético preciso y con vitalidad celular. Aproximadamente un tercio de las veces el cariograma hecho a partir de tejido placentario obtenido postparto, no entrega información ya sea por falta de vitalidad y crecimiento celular o bien por infección del tejido. Respecto al estudio citogenético surge la interrogante en relación a la dificultad del sitio y la hora a la que ocurra el parto y la posibilidad de realizar este examen. El tejido trofoblástico puede permanecer 24 horas a 4°C en un frasco estéril antes de llegar al laboratorio. Sin embargo, el amnios (capa más interna de las membranas fetales de aspecto nacarado) puede lavarse con suero fisiológico y guardarse hasta siete días a 4°C, en un frasco estéril antes de llegar al laboratorio para su cultivo. Esto hace que prácticamente no hay un lugar en Chile en que la evaluación completa no pueda ser realizada. Debe realizarse el test para detección de hemorragias feto maternas antes del parto, con el objetivo de evitar que su resultado muestre anormalidades atribuibles al proceso del parto. Es el momento de tomar una muestra de suero materno para exámenes posteriores, según sea el resultado de la evaluación fetal inmediata o posterior a los exámenes fetales. Posteriormente al parto se procede con el resto del análisis materno. Este se realiza en forma dirigida dependiendo del examen clínico materno y de los hallazgos específicos del feto y placenta: hipertensión arterial y relacionadas (precisar diagnóstico de preeclampsia y su severidad); enfermedad tiroidea (establecer grado de funcionalidad y presencia de anticuerpos anti-tiroideos). Si hay evidencia de diabetes materna/ historia familiar u obesidad, debe precisarse el grado de control metabólico. Si hay sospecha de abuso de drogas es posible realizar un tamizaje toxicológico. En caso de signos de enfermedad de tejido conectivo realizar un tamizaje materno con evaluación de la serología para enfermedades autoinmunes. En caso de que exista hidrops fetal, se debe realizar tamizaje de anticuerpos para isoinmunización materna, serología parvovirus B19, electroforesis hemoglobina y análisis del liquido amniótico para enfermedades metabólicas. Ante signos clínicos de infección, realizar una pesquisa materna de estreptococo rectal-vaginal junto con toma de cultivos superficiales del feto y placenta. Adicionalmente puede ser necesario un análisis del plasma para serología viral y análisis molecular de líquido amniótico previamente obtenido. Si hay historia personal de trombosis o familiar de trombofilias, una restricción severa del crecimiento fetal o trombosis placentaria, es necesario considerar un estudio de trombofilia congénita y/o adquirida. Realizar el estudio precoz de trombofilias adquiridas y diferido (al menos ocho semanas) de las congénitas. En casos de antecedente de trombosis venosa previa en la madre, hay que considerar el empleo de terapia antitrombótica en el período postparto (tabla 5).
Alternativas a una autopsia completa: beneficios y limitaciones.
| Examen | Beneficios y limitaciones |
|---|---|
| • Examen placentario macroscópico y microscópico y examen fetal externo por patólogo especialista (incluye mediciones, Radiografías y fotos) | • Permite identificar síndromes, anomalías congénitas, displasias esqueléticas, tiempo de muerte y anomalías del crecimiento. Detecta ínfecciones placentarias, lesiones vasculares y patología del cordón |
| • Examen fetal externo e interno por patólogo especialista sin extraer órganos y sin examinar el cerebro | • Permite entregar el cuerpo a la familia con todos los órganos. Puede omitirse patología del SNC. Permite detectar anomalías internas y rol de la infección fetal |
| • Autopsia respetando el Encéfalo | • Beneficios de autopsia completa omitiendo patología del SNC |
| • Resonancia Nuclear Magnética (con o sin biopsia dirigida) | • Buena para identifcar patología del SNC. Puede omitir otras anomalías especialmente cardíacas. Infección no detectable excepto con biopsia con aguja |
| • Ultrasonido | • Puede evaluarse encéfalo, riñones y abdomen. No tan buena como resonancia para el SNC |
SNC: Sistema Nervioso Central.
Estudio fetal: Se debe realizar un examen físico macroscópico detallado por un neonatólogo, patólogo o genetista, incluyendo fotografías y radiografías de cuerpo entero. Siempre se debe solicitar una autopsia, con autorización de los padres. En caso de negativa, puede sugerirse una autopsia parcializada (exceptuar el cráneo) o resonancia magnética fetal con biopsias dirigidas. Si se observan anomalías fetales, una radiografía simple es de utilidad. Es relevante explicar al radiólogo el objetivo de la evaluación puesto que en casos de anormalidades cráneo faciales o de extremidades puede ser necesario realizar tomas especiales desde diferentes orientaciones (tabla 5 y 6).
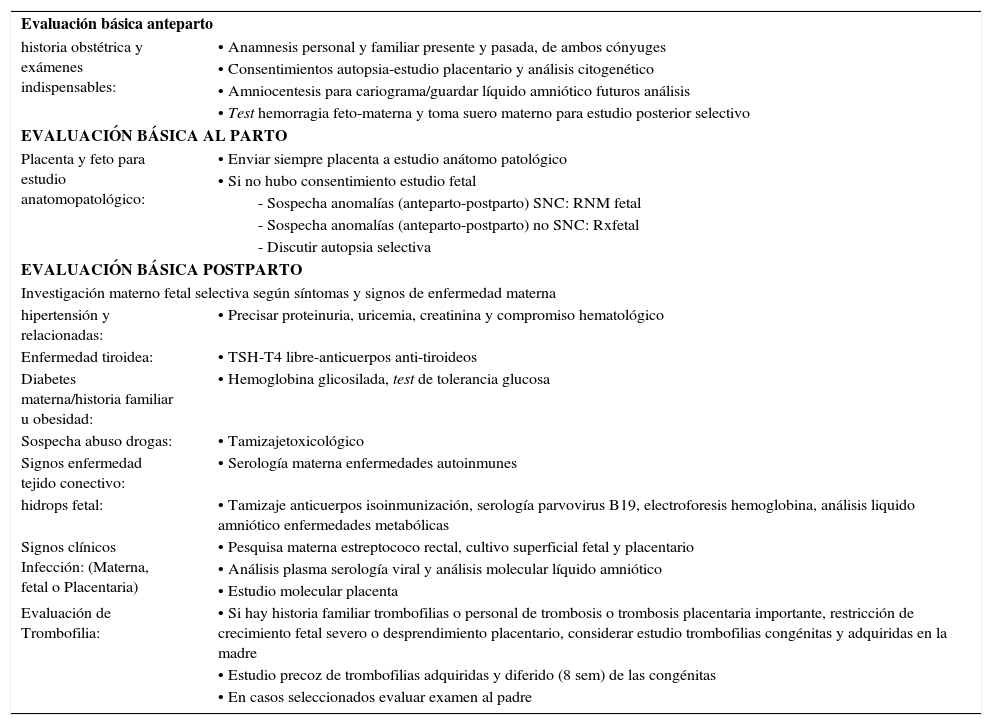
Muerte fetal anteparto: evaluación materno fetal-placentaria.
| Evaluación básica anteparto | |
| historia obstétrica y exámenes indispensables: | • Anamnesis personal y familiar presente y pasada, de ambos cónyuges |
| • Consentimientos autopsia-estudio placentario y análisis citogenético | |
| • Amniocentesis para cariograma/guardar líquido amniótico futuros análisis | |
| • Test hemorragia feto-materna y toma suero materno para estudio posterior selectivo | |
| EVALUACIÓN BÁSICA AL PARTO | |
| Placenta y feto para estudio anatomopatológico: | • Enviar siempre placenta a estudio anátomo patológico |
| • Si no hubo consentimiento estudio fetal | |
| - Sospecha anomalías (anteparto-postparto) SNC: RNM fetal | |
| - Sospecha anomalías (anteparto-postparto) no SNC: Rxfetal | |
| - Discutir autopsia selectiva | |
| EVALUACIÓN BÁSICA POSTPARTO | |
| Investigación materno fetal selectiva según síntomas y signos de enfermedad materna | |
| hipertensión y relacionadas: | • Precisar proteinuria, uricemia, creatinina y compromiso hematológico |
| Enfermedad tiroidea: | • TSH-T4 libre-anticuerpos anti-tiroideos |
| Diabetes materna/historia familiar u obesidad: | • Hemoglobina glicosilada, test de tolerancia glucosa |
| Sospecha abuso drogas: | • Tamizajetoxicológico |
| Signos enfermedad tejido conectivo: | • Serología materna enfermedades autoinmunes |
| hidrops fetal: | • Tamizaje anticuerpos isoinmunización, serología parvovirus B19, electroforesis hemoglobina, análisis liquido amniótico enfermedades metabólicas |
| Signos clínicos Infección: (Materna, fetal o Placentaria) | • Pesquisa materna estreptococo rectal, cultivo superficial fetal y placentario |
| • Análisis plasma serología viral y análisis molecular líquido amniótico | |
| • Estudio molecular placenta | |
| Evaluación de Trombofilia: | • Si hay historia familiar trombofilias o personal de trombosis o trombosis placentaria importante, restricción de crecimiento fetal severo o desprendimiento placentario, considerar estudio trombofilias congénitas y adquiridas en la madre |
| • Estudio precoz de trombofilias adquiridas y diferido (8 sem) de las congénitas | |
| • En casos seleccionados evaluar examen al padre | |
El estudio materno fetal ante la ocurrencia de la muerte fetal será la piedra angular para llegar al diagnóstico etiológico y así conocer la probabilidad de recurrencia y la forma de disminuir el riesgo en un próximo embarazo. Será importante enfatizar su utilidad ante los padres que en primera instancia, bajo el compromiso emocional, podrían rechazar cualquier estudio. El estudio materno y placentario no debiera generar resistencia. En caso de la autopsia debe recomendarse, aunque en caso de negativa podrá sugerirse estudios alternativos como resonancia, radiografías, ecografía o biopsias selectivas.
Estudio de placenta y cordón umbilical: Se encuentran hallazgos placentarios en un alto porcentaje de pacientes. Por este motivo el estudio macroscópico y microscópico son relevantes (6). Es importante que al finalizar el estudio se evalúe cuidadosa y metódicamente toda la información, para establecer un posible mecanismo causal. La clave es que la etiología definirá el riesgo de recurrencia, el cual puede ser variable. En ausencia de diagnóstico etiológico el riesgo empírico es de alrededor de un 3%. Este enfrentamiento queda esquematizado en la tabla 7(6,7).
Manejo del embarazo siguiente después de una muerte fetal.
| A.- CONSULTA PRECONCEPCIONAL O PRENATAL INICIAL POST EVENTO ADVERSO |
| • Detallada historia médica y obstétrica personal y familiar-incluye cónyuge |
| • Evaluación detallada del mortinato anterior |
| • Determinación del riesgo de recurrencia |
| • Suspender tabaco, alcohol, drogas |
| • Bajar de peso en mujeres obesas (sólo preconcepcional) |
| • Consejo genético si procede |
| • Caso a caso: Exs de diabetes, trombofilias, patologías inmunológicas |
| • Determinación suplementos necesarios |
| • Manejo especifico de condiciones crónicas maternas si procede |
| • Evaluación consolidación del duelo (considerar apoyo psicológico si es necesario) |
| B.- DURANTE EL EMBARAZO |
| Primer Trimestre: |
| • Determinación precisa de edad gestacional |
| • Evaluación completa de riesgo 11–14 semanas (ecografía, Doppler, bioquímica) |
| • Manejo específico de condiciones maternas si procede (Ej: HTA, DM, LES, Epilepsia, entre otros) |
| • Manejo emocional |
| Segundo Trimestre: |
| • Ultrasonido 22–24 semanas con evaluación estructural fetal y circulación materno fetal. Medición de Cérvix uterino |
| • Manejo específico de condiciones crónicas maternas si procede |
| • Considerar ultrasonido con Doppler umbilical a partir de 26-28 semanas (si existen condiciones crónicas maternas o alto riesgo de muerte |
| fetal en evaluación 11–14 semanas) |
| Tercer Trimestre: |
| • Ultrasonido para detectar restricción de crecimiento fetal desde las 28 semanas |
| • Monitoreo de movimientos fetales a partir de la semana 28 |
| • Evaluación del estado fetal anteparto desde la semana 32 o 2 semanas antes de muerte anterior lo que sea más precoz |
| (Doppler umbilical y perfil biofísico fetal) |
| • Manejo específico de condiciones crónicas maternas si procede |
| C.- PARTO |
| • Inducción en semana 39 semanas antes sólo con madurez pulmonar comprobada |
| • Si Doppler umbilical alterado o PBF menor a 6/8 administrar corticoides para madurez pulmonar fetal hasta 34 semanas e interrumpir el embarazo |
| D.- POSTPARTO |
| • Evaluación selectiva de Recién Nacido según causa de mortinato anterior |
HTA: Hipertensión Arterial. DM: Diabetes Mellitus. LES: Lupus Eritematoso Sistémico.
La edad gestacional es, posiblemente, la variable más relevante al decidir el momento y la forma de resolución del parto en estas pacientes. Si bien es comprensible el deseo materno de resolverlo prontamente, en general no es una situación de emergencia. En el segundo trimestre la dilatación y evacuación es posible pero limita el estudio fetal posterior. La manera más aceptada y difundida es la inducción del trabajo de parto. Antes de las 28 semanas, el empleo de Misoprostol en dosis de 200 a 400 mcg cada 4 a 6 horas por vía vaginal y ocitocina i/v son opciones aceptables. Luego de las 28 semanas se puede seguir el protocolo de inducción de parto convencional. La operación cesárea debe reservarse para las situaciones de morbilidad materna que contraindiquen un parto vaginal.
En condiciones de cesárea anterior antes de las 24 semanas puede utilizarse Misoprostol. Entre las 24 y 28 semanas no hay evidencia para respaldar su uso en forma segura. Luego de las 28 semanas en presencia de malas condiciones obstétricas puede además utilizarse una sonda folley como método adicional para generar cambios cervicales. La evidencia indica que existe una tasa de rotura uterina semejante a la de un trabajo de parto espontáneo y por lo tanto, puede realizarse una prueba de trabajo de parto. Si hay una cicatriz corporal el manejo debe ser individualizado ante la falta de evidencia respecto del manejo óptimo (8).
El siguiente embarazo. intervenciones para reducir la frecuencia de muerte fetalLo primero a considerar es que la población más vulnerable en términos socioeconómicos y culturales, tiene una mayor frecuencia de esta condición por lo que, para conseguir una reducción significativa debe existir un mayor y mejor acceso al cuidado médico general y reproductivo. Adicionalmente, un objetivo importante es influenciar los factores de riesgo biológico más potentes y ampliamente difundidos. Entre ellos el consejo preconcepcional en poblaciones médicamente en riesgo (diabetes, epilepsia, hipotiroidismo) y la reducción de:
- a.
El peso corporal preconcepcional
- b.
La frecuencia de tabaquismo
- c.
La ingesta de alcohol, drogas ilícitas
- d.
La maternidad sobre los 35 años, en especial sobre los 40 años
En relación a los factores propios del embarazo debe considerarse:
- 1.
La correcta verificación de la edad gestacional (examen médico precoz y un ultrasonido obstétrico entre las 11 y 14 semanas)
- 2.
Un correcto empleo de técnicas de fertilización asistida con disminución en la frecuencia de embarazo múltiple
- 3.
Realizar tamizaje de detección de riesgo de insuficiencia placentaria, restricción de crecimiento fetal e hipertensión arterial, detección del subgrupo de pacientes en riesgo de parto prematuro e infección
- 4.
Evitar el embarazo prolongado resolviendo los partos a las 41 semanas de edad gestacional.
Adicionalmente, desde un punto de vista de salud pública es necesario reforzar las auditorías perinatales y la investigación cuidadosa de los casos de muerte fetal en los servicios de salud (1,4,9).
Evaluación preconcepcionalDesde un punto de vista general, el riesgo de recurrencia va a ser distinto según la causa sin embargo, el riesgo global se estima que aumenta alrededor de dos veces. Por lo tanto, existe una alta probabilidad de que el evento no se repita, lo que puede tranquilizar a los padres. Las pacientes deben ser referidas a un nivel de atención especializado. El manejo se inicia tratando adecuadamente las condiciones maternas de riesgo, incluso en forma preconcepcional (tabla 7) (1,4,9).
EmbarazoLa monitorización del embarazo se hará desde el inicio de la gestación. Entre las 11 y 14 semanas va a ser importante determinar el riesgo de aneuploidías y ofrecer eventualmente el estudio genético a las pacientes que resulten de riesgo elevado. La evaluación debe incluir la determinación de facción libre de βhCG y de PAPPA y el ultrasonido Doppler, de las arterias uterinas. Estudios prospectivos de gran tamaño muestran una Razón de Oportunidad (RO) de entre 2 y 3 para muerte fetal, tanto con niveles de βhCG como PAPP A bajo 2 múltiplos de la media en fetos euploides. Por su parte, una translucencia nucal sobre percentil 95 implica una RO de entre 2 y 2.6 para muerte fetal en fetos euploides. Lo mismo se ha mostrado para onda A reversa en ducto venoso. Por lo tanto, a pesar de que para el tamizaje de aneuploidías cada vez aparece como más promisorio la determinación de riesgo con ADN fetal libre en sangre materna, el ultrasonido y la bioquímica seguirán teniendo un rol para seleccionar fetos con alto riesgo de muerte fetal y restricción de crecimiento, entre otros (1).
El ultrasonido Doppler de arterias uterinas debe repetirse entre 20 y 24 semanas. Es importante recordar que si es normal, el riesgo de restricción de crecimiento fetal y preeclampsia antes de las 34 semanas será extremadamente bajo.
Se recomienda seguir con curva de crecimiento fetal y Doppler umbilical a las 28 y 32 semanas. Desde las 32 semanas o una semana previo del episodio de muerte fetal en adelante, se recomienda perfil biofísico y Doppler umbilical en forma seriada semanal (1,10).
El momento de la interrupción no debiera ser más allá de la 38–39 semana sin embargo, desde las semanas 34 a 35 el riesgo de la prematurez, comparado con la posibilidad de repetir el evento, deben ser sopesados y ante la sospecha razonable de deterioro de la unidad fetoplacentaria está indicada la interrupción.
En esta metódica sugerida, el estudio ecográfico fetal será central para:
- 1.
Pesquisar malformaciones y síndromes genéticos fetales
- 2.
Evaluar la placentación inadecuada y por lo tanto, el riesgo de restricción de crecimiento fetal, el desprendimiento placentario, preeclampsia severa y otras patologías placentarias
- 3.
Evaluar el crecimiento fetal y el bienestar fetal en términos de oxigenación
De las muertes fetales que quedan sin diagnóstico etiológico aún con estudio exhaustivo, un porcentaje importante de ellos (52% según estudio retrospectivo noruego publicado en 2004) corresponde a restricciones de crecimiento no diagnosticadas con curvas poblacionales y sí con curvas customizadas. Estas curvas son hechas computacionalmente, considerando el origen étnico, talla y peso de los padres. Por esta razón, la búsqueda y detección de fetos con crecimiento restringido es un punto central de la estrategia para evitar la recurrencia. La ecografía deberá realizarse a las 28 y 32 semanas para determinar peso fetal y curva de crecimiento. En mujeres obesas se deberá tener especial cuidado, ya que la ultrasonografía es técnicamente más difícil y considerando el peso materno, si no existen curvas customizadas, podría haber fetos creciendo sobre el percentil 10 y que sin embargo, están cursando con restricción de crecimiento. En estos casos la caída en percentil de crecimiento deberá considerarse como alerta, por lo que el seguimiento estricto con Doppler materno y fetal es prioritario.
La base de datos Cochrane de 2009 evaluó la eficacia de estos exámenes para disminuir el riesgo de muerte fetal. En términos generales existen pocos estudios bien diseñados, controlados, para determinar cuál es el mejor método para disminuir la mortalidad fetal. La mayoría de estas pruebas tienen buena sensibilidad para determinar fetos en riesgo pero a expensas de una alta tasa de falsos positivos, lo que lleva a intervenciones innecesarias. En países desarrollados el empleo universal del monitoreo fetal anteparto e intraparto ha disminuido la mortalidad fetal pero a expensas de un aumento del porcentaje de cesáreas. La velocimetría Doppler de arteria umbilical es hoy en día el mejor predictor de mortalidad fetal, especialmente en fetos con restricción de crecimiento y por lo tanto, tendrá un rol central en el manejo. Asimismo, trabajos recientes han mostrado utilidad de la relación cerebro-placentaria para detectar fetos en riesgo aún antes de alterarse el Doppler de arteria umbilical. Esta relación o la dilatación en arteria cerebral media podrían ser considerados en un futuro cercano (1,11).
Conclusiones- 1.
La muerte fetal intrauterina ocurre en Chile, así como en países desarrollados, en una frecuencia aproximada de 5 por 1.000 nacidos vivos. Las causas por grupo son lideradas por las causas fetales y placentarias, quedando un porcentaje importante sin diagnóstico etiológico (20 a 40%). Un 10% de las veces hay patologías maternas crónicas, congénitas o infecciosas vinculadas a la muerte fetal [Evidencia IIa Nivel B].
- 2.
Es fundamental enfatizar a los padres sobre la importancia del estudio completo placentario y fetal, es decir, autopsia fetal, estudio histopatológico placentario y evaluación citogenética del líquido amniótico, ya que en forma combinada estos exámenes pueden mostrar la causa de muerte en un 70 y un 75% de los casos [Evidencia IIb Nivel B].
- 3.
El vaciamiento uterino debe propiciarse por vía vaginal con el uso de Misoprostol, salvo indicación absoluta de cesárea. En caso de una cesárea anterior, puede usarse Misoprostol hasta la semana 24. En edades gestacionales mayores, preferir métodos mecánicos como dilatación con sonda Foley [Evidencia IIb Nivel B].
- 4.
El porcentaje de recurrencia y el manejo en futuros embarazos dependerá fuertemente de la causa etiológica [Evidencia III Nivel C].
- 5.
En siguiente embarazo será primordial el manejo de patologías maternas crónicas y factores de riesgo presentes en la madre en forma pre-concepcional [Evidencia IIb Nivel B].
- 6.
La evaluación de la estructura fetal y funcionalidad placentaria con ultrasonido y Doppler umbilical, es un aspecto central del control médico durante los siguientes embarazos. La interrupción del embarazo estará indicada a las 38–39 semanas o en caso de sospecha de deterioro fetal progresivo [Evidencia IIb Nivel B].
Los autores declaran no tener conflictos de interés, en relación a este artículo.