El manejo del dolor agudo del paciente dependiente de sustancias, es un desafío para el profesional encargado de otorgar alivio a su síntoma. La dependencia de sustancias es reconocida como una enfermedad cerebral primaria crónica y recurrente. Su neurobiología y mecanismos fisiopatológicos de adaptación a la sustancia generan cambios en la percepción del dolor, en la respuesta a analgésicos opioides y cambios conductuales que interfieren con el tratamiento del dolor. Un conocimiento básico y claro respecto de lo descrito permite diseñar estrategias seguras y eficaces de alivio del dolor, sin interferir el curso de la enfermedad adictiva. Artículos de revisión, recomendaciones y guías elaboradas por expertos coinciden en que el tratamiento más eficaz del dolor incluye un manejo multimodal, un enfoque multidisciplinario, mantención de la terapia de sustitución y una estrecha vigilancia durante el episodio agudo de dolor y su seguimiento posterior.
Acute pain management in a patient with substance use disorder offers a great challenge to health providers in charge of the case. Substance dependence is recognized as a primary chronic and recurrent cerebral disease. The neurobiology and adaptive mechanisms of substance dependence generate changes in pain perception and the response to opioids, as well as behavioral changes that interfere with the pain treatment. A basic and explicit understanding of the mechanism of the disease permits to implement pain relieve strategies that are safe and efficacious without interfering with the progression of the disease. Review articles, recommendations and guidelines elaborated by experts agree that the most effective way ofpain treatment includes a multimodal drug approach, a multidisciplinary team, the maintenance of the substitution therapy, and a close vigilance of the patient throughout the episode of acute pain, as well as during the follow-up.
En la población general la presencia de dolor agudo moderado a severo deteriora la calidad de vida y reduce su funcionalidad. Si el alivio es insuficiente puede tener consecuencias negativas a mediano y largo plazo, como el desarrollo de dolor agudo persistente, cronificación del dolor, descompensación de la patología médica concomitante y secuelas psicológicas.
En el paciente dependiente de sustancias, el dolor agudo tiene características especiales en cuanto a la intensidad, interferencia con los cambios fisiopatológicos propios de su enfermedad, interacción con el tratamiento a aplicar y dificultades en el equipo de salud tratante por desconocimiento o prejuicio respecto de su condición.
La dependencia a sustancias tiene una prevalencia desconocida en nuestro país; hay información incompleta pues no incluye opioides ilícitos ni el abuso de analgésicos narcóticos. La última estadística nacional corresponde a 2013, la cual proviene de una encuesta realizada a menores de 25 años y toma como indicador el consumo de drogas ilícitas y alcohol en el último año (1). En el Informe Mundial de Drogas de la ONU se estima que un 5% de la población adulta del mundo consumió alguna sustancia ilícita por lo menos una vez en 2010 y que los consumidores problemáticos son el 0,6% de la población adulta mundial (2). Aunque esto significa una estabilización global en relación a la pasada década, Estados Unidos y otros países desarrollados han presentado un persistente crecimiento en el consumo de analgésicos narcóticos de prescripción (opioides), los que han sido utilizados sin estrategias de prevención y para todo tipo de dolor. Las consecuencias son graves: aumento en forma sostenida del consumo ilícito, el tráfico y las consultas a servicios de urgencias por problemas relacionados al consumo, además de un incremento de muertes por sobredosis (3). Es por lo tanto, útil tener nociones de los aspectos más importantes del tratamiento del dolor agudo en pacientes abusadores o dependientes de sustancias.
El tratamiento del dolor de intensidad moderada a severa en el paciente dependiente de sustancias, representa un desafío importante debido a que su condición puede interferir el manejo, especialmente cuando se plantea el uso de opioides. Frente a esto, en el paciente y el equipo de salud surgen dudas o miedos por el riesgo de interacción con sustancias de consumo activo, de generar una recaída de la adicción o de exponer al paciente al riesgo de desarrollar una nueva dependencia. Estas aprehensiones se originan principalmente en el potencial adictivo de los opioides, en el desconocimiento de las condiciones seguras de uso y en la carencia de alternativas efectivas de tratamiento del dolor. En situaciones de dolor agudo perioperatorio o crónico oncológico, existe un riesgo muy bajo de generar una dependencia a opioides cuando su uso es racional y controlado. No obstante se requiere considerar las interacciones farmacológicas y la adaptación fisiológica por consumo crónico de sustancias. Es necesario conocer las definiciones de abuso a sustancias, dependencia, factores de riesgo y su fisiopatología para poder diseñar esquemas de manejo eficaz y seguro del dolor en el paciente dependiente.
El presente artículo focaliza la discusión en los aspectos básicos a los que el equipo de salud se puede ver enfrentado, cuando tiene que tratar el dolor agudo perioperatorio de un paciente adicto o dependiente de sustancias. Entrega además herramientas prácticas de manejo recomendadas en guías clínicas y en revisiones del tema elaboradas y publicadas por expertos.
DefinicionesEn la última década ha existido preocupación por la confusión en los términos y definiciones. Debido al estigma social que acompaña a quien sufre una adicción, se cambió este término por dependencia a sustancias. No obstante la dependencia se puede presentar tanto en el sujeto que tiene una enfermedad adictiva como en el que necesita tratamiento permanente de opioides por indicación médica (4).
Abuso, adicción o dependencia de sustanciasEn el manual de enfermedades psiquiátricas de la sociedad americana de psiquiatría (DSM 4) se definían como entidades separadas, abuso y dependencia a sustancias. Como abuso se entiende el uso indebido y repetido de una sustancia adictiva con consecuencias sociales, laborales y a veces legales, pero sin desarrollo de dependencia. Para hacer diagnóstico de dependencia a sustancias se requerían los siguientes criterios: consumo crónico, desarrollo de tolerancia, dependencia física, progresión y compulsión por el consumo, generando graves consecuencias sociales, laborales y legales. Estas definiciones separaban dos entidades que han sido consideradas como un continuo de una sola enfermedad. En la más reciente clasificación de enfermedades psiquiátricas, el DSM 5, se cambió la definición englobando ambos términos, abuso y dependencia, en el término Substancie Use Disorder. Este término considera que son estadios de la misma enfermedad en grado leve hasta severo (5). Sin embargo, debido a que aún no hay traducción al español, utilizaremos indistintamente los términos dependencia a sustancias y adicción, y abuso de sustancias como previamente fue definido.
Dependencia física o fisiológicaFenómeno de tolerancia o adaptación física a una sustancia que se manifiesta en el síndrome de abstinencia (6). Puede estar presente en pacientes con prescripción médica de opioides, por dolor crónico benigno u oncológico, sin que exista desarrollo de adicción (4).
Síndrome de abstinenciaSíntomas y signos debidos a una brusca suspensión o reducción, o por el uso de antagonista específico a la sustancia. Las características del síndrome dependerán del tipo de sustancia (opioides, estimulantes, alcohol, entre otros) (6).
Uso problemático de opioidesEs un término usado para describir un conjunto de comportamientos aberrantes durante el tratamiento mantenido con opioides y puede ser señal de que el paciente los está utilizando con fines diferentes que el tratamiento de dolor. Éstos fueron descritos por Chabal (10) y aunque no permiten predecir riesgo son útiles como señales de advertencia para tener sospecha y descartar un posible mal uso de opioides (tabla 1).
Criterios de uso problemático deopioides
| 1. El paciente tiene una exagerada preocupación enfocada en el uso de opioide, la que es desproporcionada al dolor que sufre. Ocupa gran parte de la consulta en manifestar esta preocupación más allá de los efectos del dolor mismo y esto ocurre en repetidas consultas. |
| 2. El paciente tiene un patrón mantenido en que solicita le sean repetidas recetas antes del tiempo prescrito, refiriere mayor necesidad por escalamiento de la dosis sin confirmarse cambios agudos de dolor o de condición de salud que lo justifiquen. |
| 3. Múltiples llamados telefónicos al centro o consulta de dolor solicitando a personal no médico más recetas. |
| 4. Refiere frecuentes problemas con la prescripción por pérdida de fármacos, recetas o robo de los mismos. |
| 5. El paciente obtiene opioides de fuentes externas al centro donde trata su dolor como servicios de urgencia, otros centros e incluso de forma ilegal. |
Ref(7).
Término a veces utilizado para describir un comportamiento aparentemente aberrante, pero que se explica por un tratamiento insuficiente del dolor y que desaparece cuando se ajusta la terapia analgésica.
Fisiopatología de la dependencia de sustanciasHoy en día es totalmente aceptado y respaldado por la evidencia, afirmar que la dependencia a sustancias es una enfermedad cerebral primaria crónica y recurrente, caracterizada por la búsqueda compulsiva de la sustancia, pérdida del control del consumo y aparición de distress emocional y físico cuando se interrumpe la exposición. Estudios en animales y humanos demuestran que su desarrollo se explica por las características de la sustancia, el tipo de exposición y sus efectos, la presencia de factores de riesgo genético y psicosocial y la interacción con el contexto ambiental en que se produce (6,7).
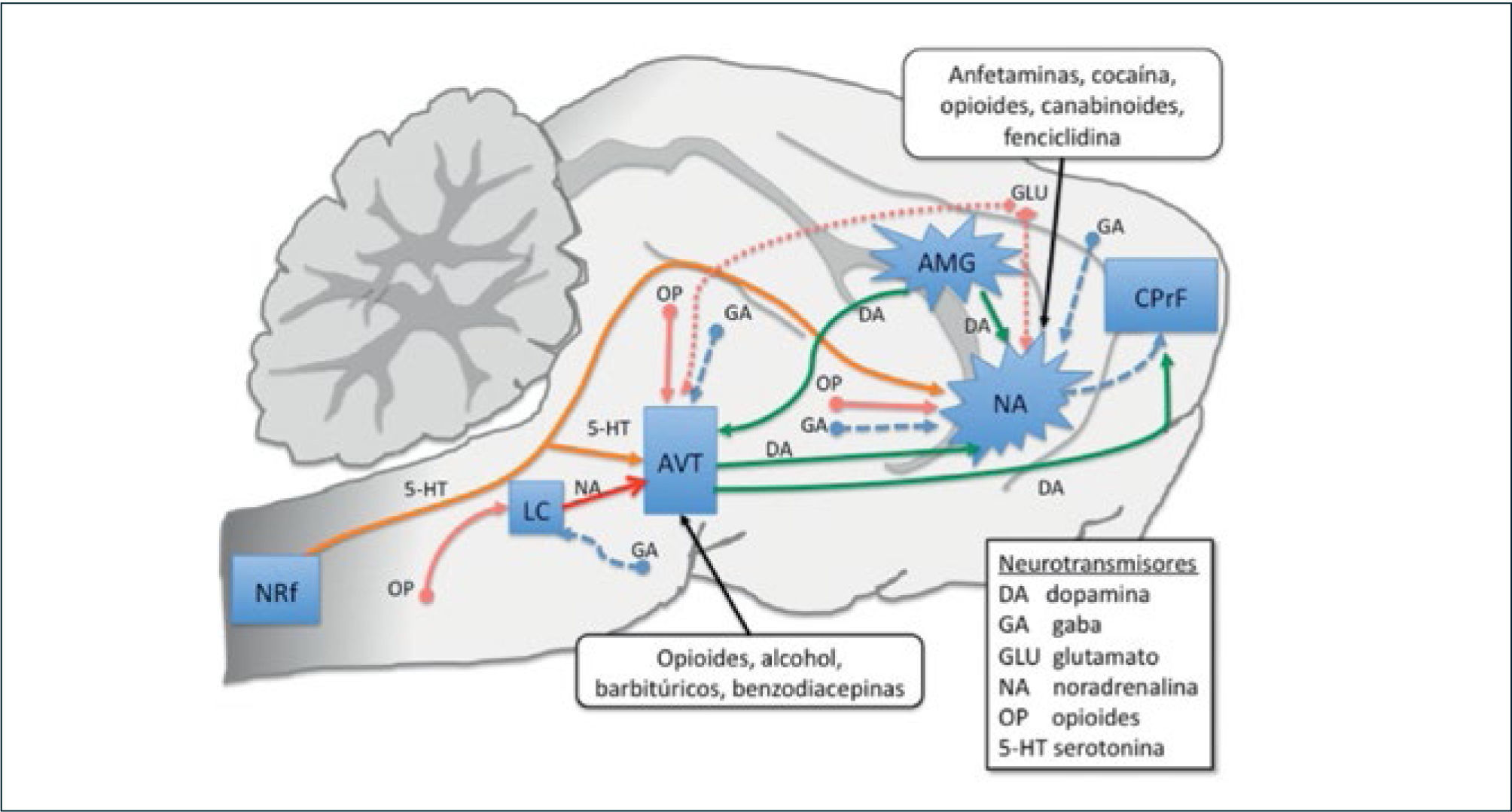
Neurobiología de la dependencia a sustanciasEl estado de adaptación y dependencia a la sustancia adictiva se ha definido como el resultado de una alteración en los mecanismos neurológicos de recompensa. Éstos se encuentran formados por el circuito mesocorticolímbico que relaciona los sitios targets de la droga con centros que procesan el estímulo, registran el contexto emocional y generan la conducta de búsqueda-recompensa para repetir la experiencia (figura 1).
Normalmente este sistema funciona para todos los estímulos que provocan placer (alimentación, sexo, entre otros). Por medio de la memoria emocional y contextual se tiende a repetir la búsqueda del estímulo. Se sabe que en el área ventral tegmental (AVT) y en el núcleo accumbens están los receptores para la mayoría de sustancias adictivas (opioides, benzodiacepinas, canabinoides, alcohol y estimulantes). Al ser estimulados estos centros por medio de sus conexiones neuronales liberarán dopamina en la amígdala, donde se procesará la calidad del estímulo. A su vez las proyecciones dopaminérgicas que van desde el AVT a la corteza prefrontal y orbitofrontal generan en estas áreas la conducta de búsqueda de recompensa. Cuando hay repetida exposición a un agente exógeno altamente estimulante se produce depleción de dopamina en el circuito y, a nivel celular, hay desensibilización y/o internalización de receptores específicos a la sustancia (5,6). Esto genera tolerancia por neuroadaptación y se requerirá cada vez una mayor cantidad de sustancia para sentir el mismo efecto placentero. En una etapa más avanzada la interrupción del consumo generará activación del locus cerúleo, el que liberará gran cantidad de noradrenalina, principal responsable del síndrome de abstinencia.
Esta alteración del sistema de recompensa es la responsable de la conducta impulsiva que se transforma en compulsiva por consumo. A su vez la memoria contextual social y emocional, asociadas a esta experiencia, son gatillos de recaídas frente a estímulos contextuales (lugares, sensaciones, estrés). Hay cambios mantenidos a largo plazo que pueden durar hasta cinco años desde la última exposición (8). Se producen aún en ausencia de consumo y son alteraciones anatómicas de las neuronas y de los neurocircuitos que forman parte.
Enfoque biopsicosocialLa dependencia se desarrollará con mayor probabilidad cuando el sujeto que interactúa con la sustancia adictiva tenga factores de riesgo genéticos y psicosociales, cuando lo hace en un patrón de consumo repetido y prolongado y si el contexto ambiental es favorecedor del consumo o es en presencia de situaciones de estrés emocional (4).
Los factores genéticos han sido estudiados en gemelos y en animales de experimentación. Se han identificado áreas cromosómicas más asociadas a riesgo de adicción a sustancias específicas como el alcohol, opioides, cocaína, nicotina y marihuana. Los factores genéticos son responsables de la vulnerabilidad del sujeto a desarrollar una dependencia. Éstos pueden determinar alteraciones del sistema dopaminérgico, serotoninérgico y noradrenérgico que se asocian a conductas impulsivas y personalidades temerarias. Pueden ser por variaciones de la disponibilidad del neurotransmisor, por diferencias en la conformación o población de receptores, o por diferencias en las señales intracelulares.
El sistema opioide endógeno es el que media el efecto hedónico de las sustancias adictivas (4,6,9) que estimulan a los centros que forman los circuitos de recompensa (figura 1). Por ello es que su bloqueo con naltrexona se utiliza para reducir la compulsión no sólo en adictos a opioides. El factor hereditario familiar es un factor de riesgo mayor para el inicio, mantención y recaída en la dependencia (6, 9).
Por último los factores genéticos pueden influir en la metabolización de las sustancias, haciendo variar la biodisponibilidad, metabolismo y proporción de metabolitos activos de la droga (4,6,7,9).
Los factores sociales y ambientales pueden ser facilitadores del inicio y la mantención del consumo (ambiente familiar y social). El consumo asociado a estresores emocionales, situación de abuso sexual o violencia intrafamiliar en la niñez o situaciones de guerra, son claves ambientales que influyen en la memoria emocional del circuito de recompensa (hipocampo, amígdala y corteza prefrontal) y se encuentran frecuentemente en portadores de dependencia. Modelos animales muestran que estos factores estresores asociados a exposición de sustancias adictivas producen cambios en los circuitos neuronales de recompensa por reorganización de redes y aumento de la excitabilidad, debido a su neuro-plasticidad funcional y estructural (4,8).
Consideraciones generalesEs importante tener en cuenta que el foco de atención debe ser lograr un tratamiento analgésico que aporte alivio significativo con bajo riesgo para el paciente. Como se describió anteriormente, una de las condiciones que diferencian al paciente dependiente de opioides es que, para tratar el dolor puede tener mayor requerimiento de analgesia que la población general. En modelos experimentales se ha determinado que el umbral y tolerancia a estímulos dolorosos controlados son inferiores a individuos no dependientes de opioides (10,11). En la evaluación del sujeto dependiente de sustancias se hará especial énfasis en la forma cómo se aborda su problema y aspectos específicos relacionados a su dependencia.
La anamnesis debe ser hecha en un ambiente receptivo, discreto y confidencial. Esto permite al paciente tener confianza para entregar toda la información respecto de su dependencia y le evitará sentir que su condición será un obstáculo para el tratamiento de su dolor. Con la evaluación clínica habitual y los datos obtenidos es posible diseñar un plan de tratamiento del dolor, que considere los cuatro aspectos esenciales de su dependencia.
- 1.
Tipo de sustancia. Las drogas que generan más intensa estimulación de los sistemas de recompensa, por su efecto hedónico, generan mayor compulsión. La estimulación intensa y repetida lleva más rápido a una depleción de dopamina en el sistema mesocorticolímbico y la abstinencia de ellas genera un refuerzo negativo (anhedónico) que intensifica el impulso por repetición del consumo (7–9).
- 2.
Tiempo de exposición. Cuando es prolongado (adicción de larga data) aumenta la magnitud de la tolerancia. Las sustancias adictivas generan tolerancia celular (internalización de receptores, cambios en segundos mensajeros) y cambios a largo plazo (neurocircuitos) que requieren una recuperación más prolongada y tienen riesgo mayor de recaída (6–8). No obstante, en abstinencia se revierte este efecto y se vuelven a exponer los receptores celulares lo que, en caso de recaída, aumenta el riesgo de intoxicación si se consumen dosis similares a las utilizadas antes de la abstinencia. Este hecho es responsable de complicaciones graves como la depresión respiratoria por opioides, el colapso cardiovascular por estimulantes o la neurotoxicidad por cualquiera de ellas (7,8).
- 3.
Vía de administración. Es importante cuando se trata de drogas utilizadas por vía intravenosa, transmucosa o inhaladas por vía pulmonar. Esto se debe a que los incrementos rápidos de concentración plasmática intensifican el efecto hedónico y la recompensa al consumo es más intensa y de duración más corta.
- 4.
Reconocimiento del Síndrome de Intoxicación y el Síndrome Abstinencia. El sujeto dependiente de sustancia puede necesitar tratamiento analgésico en situación de consumo activo de la droga, de terapia de sustitución, en abstinencia obligada o en período de rehabilitación. Por lo tanto, se deben reconocer los síndromes de intoxicación y abstinencia y las complicaciones sistémicas de las diferentes sustancias. La suspensión brusca o el uso de antagonistas durante el consumo activo es una situación de distrés fisiológico y riesgo de complicaciones. Por ello, es que el uso de naloxona está indicado solamente cuando hay una intoxicación aguda por opioides en pacientes no dependientes. Los síndromes de intoxicación y abstinencia son característicos de cada sustancia (tabla 2, tabla 3) y deben ser conocidos por el equipo dolor que tratará al paciente.
Tabla 2.Síndromes de intoxicación y abstinencia a opioides
Intoxicación aguda Síndrome abstinencia Signos vitales PA ⇓ o ⇔
FC ⇓ o ⇔
FR ⇓
T° ⇓ o ⇔PA ⇑ o ⇔
FC ⇑ o ⇔
FR ⇑ o ⇔
T° ⇔Nariz y ojos Miosis Midriasis, Lagrimeo y Rinorrea Sistema Nervioso Central Sedación o coma
Euforia, Delirio o Estupor
Convulsiones (petidina, tramadol, propoxifeno o por hipoxia)Normal, irritable, inquietud
Convulsiones, temblor, calambresSistema Gastrointestinal Ruidos intestinales disminuidos Náuseas y vómitos, diarrea Piel Prurito Piloerección y sudoración PA: presión arterial / FC: frecuencia cardíaca / FR: frecuencia respiratoria; T°: temperatura / ⇑: aumentada / ⇓: disminuida / ⇔: estable.
Ref(6).
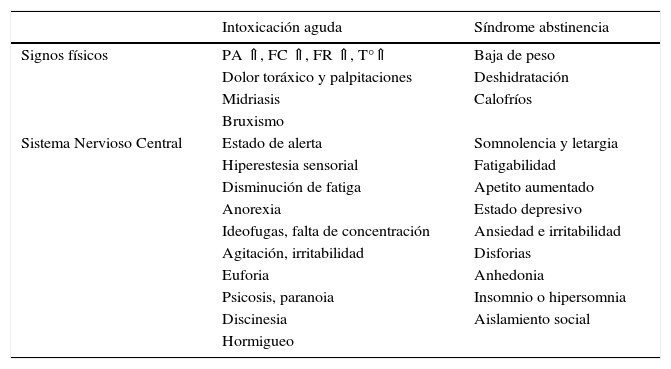
Tabla 3.Síndromes de intoxicación Y abstinencia A estimulantes, cocaína Y anfetaminas
Intoxicación aguda Síndrome abstinencia Signos físicos PA ⇑, FC ⇑, FR ⇑, T°⇑ Baja de peso Dolor toráxico y palpitaciones Deshidratación Midriasis Calofríos Bruxismo Sistema Nervioso Central Estado de alerta Somnolencia y letargia Hiperestesia sensorial Fatigabilidad Disminución de fatiga Apetito aumentado Anorexia Estado depresivo Ideofugas, falta de concentración Ansiedad e irritabilidad Agitación, irritabilidad Disforias Euforia Anhedonia Psicosis, paranoia Insomnio o hipersomnia Discinesia Aislamiento social Hormigueo PA: presión arterial / FC: frecuencia cardíaca / FR: frecuencia respiratoria; T°: temperatura / ⇑: aumentada / ⇓: disminuida
Ref(9).
Se refiere al concepto de utilizar simultáneamente terapias analgésicas con diferente mecanismo y sitio de acción, con el objetivo de aumentar la eficacia y reducir los efectos colaterales de cada terapia. En términos prácticos considera el uso simultáneo de antiinflamatorios no esteroidales (AINEs), paracetamol, técnicas loco-regionales con anestésicos locales y coadyuvantes. Este concepto de manejo ha demostrado una reducción de los requerimientos de opioides y de sus efectos adversos en el contexto de dolor agudo perioperatorio y también del tratamiento de dolor crónico.
Manejo multidisciplinarioTodo paciente dependiente de sustancias que deba ser tratado por dolor moderado a severo, agudo o crónico, benigno u oncológico, tiene que ser abordado de manera integral incluyendo a un psiquiatra. Este especialista es necesario para la estabilización aguda del paciente, reduciendo el riesgo de toxicidad o en el manejo de la abstinencia a la sustancia. Además será necesario para el tratamiento de los trastornos afectivos y las psicomorbilidades que pueden estar presentes.
Tratamiento del dolor agudoConsideraremos situaciones de dolor agudo en grado moderado a severo y secundario a patología médica, traumática o en un contexto perioperatorio. Estas son las condiciones en que hay distrés físico y/o emocional que pueden necesitar el uso de opioides. La mayoría de las publicaciones recomiendan utilizar un manejo multimodal del dolor. No hay estudios controlados que permitan anticipar el resultado de alguna estrategia específica en el manejo de pacientes dependientes de sustancias. No obstante, hay publicaciones que entreguen útiles recomendaciones basadas en la experiencia de centros de tratamiento del dolor, revisión de casos reportados, opiniones de expertos y desarrollo de guías clínicas basadas en la opinión de expertos (11).
Manejo general del dolorTécnicas regionalesSon recomendadas en guías y artículos de revisión para el tratamiento del dolor agudo perioperatorio en el sujeto dependiente que es sometido a una cirugía de urgencia o electiva (11,15,16). Las técnicas locore-gionales y neuroaxiales con anestésicos locales permiten analgesia preventiva y en muchos tipos de cirugía traumatológica y de hemiabdomen inferior, son técnicas anestésicas que evitan la anestesia general y el uso de opioides para control del dolor severo. Las técnicas usadas incluyen la infiltración preincisional de la herida operatoria, los bloqueos de nervio periférico, de plexo braquial, anestesia espinal y anestesia epidural. En muchas de ellas es posible prolongar su uso más allá de la cirugía utilizando catéteres para la infusión continua de anestésicos locales. Estas técnicas pueden ser configuradas como sistemas de analgesia controlada por paciente (PCA) adicionando a la infusión continua bolos demandados por el paciente, lo que otorga a la técnica eficacia adaptada a cada individuo. Por lo tanto, cuando es factible, se recomienda utilizar siempre técnicas locoregionales como anestesia y/o analgesia.
Analgésicos sistémicosLos AINEs no selectivos y los COX2 selectivos son recomendados para todo paciente a menos que exista una contraindicación específica (13,15). Administrados por vía parenteral desde el intraoperatorio y cuando es posible, como analgesia preventiva antes de la noxa, otorgan analgesia eficaz. Hay evidencia de que en población no dependiente se reduce el consumo de opioides y sus efectos colaterales (16,20). Esquemas de Ketoprofeno 300mg/24hrs., Ketorolaco 90 a 120mg/24 hrs. o Clonixinato de lisina 300mg/24 hrs. por vía intravenosa son recomendables en pacientes adultos que no tienen contraindicación. No está demostrado que la alteración de la coagulación pudiera producir aumento del riesgo de sangrado perioperatorio, por lo que han sido recomendados en guías clínicas de manejo de dolor agudo postoperatorio (20). Se recomienda administrar en infusión continua o en régimen horario, pero no a demanda (13,16,20). El paracetamol por vía intravenosa, debido a que su sitio y mecanismo de acción es diferente, otorga un efecto sinérgico a los AINEs. Los analgésicos COX2 selectivos (parecoxib) por vía parenteral son otra alternativa eficaz y puede tener efecto sinérgico con AINEs no selectivos. En muchos tipos de cirugía estos fármacos pueden ser utilizados como analgésicos únicos sin requerir opioides para el control del dolor agudo postoperatorio. Además pueden ser mantenidos por vía oral para tratamiento del dolor en domicilio por una a dos semanas.
CoadyuvantesEl uso de coadyuvantes o coanalgésicos en el tratamiento de dolor agudo postoperatorio tiene como objetivo potenciar el efecto de los analgésicos y disminuir los requerimientos de ellos.
KetaminaEs un hipnótico disociativo de utilidad como coanalgésico cuando es administrado en el período intraoperatorio y postoperatorio inmediato en sujetos no dependientes, como también en pacientes tolerantes a opioides (13,17). Esto se debe a su efecto agonista adrenérgico y serotoninérgico sobre la vías inhibidoras de la transmisión del dolor y también por su acción antagonista del neurotransmisor glutamato excitatorio, bloqueando el receptor NMDA de la vía excitatoria del dolor. También es importante su acción en la reversión de la hiperalgesia inducida por opioides observada en los pacientes con tolerancia crónica a ellos. Su uso clínico se ha demostrado en cirugía abdominal mayor y traumatológica realizadas con anestesia general. Se describe un esquema de ketamina en carga intravenosa intraoperatoria de 0,2 a 0,5mg/kg seguidas de infusión continua a 2 microgramos/Kg/min mantenida hasta 48 horas del postoperatorio. A estas dosis se ha observado reducción de los requerimientos de morfina y del EVA al compararlas con placebo (18).
Dexmetomedina y ClonidinaSon agonistas α-adrenérgicos que han demostrado efecto analgésico coadyuvante reduciendo los requerimientos de opioides en el perioperatorio de diverso tipo de cirugías (18). No obstante, su uso parenteral requiere titulación de dosis endovenosa y monitoreo hemodinámico por sus efectos cardiovasculares. Por lo tanto, su uso está restringido a las condiciones de monitoreo y experiencia en su empleo. No hay evidencia que permita recomendar esquemas en pacientes dependientes de sustancias.
Gabapentina y PregabalinaSon fármacos antiepilépticos bloquea-dores de canales de sodio que han demostrado tener un efecto coadyuvante analgésico cuando son administrados en el preoperatorio. Dada la poca interacción que ofrecen con opioidesy sustancias adictivas estimulantes su uso es seguro. Gabapentina 300mg o Pregabalina 150mg VO han sido utilizadas en el preoperatorio con un efecto coanalgésico postoperatorio (18).
Analgésicos opioidesHoy es aceptado y mencionado en artículos de revisión que un individuo dependiente de sustancias con dolor agudo moderado a severo, benigno u oncológico, puede ser tratado con opioides y que, correctamente utilizados y en condiciones controladas, no representan un riesgo mayor de desarrollar una nueva dependencia (4,11,13,15,16). Su empleo se debe ajustar a la tolerancia en los consumidores activos de opioides con el objetivo de evitar los síntomas de abstinencia, la persistencia del dolor por dosis insuficientes y el riesgo de sufrir efectos adversos por toxicidad (depresión respiratoria y neurotoxicidad) cuando se sobrestima la tolerancia. En individuos dependientes de otro tipo de sustancias (cocaína, marihuana, anfetaminas) el uso agudo de opioides no representa riesgo aumentado, siempre y cuando se realice una juiciosa indicación, adecuado seguimiento y su empleo sea por un período corto (9). Trataremos a continuación el manejo de acuerdo a la diferente presentación de la dependencia a opioides.
Dependiente de opioides en tratamiento y abstinenciaEs importante determinar esta condición con el dato clínico o con la información proporcionada por el paciente y el psiquiatra tratante. Como primera elección se utilizará un tratamiento analgésico multimodal favoreciendo las técnicas regionales que son más efectivas en el control del dolor y con menos efectos adversos. Cuando no es factible realizarlas, se utilizarán opioides, restringiendo su uso a este episodio sin prolongar innecesariamente su empleo. No hay evidencia de que el uso de opioides para tratar el dolor agudo aumente el riesgo de recaída y es más probable que un dolor severo insuficientemente tratado sí lo haga. Es posible racionalizar su empleo a modo de una escala analgésica reversa al de la recomendada por la OMS permaneciendo en el 3er escalón (opioides potentes+ AINEs + coadyuvantes) un período corto de siete días y descender gradualmente hasta el 1er escalón en donde podrá permanecer por un tiempo más largo (17).
Dependiente de opioides en consumo activo no tratado o en terapia de mantenciónComo señalamos anteriormente, en la evaluación del paciente dependiente hay negación del problema adictivo y tendencia a ocultar datos por temor a ser subtratados, denunciados o estigmatizados. La entrevista debe realizarse conservando la confidencialidad, el respeto y una actitud receptiva. El equipo de salud debe considerar su condición como cualquier otra enfermedad y tener claro que el episodio de dolor o el procedimiento quirúrgico no son situaciones en que sea factible una suspensión del consumo o el inicio de un tratamiento de la dependencia. Recomendaciones y guías con objetivos definidos se han descrito para facilitar el tratamiento del dolor perioperatorio en dependientes de opioide (tabla 4). Éstas permiten tener un marco de referencia del manejo que facilita un adecuado tratamiento con menor riesgo y que también conecta al paciente con una alternativa para un posterior tratamiento de su enfermedad adictiva.
Guías para el manejo del dolor perioperatorio en pacientes dependientes de opioides
| Perioperatorio |
| 1. Evaluación: debe incluir un temprano reconocimiento o un alto índice de sospecha. |
| 2. Identificación: conocer datos tales como dosis basal o de mantención de opioides; eventos traumáticos o quirúrgicos que hayan resultado en un dolor mal controlado o en episodio de recaída. |
| 3. Consulta a especialistas: solicitar evaluación a psiquiatra que preste apoyo en el manejo perioperatorio. |
| 4. Entregar completa información al paciente, contestar preguntas y aclarar dudas respecto al control del dolor, ansiedad y riesgo de recaídas. |
| 5. Medicación: calcular la dosis de mantención de opioide y los modos de administración; administrar ansiolíticos y otros fármacos que estén indicados al caso. |
| Intraoperatorio |
| 1. Mantener la dosis basal de opioide (oral, transdérmica o intravenosa). |
| 2. Entregar una dosis incremental de acuerdo al requerimiento y la tolerancia en el período intraoperatorio y postoperatorio. |
| 3. Realizar bloqueo con anestésico local de tronco nervioso, plexo o neuroaxial según el caso. |
| 4. Utilizar analgésicos no opioides (AINEs) y coadyuvantes (ketamina, gabapentina). |
| Postoperatorio |
| 1. Planificar antes de la cirugía la analgesia postoperatoria: formular una estrategia primaria y alternativas factibles. |
| 2. Mantener dosis basal de opioide. |
| 3. Técnicas de Analgesia Multimodal. |
| 4. Analgesia controlada por paciente: utilizar como técnica primaria o suplementaria a técnicas regionales. |
| 5. Uso de opioides neuroaxialesvía intratecal o epidural. |
| 6. Bloqueo continuo de troncos nerviosos con anestésicos locales. |
| Manejo posterior al alta |
| 1. Si hay completo alivio del dolor después de la cirugía, el opioide debe ser reducido lentamente y en ningún caso en forma abrupta. |
| 2. Diseñar antes del alta, un plan de manejo de dolor en domicilio con dosis adecuadas de opioides y otra clase de analgésicos (AINEs, coadyuvantes). |
| 3. Antes del alta, concertar derivación del paciente hacia una unidad de dolor para su seguimiento y a un centro de salud mental para el manejo de su dependencia. |
Ref(8).
En condición de consumo activo o de terapia de mantención, se requiere conocer cuál es el opioide y la dosis diaria. Lo anterior con el objetivo de tener una referencia de la magnitud de la tolerancia y evitar el síndrome de abstinencia. Cuando la sustancia es obtenida por tráfico, habitualmente no es una droga pura y la estimación es poco exacta. En estos casos se optará por un manejo con titulación de dosis y vigilancia más estricta. El consumo de sustancias ilícitas hace siempre más difícil el manejo del dolor y no se puede intentar un tratamiento seguro sin el apoyo de un especialista de salud mental con manejo en adicciones. En el caso de pacientes en tratamiento por dependencia que están en fase de sustitución, con metadona o buprenorfina, es más fácil administrar la misma dosis como basal o hacer una rotación a otro opioide con el cálculo de equipotencia (tabla 5). En estos casos se recomienda mantener igual dosis o equipotente hasta antes de la cirugía o durante el episodio de dolor (14,19). Es muy importante tener claro que las dosis de mantención no confieren efecto analgésico, muy por el contrario está demostrado que por mecanismos de neuroplasticidad la exposición crónica a opioides induce hiperalgesia. Por este motivo si se necesita rotar el opioide debemos consultar una tabla de equipotencia (tablas 5 y 6) o consultar tablas disponibles en sitios de internet confiables (14). Se debe considerar que la tolerancia cruzada no es completa por lo que se dará una dosis 30 a 50% menor a la de mantención. En suma, en todos los casos en que hay consumo actual, éste no se debe interrumpir frente a un episodio de dolor agudo o frente a la realización de una cirugía electiva.
Conversión de parches de administración transdérmica de opioides
| Buprenorfina TD | 35mcghr | 52,5 mcg/hr | 105 mcg/hr |
| Fentanilo TD | - | 25 mcg/hr | 50 mcg/hr |
| Morfina VO/24 hr | 60mg | 90mg | 180mg |
| Morfina IV/24hr | 20mg | 30mg | 60mg |
Conversiones referenciales en valores aproximados extraídos y adaptados de diferentes fuentes. TD: transdérmico / VO/24 hr: dosis diaria vía oral / IV/24 hr: dosis diaria vía intravenosa.
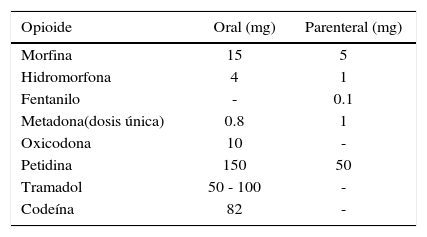
Conversión de opioides dosis equianalgésicas
| Opioide | Oral (mg) | Parenteral (mg) |
|---|---|---|
| Morfina | 15 | 5 |
| Hidromorfona | 4 | 1 |
| Fentanilo | - | 0.1 |
| Metadona(dosis única) | 0.8 | 1 |
| Oxicodona | 10 | - |
| Petidina | 150 | 50 |
| Tramadol | 50 - 100 | - |
| Codeína | 82 | - |
Opioids in Medicine: A Comprehensive Review on the Mode of Action and the Use ofAnalgesics in Different Clinical Pain States. 2008 Springer Science Business Media(18).
Como fue mencionado anteriormente, la dependencia de sustancias posee mecanismos fisiopatológicos similares para las diferentes drogas, ya que todas tienen efectos negativos en el sistema de recompensa mesocorticolímbico (4,6,7). No obstante, se producen diferencias en el patrón de consumo, en los síndromes de intoxicación y de abstinencia. Con sustancias ilícitas es más difícil que el paciente aporte el antecedente y tampoco es posible realizar pruebas de orina, sangre o pelo sin su autorización. Por lo tanto, en estos casos será indispensable contar con el apoyo de un psiquiatra que pueda obtener información, prevenir el síndrome de abstinencia y continuar con el seguimiento para detectar posibles complicaciones asociadas al uso de opioides. En todos estos casos se realizará un manejo del dolor general como el que fue descrito más arriba y ante la necesidad de utilización de opioides se recomienda aportar esquemas iguales a la población general. Durante el manejo del dolor agudo es posible que el paciente intente tratar síntomas de abstinencia con la sobre utilización de bolos de morfina u otro opioide. Ante esta sospecha se debe estar muy seguro de que el dolor está siendo bien tratado y por otro lado, informar al psiquiatra para evaluación de esta situación. En estos casos también es recomendable no prolongar más allá de lo necesario el uso de opioides potentesy optimizar un manejo multimodal del dolor.
Recomendaciones en el uso de opioides para tratamiento de dolor agudo en sujetos dependientes- 1.
Es preferible la administración por horario o de forma continua más que de rescate o PRN. Se debe hacer una estimación de la analgesia basal requerida la que se sumará a la dosis de mantención. Se puede agregar una dosis mayor del mismo opioide u otro alternativo en dosis equianalgésica (tabla 6). La magnitud de este suplemento dependerá de cuánto es necesario para lograr alivio del dolory deberá ser limitado sólo por el riesgo de complicaciones (depresión respiratoria y sedación). Por ejemplo en un paciente que está en terapia de su adicción con buprenorfina transdérmica de sustitución, sometido a una cirugía, podría requerir morfina en infusión continua para el dolor de reposo y bolos de rescate para el dolor incidental.
- 2.
Se recomienda hacer rotación de opioides cuando no es posible controlar el dolor al subir la dosis del mismo fármaco. Se realiza sustituyendo con otro opioide en dosis equianalgésicas (tablas 5 y 6) pero considerando que la tolerancia cruzada no es completa. Así la dosis a administrar debe ser 30 a 50% inferior a la dosis equipotente del nuevo opioide. Debe ser un opioide de acción prolongada, liberación sostenida o administrada por sistemas de infusión continua para evitar la aparición de síntomas de abstinencia. La metadona, debido a su efecto sobre el receptor NMDA, es una buena alternativa de rotación cuando la morfina es insuficiente para controlar el dolor en el paciente opioide dependiente. No obstante, la metadona no sigue un curso lineal en dosis equianalgésicas y cuando se requieren sustituir altas dosis diarias de morfina puede ocurrir toxicidad si no se hace una rotación gradual (13).
- 3.
Las bombas de administración intravenosa de morfina controladas por el paciente (PCA) son una alternativa rápida para titular la dosis necesaria y aliviar adecuadamente el dolor. Tienen la ventaja de mantener niveles estables de opioide, proporcionando analgesia y evitando síntomas de abstinencia. Además le dan seguridad al paciente ya que es él quien controla el tratamiento del dolor. No obstante, la desventaja es que el paciente dependiente requiere dosis de mantención y bolos sustancialmente mayores que el resto por lo que pueden ser calificados como conductas aberrantes por el equipo de salud. Otro inconveniente puede ser que la utilización de los bolos sea para tratar síntomas psicológicos (ansiedad, insomnio) y no alivio del dolor. Por todo lo mencionado es recomendable dar adecuada analgesia por medio de una infusión basal, configurar bolos de mayor dosis de lo habitual y con períodos de bloqueo más cortos.
- 4.
Cuando un opioide de administración transdérmica ha sido suspendido y se quiere reiniciar, pueden ser necesarias unas 12 horas desde la aplicación del parche para alcanzar niveles en sangre efectivos. Por lo anterior se recomienda mantener un opioide de corta duración hasta establecer una adecuado efecto del opioide transdérmico y tener como referencia de dosis la equipotencia (tabla 6).
El médico que está cargo del paciente o el que está manejando el dolor tiene la responsabilidad de solicitar la evaluación de un especialista en tratamiento de adicciones desde el momento en que se obtiene el antecedente de dependencia, consumo o si existe una sospecha fundada. Aunque no es el objetivo de este artículo profundizar en este aspecto del tratamiento, es necesario tener presente las consideraciones
Seguimiento y signos de alertaUna vez que la causa de dolor agudo ha cesado o la intensidad de dolor ha disminuido es necesario realizar la interrupción del opioide usado como analgésico. Lo esperable es que este paso no presente ninguna dificultad si su uso ha sido de corta duración y si el paciente dependiente ha reiniciado su terapia de mantención. En caso que exista imperiosa solicitud del paciente por seguir con la analgesia con opioides, lo primero es descartar una complicación quirúrgica o la persistencia de la causa del dolor. De no haber causa se recomienda hacer una retirada gradual y reglada de la analgesia a modo de escala analgésica reversa (16), asegurando que la terapia de sustitución sea la adecuada y que el paciente está siendo evaluado por su psiquiatra a cargo. En este período pueden aparecer comportamientos aberrantes similares a los descritos por Chabal (10) en dolor crónico benigno tratados con opioides (tabla 1). Estos comportamientos aberrantes son señal de alerta y su presencia debe obligar a la derivación a su psiquiatra tratante.
ConclusionesEl tratamiento del dolor agudo en el paciente dependiente de sustancias representa para el equipo de salud un manejo más complejo que el de la población general. En ellos hay cambios farmacocinéticos y farmacodinámicos producto de neuroadaptación, por internalización y desensibilización de receptores opioides; por alteraciones de segundos mensajeros intracelulares; y por la neuroplasticidad adaptativa que genera cambios de neurocircuitos a largo plazo. Entender la fisiopatología de la dependencia permite detectar precozmente conductas patológicas de búsqueda de consumo y las situaciones que aumentan el riesgo de producir una recaída en el paciente dependiente.
Estas nociones han permitido tratar en forma eficaz el dolor en el paciente adicto a sustancias. Por un lado está la analgesia multimodal compuesta por técnicas de bloqueo locoregional con anestésicos locales, uso de AINEs y coadyuvantes. Por otro lado estudios publicados, recomendaciones de expertos y guías clínicas preconizan que es posible utilizar opioides en dolor agudo con un riesgo bajo para el paciente dependiente. Lo anterior se logra diseñando un esquema individualizado que considere primero una dosis de mantención de opioides, equivalente al consumo previo o alternativamente hacer rotación de opioide. Simultáneamente, prescribir una analgesia opiácea de entrega continua para el dolor basal, con la posibilidad de rescates autoadministrados para el dolor incidental mediante el uso bombas de analgesia controlada por paciente. No obstante, para ello es necesario contar con un equipo de tratamiento organizado de dolor y con la posibilidad de ser apoyados por especialistas en tratamiento de pacientes adictos cuando se reconozcan situaciones riesgosas para el sujeto.
Finalmente debemos considerar que un dolor agudo severo insuficientemente tratado puede llegar a ser persistente o cronificarse, lo que en el paciente dependiente constituye un riesgo más alto que el uso racional de opioides para tratarlo.
El autor declara no tener conflictos de interés, con relación a este artículo.