En el tratamiento de la transposición de grandes arterias con septo interventricular íntegro (d-TGA/SI) clásicamente se ha asociado la realización de un switch arterial después de las 2-3 primeras semanas de vida, con mayor incidencia de disfunción ventricular izquierda y aumento de la mortalidad, debido a la bajada de las resistencias vasculares pulmonares y, por tanto, a la pérdida de la geometría del ventrículo izquierdo (VI).
Presentamos el caso de un paciente con diagnóstico tardío de d-TGA/SI al que se le realiza switch arterial primario en la 10.a semana de vida, pese a criterios de pérdida de la geometría del VI. Evolución inicial con disfunción ventricular severa, que evoluciona favorablemente en días posteriores, hasta la recuperación completa de la fracción de eyección ventricular izquierda.
Aprovechamos el caso para hacer una revisión de las diferentes series publicadas y elaborar un protocolo de actuación.
In the treatment of transposition of the great arteries with intact ventricular septum (d-TGA/IVS) the arterial switch operation after the first 2-3 weeks of life has traditionally been associated with a higher incidence of left ventricular dysfunction and increased mortality due to the decrease in pulmonary vascular resistance, and therefore to the loss of geometry of the left ventricle (LV).
The case is presented of a patient with a late diagnosis of d-TGA/IVS in whom a primary arterial switch is performed in the 10th week of life, despite the loss of LV geometry. Initial course with severe ventricular dysfunction and progressive improvement on subsequent days until complete recovery of left ventricular ejection fraction.
The case is used in order to present a review of the literature and develop a protocol.
En el tratamiento de la transposición de grandes arterias con septo interventricular íntegro (d-TGA/SI) clásicamente se ha asociado la realización de un switch arterial después de las 2-3 primeras semanas de vida, con mayor incidencia de disfunción ventricular izquierda y aumento de la mortalidad, debido a la bajada de las resistencias vasculares pulmonares y, por tanto, a la pérdida de la geometría del ventrículo izquierdo (VI).
CasoPresentamos el caso de una paciente de 6 semanas de vida referida a nuestro centro, donde se realiza el diagnóstico de d-TGA/SI con comunicación interauricular (CIA) restrictiva y ductus pequeño. Se inicia tratamiento con prostaglandinas y se realiza auriculoseptostomía de Rashkind, eficaz.
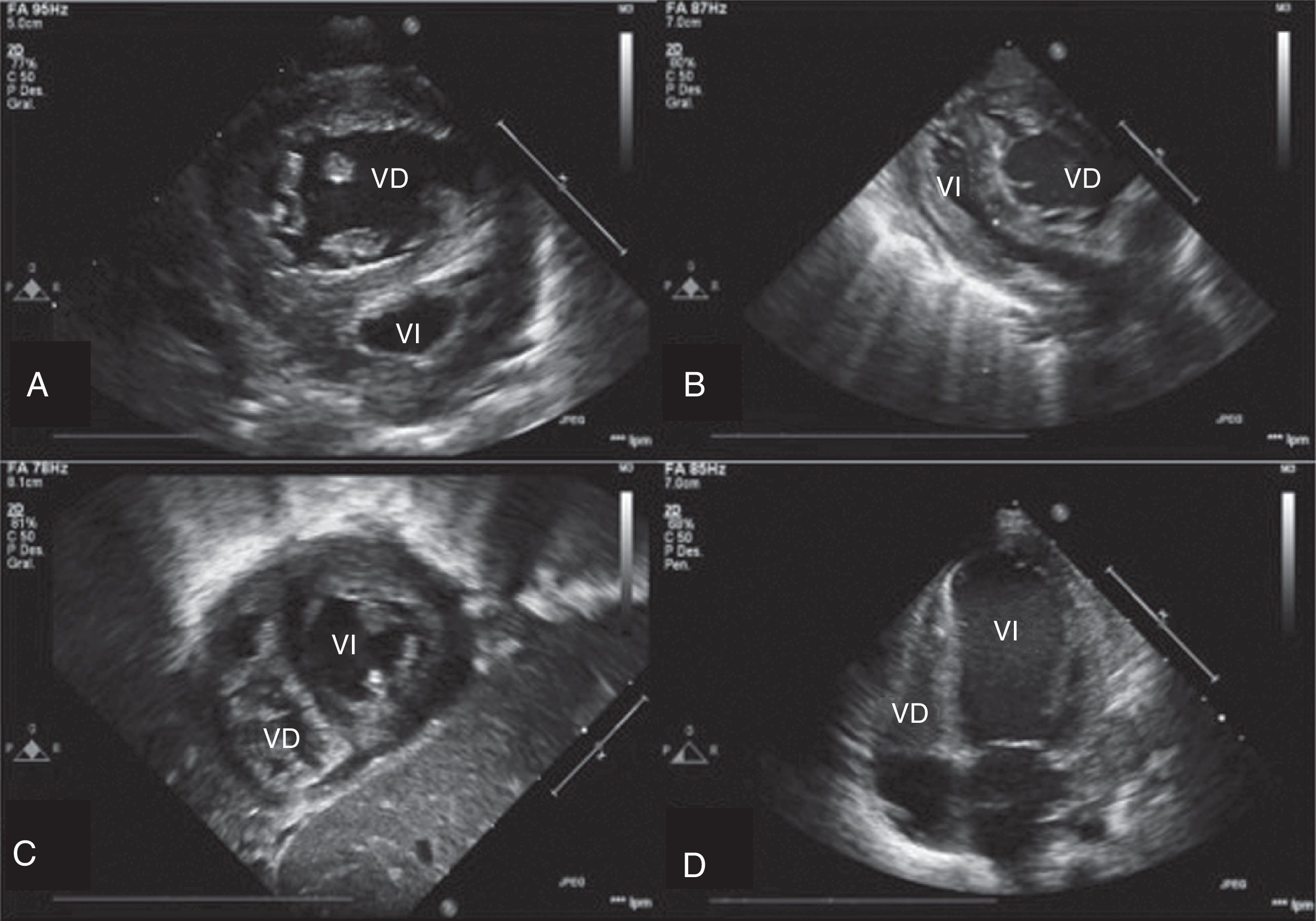
El ecocardiograma-Doppler al ingreso muestra evidencias de regresión del VI; tabique interventricular tipo iii (abombando hacia el VI valorado en plano paraesternal eje corto) y las siguientes medidas indexadas por superficie corporal: masa ventricular izquierda: 15,7g/m2: volumen VI: 11,9ml/m2; relación masa/volumen: 1,3 (fig. 1A yB, vídeos 1 y 2 disponibles en el material adicional de la versión electrónica del artículo).
A) Paraesternal eje corto prequirúrgico. Aumento de presión en el VD. Tabique interventricular tipo iii. B) Paraesternal eje largo prequirúrgico. VI colapsado. C) Subcostal corto posquirúrgico. Morfología normal del VI. D) Apical 4 cámaras posquirúrgico con disfunción VI severa.VD: ventrículo derecho; VI: ventrículo izquierdo.
Se decide posponer la cirugía de switch arterial por infarto en territorio de la cerebral media izquierda y enterocolitis necrotizante objetivadas al ingreso.
Por episodios de desaturación extrema y sospecha de mezcla insuficiente a nivel auricular se decide realizar atrioseptostomía quirúrgica bajo circulación extracorpórea.
Se decidió no realizar la reparación en este momento por el riesgo de empeoramiento de los cuadros de infarto cerebral y enterocolitis necrotizante durante una circulación extracorpórea más prolongada y la posibilidad de necesidad de ECMO en el postoperatorio, cuya anticoagulación podría generar una conversión hemorrágica del infarto cerebral. Se valoró, además, la realización de un banding de la arteria pulmonar para preparar el VI, desestimada por la inestabilidad hemodinámica de la paciente con hipoxemia marcada.
En la evolución presenta cuadro de sepsis con trombocitopenia severa, que demora la reparación hasta la 10.ª semana de vida. Tras la mejoría del mismo, se decide realizar switch arterial primario, inicialmente bien tolerado. A su llegada a cuidados intensivos se objetiva disfunción ventricular izquierda grave en el ecocardiograma (vídeo 3 disponible en el material adicional de la versión electrónica del artículo). Se inicia ciclo de levosimendán con mejoría clínica y ecocardiográfica progresiva hasta la normalización de la fracción de eyección ventricular izquierda (fig. 1C y D; vídeos 4 y 5 disponibles en el material adicional de la versión electrónica del artículo), que permite realizar el cierre de tórax diferido el tercer día postoperatorio. Es extubada al octavo día postoperatorio. La evolución posterior, tanto en cuidados intensivos como en planta de hospitalización, es buena, no presentando complicaciones y permitiendo el alta domiciliaria 3 semanas después de la cirugía reparadora.
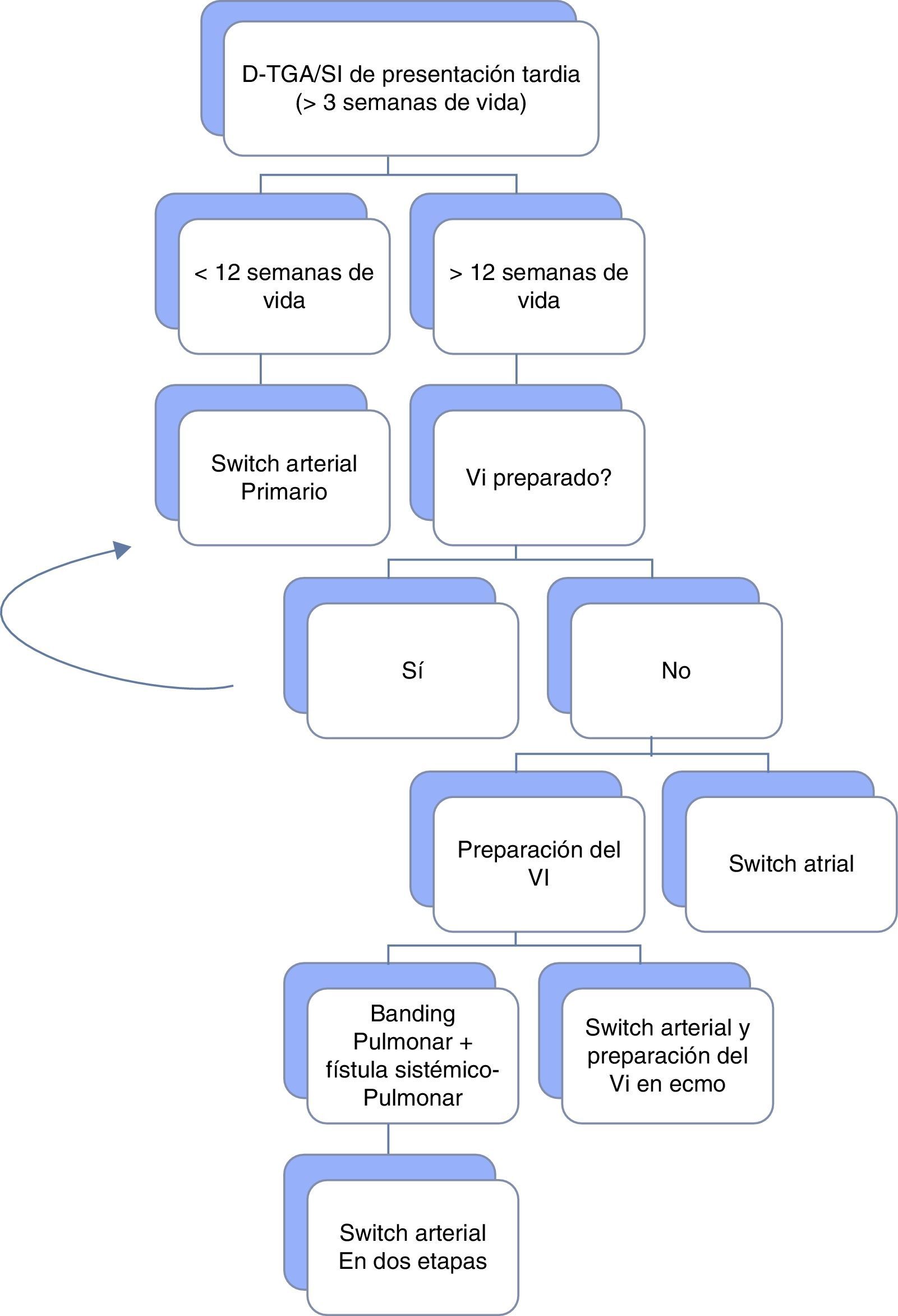
DiscusiónNuestra intención es realizar una revisión de los protocolos de actuación en el caso de una d-TGA/SI de presentación tardía, a propósito del caso (fig. 2).
Para definir la preparación del VI existen una serie de criterios1, tales como el tipo de tabique interventricular en el plano paraesternal eje corto, la ratio de presiones entre ambos ventrículos, la masa indexada de VI>35g/m2 o la ratio masa indexada de VI/volumen indexado de VI>1,5.
Existe controversia de si a partir de las 3 primeras semanas de vida es necesario preparar el VI cuando haya evidencia de regresión de la geometría del mismo.
El mantenimiento de la geometría del VI más allá de las 3 primeras semanas de vida depende de: la existencia de un ductus arterioso permeable, el tamaño de la CIA, la existencia de una obstrucción al tracto de salida del VI y la persistencia de presiones pulmonares elevadas1.
Existen varios trabajos que apoyan la realización de un switch arterial primario en d-TGA/SI hasta la edad de 3 meses, independientemente de la geometría del VI2-5.
Además, Lev etal.6, en un estudio post mórtem en d-TGA/IVS en 61 pacientes demostró que el grosor del VI se mantiene al menos hasta los 2 meses.
Por encima de esta edad, existe escasa evidencia pero parece segura la necesidad de realizar preparación del VI, ya sea mediante banding de la arteria pulmonar7 o mediante el uso de ECMO postoperatoria.
Por otra parte, existe controversia en el caso del banding en cuanto al tiempo interestadio hasta la realización del switch arterial, si es necesario realizar una fístula sistémico-pulmonar asociada, y si aumenta el riesgo de insuficiencia aórtica y disfunción del VI tardía.
En cuanto al tiempo interestadio, se ha demostrado que la mayor tasa de crecimiento de la masa del VI se produce en las primeras 48 h post-banding, y que llega a ser el doble aproximadamente al séptimo día8. Además, existen series con tiempo interestadio de 7-10 días y con excelentes resultados en cuanto a tasa de insuficiencia aórtica y disfunción del VI1,9, por lo cual no se justifican tiempos interestadio prolongados.
También segura parece la asociación de una fístula sistémico-pulmonar en el momento del banding, no solo por el riesgo de hipoxemia1, sino también porque produce una sobrecarga de volumen del VI10.
Como conclusión, la edad límite para realizar switch arterial primario no está bien definida, pero parece que hasta las 12 semanas de vida existe algún mecanismo (¿reserva miocárdica?) por el cual el VI responde de forma adecuada en posición sistémica, aunque preoperatoriamente se encuentre desentrenado. Basándonos en los estudios más numerosos, como el de Kang et al.2, Sarris et al.3, Bisoi et al.5 y el metaanálisis de Edwin et al.4, aconsejamos realizar por debajo de los 3 meses de edad switch arterial primario utilizando la ECMO para la preparación del VI, en caso de ser necesario.
La realización de un banding puede ser una opción igualmente válida, siempre que se realice con una duración corta y asociando una fístula sistémico-pulmonar, ya que ha presentado mejores resultados en cuanto a mortalidad, la tasa de insuficiencia aórtica y la disfunción ventricular1.
Por encima de los 3 meses de edad, la tasa de disfunción del VI es significativamente mayor, fundamentalmente en aquellos en los que existe evidencia de regresión del VI. En estos casos tenemos 3 posibilidades: 1) la preparación del VI mediante banding; 2) mediante el uso de ECMO postoperatorio, y 3) la realización de un switch auricular, opción a tener en cuenta, especialmente si existe evidencia de regresión de la geometría del VI2, y cuando la edad de presentación se encuentra por encima de los 6 meses.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.