La hipercolesterolemia familiar (HF) es el trastorno genético más prevalente en edad pediátrica; sin embargo, en la inmensa mayoría de los casos pasa totalmente desapercibida. La elevación del colesterol ligado a las lipoproteínas de baja densidad presente desde el nacimiento comportará el desarrollo silente de arteriosclerosis de forma precoz. Este hecho podrá manifestarse en forma de enfermedad coronaria antes de los 20 años en la HF homocigota o en la edad media de la vida en la HF heterocigota. A pesar de las evidencias científicas, no existe un acuerdo común de cómo y cuándo se debe hacer el cribado, hecho que se pone de manifiesto al revisar las diferentes guías de consenso de expertos. La historia familiar de enfermedad cardiovascular prematura, junto con la presencia de hipercolesterolemia en uno de los progenitores, es crucial en la detección y el diagnóstico. Alcanzar los objetivos terapéuticos desde edades tempranas es un elemento clave en el pronóstico, aunque sigue siendo un tema de amplio debate. El primer eslabón del tratamiento siempre serán las recomendaciones de hábitos de vida cardiosaludables. En la actualidad, existe controversia sobre a qué edad se debe iniciar el tratamiento farmacológico, siendo las estatinas el fármaco de primera elección. En este artículo se revisan las recomendaciones actuales de las guías de consenso de expertos en el manejo del niño y adolescente con HF, así como las nuevas terapias emergentes.
Familial hypercholesterolemia (FH) is the most common genetic disorder in childhood, but in most cases is not detected. High levels of low-density lipoprotein cholesterol are present since the child's birth and this fact will suppose silent development of early atherosclerosis. In cases of homozygous FH, the coronary disease will appear before 20s and in cases of heterozygous FH will occur in middle age. Despite published data, there is not agreement about how and when perform the screening. Familial history of early cardiovascular disease plus presence of hypercholesterolemia in parents is crucial for detection and diagnosis. Actually, it is topic of discussion that it is necessary to achieve therapeutic goals from an early age to improve prognosis. Lifestyle changes are the first line therapy. Statins are the lipid-lowering drugs of choice but the optimal age to start therapy it is still controversial. In this article, current recommendations of expert consensus guidelines about the management and new line therapies of child and adolescents are reviewed.
La hipercolesterolemia familiar (HF) es un trastorno genético autosómico dominante, lo que significa que se transmite al 50% de la descendencia. Está causada mayoritariamente por mutaciones en el gen que codifica el receptor de las lipoproteínas de baja densidad. En la actualidad, se han descrito más de 1.700 mutaciones diferentes en este gen, representando más del 90% de todos los casos de HF. En menor proporción, se han descrito defectos en el gen que codifica la apolipoproteína B (ApoB) y en el gen que codifica la proprotein convertase subtilisin-kexin type 9 (PCSK9), representando aproximadamente el 5 y el 1%, respectivamente. Se expresan clínicamente de la misma forma y solo el estudio genético nos permitirá diferenciarlas. Sin embargo, en la actualidad, en entre el 5-30% de los casos con fenotipo de HF no es posible identificar el gen causante de esta enfermedad1.
Existen 2 formas de HF, la heterocigota (HFHe), siendo el trastorno hereditario más frecuente con una prevalencia de 1/250-500 individuos, y la forma homocigota (HFHo), con una prevalencia de 1/160.000-300.000 individuos según los últimos datos publicados en población europea2,3. Zamora et al. han analizado los registros electrónicos de 2.764.917 pacientes de Cataluña mediante la metodología Big Data. Utilizando el punto de corte del colesterol ligado a lipoproteínas de baja densidad (c-LDL), descrito previamente en población española, se detectaron 14.274 con fenotipo compatible con HF. Estos datos nos indican una prevalencia de HFHe de 1/256 sujetos en población española4. Sánchez ha comunicado una prevalencia de HFHo de 1/495.000 sujetos tras analizar los 16.744 estudios genéticos realizados en España durante el periodo comprendido entre 1996 y 20155.
Se calcula que en Europa, la cifra de afectos se eleva a unos 4,5 millones, de los cuales el 20-25% son niños y adolescentes. Es un problema de máxima relevancia clínica el hecho de que menos del 10% estén diagnosticados. En países con programas intensivos de cribado genético, como Holanda, se alcanzan porcentajes de detección superiores al 70%. En España la tasa de pacientes con HF a los que se ha estudiado y diagnosticado genéticamente se situaría alrededor del 6%6. Los individuos afectos de HF tienen 100 veces más posibilidades de desarrollar enfermedad cardiovascular prematura (ECVP) que los no afectos7. Se calcula que el 85% de los hombres y el 50% de las mujeres presentarán algún episodio coronario antes de los 65 años de vida si no reciben un tratamiento adecuado8. Los niños con HFHo presentan un elevado riesgo, desarrollando enfermedad coronaria antes de los 20 años si no son tratados intensamente2,9. Por ello, el diagnóstico y el tratamiento precoz son importantes para su pronóstico y evolución a largo plazo.
Los pacientes afectos de HF presentan elevadas concentraciones plasmáticas de c-LDL que pueden detectarse ya desde el nacimiento. Los niños con HFHe tienen niveles de c-LDL 3 veces más altos que los no afectos10 y podría manifestarse como enfermedad coronaria prematura en la edad adulta2.
A pesar de todo ello, no existe ninguna expresividad clínica durante la infancia, siendo necesario el diseño y aplicación de diferentes estrategias para su detección. Los criterios clínicos del Dutch Lipid Clinic Network no son aplicables a menores de 18 años11. En los niños, la sospecha diagnóstica deberá establecerse con base en los niveles elevados de c-LDL, la historia familiar de hipercolesterolemia y/o de ECVP.
En la actualidad, se considera que la edad ideal para su detección es entre los 8-10 años, ya que es la edad de máxima discriminación. Durante la adolescencia los valores de colesterol total (CT) y de c-LDL descienden entre un 10 y un 20%, lo que convierte esta época de la vida en menos sensible para la realización de cribado12,13. Recientemente, Eissa et al. han comunicado que el perfil lipídico varía considerablemente en función de la etapa del desarrollo puberal. Plantean que debería considerarse en el momento de indicar el cribado14. Pang et al. estudiaron a 1.602 adolescentes sanos entre 14 y 17 años, definiendo la HF en función de los niveles de c-LDL junto con la historia familiar de hipercolesterolemia y/o de ECVP. La prevalencia de HF fue de 1/267 adolescentes, destacando la ausencia de ECVP en los padres, pero su presencia en los abuelos15.
Se han publicado diversos estudios en los que se ha observado que el grosor íntima-media de la carótida de niños con fenotipo de HF es superior si lo comparamos con el de niños normolipémicos, estando relacionado directamente con los niveles de c-LDL. Esta diferencia significativa del grosor íntima-media carotídeo fue observada en niños a partir de los 7 años2. También se ha observado que hay presencia de calcificaciones coronarias en el 25% de los niños de 11-23 años afectados de HFHe y especialmente en la arteria aorta en la mayoría de los adolescentes con HFHo.
La detección de la HF en la población infantil sigue siendo un gran reto, ya que la inmensa mayoría no son diagnosticados, lo que conlleva un retraso en el inicio del tratamiento, tanto de cambios de estilo de vida como farmacológico, hecho que puede contribuir a elevar el riesgo coronario de esta población en la edad media de la vida.
El punto de corte de c-LDL, la edad de realización o los criterios de sospecha de afectación de un progenitor son en la actualidad motivo de controversia, por lo que en esta revisión se describen diferentes estrategias de cribado para mejorar la detección y el diagnóstico de los niños con HF. A su vez, esta revisión incluye una actualización de las recomendaciones de cambios de estilo de vida y de tratamiento farmacológico.
Niño y adolescente con hipercolesterolemia familiarPor qué hacer el cribadoEl cribado en la infancia y adolescencia está plenamente justificado:
- -
La hipercolesterolemia incrementa el riesgo de acelerar el desarrollo de la arteriosclerosis y, consecuentemente, de ECVP.
- -
El cribado puede identificar a esta población de alto riesgo.
- -
En la actualidad disponemos de terapias farmacológicas efectivas y seguras que pueden enlentecer o incluso revertir la arteriosclerosis y disminuir el riesgo cardiovascular (CV) de estos niños.
En la realidad actual, a pesar de las evidencias, no existe un consenso único. Si comparamos las estrategias recomendadas entre continentes podemos observar diferencias entre ellas e incluso existen desemejanzas entre países europeos7.
Tipos de estrategias de cribadoExisten diferentes estrategias, no excluyentes entre sí, para el diagnóstico de casos nuevos entre la población pediátrica.
Cribado universal: consiste en la determinación de los niveles de CT de forma rutinaria a los niños en una edad concreta. Se ha demostrado que este método permite detectar el 90% de los niños con HF entre 1-9 años con una ratio de falsos positivos<1%16. Un ejemplo de este tipo de cribado es el que se aplicó en Eslovenia a la edad de 5 años17.
En su defecto, se recomienda el cribado oportunista, es decir, la inclusión de la determinación de CT en cualquier estudio analítico que el pediatra indique entre los 2 y los 9 años.
Cribado selectivo: consiste en la determinación de los niveles de CT en los niños con historia familiar de ECVP o bien con historia familiar de hipercolesterolemia en alguno de los progenitores. Este tipo de cribado fue recomendado por el primer panel de expertos en pediatría, el National Cholesterol Education Program17, por la American Heart Association18 y la American Academy of Pediatrics19. Sin embargo, se ha visto que al aplicar este cribado, entre el 30 y el 60% de los niños afectos de HF no son detectados.
Cribado en cascada directa: si conocemos la mutación causal de la HF del progenitor se extiende el estudio genético a los familiares de primer grado, incluyendo a los niños. Este tipo de cribado genético tiene el 100% de sensibilidad y especificidad en el estudio de los familiares, recomendándose por ser la mejor técnica por su coste-efectividad. Un ejemplo claro de este tipo de cribado es el que se realizó en Holanda desde 1994 hasta finales de 201420,21. En el Reino Unido se recomienda realizar el test genético en el individuo adulto y extender la cascada en los niños a partir de los 10 años7.
En España, en el estudio SAFEHEART a partir de 768 casos índices se detectaron un total de 1.984 familiares nuevos con HF. Los autores destacan que a pesar de ser un trastorno hereditario, el 25% de los familiares detectados desconocían ser portadores de la enfermedad y el 20% no recibía tratamiento22.
Datos de Oliva et al. indican que el cribado familiar en cascada con estudio genético y tratamiento posterior con estatinas es coste-efectivo23.
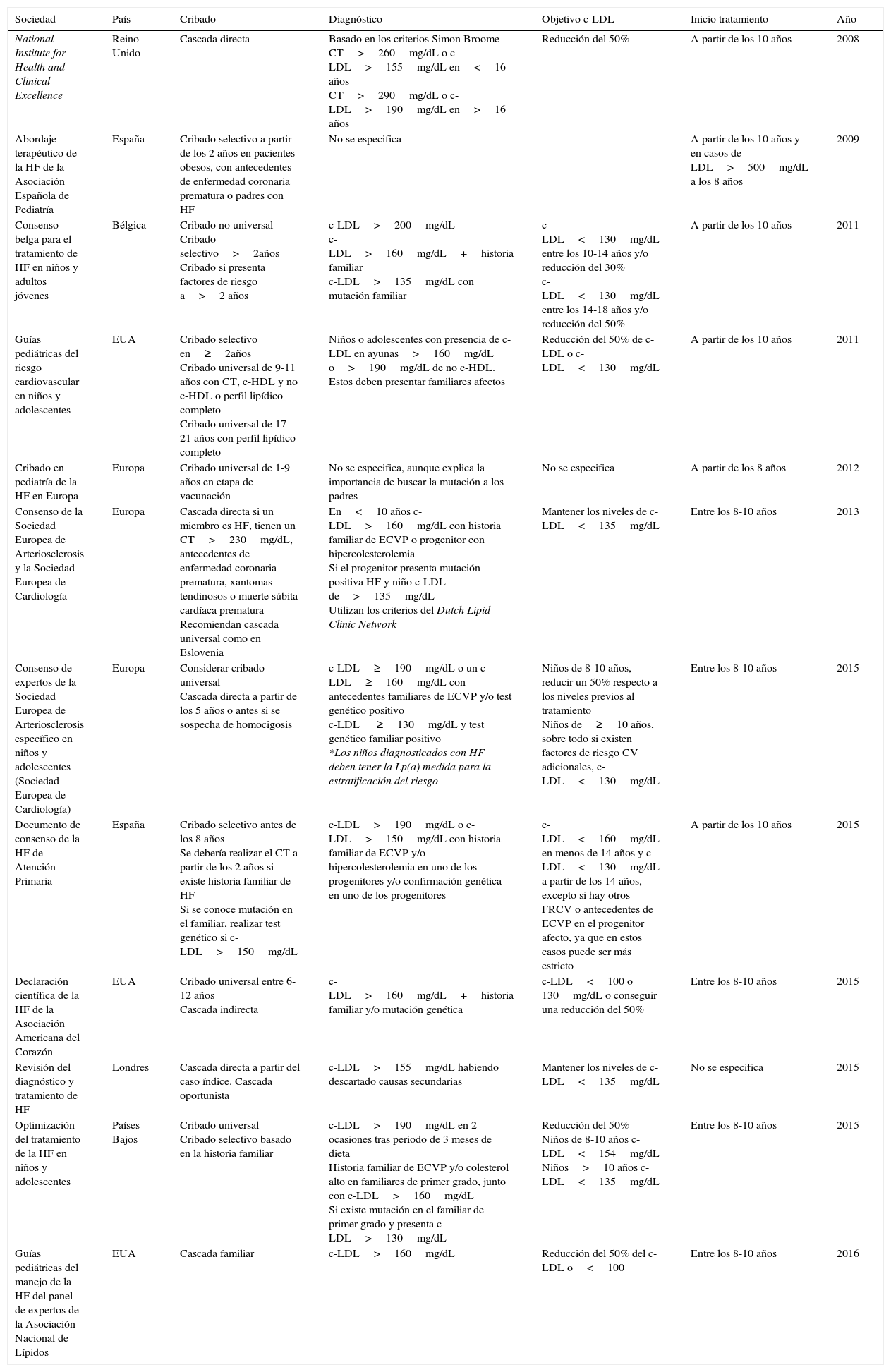
Cribado en cascada inversa: a partir de la detección de hipercolesterolemia en el niño se inicia el estudio de los progenitores. Si uno de estos presenta una puntuación≥6 en los criterios clínicos del Dutch Lipid Clinic Network, se solicitará el estudio genético. Si se detecta la mutación se realizará el estudio genético en el niño. En cambio, si el resultado ha sido negativo, no se realizará en el niño, pero podrá ser diagnosticado de HF si los niveles de c-LDL están por encima del percentil 95. Diferentes guías recomiendan hacer este tipo de cribado, pero en la práctica clínica está infrautilizado. En la tabla 1 podemos ver una actualización de las diferentes guías y el tipo de cribado que recomiendan.
Resumen de las principales guías sobre hipercolesterolemia familiar en la infancia y la adolescencia
| Sociedad | País | Cribado | Diagnóstico | Objetivo c-LDL | Inicio tratamiento | Año |
|---|---|---|---|---|---|---|
| National Institute for Health and Clinical Excellence | Reino Unido | Cascada directa | Basado en los criterios Simon Broome CT>260mg/dL o c-LDL>155mg/dL en<16 años CT>290mg/dL o c-LDL>190mg/dL en>16 años | Reducción del 50% | A partir de los 10 años | 2008 |
| Abordaje terapéutico de la HF de la Asociación Española de Pediatría | España | Cribado selectivo a partir de los 2 años en pacientes obesos, con antecedentes de enfermedad coronaria prematura o padres con HF | No se especifica | A partir de los 10 años y en casos de LDL>500mg/dL a los 8 años | 2009 | |
| Consenso belga para el tratamiento de HF en niños y adultos jóvenes | Bélgica | Cribado no universal Cribado selectivo>2años Cribado si presenta factores de riesgo a>2 años | c-LDL>200mg/dL c-LDL>160mg/dL+historia familiar c-LDL>135mg/dL con mutación familiar | c-LDL<130mg/dL entre los 10-14 años y/o reducción del 30% c-LDL<130mg/dL entre los 14-18 años y/o reducción del 50% | A partir de los 10 años | 2011 |
| Guías pediátricas del riesgo cardiovascular en niños y adolescentes | EUA | Cribado selectivo en≥2años Cribado universal de 9-11 años con CT, c-HDL y no c-HDL o perfil lipídico completo Cribado universal de 17-21 años con perfil lipídico completo | Niños o adolescentes con presencia de c-LDL en ayunas>160mg/dL o>190mg/dL de no c-HDL. Estos deben presentar familiares afectos | Reducción del 50% de c-LDL o c-LDL<130mg/dL | A partir de los 10 años | 2011 |
| Cribado en pediatría de la HF en Europa | Europa | Cribado universal de 1-9 años en etapa de vacunación | No se especifica, aunque explica la importancia de buscar la mutación a los padres | No se especifica | A partir de los 8 años | 2012 |
| Consenso de la Sociedad Europea de Arteriosclerosis y la Sociedad Europea de Cardiología | Europa | Cascada directa si un miembro es HF, tienen un CT>230mg/dL, antecedentes de enfermedad coronaria prematura, xantomas tendinosos o muerte súbita cardíaca prematura Recomiendan cascada universal como en Eslovenia | En<10 años c-LDL>160mg/dL con historia familiar de ECVP o progenitor con hipercolesterolemia Si el progenitor presenta mutación positiva HF y niño c-LDL de>135mg/dL Utilizan los criterios del Dutch Lipid Clinic Network | Mantener los niveles de c-LDL<135mg/dL | Entre los 8-10 años | 2013 |
| Consenso de expertos de la Sociedad Europea de Arteriosclerosis específico en niños y adolescentes (Sociedad Europea de Cardiología) | Europa | Considerar cribado universal Cascada directa a partir de los 5 años o antes si se sospecha de homocigosis | c-LDL≥190mg/dL o un c-LDL≥160mg/dL con antecedentes familiares de ECVP y/o test genético positivo c-LDL ≥130mg/dL y test genético familiar positivo *Los niños diagnosticados con HF deben tener la Lp(a) medida para la estratificación del riesgo | Niños de 8-10 años, reducir un 50% respecto a los niveles previos al tratamiento Niños de≥10 años, sobre todo si existen factores de riesgo CV adicionales, c-LDL<130mg/dL | Entre los 8-10 años | 2015 |
| Documento de consenso de la HF de Atención Primaria | España | Cribado selectivo antes de los 8 años Se debería realizar el CT a partir de los 2 años si existe historia familiar de HF Si se conoce mutación en el familiar, realizar test genético si c-LDL>150mg/dL | c-LDL>190mg/dL o c-LDL>150mg/dL con historia familiar de ECVP y/o hipercolesterolemia en uno de los progenitores y/o confirmación genética en uno de los progenitores | c-LDL<160mg/dL en menos de 14 años y c-LDL<130mg/dL a partir de los 14 años, excepto si hay otros FRCV o antecedentes de ECVP en el progenitor afecto, ya que en estos casos puede ser más estricto | A partir de los 10 años | 2015 |
| Declaración científica de la HF de la Asociación Americana del Corazón | EUA | Cribado universal entre 6-12 años Cascada indirecta | c-LDL>160mg/dL+historia familiar y/o mutación genética | c-LDL<100 o 130mg/dL o conseguir una reducción del 50% | Entre los 8-10 años | 2015 |
| Revisión del diagnóstico y tratamiento de HF | Londres | Cascada directa a partir del caso índice. Cascada oportunista | c-LDL>155mg/dL habiendo descartado causas secundarias | Mantener los niveles de c-LDL<135mg/dL | No se especifica | 2015 |
| Optimización del tratamiento de la HF en niños y adolescentes | Países Bajos | Cribado universal Cribado selectivo basado en la historia familiar | c-LDL>190mg/dL en 2 ocasiones tras periodo de 3 meses de dieta Historia familiar de ECVP y/o colesterol alto en familiares de primer grado, junto con c-LDL>160mg/dL Si existe mutación en el familiar de primer grado y presenta c-LDL>130mg/dL | Reducción del 50% Niños de 8-10 años c-LDL<154mg/dL Niños>10 años c-LDL<135mg/dL | Entre los 8-10 años | 2015 |
| Guías pediátricas del manejo de la HF del panel de expertos de la Asociación Nacional de Lípidos | EUA | Cascada familiar | c-LDL>160mg/dL | Reducción del 50% del c-LDL o<100 | Entre los 8-10 años | 2016 |
Se han publicado recientemente diversas revisiones y consensos en HF.
La Asociación Española de Pediatría publicó una guía de abordaje del niño con hipercolesterolemia24 que podemos resumir de la siguiente forma:
- -
No recomienda cribado universal.
- -
Recomienda cribado selectivo si hay historia de ECVP en familiares de primer y segundo grado y/o CT>240mg/dL en un progenitor.
- -
Edad ideal del cribado entre los 2-10 años.
La Sociedad Española de Arteriosclerosis publicó un documento de consenso de expertos11:
- -
Cribado universal en todos los niños entre 8-10 años.
- -
Cribado en cascada directa a los familiares de primer grado del paciente con diagnóstico genético de HF, independientemente de las cifras de CT. Si el estudio genético es negativo, se deberán determinar las cifras de c-LDL en todos los familiares de primer grado.
- -
Cribado en cascada inversa de los familiares de primer grado de los niños con c-LDL>135mg/dL o bien con estudio genético establecido.
- -
Cribado selectivo de los niños con historia familiar de ECVP y/o hipercolesterolemia.
La Fundación de Hipercolesterolemia Familiar publicó un documento de consenso de expertos25:
- -
Cribado en cascada directa a partir de los 2 años cuando uno de los progenitores está diagnosticado y, si es posible, antes de los 8 años.
- -
Sospechar HF en niños con cifras de c-LDL>190mg/dL o c-LDL>150mg/dL con historia familiar de ECVP y/o hipercolesterolemia en uno de los progenitores y/o confirmación genética en uno de ellos.
El diagnóstico clínico de la HF en la infancia puede ser difícil, ya que en ocasiones podemos observar un solapamiento fenotípico con la hipercolesterolemia poligénica. El diagnóstico en el niño debe ser preferiblemente genético; sin embargo, no siempre es posible. En este caso, nos basaremos en su expresión fenotípica junto con los antecedentes familiares de ECVP y/o hipercolesterolemia indicativa de HF.
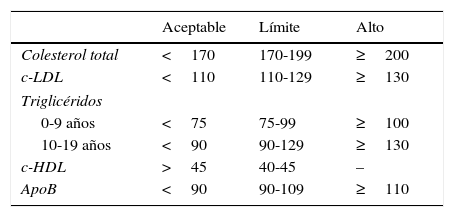
En la actualidad, en nuestro entorno la sospecha clínica se basará en los antecedentes familiares y los niveles de CT. En la tabla 2 podemos ver el perfil lipídico considerado dentro del rango normal y patológico en función de la edad.
Perfil lipídico de referencia en la infancia y la adolescencia
| Aceptable | Límite | Alto | |
|---|---|---|---|
| Colesterol total | <170 | 170-199 | ≥200 |
| c-LDL | <110 | 110-129 | ≥130 |
| Triglicéridos | |||
| 0-9 años | <75 | 75-99 | ≥100 |
| 10-19 años | <90 | 90-129 | ≥130 |
| c-HDL | >45 | 40-45 | – |
| ApoB | <90 | 90-109 | ≥110 |
Datos expresados como mg/dL.
Fuente: Moráis-López et al.24.
Se recomienda que ante niveles de CT≥200mg/dL, se realice una segunda determinación en un plazo máximo de 3 meses, solicitando un perfil lipídico completo. Sería recomendable aprovechar la segunda extracción sanguínea para descartar las causas secundarias de hipercolesterolemia en la infancia (tabla 3). Si se confirman valores de CT≥200mg/dL y c-LDL≥130mg/dL y se han descartado las causas secundarias, deberemos recomendar un periodo de dieta no inferior a 6 meses. Si tras este periodo en una nueva determinación persisten los niveles de c-LDL≥130mg/dL, deberemos sospechar la HF si van acompañados de alguna otra condición (tabla 4). Si el estudio del niño es fruto de un cribado selectivo, se solicitará de forma inicial un perfil lipídico completo.
Causas secundarias de hipercolesterolemia en la infancia
| Fármacos: amiodarona, corticoides, esteroides anabólicos, ciclosporina, fenobarbital, progestágenos, fenitoína, tiazidas, etc. Anorexia nerviosa Colestasis: cirrosis biliar, atresia de vías biliares Déficit de la hormona de crecimiento Enfermedades endocrinas: hipotiroidismo, hipopituitarismo Enfermedades renales: síndrome nefrótico Hipercalcemia idiopática Porfiria intermitente aguda Enfermedades de depósito: glucogenosis, Tay-Sachs, Gaucher, Niemann-Pick Factores dietéticos |
Criterios de sospecha de hipercolesterolemia familiar en la infancia y la adolescencia
| Niño con c-LDL≥130mg/dL y uno de los siguientes: |
| Antecedentes de ECVP<55 años en familiares de primer grado y<50 años en familiares de segundo grado |
| Progenitor con niveles de colesterol total>300mg/dL o en tratamiento hipolipidemiante |
| Ausencia de información acerca de los progenitores |
| Un progenitor afecto de HF con diagnóstico clínico o genético de HF |
Si los niveles de c-LDL son≥190mg/dL, obtenidos en 2 determinaciones consecutivas con un intervalo de 3 meses, las probabilidades de hallar una mutación causal de la HF son muy elevadas. Si los niveles de c-LDL son≥160mg/dL tras un periodo dietético más una historia de ECVP en familiares de primer grado (hombres<55 años, mujeres<60 años) o de segundo grado (hombres<45 años, mujeres<50 años) y/o hipercolesterolemia (c-LDL≥190mg/dL) o alguno de los progenitores está recibiendo tratamiento farmacológico hipolipidemiante, existe una alta probabilidad de ser portador de una mutación causal de la HF. Si se ha detectado la mutación causal en alguno de los progenitores, muy probablemente, si el niño tiene niveles de c-LDL≥130mg/dL, también será portador de dicha mutación. Si el progenitor ha fallecido por ECVP y el niño presenta niveles de c-LDL≥130mg/dL, se deberá intentar realizar el estudio genético.
Es recomendable realizar el estudio genético, pero en la actualidad no es posible llevarlo a cabo en toda la población española, sino que existen grandes diferencias entre comunidades autónomas con realidades y situaciones muy diferentes. Un claro ejemplo de ello es que mientras en las comunidades de Canarias y Murcia no se subvenciona el estudio genético, en la Comunidad de Castilla y León no hay ningún tipo de restricción26.
Los niveles de c-LDL en niños con HFHe oscilan entre 190-500mg/dL, mientras que en los afectos de HFHo oscilan entre 500-1.000mg/dL junto con la presencia de xantomas tuberosos y arco corneal antes de los 10 años. Sin embargo, puede observarse un solapamiento de los niveles de c-LDL entre 300-500mg/dL entre ambas formas27.
Recientemente ha sido diseñado un programa informático que calcula la probabilidad de detectar una mutación en un paciente con sospecha de HF y que tiene la finalidad de incrementar la detección en la población joven. Esta herramienta se basa en los datos recogidos durante 20 años en el programa de detección de la HF en Holanda (http://vasculaironderzoekamc.nl/fh-calculator/)28.
Objetivos terapéuticosNo hay una evidencia absoluta de cuáles son los objetivos terapéuticos en los niños con HF. En la tabla 1 se resumen los diferentes objetivos terapéuticos en relación con las distintas guías publicadas en los últimos años.
Recomendaciones terapéuticasEs importante iniciar de forma temprana la intervención terapéutica del niño con HF29.
Cambios en el estilo de vidaUna alimentación equilibrada y saludable es clave para el tratamiento de la HF y para la prevención de la arteriosclerosis. Se ha observado que la dieta puede reducir entre un 10-15% los niveles de c-LDL, siendo muy variables según el tipo de paciente y el tipo de mutación24,25. Cabe destacar que en estos niños las recomendaciones dietéticas van a ser insuficientes para alcanzar objetivos terapéuticos; aun así, sigue siendo importante mantener un peso adecuado para no añadir más factores de riesgo CV30.
Las recomendaciones deben ser indicadas a partir de los 2 años bajo la supervisión de un dietista-nutricionista cualificado que ayude a reforzar la terapia de nutrición en el ámbito familiar para conseguir una mejor adherencia al tratamiento31.
GrasasEl consumo de grasas debe ser limitado a<30% de las calorías totales ingeridas. Hasta el momento, muchas de las guías publicadas especifican la necesidad de bajar todo tipo de grasa y hacer especial hincapié en la importancia de disminuir la ingesta de colesterol (<200-300mg/día). En cambio, actualmente se incide más en la calidad que en la cantidad.
El consumo de ácidos grasos saturados debe ser<10%; aun así, algunas guías son más estrictas y especifican que es mejor por debajo del 7%. La reducción de la grasa saturada y del colesterol en la dieta del niño se ha visto que no modifica ni su estado nutricional ni el crecimiento ni el desarrollo puberal32. El aporte de grasa monoinsaturada debe ser de alrededor del 10%, básicamente en forma de ácido oleico. Deben evitarse las grasas de tipo trans presentes en los alimentos elaborados.
Diferentes ensayos clínicos han demostrado que el consumo diario de estanoles/esteroles vegetales a dosis de 1,5-3g/día en niños y adolescentes con HFHe puede ser beneficioso para reducir los niveles de c-LDL aproximadamente entre un 9-19%33. Recientemente, la Sociedad Europea de Arteriosclerosis ha publicado un panel de consenso donde se recomienda su consumo en pacientes con HF a partir de los 6 años, siempre y cuando la ingesta de verduras y frutas sea la adecuada para evitar el déficit de vitaminas liposolubles34.
No se recomienda ningún tipo de suplemento en forma de ácido linoleico ni omega 3, aceite de colza35, proteína de soja, extractos de ajo36 ni cereales con extracto de psyllium37.
Hidratos de carbonoDentro de los hidratos de carbono se incluyen fibras, almidones y azúcares. Además pueden clasificarse en 2 tipos: complejos y simples. Los que se deben promocionar son los complejos, ya que tienen un menor porcentaje de calorías y un elevado contenido de fibra (cereales integrales, pasta, arroz, pan, patata, legumbres, fruta y verdura).
Las últimas guías europeas de prevención del riesgo CV aconsejan un aporte de fibra de entre 30-45g/día. La ingesta de fibra hidrosoluble en forma de cereales enriquecidos se puede añadir a las dietas bajas en grasa o bajas en grasa saturada y la dosis diaria recomendada es de 6g/día para niños de 2-12 años y de 12g/día en los mayores de 12 años.
Se debe reducir la cantidad de azúcar simple y el azúcar contenido en las bebidas comercializadas38,39.
ProteínasSe debe aconsejar un aporte de alrededor de un 15% de proteínas. Se debe consumir preferentemente carnes blancas y pescado.
SalMuchas de las guías clínicas recomiendan una ingesta máxima de 5g/día (2g de sodio). En niños menores de 10 años es recomendable menos de 3-4g/día; en cambio, el consumo medio de esta población es de 8,1g/día40. Alrededor de un 75% procede de los alimentos procesados.
AlcoholLa bebida más consumida a diario en la población escolar de entre 14-18 años es la cerveza, y durante los fines de semana, los combinados.
Es muy importante educar bien a los niños para evitar el consumo de alcohol.
Ejercicio físicoMantener el peso ideal y fomentar la práctica de actividad física son claves dentro del conjunto de medidas a seguir.
De forma ideal, los niños deberían realizar más de una hora diaria de ejercicio y menos de 2 de actividades sedentarias como jugar a máquinas u ordenadores y/o sentarse delante del televisor4.
Se ha observado que los patrones de actividad física establecidos durante la niñez permanecerán a lo largo de la vida y se asocian a mayor colesterol ligado a lipoproteínas de alta densidad y menor c-LDL41,42.
FumarLa guía europea de prevención CV propone diferentes estrategias para promocionar el no consumo de tabaco13. El descenso del consumo en la última década es del 60%, según el informe presentado por el Ministerio de Sanidad español; aun así, el 38,4% de los adolescentes españoles reconoce que ha fumado en alguna ocasión y un 8,9% lo hace a diario.
El tabaco es un factor de riesgo CV adicional y en la población con HF este riesgo se ve incrementado43.
Tratamiento farmacológicoEficacia y tolerancia de las estatinasSon los fármacos de elección en el manejo farmacológico de los niños con HF. Siempre irá precedido de un periodo de tratamiento dietético. El inicio del tratamiento farmacológico debe ser antes de la pubertad, ya que mejora el control, la adherencia por parte de los padres y la aceptación del niño es mayor.
Las estatinas actúan inhibiendo de forma competitiva la enzima 3-HMG-CoA reductasa, dando lugar a una disminución de la síntesis intrahepática de colesterol y a un aumento de la síntesis del receptor de las LDL.
Diferentes consensos de expertos recomiendan iniciar tratamiento con estatinas entre los 8-10 años en la forma HFHe, y en la forma HFHo, en el momento del diagnóstico, antes de los 5 años y no más tarde de los 8 años27.
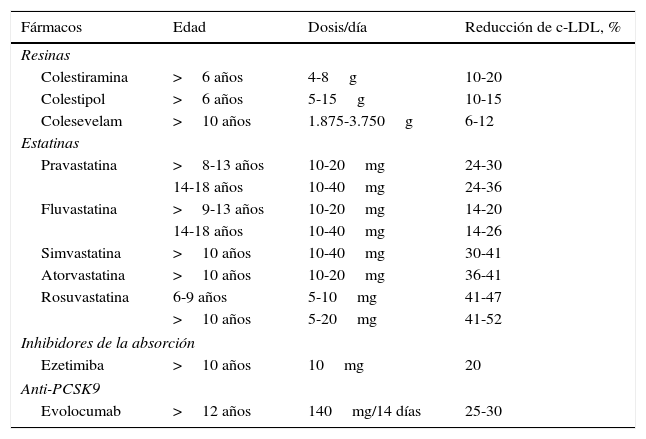
En la actualidad, están aprobadas por la Food and Drug Administration y la Agencia Europea del Medicamento las estatinas que veremos a continuación (tabla 5). La pitavastatina no ha sido aprobada en niños, aunque recientemente ha sido publicado un estudio que demuestra su seguridad entre los 6-17 años44. Diversos trabajos han mostrado la eficacia y la seguridad de las estatinas a corto plazo. Recientemente ha sido publicado el seguimiento de una cohorte de 214 niños con HF tratados con pravastatina durante un periodo de 10 años, demostrando que la seguridad a largo plazo no difiere de la comunicada en pacientes adultos45.
Tratamiento farmacológico en niños y adolescentes con hipercolesterolemia familiar
| Fármacos | Edad | Dosis/día | Reducción de c-LDL, % |
|---|---|---|---|
| Resinas | |||
| Colestiramina | >6 años | 4-8g | 10-20 |
| Colestipol | >6 años | 5-15g | 10-15 |
| Colesevelam | >10 años | 1.875-3.750g | 6-12 |
| Estatinas | |||
| Pravastatina | >8-13 años | 10-20mg | 24-30 |
| 14-18 años | 10-40mg | 24-36 | |
| Fluvastatina | >9-13 años | 10-20mg | 14-20 |
| 14-18 años | 10-40mg | 14-26 | |
| Simvastatina | >10 años | 10-40mg | 30-41 |
| Atorvastatina | >10 años | 10-20mg | 36-41 |
| Rosuvastatina | 6-9 años | 5-10mg | 41-47 |
| >10 años | 5-20mg | 41-52 | |
| Inhibidores de la absorción | |||
| Ezetimiba | >10 años | 10mg | 20 |
| Anti-PCSK9 | |||
| Evolocumab | >12 años | 140mg/14 días | 25-30 |
Se recomienda iniciar tratamiento si los niveles de c-LDL≥190mg/dL o bien≥160mg/dL si se acompaña de una de las siguientes condiciones: antecedente de ECVP en familiar de primer grado, presencia de otras enfermedades en el niño que cursan con elevado riesgo CV (diabetes, síndrome metabólico, hipertensión, lupus eritematoso, trasplante de órgano y enfermedad de Kawasaki), o bien si existen factores de riesgo CV elevados (obesidad, tabaco, Lp[a] elevada y homocisteinemia)13.
Al iniciar el tratamiento con estatinas, escogeremos la dosis más baja recomendada, que posteriormente podremos titular en función de su respuesta y tolerancia. En algún caso puede ser necesaria la combinación con otros fármacos (ezetimiba o resinas) para alcanzar los objetivos terapéuticos. La tabla 6 muestra los parámetros a monitorizar. Los efectos secundarios son infrecuentes; sin embargo, están descritos: sensación de calambres, dolores musculares, efectos gastrointestinales y elevación de las transaminasas. No se han descrito alteraciones en las hormonas de crecimiento ni en las hormonas sexuales46.
Recomendaciones antes y después del uso de estatinas en el niño
| Antes de iniciar tratamiento, determinar transaminasas hepáticas, CPK, creatinina y glucosa Tras el inicio del tratamiento, monitorizar perfil lipídico y transaminasas hepáticas Monitorizar CPK si refiere mialgias Monitorizar glucosa en niños que reciban altas dosis de estatinas y estén obesos Control de crecimiento y desarrollo puberal Control anual una vez alcanzado el objetivo terapéutico |
Si se observa una elevación de las transaminasas, 3 veces por encima del límite superior de la normalidad, deberemos reducir la dosis o suspenderla y programar un nuevo control de seguimiento. Si el niño realiza ejercicio intenso, recomendaremos suspenderlo al menos 3 días antes de la extracción de sangre para evitar elevaciones de CPK secundarias al ejercicio.
En los niños que requieran tratamiento farmacológico por otras enfermedades acompañantes deberemos conocer qué citocromo P450 utiliza el fármaco para ser metabolizado. La decisión del tipo de estatina que vamos a escoger para iniciar el tratamiento dependerá de este hecho. Si un niño presenta insuficiencia renal, la estatina que escogeremos será atorvastatina, ya que su eliminación renal es mínima. El pediatra debe conocer las posibles interacciones farmacológicas de las estatinas y evitar la prescripción de fármacos tan habituales como los macrólidos.
Deberemos asesorar a las adolescentes en edad fértil sobre los diferentes métodos anticonceptivos e informarlas de que debe ser evitado un embarazo no programado. En caso de embarazo accidental, el tratamiento farmacológico deberá ser suspendido de forma inmediata.
Eficacia y tolerancia de ezetimibaEzetimiba es un fármaco que actúa inhibiendo selectivamente la absorción de colesterol y esteroles vegetales a nivel del intestino delgado, sin afectar la absorción de las vitaminas liposolubles ni de otras sustancias.
En general, es un fármaco hipolipidemiante de segunda línea y habitualmente se administra de forma combinada junto con una estatina. Está indicado en monoterapia si existe intolerancia a las estatinas. La experiencia en niños no es muy extensa; los estudios que han evaluado su seguridad y eficacia han sido a corto y medio plazo, por ello se necesitan más estudios para su valoración a largo plazo47,48 (tabla 5).
Eficacia y tolerancia de las resinasLas resinas de intercambio iónico actúan inhibiendo la absorción de los ácidos biliares a nivel del intestino49.
En la actualidad disponemos de diferentes resinas comercializadas (tabla 5). Sin embargo, su intolerancia digestiva y difícil ingesta son causa de abandono del tratamiento. Para intentar disminuir este problema se recomienda disolver la presentación de polvos o de granulados en zumos de frutas y administrarlo antes de las comidas. Hay que recordar que no se debe administrar conjuntamente con otros fármacos (una hora antes o 4h después). En tratamientos prolongados se puede alterar la absorción de las vitaminas liposolubles (A, D, E y K) y el ácido fólico, por lo que puede ser necesaria su suplementación. El efecto secundario más frecuentes es el estreñimiento, por lo que se recomendará una dieta rica en fibra.
Colesevelam es la resina que más recientemente ha sido comercializada. Su seguridad y eficacia han sido evaluadas en niños con HFHe entre los 10-17 años. Al parecer, debido a su presentación, su tolerancia es mayor que la del resto de las resinas50,51.
Eficacia y tolerabilidad de los inhibidores PCSK9PCSK9 es una proteína segregada por los hepatocitos que interviene en la regulación del metabolismo del colesterol52.
La inhibición de PCSK9 permite reducir el número de receptores que van a ser degradados y aumentar así su densidad en la superficie celular, con la subsiguiente reducción del colesterol plasmático.
Los anticuerpos anti-PCSK9 son un nuevo grupo de fármacos que ya han demostrado a corto plazo su gran eficacia y seguridad. En la actualidad, en España han sido aprobados evolocumab y alirocumab, estando indicados para la población con HF en la que con una dosis máxima tolerada de hipolipidemientes no se consigan alcanzar objetivos terapéuticos53,54.
Niños con HFHo también han sido incluidos en los ensayos clínicos con evolocumab. Se han observando reducciones adicionales de c-LDL en aquellos niños portadores de receptores defectuosos; sin embargo, no se observó ningún efecto en los portadores de receptores nulos55,56. Sin duda, será una opción terapéutica para un grupo muy seleccionados de niños con HFHo, que incluso podría implicar la disminución de las sesiones de LDL-aféresis a los que están sometidos (tabla 5).
Futuras novedades terapéuticasLomitapidaLomitapida es un inhibidor oral de la proteína microsomal de transferencia de triglicéridos, presente en el retículo endoplásmico de los hepatocitos y de los enterocitos. Ha sido aprobada por la Food and Drug Administration y la Agencia Europea del Medicamento para el tratamiento de la HFHo. Se ha demostrado que puede llegar a reducir hasta en un 50% adicional la concentración de c-LDL con respecto a la terapia habitual en un estudio tras 12 meses de seguimiento57. Los efectos secundarios son muy frecuentes y fundamentalmente son de tipo gastrointestinal. Se han descrito elevaciones de las transaminasas y desarrollo de esteatosis hepática; ello comportará su monitorización a lo largo del tratamiento.
En España se ha publicado la primera experiencia clínica con lomitapida58. Todavía no se dispone de datos en niños, aunque está aprobada como uso compasivo.
MipomersenMipomersen es un oligonucleótido antisentido que inhibe la transcripción del ARNm de la ApoB. La reducción de la síntesis de la ApoB da lugar a una disminución de las VLDL a nivel intrahepático y, consecuentemente, del c-LDL. Recientemente, se ha publicado un estudio a largo plazo donde el tratamiento con este fármaco se asocia a una reducción de eventos CV en pacientes con HF59.
No ha sido aprobado por la Agencia Europea del Medicamento debido a la presencia de numerosos efectos adversos, fundamentalmente reacciones locales en el lugar de la inyección y elevación de las transaminasas60.
Hipercolesterolemia familiar homocigotaSe trata de la HF con una expresión de máxima severidad. Si no reciben tratamiento, la mayoría de los niños desarrollarán arteriosclerosis antes de los 20 años y su perspectiva de vida no superará los 30 años27.
Se recomienda iniciar el tratamiento lo más pronto posible para intentar retrasar la aparición de enfermedad CV. El objetivo terapéutico es el mismo que en el niño HFHe; sin embargo, en caso de enfermedad CV establecida, el objetivo debe ser c-LDL<70mg/dL. Estos objetivos son muy difíciles de alcanzar. Se deberá realizar tratamiento hipolipidemiante oral lo más precoz posible a partir de los 2 años, combinando estatinas con ezetimiba o resinas. A pesar de ello, las reducciones de c-LDL van a ser muy moderadas.
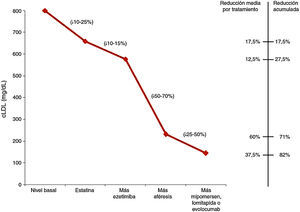
La mayoría de los niños tendrán que ser sometidos a LDL-aféresis. Se trata de un método de eliminación extracorpórea de las lipoproteínas que contienen ApoB. Se obtienen descensos adicionales de entre el 55-70% de c-LDL. Esta reducción es temporal, por lo que se deben realizar sesiones semanales o bien cada 15 días. Se recomienda iniciar la aféresis antes de los 5 años y nunca después de los 8. La LDL-aféresis es bien tolerada, habiéndose descrito efectos adversos en menos del 5% de los procedimientos. Un problema en niños de corta edad es el acceso venoso. En ocasiones será necesario colocar un acceso central, habiéndose descrito complicaciones en forma de infecciones o trombosis.
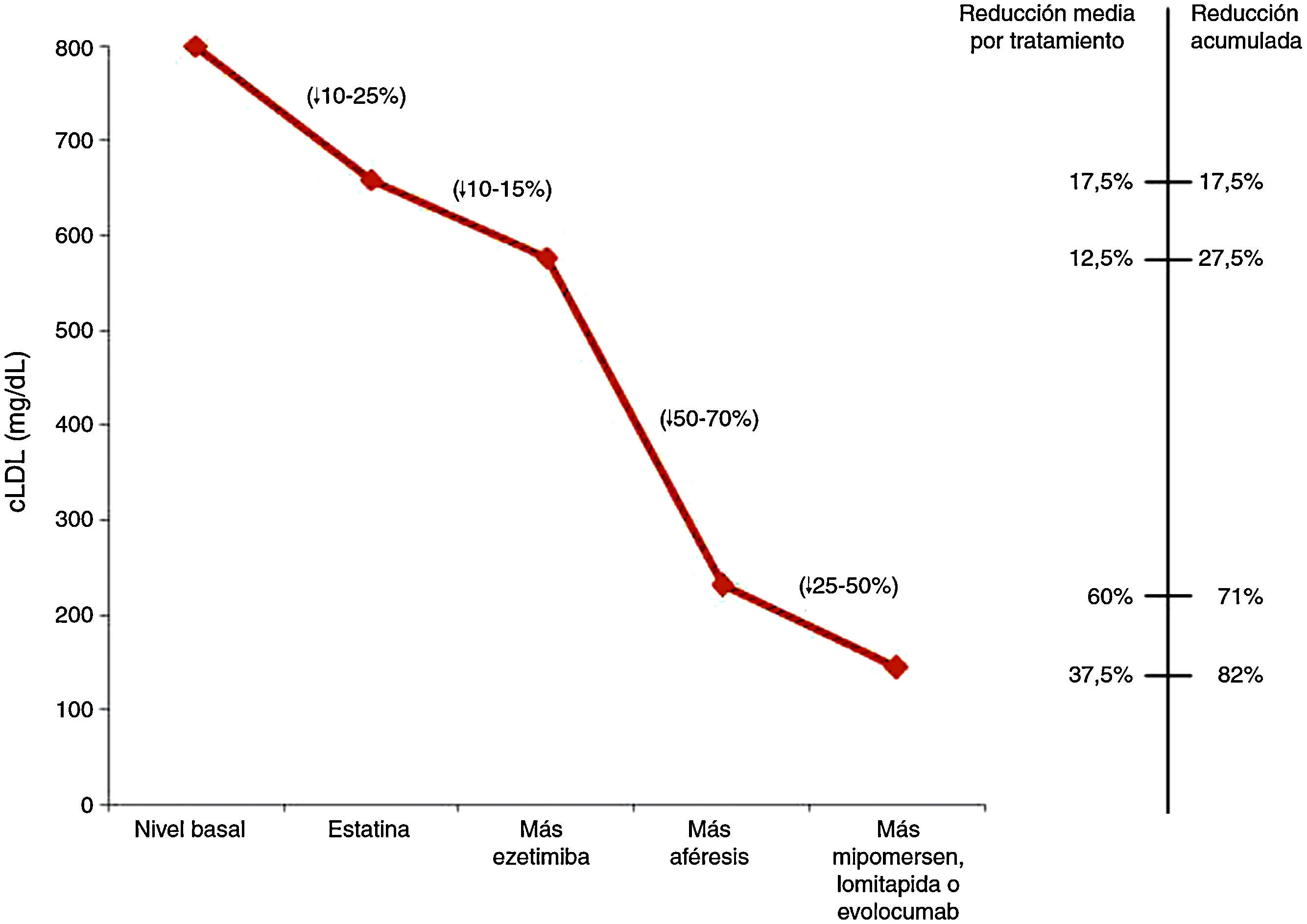
En la figura 1 podemos observar los descensos de c-LDL en función del tratamiento aplicado a los niños con HFHo27.
Descenso del colesterol LDL según el tratamiento aplicado en niños con hipercolesterolemia familiar homocigota27.
Los niños con HFHo deberán ser remitidos a unidades especializadas para su tratamiento.
ConclusionesLa HF es una alteración genética hereditaria con un elevado riesgo CV. La detección debe iniciarse en la edad infantil, ya que es fundamental para la prevención de la morbimortalidad en la edad adulta. Creemos que el pediatra juega un papel crucial y sería recomendable la realización de un cribado universal antes de los 10 años, aunque en estos momentos no es una práctica aceptada de forma generalizada. Como alternativa recomendamos el cribado oportunista. El cribado en cascada directa y el selectivo deben realizarse dentro de la práctica clínica habitual. El cribado en cascada inversa también ha demostrado ser una herramienta eficaz; se debe aprovechar cualquier extracción sanguínea para solicitar la determinación del CT. Se deben fomentar de forma precoz en los niños los hábitos de cambio de estilo de vida saludables e instaurar tratamiento farmacológico cuando esté indicado. Es importante realizar el estudio genético para estratificar el riesgo, pero también como método de adherencia familiar.
Los niños con HF deben ser remitidos a las unidades especializadas de referencia con capacidad de realizar el estudio genético y experiencia en su manejo. Los niños con HFHo van a requerir tratamiento intensivo farmacológico a dosis máximas junto con LDL-aféresis.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.