El tumor sólido pseudopapilar de páncreas (SPT) o tumor de Frantz presenta un comportamiento benigno con un bajo potencial de malignidad incluso en aquellos con enfermedad metastásica1–4. En la mayoría de los casos se presenta con clínica inespecífica, algunos de ellos son completamente asintomáticos y el diagnóstico es incidental en pruebas de imagen solicitadas por otros motivos1–6. Su resección quirúrgica es el tratamiento de elección, siendo en la mayoría de los casos curativa1–4.
Presentamos el caso de una paciente diagnosticada a través de ecoendoscopia (USE) y punción biopsia con aguja fina (BAAF).
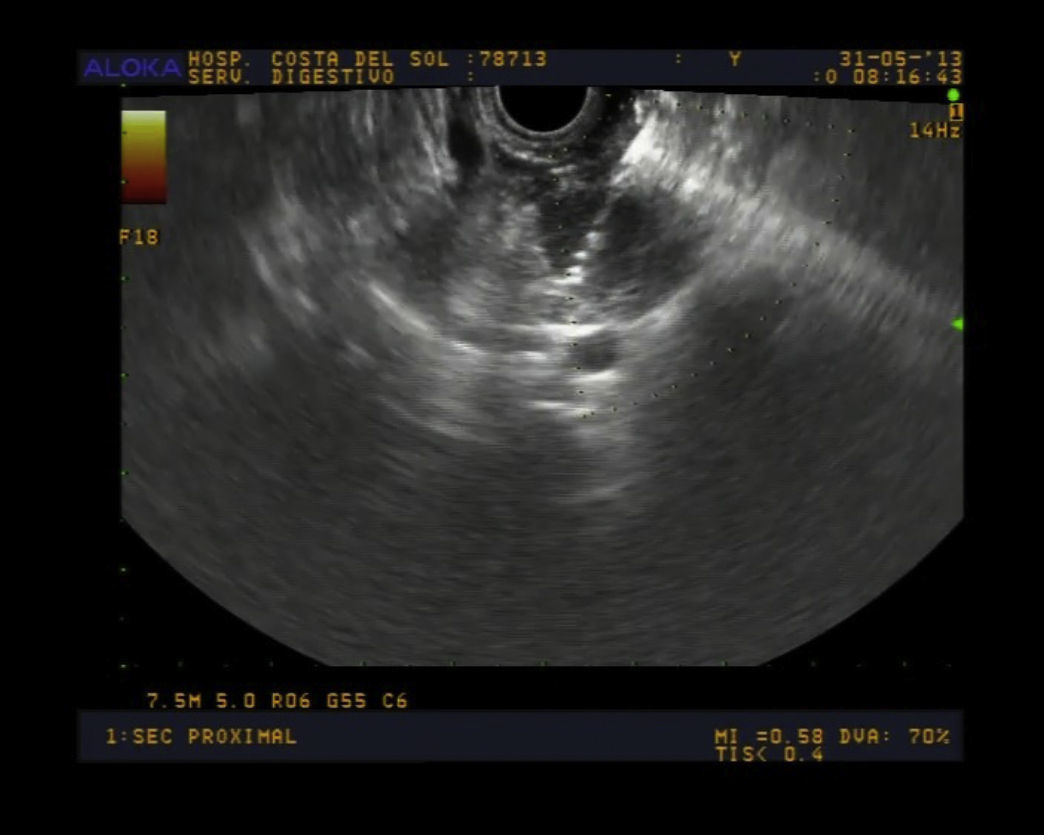
Mujer de 26 años sin antecedentes de interés y sin clínica pancreática, estudiada en cirugía tras un traumatismo torácico. En RMN se objetiva de forma incidental una lesión pancreática de 12mm aproximadamente, homogénea e hipoecoica, de bordes bien definidos y realce posterior, que sugiere un origen quístico, confirmándose dichas características con estudio ultrasonográfico abdominal. Se completa el estudio con USE, donde se observa un páncreas con parénquima homogéneo y lesión hipoecoica en cola de 15,5×11,4mm de diámetro, con contenido heterogéneo (estructuras hipoecoicas en el interior), que plantea dudas acerca del origen de la lesión (fig. 1). Se descarta comunicación con el Wirsung y se toman muestras mediante BAAF de 22G ProCore vía transgástrica. En el estudio citológico se observan células con formación pseudopapilar características del SPT y se confirma el diagnóstico con tinción positiva para progesterona, CD56, CD 10 y vimentina (fig. 2). Se realizó estudio de extensión sin detectar enfermedad a distancia, por lo que se decide su resección quirúrgica, mediante prancreatectomía distal por laparotomía, y se confirma dicho diagnóstico.
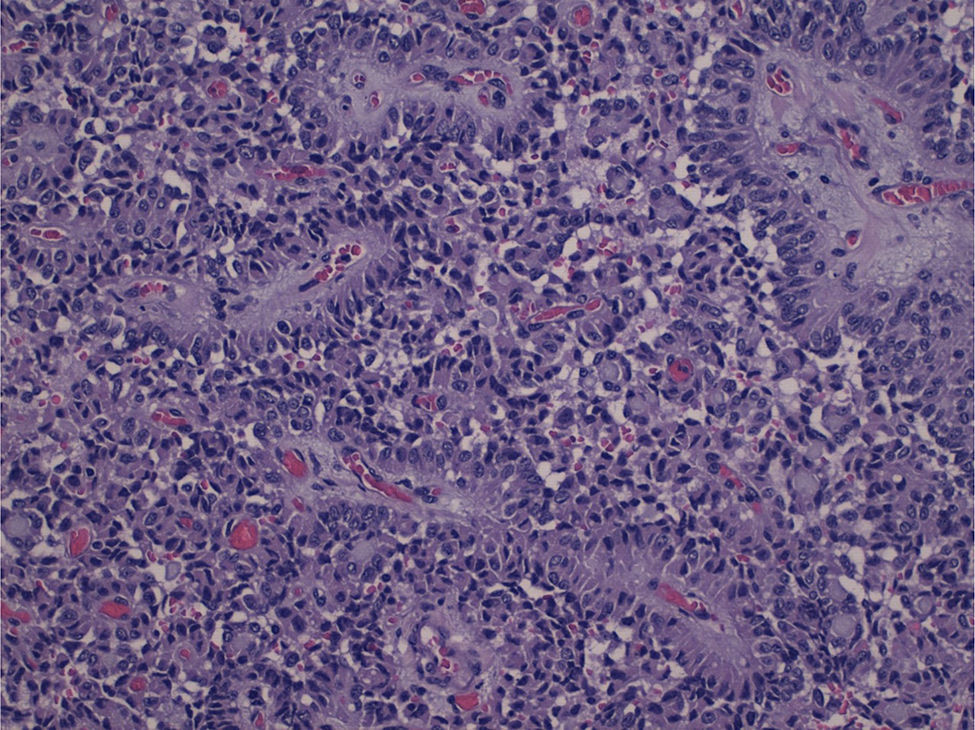
Anatomía patológica de la muestra en la que se observan células neoplásicas monomorfas pobremente cohesivas que forman estructuras sólidas, aunque con predominio de estructuras pseudopapilares, compuestas por ejes de tejido fibrovascular rodeados por una hilera de células con citoplasma claro, núcleos apicales, cromatina granular, nucléolo evidente y escasa atipia citológica.
El SPT es un tumor poco frecuente (1% de los tumores pancreáticos3,6) que afecta principalmente a mujeres jóvenes entre los 20-30 años1–6 y su localización más habitual es la cola del páncreas2–6. Se consideran neoplasias de bajo nivel de malignidad y su pronóstico es bueno. El tratamiento de elección es la resección quirúrgica1–4,6. No es adecuado realizar una enucleación y tampoco es necesario realizar una linfadenectomía amplia. No están indicadas la quimioterapia ni la radioterapia6. Su correcto diagnóstico preoperatorio es esencial para adecuar el mejor tratamiento y no sobre ni infratratar al paciente, sin embargo es difícil debido a su similitud con otras lesiones quísticas1–3. De hecho, solo el 25-50% de los pacientes se diagnostican correctamente antes de la cirugía2,3.
Típicamente en ecografía, TC y RM se muestra como una masa heterogénea bien delimitada con componentes sólidos y quísticos, generalmente con cápsula y a veces con calcificaciones. También por USE son inespecíficas, generalmente como un tumor bien definido anecoico con cápsula que en la mayoría de ocasiones es una masa sólida o bien un tumor mixto (sólido y líquido) y menos frecuentemente quístico5. En ocasiones el diagnóstico no queda claro y es necesario realizar biopsia. La punción por vía percutánea guiada por TC se ha visto hoy en día sustituida por la vía ecoendoscópica: bien usando la punción aspiración con aguja fina (PAAF) o la BAAF. El caso presentado nos hace ver la importancia de la USE y la BAAF en el diagnóstico y clasificación de las lesiones pancreáticas, sobre todo en las de menor tamaño como ocurría en nuestro caso, en el que tanto la RMN como la ecografía abdominal no aportaron un diagnóstico etiológico claro.
La USE parece ser la mejor prueba de imagen para el estudio de lesiones quísticas pancreáticas, debido a su mayor capacidad para caracterizar estas lesiones, detectar comunicación con el Wirsung y nódulos murales, y mediante la PAAF de obtener muestra para estudio citológico y bioquímico7. La sensibilidad de la USE-PAAF es del 75%2,3,5,7. En un estudio del 2013 comparan el incremento diagnóstico de la USE+/-PAAF en lesiones quísticas pancreáticas con respecto al TC y la RMN, se observa un incremento diagnóstico del 36% con respecto al TC y del 54% con la RMN. Además la USE demuestra ser considerablemente más sensible en la predicción de malignidad en lesiones de menor tamaño (<3cm) que el TC (59 vs 5%), por lo que sobre todo para estas lesiones ofrece más información y debería ser una prueba que se hiciera de inicio7.
Gracias a la PAAF se obtiene material para estudio citológico. Para lesiones quísticas se ha visto que en el 81% de los casos se obtiene una adecuada celularidad y en un 68% de ellos se obtiene un diagnóstico citológico7. Para lesiones sólidas pancreáticas se ha descrito una sensibilidad del 86,9% y especificidad del 95,9%8. Se ha demostrado que disponer de un citólogo en la sala aumenta esta sensibilidad pero no siempre es posible. Para solventar este problema se ha desarrollado la BAAF, cuyas principales ventajas son la obtención de mayor cantidad de material, con una mejor preservación de la arquitectura celular, y así poder realizar técnicas citológicas e identificar marcadores tumorales específicos9. La BAAF ofrece similar rentabilidad diagnóstica, complejidad de la técnica y complicaciones con respecto a la PAAF10. Con una media de 3 pases se obtiene material óptimo para el estudio citológico de la lesión (90%)2,9,10. Se puede abordar las lesiones pancreáticas por vía transgástrica o transduodenal. Para la BAAF se usan habitualmente agujas TruCut de 19G pero, debido a la rigidez inducida por la aguja, a la fricción mecánica del mecanismo de disparo y a la desviación de la punta del USE requerida para posicionar la lesión, tiene limitaciones en cabeza de páncreas y duodeno9. Para solventar esta limitación se han desarrollado las agujas flexibles, y más recientemente las agujas ProCore, con tecnología de bisel inverso que ofrecen una mayor flexibilidad y simplicidad en la técnica y mayor beneficio en la vía transduodenal9,10. En nuestro caso se realizó una BAAF con una aguja de 22G ProCore (Cook Medical, Limerick, Irlanda) por vía transgástrica, que permitió el correcto estudio citológico de la lesión y su diagnóstico.