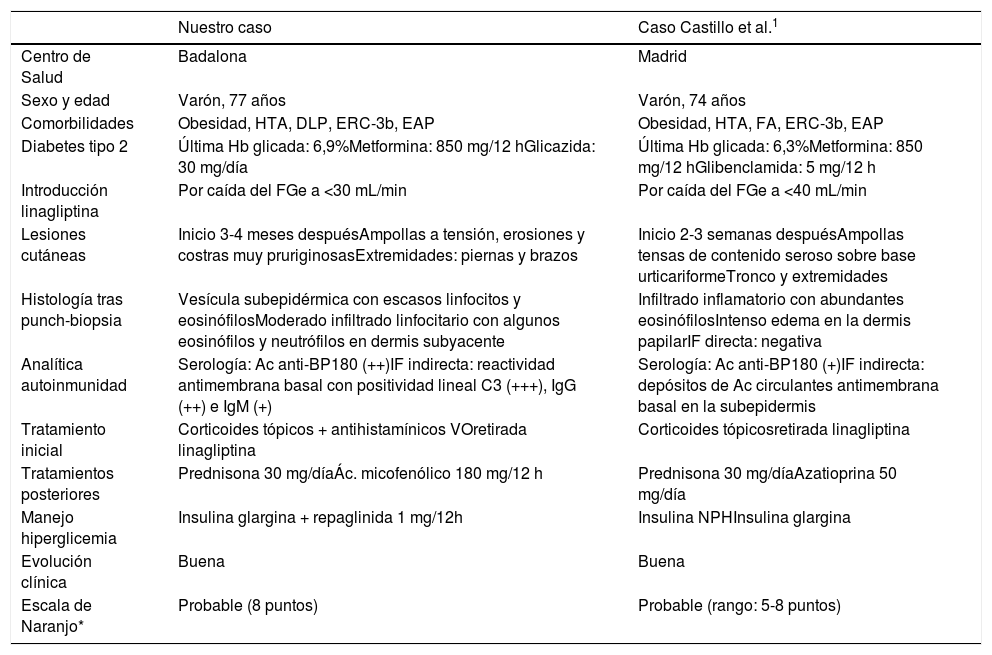
Hemos leído con gran interés la carta clínica de Castillo et al. recientemente publicada sobre penfigoide ampolloso (PA) inducido por linagliptina1 porque hemos detectado otro caso relacionado con el mismo antidiabético y con un perfil clínico muy similar, como se aprecia en la tabla 1.
Comparativa entre ambos casos: obsérvense las numerosas coincidencias
| Nuestro caso | Caso Castillo et al.1 | |
|---|---|---|
| Centro de Salud | Badalona | Madrid |
| Sexo y edad | Varón, 77 años | Varón, 74 años |
| Comorbilidades | Obesidad, HTA, DLP, ERC-3b, EAP | Obesidad, HTA, FA, ERC-3b, EAP |
| Diabetes tipo 2 | Última Hb glicada: 6,9%Metformina: 850 mg/12 hGlicazida: 30 mg/día | Última Hb glicada: 6,3%Metformina: 850 mg/12 hGlibenclamida: 5 mg/12 h |
| Introducción linagliptina | Por caída del FGe a <30 mL/min | Por caída del FGe a <40 mL/min |
| Lesiones cutáneas | Inicio 3-4 meses despuésAmpollas a tensión, erosiones y costras muy pruriginosasExtremidades: piernas y brazos | Inicio 2-3 semanas despuésAmpollas tensas de contenido seroso sobre base urticariformeTronco y extremidades |
| Histología tras punch-biopsia | Vesícula subepidérmica con escasos linfocitos y eosinófilosModerado infiltrado linfocitario con algunos eosinófilos y neutrófilos en dermis subyacente | Infiltrado inflamatorio con abundantes eosinófilosIntenso edema en la dermis papilarIF directa: negativa |
| Analítica autoinmunidad | Serología: Ac anti-BP180 (++)IF indirecta: reactividad antimembrana basal con positividad lineal C3 (+++), IgG (++) e IgM (+) | Serología: Ac anti-BP180 (+)IF indirecta: depósitos de Ac circulantes antimembrana basal en la subepidermis |
| Tratamiento inicial | Corticoides tópicos + antihistamínicos VOretirada linagliptina | Corticoides tópicosretirada linagliptina |
| Tratamientos posteriores | Prednisona 30 mg/díaÁc. micofenólico 180 mg/12 h | Prednisona 30 mg/díaAzatioprina 50 mg/día |
| Manejo hiperglicemia | Insulina glargina + repaglinida 1 mg/12h | Insulina NPHInsulina glargina |
| Evolución clínica | Buena | Buena |
| Escala de Naranjo* | Probable (8 puntos) | Probable (rango: 5-8 puntos) |
Ac: anticuerpos; C: complemento; DLP: dislipemia; EAP: enfermedad arterial periférica; ERC: enfermedad renal crónica; FA: fibrilación auricular; FGe: filtrado glomerular estimado; Hb: hemoglobina; HTA: hipertensión arterial; IF: inmunofluorescencia; Ig: inmunoglobulina; VO: vía oral.
A raíz de estos casos aislados profundizamos en el tema y descubrimos que el PA se ha relacionado, en mayor o menor grado, con casi todos los inhibidores de la dipeptidilpeptidasa-4 (IDPP-4). Hasta el 30 de junio de 2019 el Sistema Español de Farmacovigilancia había recibido 1300 sospechas de reacciones adversas por IDPP-4, de las cuales 85 fueron notificadas como enfermedades ampollosas y de estas 28 (33%) atribuidas a linagliptina2. En un artículo de revisión, García et al.3 encuentran que el IDPP-4 más relacionado con PA es vildagliptina (n=168), seguido de sitagliptina (n=61), linagliptina (n=25) y otras gliptinas (n=12). Por su parte Magdaleno et al.4, de 70 pacientes con PA estudian los 31 casos en tratamiento con algún IDPP-4 con la siguiente distribución: 13 por linagliptina, 12 por vildagliptina y 6 por las restantes gliptinas.
Asimismo, Sánchez et al.5 describen tres pacientes con PA desencadenado por linagliptina en ancianos diabéticos con enfermedad renal crónica (ERC) avanzada (estadio 4 con albuminuria), planteándose si el deterioro de la función renal –en individuos susceptibles– influye o desencadena la aparición del cuadro. Nuestro caso también presentaba proteinuria (cociente albúmina/creatinina entre 465-837mg/g) y en el de Castillo et al. no consta este dato, pero de cualquier modo las coincidencias son numerosas. De hecho, aunque el control metabólico era bueno, el origen del cese de metformina y sulfonilureas en ambos casos fue el deterioro de la función renal y la seguridad de linagliptina en ERC. Quizá, si se hubiera optado por otras alternativas terapéuticas –también seguras en esta situación (repaglinida, pioglitazona o insulina)– no se habría desarrollado esta grave complicación.
Como vemos, no es excepcional el PA desencadenado por IDPP-4 y, dentro de este grupo, la contribución de linagliptina no es infrecuente. En base a lo expuesto podría establecerse un cierto perfil clínico de riesgo, útil para el médico de familia (MF), que sería: anciano diabético y pluripatológico con nefropatía crónica en el cual, al caer el filtrado glomerular (FG) por debajo de 30mL/min y pasar a estadio 4, el profesional se ve obligado (si es que no lo ha hecho antes, con FG<45mL/min) a sustituir los hipoglicemiantes contraindicados en esta situación (metformina, sulfonilureas, acarbosa, glucosúricos). En este contexto clínico, la única gliptina que no requiere ajuste de dosis en caso de ERC –en cualquier estadio– precisamente es linagliptina… este factor y su dosificación en toma única diaria, probablemente, la marcan para su uso en este perfil de paciente.
Desde la perspectiva del MF, coincidimos con Castillo et al.1 en reforzar la alerta sobre los iDPP-4 en general, y sobre linagliptina en particular, por el riesgo de PA en ancianos diabéticos pluripatológicos. En caso de presentar lesiones cutáneas sugestivas se debería retirar el fármaco sospechoso así como derivar a Dermatología para confirmación diagnóstica y tratamiento corticoideo sistémico.