El paciente VIH+ tiene un riesgo incrementado de desarrollar una enfermedad musculoesquelética, en especial cuando está siguiendo un tratamiento antirretroviral de gran actividad (TARGA). Presentamos el caso de un paciente VIH+ que consultó por una coxalgia mecánica y cuyo diagnóstico final fue de necrosis avascular (NAV) de ambas cabezas femorales.
Se trata de un varón de 37 años, con los siguientes antecedentes personales: Tabaquismo activo, con un consumo de 11,3 paquetes/año. Seropositividad al VIH desde 2013 (categoría A2). Desde enero-2014 en régimen TARGA con un inhibidor de la proteasa (IP) —darunavir— (Rezolsta®) y etravirina (Intelence®). Úlcera rectal solitaria (2013-2016), en tratamiento discontinuo con lactulosa y espuma de budesonida rectal (Intestifalk®), una aplicación/24h. Hipercolesterolemia secundaria a TARGA (atorvastatina, 20mg).
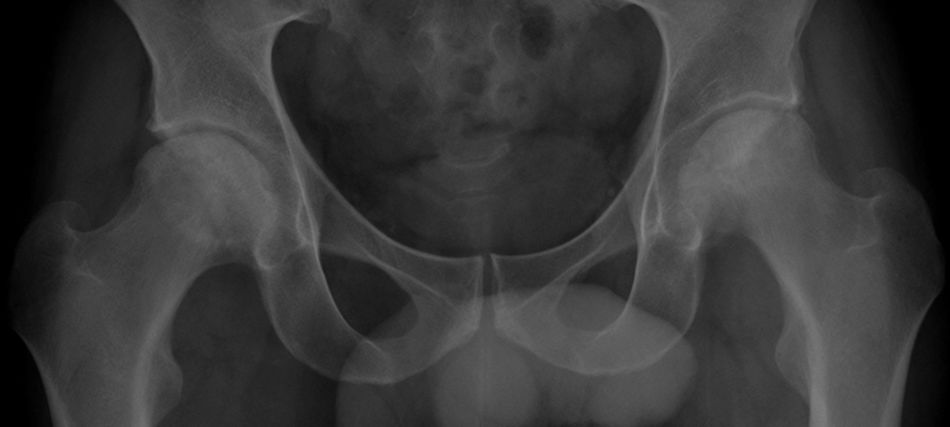
En julio-2015, el paciente refería un dolor mecánico en trocánter y cadera izquierda, de varias semanas y en los últimos días, asimismo en la cadera derecha, motivo por el que acudió a su médico de AP. En la exploración se objetivaban dolor a la presión sobre trocánter e inserción de musculatura glútea, así como en la abducción y rotación interna de cadera izquierda. En una analítica reciente se observaba únicamente una elevación del colesterol total, colesterol-LDL y triglicéridos (250, 154 y 245mg/dl, respectivamente). En la radiografía simple de pelvis/caderas (fig. 1) se apreciaba una irregularidad de las cabezas femorales, así como áreas radiolucentes parcheadas junto a zonas de hiperdensidad, signos sugerentes de una NAV bilateral. La RM evidenció signos bilaterales de necrosis, especialmente avanzados en la cabeza femoral izquierda, con estrechamiento del espacio articular, abundante derrame articular y edema muscular en la inserción del glúteo menor izquierdo, imágenes informadas como NAV bilateral en estadio iii de Ficat. El estudio densitométrico mostró una osteopenia (T scores=−2,3, −2,2, −1,9, para columna lumbar, cuello femoral y cadera total, respectivamente).
El paciente fue derivado a traumatología para establecer la indicación quirúrgica, y en la actualidad (2017) es portador de prótesis en ambas caderas.
Nuestro diagnóstico diferencial contemplaba 4 posibilidades. En primer lugar, la artritis asociada al VIH. Esta entidad suele ser de inicio brusco y puede aparecer como una poliartritis asimétrica de grandes articulaciones, con o sin fiebre, marcadores negativos (anticuerpos antinucleares y HLA-B27) y positividad del VIH en el líquido sinovial hasta en un 30-35% de los casos1. Se prolonga durante 1-6 semanas, responde bien a antiinflamatorios y no suele ser erosiva; sin embargo, algunos pacientes desarrollan una artritis crónica destructiva que ocasiona una gran limitación funcional2.
El segundo cuadro, la miopatía asociada al VIH, es una entidad poco frecuente. Su presentación clínica más habitual es una polimiositis progresiva, proximal y simétrica, con elevación de la creatinfosfoquinasa (CPK) y riesgo de rabdomiólisis en cualquier estadio de la infección. Su evolución y pronóstico no se conocen con certeza3.
El tercer diagnóstico diferencial era una miopatía tóxica. Bien conocida desde la era pre-TARGA, cuando se utilizaban dosis elevadas de zidovudina en monoterapia y los pacientes presentaban un cuadro similar a una polimiositis3. Algunos IP han sido asociados a miopatía y el efecto se puede potenciar por una estatina4. Nuestro paciente consumía ambos fármacos (darunavir y atorvastatina), y ese dato, junto a la clínica referida, apuntaban a la miopatía tóxica como un posible diagnóstico. Sin embargo, en una analítica reciente la CPK presentaba un valor normal (44U/l). En uso concomitante con antirretrovirales, la atorvastatina es segura, mientras que lovastatina y simvastatina presentan un riesgo elevado de reacciones adversas5.
Por último, la NAV, necrosis aséptica u osteonecrosis. Se cree que es el resultado de la combinación de una predisposición genética, factores metabólicos y factores locales, como un daño vascular y una elevación de la presión intraósea. Afecta más frecuentemente a la cabeza femoral, y ha sido asociada, entre otros, a tratamientos sistémicos con corticoides, consumo excesivo de alcohol, traumatismos o el uso de bifosfonatos (osteonecrosis mandibular)6 (tabla 1). Cursa fundamentalmente con dolor insidioso y limitación de la movilidad articular en fases tardías. La radiología simple puede ser normal incluso varios meses después del inicio de síntomas. Los hallazgos más precoces son cambios ligeros en la densidad y áreas de esclerosis a medida que la enfermedad progresa. En estadios finales se observan pérdida de la esfericidad, colapso de la cabeza femoral y signos de artrosis secundaria6.
Factores etiológicos de necrosis avascular
| Fractura de cuello femoral |
| Luxación o fractura-luxación |
| Traumatismo menor |
| Tratamiento corticoideo |
| Alcohol |
| Hemoglobinopatía falciforme |
| Disbarismo (enfermedad por descompresión) |
| Lupus eritematoso sistémico |
| Enfermedad de Gaucher |
| Insuficiencia renal crónica o hemodiálisis |
| Pancreatitis |
| Embarazo |
| Hiperlipemia |
| Radiación |
| Trasplante de órgano |
| Coagulación intravascular |
| Tromboflebitis |
| Tabaquismo |
| Hiperuricemia/gota |
| Infección por VIH |
| Idiopática |
Fuente: Jones y Mont6.
La NAV es una enfermedad de frecuencia creciente en el contexto de la infección VIH1,4. Existe un importante debate sobre la implicación de los TARGA en su aparición4,6, en concreto los fármacos IP7, posiblemente a través de la hiperlipemia y osteopenia que suelen ocasionar8. Cabe recordar que nuestro paciente seguía tratamiento con un IP, darunavir, desde hacía 15 meses, y presentaba ambas complicaciones. Sin embargo, aunque escasos, hay algún caso descrito de NAV en pacientes VIH+ antes de la aparición de los TARGA9, lo cual sugiere tanto un efecto directo del VIH como una etiología multifactorial de NAV en estos pacientes4.
Respecto al tabaquismo, factor de riesgo conocido de la NAV6, un metaanálisis reciente ha demostrado que se asocia a la NAV con una odds ratio de 2,53 (IC 95%: 1,6-3,7), y que aquéllos que consumen más de 20 paquetes/año presentan un riesgo aún mayor10.
Finalmente, en relación con el corticoide rectal, 2mg de espuma de budesonida/día es equivalente a 8,6mg/día de prednisona. La NAV no suele observarse como consecuencia de ciclos cortos de corticoides, y el riesgo es bajo (<3%) con dosis de prednisona <15-20mg/24h6.
Este caso ilustra el debate de los IP como agentes potencialmente relacionados con la aparición de NAV en los pacientes VIH+. Sin embargo, según lo publicado, probablemente se trate de una etiología multifactorial y, de hecho, en el paciente se identifican 3 factores de riesgo de NAV: Infección VIH, tratamiento con darunavir y tabaquismo. Es dudosa la implicación de la budesonida rectal, pues la dosis era inferior a la considerada de riesgo. En relación con la práctica asistencial del médico de AP, parece recomendable mantener un elevado grado de sospecha de NAV ante una coxalgia en un paciente VIH+.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.