Las distonías focales son la forma más frecuente de distonía primaria, con una prevalencia de 110 casos por millón de habitantes1. La distonía cervical y el blefaroespasmo son las formas más frecuentes de distonía focal.
El tratamiento de elección para las distonías focales consiste en inyecciones periódicas de toxina botulínica (TXB)2,3. En la práctica clínica, la toxina botulínica se administra a intervalos fijos, generalmente superiores a 3 meses. Estos intervalos se recomendaban hace más de 2 décadas para intentar reducir el riesgo de aparición de anticuerpos neutralizantes frente a la TXB. Sin embargo, a pesar de que las TXB tipo A altamente purificadas que se utilizan en la actualidad prácticamente no se asocian a la aparición de anticuerpos neutralizantes4 clínicamente relevantes se siguen manteniendo estos intervalos prolongados. No obstante, la duración de la mejoría clínica inducida por la administración de TXB puede ser inferior a 3 meses en los pacientes con distonías focales5,6.
El objetivo de esta carta al editor es presentar los resultados de un estudio realizado en nuestro centro en el que se evaluó la duración del efecto de la TXB en pacientes con distonías focales. Desde septiembre de 2015 a marzo de 2016 se evaluaron 90 pacientes de forma consecutiva con el diagnóstico de blefaroespasmo y distonía cervical tratados con TXB. Mediante un cuestionario estructurado se recogió la duración del efecto de la última infiltración de TXB, así como la duración real de los intervalos de infiltración de las 3 últimas sesiones de tratamiento. Además se recogieron la duración de la enfermedad, la duración del tratamiento con TXB, la dosis usada, el tipo de TXB, y los datos demográficos de los pacientes (sexo y edad).
Los datos recogidos se analizaron mediante estadística descriptiva y para la comparación de medias se utilizó el test de ANOVA de un factor.
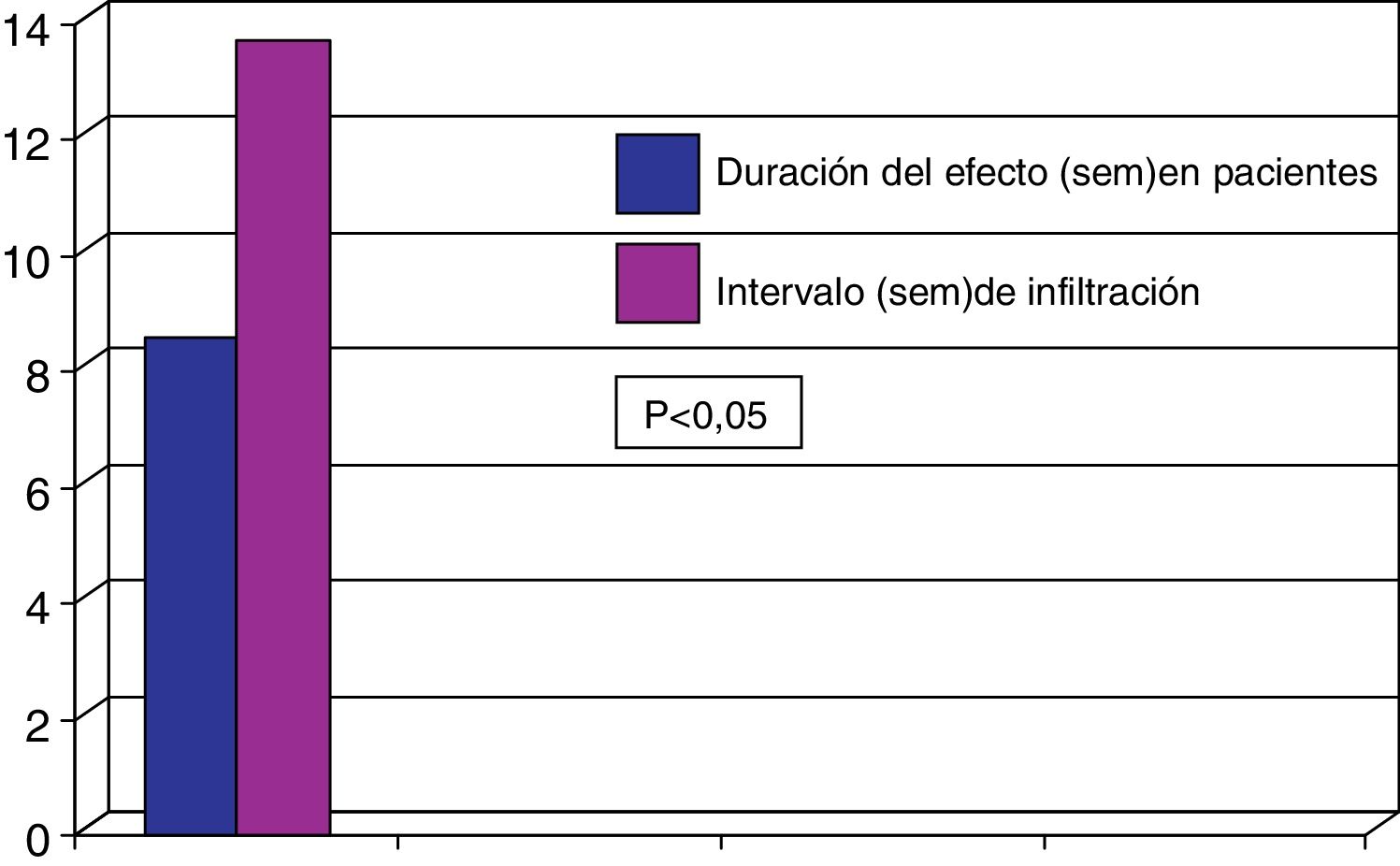
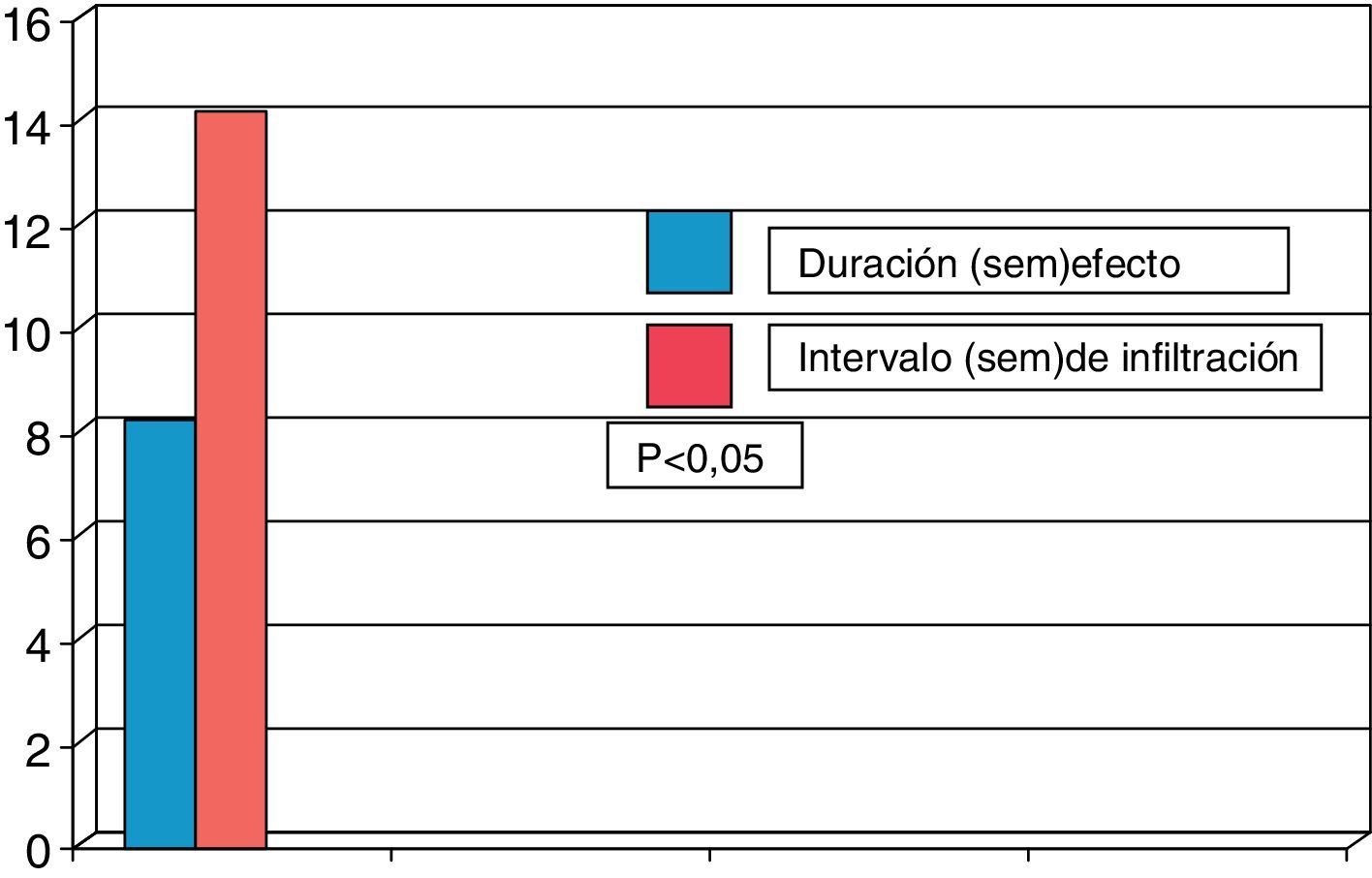
El 73% de los pacientes eran mujeres y la edad media fue de 67,8±14,0 años; 31 pacientes presentaban distonía cervical y 59 blefaroespasmo. La duración media de la enfermedad fue de 11,5±8,4 años. El 77,8% de los pacientes eran tratados con toxina onabotulínica A y el 22,2% con toxina incobotulínica A. La dosis media usada era de 46,3±11,8 unidades en los pacientes con blefaroespasmo y de 191,3±62,1 unidades en los pacientes con distonía cervical. La duración del efecto de la TXB fue de 11,6±4,0 semanas, siendo los intervalos reales de infiltración de 15,3±3,2 semanas (p<0,02). De forma global 38 pacientes (42,2%) presentaban reaparición de los síntomas antes de los 3 meses. En estos pacientes la duración media del efecto fue de 8,4±2,1 semanas siendo el intervalo real de infiltración en estos pacientes de 14,2±2,7 semanas (p<0,05). De los 59 pacientes con blefaroespasmo el 44% presentaban reaparición de los síntomas antes de los 3 meses, y el 42% de los 31 pacientes con distonía cervical. Analizando la duración del efecto en aquellos pacientes que presentaban reaparición de los síntomas antes de las 12 semanas se observó que la duración del efecto en los pacientes con blefaroespasmo fue 8,3±1,7 semanas y de 8,6±2,1 semanas en los pacientes con distonía cervical. El intervalo medio de infiltración real en estos pacientes fue de 14,3±2,3 semanas en pacientes con blefaroespasmo y de 13,7±3,4 semanas en distonía cervical, existiendo una diferencia estadísticamente significativa (p<0,05) en ambos casos en relación con la duración del efecto clínico (figs. 1 y 2). No se estudiaron las diferencias entre las distintas toxinas.
En conclusión, hemos observado que en aproximadamente el 40% de los pacientes con distonía focal estudiados, la duración del efecto clínico de la TXB fue inferior a 3 meses mientras que la aplicación de TXB se realizó a intervalos que, en general, superaban las 12 semanas.
Hay que tener en cuenta que la medición de la duración del efecto clínico se ha realizado mediante preguntas directas al paciente, sin valoraciones objetivas mediante escalas, porque el objetivo era estudiar la valoración subjetiva de los pacientes con respecto a sus síntomas. Tampoco hemos valorado otros factores objetivos que puedan suponer un retraso en la respuesta terapéutica, como puede ser el grado de atrofia muscular en la distonía cervical.
Resulta obvio que el abordaje terapéutico actual, con intervalos fijos prolongados entre sesiones de tratamiento, es inadecuado, en la medida en que no controla los síntomas distónicos durante todo el tiempo que transcurre entre inyecciones repetidas de TXB en un alto porcentaje de pacientes.
Para optimizar el resultado terapéutico de la TXB en las distonías focales, esta debería administrarse a intervalos flexibles, individualizados en función de la duración de la respuesta clínica de cada paciente4,5.