Describir las características demográficas y clínicas de los pacientes que presentaron infecciones relacionadas con los dispositivos cardiovasculares electrónicos implantables.
MétodosSe revisaron las historias clínicas de los pacientes que ingresaron por infecciones de los dispositivos cardiovasculares implantables entre enero de 2006 y septiembre de 2015. Se describieron las características relacionadas con el paciente, el procedimiento, el dispositivo y el microorganismo aislado.
Resultados22 pacientes fueron admitidos por infecciones relacionadas con los dispositivos electrónicos cardiovasculares implantables. El promedio de edad fue 63 años (DE 13,7) y 86% fueron del sexo masculino. La mitad de los pacientes tenían enfermedad renal crónica y solo el 27% diabetes mellitus. Todos los casos tenían al menos 2 electrodos intracardiacos y el 40,91% refirieron el antecedente de recambio del dispositivo. El germen más frecuentemente aislado fue el Staphylococcus epidermidis. La mortalidad fue del 22,73%.
ConclusionesLas infecciones por los dispositivos cardiovasculares son cada vez más frecuentes. Se debe identificar la presencia de infección local o sistémica con o sin compromiso intracardiaco. Los objetivos del tratamiento van dirigidos a la remoción del dispositivo cardiovascular y el tratamiento antibiótico dirigido.
To describe demographic and clinical characteristics of patients who developed infections related to cardiovascular implantable electronic devices.
MethodsMedical records of patients who were admitted for infections of cardiovascular implantable devices between January 2006 and September 2015 were reviewed. Characteristics related to the patient, the procedure, the device and the isolated microorganism were described.
Results22 patients were admitted for infections related to cardiovascular implantable electronic devices Average age was 63 years (SD 13.7) and 86% were male. Half of the patients suffered from chronic renal disease and only 27% diabetes mellitus. All cases had at least 2 intracardiac electrodes and 40.91% had required a previous replacement of the device. The most frequently isolated germ was Staphylococcus epidermidis. Mortality rate was 22.73%.
ConclusionsCardiovascular device-related infections are more and more frequent. The presence of a local or systemic infection with or without intracardiac involvement must be identified. The goals of the treatment are oriented towards the removal of the cardiovascular device and empirical antibiotic therapy.
Los dispositivos electrónicos cardiovasculares implantables son, en la actualidad, parte esencial de la práctica clínica de la cardiología. Una población adulta mayor con múltiples comorbilidades y un amplio número de indicaciones ha llevado al aumento de los dispositivos electrónicos cardiovasculares implantables1. Cerca del 70% de los pacientes son mayores de 65 años de edad y más del 75% tienen al menos una comorbilidad2. No obstante, el beneficio del uso de estos dispositivos se ha visto afectado por la mayor incidencia de infecciones, además, de la dificultad en su manejo por los costos de las técnicas del diagnóstico y la extracción de los mismos1,3. La incidencia de infección en el primer implante se estima en 1,9 por 1.000 dispositivos-año (0,5 a 6%), mientras que en los reimplantes la incidencia asciende a 5,32 por 1.000 dispositivos-año con una mortalidad hasta del 18% a 6 meses que puede llegar hasta 35%2,4,5. Se describe a continuación una serie de casos de las infecciones relacionadas con los dispositivos implantables en una institución de cuarto nivel de atención.
Materiales y métodosSerie de casos de pacientes hospitalizados con infecciones por los dispositivos cardiovasculares identificados por palabras clave “marcapaso”, “resincronizador”, “dispositivo implantable” en las bases de datos del servicio de infectología y electrofisiología durante el período de enero de 2006 hasta septiembre de 2015 en una clínica de cuarto nivel de atención en Cali, Colombia. Se obtuvo la información del paciente respecto a: sexo, edad, antecedentes médicos, características del dispositivo, tipo de dispositivo implantado, número de electrodos, necesidad de marcapaso transitorio preprocedimiento, fiebre en las 24 horas antes del implante del dispositivo, reintervención temprana por hematoma, y características de la infección tipo de infección (local o sistémica), el microorganismo aislado, la presencia de bacteremia, la infección del bolsillo, el tiempo entre la colocación o el recambio del dispositivo y la infección, el tipo de retiro realizado y el estado vital luego del proceso infeccioso. Lo anterior se graficó en las tablas de frecuencia. El presente estudio tuvo la aprobación del comité de ética en investigación biomédica institucional.
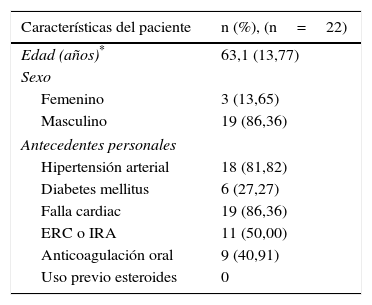
ResultadosSe hospitalizaron 22 pacientes en el período de enero de 2006 y septiembre de 2015 por infecciones relacionadas con los dispositivos electrónicos cardiovasculares implantables. La incidencia de la infección por cardiorresincronizador implantable con o sin desfibrilador fue 4,6% para los dispositivos implantados en la institución (13 de 281). Las características sociodemográficas se describen en la tabla 1. El promedio de edad fue 63 años de edad, con un rango entre 34 y 84 años. Hubo predominio del sexo masculino en el 86,36% de los casos. La falla cardiaca y la hipertensión arterial fueron los antecedentes más frecuentemente observados con el 86,36 y 81,82%, respectivamente. Así mismo, el 50% de los pacientes tenían enfermedad renal crónica o falla renal aguda (11 de 22 pacientes), y solo se presentó un caso de enfermedad renal crónica en hemodiálisis que cursó con la infección del dispositivo cardiaco por diseminación hematógena a los electrodos.
Características sociodemográficas y de antecedentes personales de los casos de infección por dispositivos electrónicos cardiovasculares implantables
| Características del paciente | n (%), (n=22) |
|---|---|
| Edad (años)* | 63,1 (13,77) |
| Sexo | |
| Femenino | 3 (13,65) |
| Masculino | 19 (86,36) |
| Antecedentes personales | |
| Hipertensión arterial | 18 (81,82) |
| Diabetes mellitus | 6 (27,27) |
| Falla cardiac | 19 (86,36) |
| ERC o IRA | 11 (50,00) |
| Anticoagulación oral | 9 (40,91) |
| Uso previo esteroides | 0 |
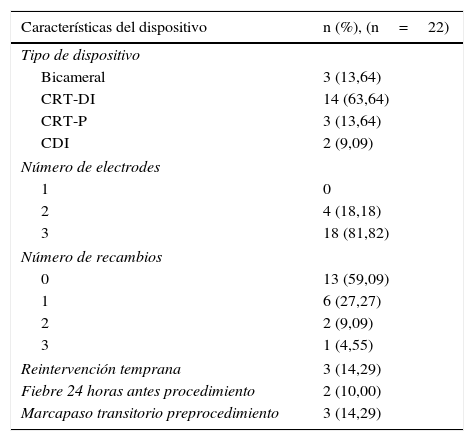
En relación con las características del dispositivo y el procedimiento (tabla 2) se documentó que el 63,64% (14 de 22) de los pacientes presentaron cardiorresincronizador con desfibrilador implantable y todos los pacientes tenían al menos dos electrodos implantados. Se observó el recambio del dispositivo en el 40,91% de los pacientes y 2 de los casos que no tenían el recambio previo se trataron de infecciones de origen hematógeno con compromiso intracardiaco.
Características del dispositivo, procedimiento y necesidad de recambios de los pacientes con infección relacionada con los dispositivos electrónicos cardiovasculares implantables
| Características del dispositivo | n (%), (n=22) |
|---|---|
| Tipo de dispositivo | |
| Bicameral | 3 (13,64) |
| CRT-DI | 14 (63,64) |
| CRT-P | 3 (13,64) |
| CDI | 2 (9,09) |
| Número de electrodes | |
| 1 | 0 |
| 2 | 4 (18,18) |
| 3 | 18 (81,82) |
| Número de recambios | |
| 0 | 13 (59,09) |
| 1 | 6 (27,27) |
| 2 | 2 (9,09) |
| 3 | 1 (4,55) |
| Reintervención temprana | 3 (14,29) |
| Fiebre 24 horas antes procedimiento | 2 (10,00) |
| Marcapaso transitorio preprocedimiento | 3 (14,29) |
CRT-P: dispositivo de resincronización cardiaca, CRT-DI: Resincronización cardiaca con cardiodesfibrilador implantable, CDI: cardiodesfibrilador implantable.
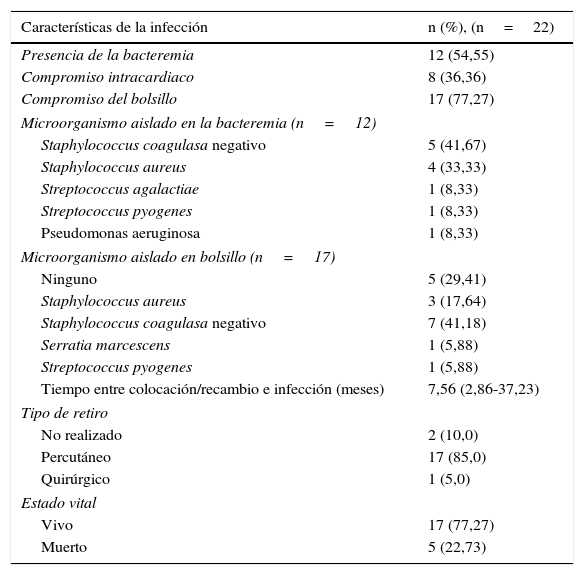
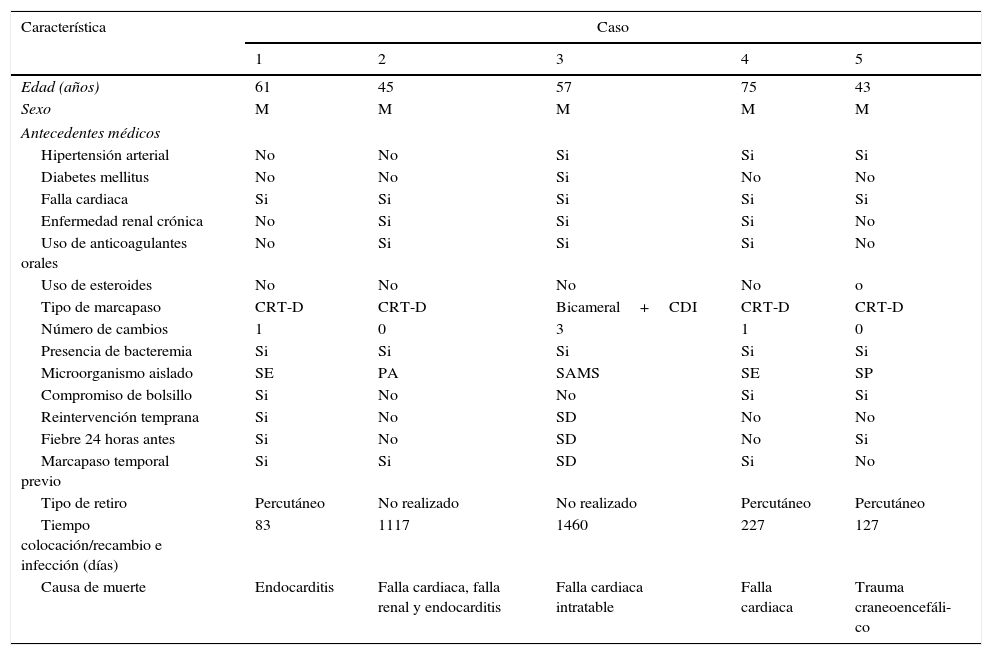
Se presentó la bacteremia en el 54,55% de los pacientes (tabla 3). Los microorganismos aislados en los pacientes que presentaron la bacteremia fueron Staphylococcus epidermidis en el 41% de los casos, Staphylococcus aureus meticilino sensible en el 33%, Streptococcus pyogenes en un caso, Pseudomonas aeruginosa en un paciente con siembra hematógena en el dispositivo cardiaco, Streptococcus agalactiae en un paciente con los dispositivos electrónicos cardiovasculares implantables e implante valvular aórtico transcatéter. Hubo un paciente que cursó con la bacteremia por Staphylococcus epidermidis y Staphylococcus aureus concomitante. Se presentó compromiso del bolsillo en el 77% de los casos. Entre los pacientes que presentaron la bacteremia y el compromiso del bolsillo se observó Staphylococcus epidermidis como germen predominante. La mediana de colocación o recambio del dispositivo fue de 7 meses, presentándose la infección hasta en los 85 meses posteriores al implante. Se logró el retiro del dispositivo de forma percutánea en el 85% de los casos y en un caso se requirió la intervención quirúrgica. Hubo dos pacientes en los cuales no se intentó el retiro del dispositivo por la inestabilidad hemodinámica y el desenlace adverso en el corto plazo. De los 22 pacientes con las infecciones relacionadas con los dispositivos fallecieron 5 de los cuales uno de los casos fue una muerte no relacionada con el proceso infeccioso (22,73%). En la tabla 4 se describen los casos que fallecieron.
Características de la infección relacionada con los dispositivos electrónicos cardiovasculares implantables, tratamiento y estado vital
| Características de la infección | n (%), (n=22) |
|---|---|
| Presencia de la bacteremia | 12 (54,55) |
| Compromiso intracardiaco | 8 (36,36) |
| Compromiso del bolsillo | 17 (77,27) |
| Microorganismo aislado en la bacteremia (n=12) | |
| Staphylococcus coagulasa negativo | 5 (41,67) |
| Staphylococcus aureus | 4 (33,33) |
| Streptococcus agalactiae | 1 (8,33) |
| Streptococcus pyogenes | 1 (8,33) |
| Pseudomonas aeruginosa | 1 (8,33) |
| Microorganismo aislado en bolsillo (n=17) | |
| Ninguno | 5 (29,41) |
| Staphylococcus aureus | 3 (17,64) |
| Staphylococcus coagulasa negativo | 7 (41,18) |
| Serratia marcescens | 1 (5,88) |
| Streptococcus pyogenes | 1 (5,88) |
| Tiempo entre colocación/recambio e infección (meses) | 7,56 (2,86-37,23) |
| Tipo de retiro | |
| No realizado | 2 (10,0) |
| Percutáneo | 17 (85,0) |
| Quirúrgico | 1 (5,0) |
| Estado vital | |
| Vivo | 17 (77,27) |
| Muerto | 5 (22,73) |
Características de las defunciones en pacientes con infección por dispositivos implantables
| Característica | Caso | ||||
|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | |
| Edad (años) | 61 | 45 | 57 | 75 | 43 |
| Sexo | M | M | M | M | M |
| Antecedentes médicos | |||||
| Hipertensión arterial | No | No | Si | Si | Si |
| Diabetes mellitus | No | No | Si | No | No |
| Falla cardiaca | Si | Si | Si | Si | Si |
| Enfermedad renal crónica | No | Si | Si | Si | No |
| Uso de anticoagulantes orales | No | Si | Si | Si | No |
| Uso de esteroides | No | No | No | No | o |
| Tipo de marcapaso | CRT-D | CRT-D | Bicameral+CDI | CRT-D | CRT-D |
| Número de cambios | 1 | 0 | 3 | 1 | 0 |
| Presencia de bacteremia | Si | Si | Si | Si | Si |
| Microorganismo aislado | SE | PA | SAMS | SE | SP |
| Compromiso de bolsillo | Si | No | No | Si | Si |
| Reintervención temprana | Si | No | SD | No | No |
| Fiebre 24 horas antes | Si | No | SD | No | Si |
| Marcapaso temporal previo | Si | Si | SD | Si | No |
| Tipo de retiro | Percutáneo | No realizado | No realizado | Percutáneo | Percutáneo |
| Tiempo colocación/recambio e infección (días) | 83 | 1117 | 1460 | 227 | 127 |
| Causa de muerte | Endocarditis | Falla cardiaca, falla renal y endocarditis | Falla cardiaca intratable | Falla cardiaca | Trauma craneoencefáli-co |
M: masculino. CRT-D: Cardiorresincronizador con desfibrilador. CDI: Cardiodesfibrilador implantable. SE: Staphylococcus epidermidis. PA: Pseudomonas aeruginosa. SAMS: Staphylococcus aureus meticilino sensible. SP: Streptococcus pyogenes. SD: Sin dato.
El amplio número de indicaciones para el uso de los dispositivos electrónicos cardiovasculares implantables, observado en el 25-30% de los pacientes con la falla cardíaca sintomática, ha llevado al aumento de las infecciones relacionadas con estos dispositivos6–8. Se ha reportado una incidencia de infecciones del 0,5-7% y que varía de acuerdo con cada centro y una mortalidad entre el 4,6 al 11,3% al ingreso hospitalario y hasta el 35% a largo plazo9.
Nuestra serie de casos incluye los pacientes con infecciones por los dispositivos electrónicos implantables cardiovasculares de los últimos 9 años. La incidencia para los cardiorresincronizadores y los cardiodesfibriladores implantables fue del 4,6% en este período de tiempo, similar a la reportada por la literatura mundial, teniendo en cuenta, que algunos de los pacientes incluidos en nuestro estudio, el implante del dispositivo no se realizó en la institución. La mortalidad observada fue del 23% (5 de 22 casos) acorde con las estadísticas mundiales, aunque solo 2 de estos 5 casos (9%) la causa directa fue el proceso infeccioso, las otras defunciones se presentaron en el contexto de la falla cardiaca terminal y un evento de trauma craneoencefálico.
Aunque la mayoría de las infecciones se encuentran limitadas al bolsillo del generador también se puede observar la endocarditis infecciosa, ya sea por compromiso del electrodo o valvular, en el 10% de los casos2,10–12. En nuestra experiencia, cerca del 77% de los pacientes presentaron compromiso del bolsillo, de estos el 54% tuvieron evidencia de la bacteremia, y el 36% de los pacientes (8 de 22) presentaron lesiones evidentes por la ecocardiografía, sugestivas de vegetaciones a nivel de los cables del dispositivo. Esta frecuencia es mayor a la reportada en otros centros, sin embargo, esta cifra es esperable teniendo en cuenta las características de los pacientes donde 72% tenían la falla cardiaca con indicación de resincronizador, enfermedad renal crónica en la mitad de los pacientes, uso de anticoagulantes en el 40% de los pacientes lo que indica que, probablemente, eran individuos más enfermos con mayor susceptibilidad a las infecciones.
Los principales factores de riesgo reportados en la literatura están relacionados con las características del paciente, del dispositivo, la técnica del operador y las medidas de asepsia6,7,13. Aunque nuestra serie no tiene el diseño para evaluar los factores de riesgo, se observó la mayor frecuencia en el sexo masculino (86,36%), enfermedad renal crónica (50%), anticoagulantes orales (40,91%), diabetes mellitus (27,27%) en los pacientes con infecciones por los dispositivos implantables, sin ser esto un indicador de asociación entre estos factores y el desarrollo de la enfermedad. Otros factores de riesgo de infección de los dispositivos son la presencia de los procedimientos previos, la ausencia de profilaxis antibiótica, en el caso de nuestra institución, por protocolo se realiza profilaxis antibiótica con la cefazolina 2g dosis única y, en caso de una hospitalización mayor a 72 horas se adiciona la vancomicina 1g dosis única5,7,14,15. La presencia de un procedimiento y el recambio previo se observó en el 40% de los casos, la reintervención temprana en el 14% y el uso del marcapaso transitorio en el 14% de los casos.
Los principales microorganismos relacionados son del género Staphylococcus siendo la principal causa de las infecciones por los dispositivos electrónicos cardiovasculares implantables, se reportó el 41% para coagulasa negativo y el 33% para Staphylococcus aureus en nuestra serie comparado con el 56% en la literatura mundial1. Se reportó una mayor frecuencia de las infecciones del bolsillo en el primer año postimplante que puede variar entre el 75 a 93%, para nuestra serie la mediana de meses entre el implante y la infección fue de 7 meses, pero, se observaron infecciones hasta en los 23 meses siguientes al implante5.
El principal método de la remoción del dispositivo y los electrodos fue la extracción simple. Esta consiste en la tracción del dispositivo y los cables por vía percutánea, en nuestro reporte se observó que el 85% de los dispositivos implantados lograron ser retirados a través de la vía percutánea. Este porcentaje de éxito aparenta ser más bajo que el reportado en la literatura (< 5%) probablemente debido a que en dos pacientes no se intentó el retiro del dispositivo y los cables por el estado hemodinámico y el pronóstico adverso a corto plazo.
La principal fortaleza del estudio es el registro de la información sistemática de todas las infecciones por el resincronizador cardiaco y el desfibrilador implantable a nivel institucional, lo cual permitió calcular la incidencia de las infecciones, el tratamiento y la probabilidad del retiro exitoso. Las principales debilidades son la recolección retrospectiva de la información, así que, en ciertos casos, reconocer la relación temporal entre el factor de riesgo y el inicio de la enfermedad se encuentra más allá del alcance de este estudio.
A continuación, se describe el enfoque diagnóstico y terapéutico de los pacientes con infección por los dispositivos electrónicos implantables.
Para los pacientes con sospecha de la infección del dispositivo, se recomienda realizar dos conjuntos de hemocultivos antes del inicio del antibiótico, cultivos del tejido del bolsillo del generador y cultivos de los electrodos cuando el dispositivo sea explantado2,16. No se recomienda la aspiración percutánea del bolsillo del generador dado que esto aumenta el riesgo de introducción de gérmenes de la piel al bolsillo2,7,16,17. Los cultivos identifican el patógeno en el 33-40% de los casos de la infección de los dispositivos electrónicos cardiovasculares implantables y en 68-100% de los casos de endocarditis asociada con los dispositivos electrónicos cardiovasculares implantables. Así mismo, un ecocardiograma transesofágico aporta información en caso de sospecha de la endocarditis ya sea por la presencia de los hemocultivos positivos o por los signos y síntomas de la infección sistémica7,16.
Los hemocultivos deben repetirse luego del explante del dispositivo para confirmar el aclaramiento de la bacteremia y para determinar la duración de la terapia antimicrobiana17.
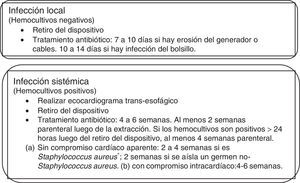
El abordaje terapéutico va encaminado a dos objetivos principales que incluyen el tratamiento antibiótico dirigido y la remoción completa del dispositivo y sus electrodos (fig. 1)11,13,16,18. No obstante, se observa recurrencia infecciosa en el 7,8% en 1 a 14 meses luego del retiro del dispositivo aunque esto está relacionado con el retiro incompleto de los electrodos en el 71,4% de los casos13.
La mayoría de los dispositivos se podrán retirar por vía percutánea y solo una minoría de pacientes requerirán remoción vía quirúrgica16. La principal técnica de extracción por vía percutánea es la simple. El retiro con láser se emplea en los casos en los que los cables no pudieran ser retirados por extracción simple y consiste en la aplicación del láser en los sitios de unión hasta que el cable es liberado. Una vez en el miocardio se realiza una combinación de tracción y contratracción hasta que se libera el electrodo3. Dentro de las complicaciones descritas, se reportan el 4% de eventos adversos mayores (avulsión cardiaca, compromiso vascular axilar con necesidad de intervención quirúrgica, sangrados con necesidad de transfusión, hemotórax) y el 1,8% de eventos menores (trombosis de la vena implantada, arritmia, embolismo pulmonar, falla respiratoria, reparo vascular cerca del sitio de implante) con una mortalidad del 1,86% relacionada al procedimiento de extracción3.
Para definir la vía de extracción se tiene en cuenta el tamaño de la vegetación (menor a 2 centímetros), edad del paciente, tiempo del dispositivo, tipo de dispositivo, electrodos dejados previamente, historia de dificultad para el retiro de los dispositivos o extracciones percutáneas fallidas y las comorbilidades2,16.
La terapia antimicrobiana va dirigida según la identificación y las pruebas de susceptibilidad de los cultivos. Sin embargo, teniendo en cuenta que la mayoría de las infecciones serán causadas por especies del género Staphylococcus y algunas de ellas pueden ser meticilino resistente, se indica la administración de la vancomicina como terapia empírica hasta que se conozcan los resultados microbiológicos. En caso de aislarse un germen meticilino sensible, se puede desescalar el tratamiento a la cefazolina sola2. El tiempo del antibiótico dependerá del contexto clínico. Para las infecciones del bolsillo se recomiendan 14 días y en el caso de extrusión del generador sin cambios inflamatorios, 7 a 10 días. El tiempo del antibiótico se prolongará entre 4 a 6 semanas de acuerdo con la presencia de la infección sistémica con o sin endocarditis, de estas al menos dos semanas de tratamiento antibiótico parenteral posterior al retiro del dispositivo (fig. 1)2,12,19.
Luego de la remoción completa del dispositivo infectado y antes del implante de un nuevo dispositivo debe determinarse si aún se requiere el dispositivo. Se debe colocar el nuevo dispositivo electrónico cardiovascular implantable en una localización anatómica remota al sitio del dispositivo infectado (usualmente en el hombro contralateral). Aunque el tiempo más apropiado para la colocación del dispositivo continúa siendo controvertido, no debe ser realizado hasta que los hemocultivos sean negativos en aquellos que tenían cultivos positivos y hasta que la infección del bolsillo se haya controlado para los cultivos negativos (72 horas para la infección del bolsillo, y hemocultivos positivos con eco transesofágico negativo, 72 horas para el cultivo positivo y el eco transesofágico positivo con retiro del dispositivo y cables, 14 días para la endocarditis asociada)2.
ConclusionesLos dispositivos electrónicos cardiovasculares implantables son cada vez más frecuentes debido al mayor número de indicaciones para su uso con la consecuente mayor incidencia de las infecciones relacionadas. El factor de riesgo más importante continúa siendo el recambio del dispositivo y los gérmenes más frecuentemente observados son los relacionados con la flora de la piel adyacente al área del implante. El diagnóstico va dirigido a determinar la localización de la infección, ya sea en el sitio del implante del dispositivo o la infección sistémica dada por el compromiso intracardiaco de los electrodos, el compromiso valvular o la presencia de la bacteremia. En todos los casos se indica el retiro completo del dispositivo y el tiempo de la terapia antibiótica varía según la presencia de la infección local o sistémica. Una vez retirado el dispositivo, se debe tener en cuenta que un porcentaje no despreciable de los casos ya no tendrán la indicación de reimplante de un dispositivo electrónico cardiovascular implantable.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesNo hay conflicto de intereses por parte de los autores.
Estudio Institucional de la Fundación Valle del Lili.
Dr. Juan Diego Vélez, Servicio de Infectología, Fundación Valle del Lili.
Dr. Nelson Murillo, Departamento de Cardiología.
Dr. Juan Santiago Villadiego, Departamento de Cardiología.