INTRODUCCIÓN
El estudio de la meiosis en biopsia testicular forma parte de los protocolos de exploración del varón estéril desde que en los años setenta se describió que alrededor del 6% de los pacientes estudiados presentaba anomalías en este importante proceso celular1. Los resultados obtenidos2,3 ponen de relieve su importancia en el estudio del factor masculino en parejas con esterilidad/infertilidad o que son candidatos a técnicas de reproducción asistida (TRA). El diagnóstico de anomalías en alguna de sus fases permite establecer un pronóstico, ofrecer un adecuado consejo genético y orientar a la pareja en la toma de decisión entre las alternativas terapéuticas que se les pueden ofrecer.
El objetivo de este trabajo de revisión es presentar una interpretación diagnóstica de los estudios meióticos y sus implicaciones en el consejo reproductivo.
ESTUDIOS MEIÓTICOS
Los estudios meióticos con finalidad diagnóstica se basan en el análisis de las 3 fases más representativas del proceso de meiosis: profase I, metafase I y metafase II.
- Profase I. Su valoración permite determinar la presencia o no de anomalías de apareamiento de los cromosomas homólogos (sinapsis) y del par de cromosomas sexuales (XY).
- Metafase I. Su análisis permite valorar las anomalías sinápticas, que se ponen de manifiesto por una baja frecuencia de quiasmas entre bivalentes, la presencia de univalentes y otras alteraciones del patrón esperado1,3,4.
- Metafase II. Es una fase de corta duración y, por lo tanto, su número suele ser escaso. Aunque su valoración es compleja, el análisis del número total de cromosomas que presentan (ploidía) ofrece información del resultado final de la primera división meiótica.
En todas las fases observadas, el aspecto de las figuras meióticas (normal o degenerativo) aporta información acerca de las características generales del proceso.
Parte de la dificultad que conllevan los estudios meióticos reside en la identificación y caracterización de las anomalías que pueden presentarse. Las anomalías meióticas son variadas: disminución generalizada de quiasmas entre bivalentes cromosómicos; desinapsis de bivalentes; presencia de univalentes de pequeño tamaño; separación de los cromosomas sexuales; metafases I hiperploides, metafases II diploides o poliploides; etc. Por otra parte, estas anomalías pueden presentarse de forma individual o combinadas entre sí dificultando la valoración de los estudios meióticos3,4.
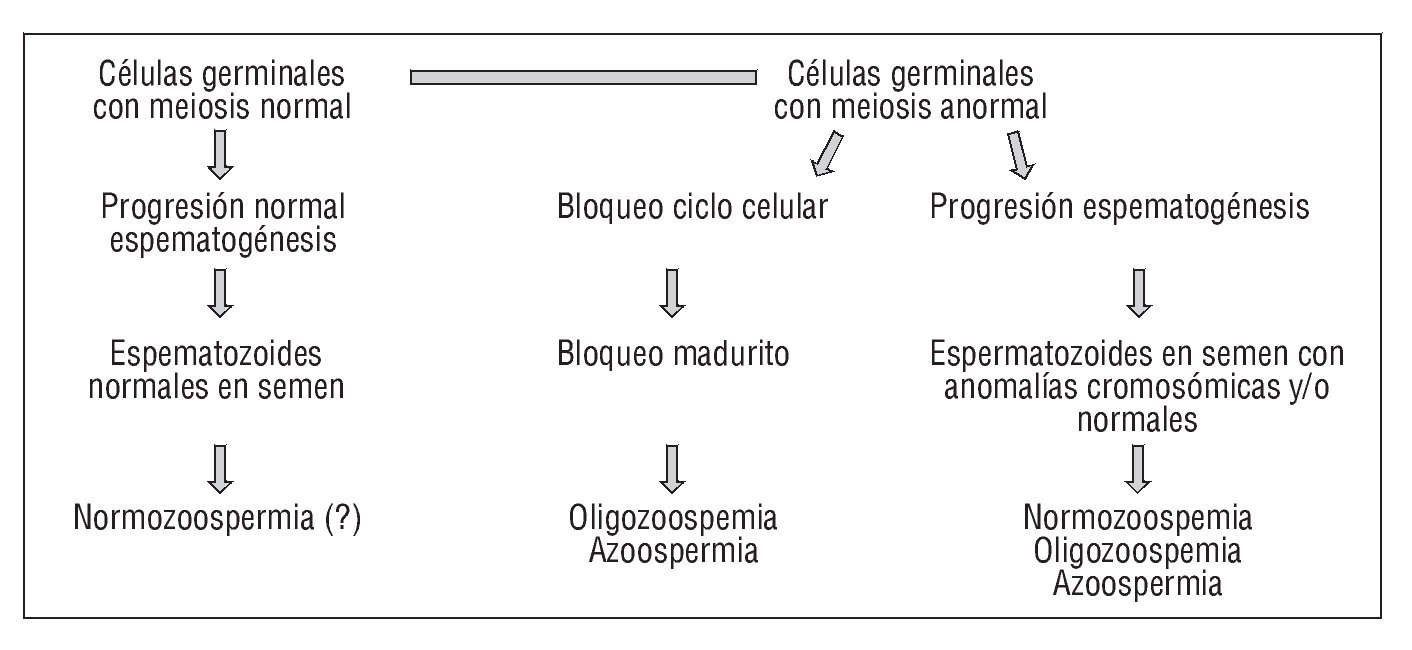
En cuanto a sus consecuencias, las anomalías meióticas pueden afectar a distintos niveles en el proceso de espermatogénesis: provocar un bloqueo meiótico de las células efectadas, dar lugar a la producción de espermatozoides portadores de anomalías cromosómicas (aneuploides o diploides) o incluso traducirse en la obtención de espermatozoides cromosómicamente normales que provengan de la coexistencia de líneas celulares no afectadas por anomalías meióticas (fig. 1).
Figura 1. Relación entre el proceso meiótico y las consecuencias esperadas.
INTERPRETACIÓN DE LOS RESULTADOS
La dificultad en la interpretación de los resultados de los estudios meióticos deriva de la propia complejidad del proceso de meiosis (figs. 1y 2).
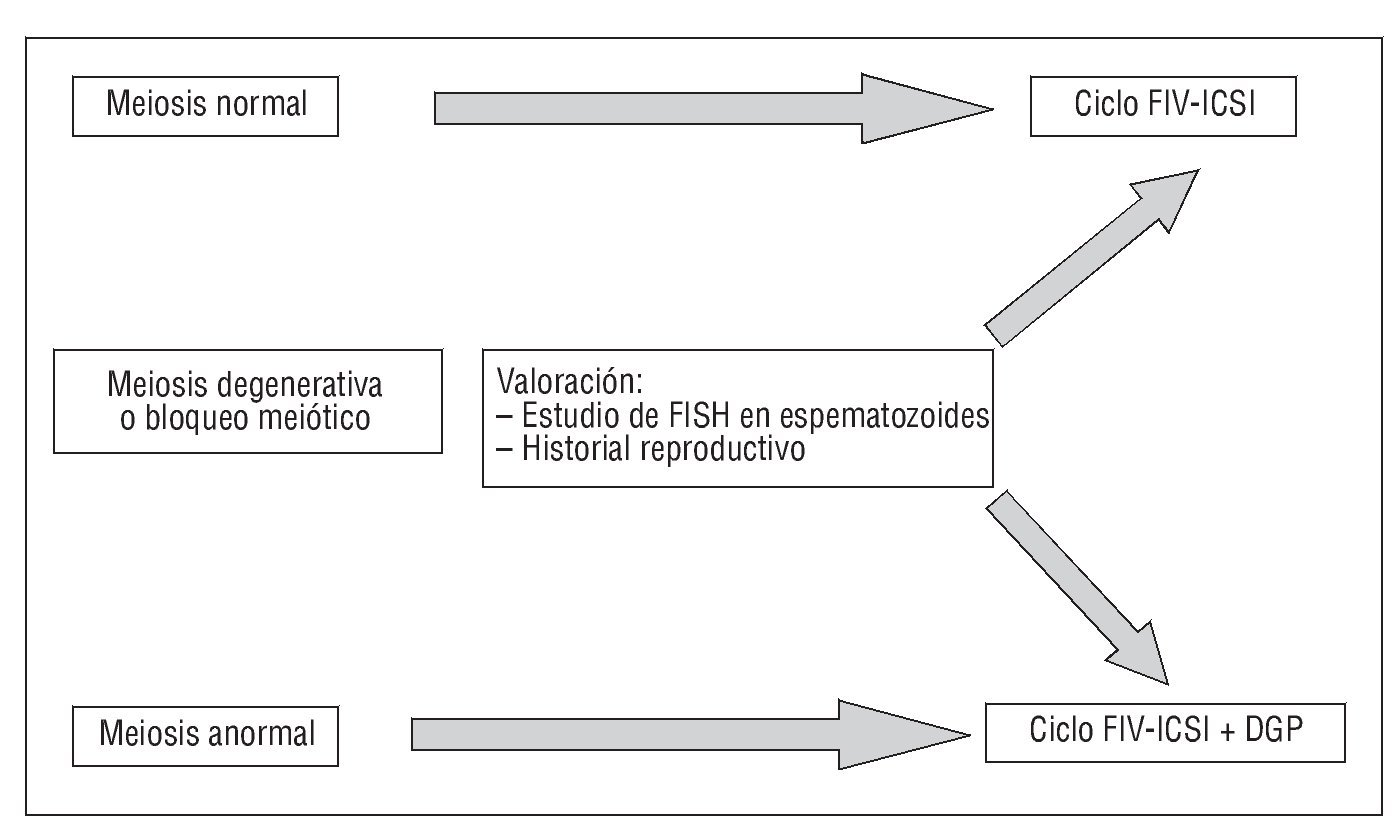
Figura 2. Diagnóstico, interpretación y orientación terapéutica. DGP: diagnóstico genético preimplantacional; FISH: fluorescent in situ hybridization; FIV: fecundación in vitro; ICSI: inyección intracitoplasmática de espermatozoides.
En los casos en que las profases I, las metafases I o las metafases II observadas presentan características normales, la conclusión será de meiosis normal y es de esperar la producción de espermatozoides normales.
La presencia casi exclusiva de estadios de profase I temprana es indicativa de un bloqueo en fases iniciales espermatocito primario. Los bloqueos meióticos constituyen uno de los capítulos más intrigantes en la patología de la esterilidad masculina. La presencia de bloqueos en las distintas fases de la espermatogénesis es un problema bien conocido por los anatomopatólogos, pero su etiología aún no se ha dilucidado. Aunque los bloqueos meióticos se han relacionado con la activación de puntos de control del ciclo celular debido a anomalías sinápticas5, la ausencia de imágenes o datos que lo confirmen no permite un diagnóstico completo a partir del estudio meiótico.
La observación de profases I, metafases I y/o meta-fases II con anomalías sinápticas, lleva a la conclusión evidente de que el proceso de meiosis es anormal. En función del grado de afectación y de activación de los sistemas de control del proceso de meiosis/espermatogénesis, puede producirse un bloqueo del ciclo celular y un proceso marcado de apoptosis (pudiendo derivar en un bloqueo madurativo, azoospermia, oligozoospermia e incluso normozoospermia), dar lugar a la producción de espermatozoides con anomalías cromosómicas o resultar en la producción de espermatozoides normales.
Las imágenes de metafases I y/o metafases II de aspecto degenerativo son difíciles de valorar en cuanto a la normalidad del proceso de meiosis. La imposibilidad de diferenciar entre fenómenos de apoptosis (que sería indicador de un control celular estricto, que implicaría no progresión meiótica y riesgo mínimo de producción de espermatozoides anormales) y la presencia de múltiples anomalías sinápticas (que pueden permitir la progresión meiótica de algunas célula y dar lugar a espermatozoides aneuploides o diploides) complican la interpretación de estos resultados. Especialmente en esta última situación, los estudios citogenéticos de FISH (del inglés, fluorescent in situ hybridization) en espermatozoides podrían ser un complemento especialmente útil para establecer un diagnóstico6,7.
En todos los casos, para poder ofrecer un consejo genético y reproductivo adecuado, los resultados de los estudios meióticos deben integrarse y valorarse en el contexto de la historia clínica de cada pareja.
INDICACIONES
Como se ha citado anteriormente, la incidencia de anomalías sinápticas en la meiosis de varones infértiles o estériles es de un 6-8%1,2. En pacientes con oligoastenozoospermia severa (< 1,5 [H11003] 10 móviles/ml) se ha descrito una incidencia de 17,6%8,9. Estudios recientes10,11 ya indican una incidencia del 20,4% en oligoastenoteratozoospermias, del 18% en astenoteratozoospermias y de hasta un 27% en pacientes normozoospérmicos con uno o más fallos previos de fecundación in vitro.
La presencia de anomalías sinápticas se ha relacionado con la producción de espermatozoides aneuploides o diploides en casos de abortos de repetición, fracasos de fecundación, bajas tasas de fecundación, anomalías cromosómicas en embriones, desarrollo embrionario lento, bloqueo embrionario y abortos preclínicos12-16. Por ello, las indicaciones para realizar un estudio meiótico serían:
A. Según el patrón seminológico.
- Oligoastenoteratozoospermia severa/moderada.
- Astenoteratozoospermia severa/moderada.
- Azoospermia (especialmente no obstructiva).
B. Con independencia del patrón seminológico.
- Esterilidad de larga evolución sin diagnóstico.
- Abortos de repetición.
- Fracasos repetidos en TRA.
El estudio de meiosis en biopsia testicular es de utilidad en el diagnóstico de la esterilidad de causa masculina. En muchos casos resolverá interrogantes de la historia reproductiva previa de la pareja, en otros muchos evitará que la pareja se agote psicológica, física y económicamente pudiendo decidir, tras un diagnóstico, un pronóstico y un consejo genético apropiado entre las diferentes opciones reproductivas que se presentan (donación de gametos, diagnóstico genético preimplantacional, donación de embriones, adopción, etc.).
A pesar de la información que aportan los estudios meióticos, es evidente que no se debe olvidar el papel de otros estudios (cariotipo, análisis de deleciones en el cromosoma Y, estudio del gen CFTR, FISH en espermatozoides, valoración de fragmentación del ácido desoxirribonucleico [ADN] espermático, etc.)17,18 para orientar cada caso particular e intentar aumentar la probabilidad de que la pareja alcance su objetivo que no es un embarazo sino un hijo nacido sano.
CONCLUSIONES
Los resultados del estudio de meiosis en biopsia testicular ponen de relieve la importancia del estudio del factor masculino y permiten obtener un diagnóstico etiológico y establecer un pronóstico de fertilidad. Integrados en la historia clínica de cada pareja, ofrecen información relevante para orientar el consejo genético y ayudar en la toma de decisiones de alternativas terapéuticas.
Correspondencia:
Dra. S. Egozcue Vilarasau.
Laboratorio Egozcue Genetics.
Numancia, 95-97. 08029 Barcelona. España.
Correo electrónico: 31059sev@comb.cat