INTRODUÇÃO
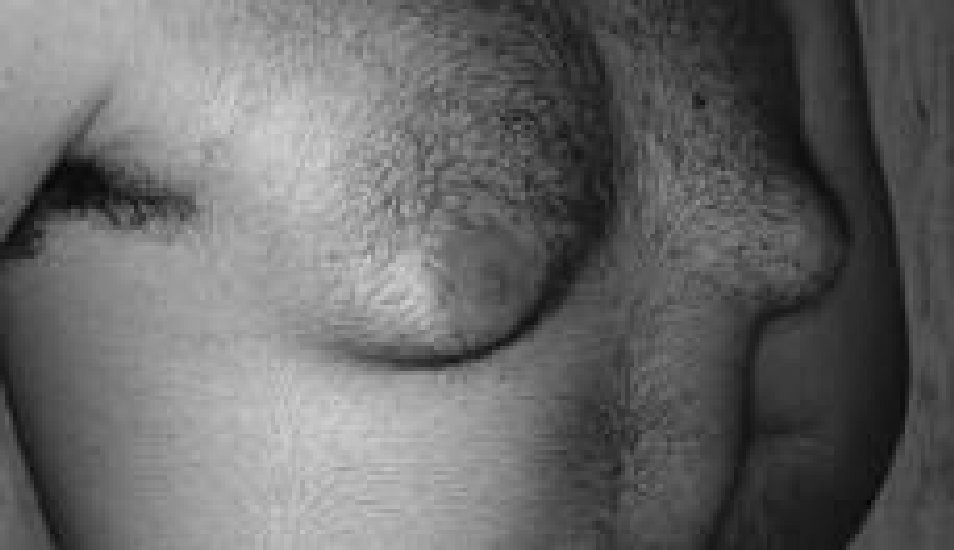
A ginecomastia (fig. 1) resulta do desenvolvimento do componente glandular da mama no sexo masculino. É considerada fisiológica1 no período neonatal, na puberdade e acima dos 60 anos.
Figura 1. Ginecomastia em adulto jovem.
Na presença de aumento do volume mamário, no homem, devem excluir-se outras patologias, tais como o carcinoma da mama masculina, a pseudo-ginecomastia (prevalente nos obesos, onde não existe a proliferação do tecido glandular da mama mas sim dos adipócitos), neurofibroma, lipoma ou quisto dermóide mamário. Em 50% dos casos a ginecomastia tem etiologia idiopática e resulta do excesso, absoluto ou relativo, de estrogéneos circulantes.
Além da etiologia idiopática, a ginecomastia pode estar presente em diferentes situações como:
- Terapêutica com antiandrogéneos, estrogéneos, espironolactona, isoniazida, digitálicos, esteróides anabolizantes, cimetidina, ranitidina, inibidores da protease, omeprazol, diazepam, antidepressivos tricíclicos, teofilina ou metildopa.
- No Síndrome de Klinefelter e outros hipogonadismos.
- Insuficiência hepática, renal ou desnutrição.
- Neoplasia pulmão, fígado ou supra renal.
- Hipertiroidismo.
- Tuberculose.
- Tumor do testículo (3%).
Os primeiros tumores de células de Leydig (TCL) foram descritos por Sacchi em 1895. São uma patologia rara, com 480 casos publicados na literatura mundial. São a neoplasia do estroma testicular mais frequente (1 a 3% dos tumores de testículo), com maior prevalência nas crianças, dos 3 aos 9 anos e nos adultos dos 30 aos 60. Cursam por vezes associados à síndrome de Klinefelter. Em 3% casos sNão bilateraìs.
Em 90% dos casos apresentam-se como uma massa testicular associada, ou não, a manifestações endócrinas (em 20 a 30% do total). Estes tumores têm um comportamento clínico benigno na maioria dos casos, mas em 10% dos casos metastizam, habitualmente, para os gânglios retroperitoneais, pulmão, fígado e osso.
Os TCL podem apresentar diversos padrões histológicos, embora, sejam frequentemente compostos por células poligonais com citoplasma eosinófílico abundante, de limites celulares bem definidos (fig. 2), tendo em 30 a 40% dos casos inclusões de cristais intracitoplasmáticos (cristais de Reinke).
Figura 2. Tumor de células de Leydig - Células poligonais com abundante citoplasma eosinofílico.
São considerados sinais histopatológicos de malignidade: a presença de atipia citológica, índice mitótico superior a 3 por campo de grande ampliação, aneuploidia, expressão aumentada de MIB-1, necrose, sinais de invasão vascular, infiltração extra testicular ou tumores superiores a 5 cm. No entanto o único critério seguro é o aparecimento de metástases.
As manifestações endócrinas são variáveis e de acordo com a idade: androgenização precoce na infância e feminização na idade adulta2. A ginecomastia é o sinal mais proeminente nestes doentes. A sua etiologia não está completamente esclarecida, existindo várias considerações teóricas acerca deste assunto. A sua evolução pós tratamento é variável, sendo frequente a regressão espontânea.
Os autores relatam a experiência clínica do seu Serviço com esta síndrome.
METODOLOGIA
Estudo retrospectivo dos doentes com TCL seguidos no Serviço de Urologia entre Janeiro de 1993 e Abril de 2008. Revisão da história clínica, estudo hormonal, terapêutica, seguimento e evolução da ginecomastia.
RESULTADOS
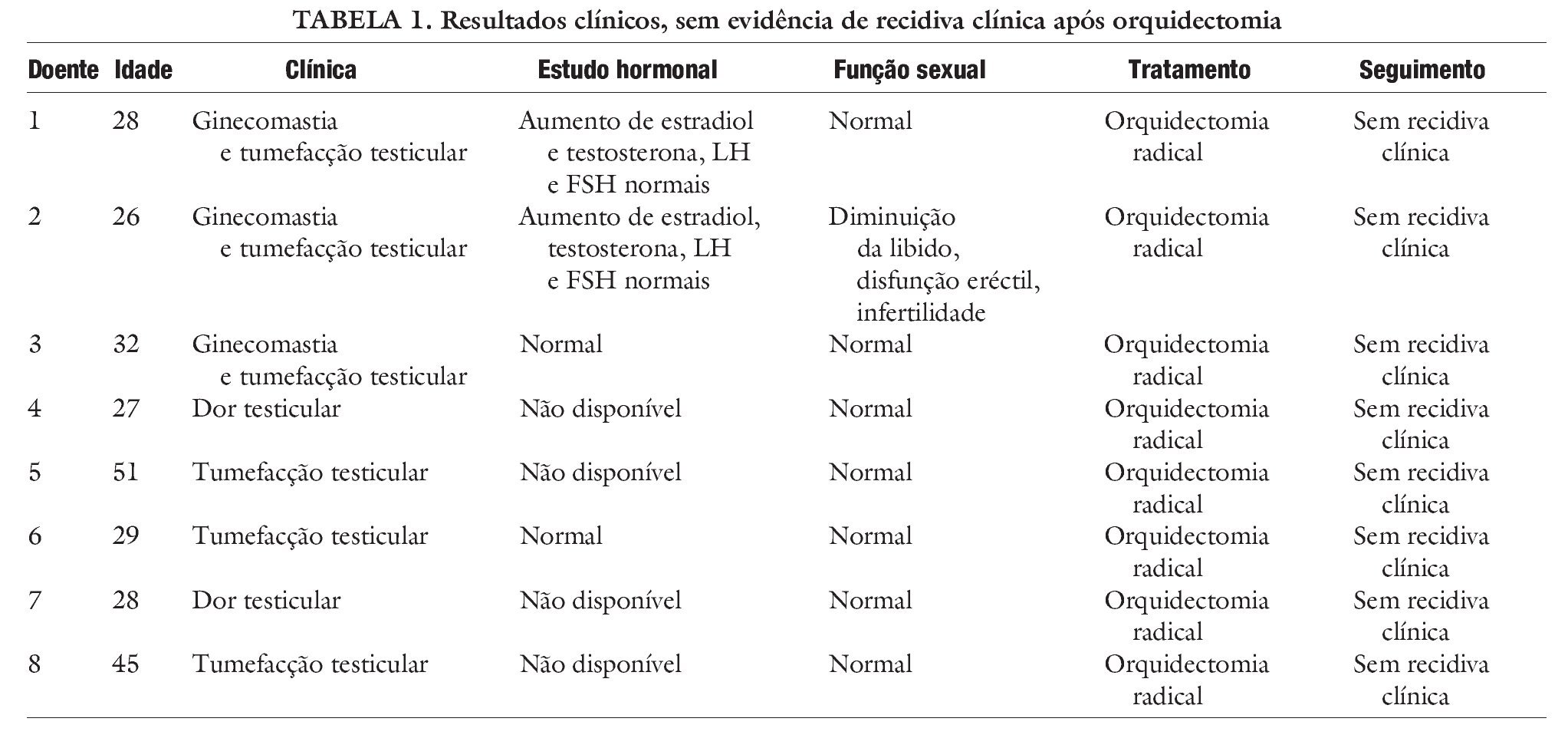
Foram avaliados 8 doentes com idade média de 33,0 ± 9,5 anos, um follow-up médio de 59,9 ± 72 meses. Três tinham recorrido à consulta (tabela 1) por ginecomastia e tumefacção testicular; outros 3 tinham apenas tumefacção testicular palpável e os restantes 2 referiam desconforto testicular e apresentavam um nódulo testicular na ultrassonografia.
Os marcadores tumorais (gonadotrofina coriónica [beta-HCG*], alfa-fetoproteína e DHL), efectuados em todos os doentes, encontravam-se dentro dos parâmetros normais. No estadiamento, a Tomografia axial computorizada abdominopélvica, e a radiografia de tórax, não mostravam sinais de doença metastizada.
Nos doentes com aumento do volume mamário (1-3, n = 3), o estudo hormonal revelou aumento do estradiol - 126,6 pg/ml (normal inferior a 56 pg/ml) e diminuição da testosterona total - 2,02 ng/ml (normal superior a 2,41 ng/ml) num caso. Este evoluiu com diminuição da líbido e disfunção eréctil. Noutro doente, existia aumento do estradiol (114 pg/ml) e testosterona total normal (3,15 ng/ml). Num doente os valores de estradiol (37 pg/ml) e testosterona total (4,39 ng/ml) eram normais.
Nos restantes doentes (casos 4-8, n = 5) o diagnóstico definitivo foi obtido pós-orquidectomia, não tendo sido efectuados estudos hormonais pré operatórios. Todos os doentes foram submetidos a orquidectomia radical. Nos 2 casos em que foi identificado um nódulo testicular por ultrassonografia foi efectuada, inicialmente, uma abordagem por via inguinal com clampagem do cordão espermático e tumorectomia sob controlo ecográfico. Os resultados dos exames anatomopatológicos extemporâneos eram suspeitos de lesões malignas, embora sem diagnóstico definitivo, pelo que, perante a possibilidade de um tumor de células germinativas testiculares se efectuou orquidectomia radical.
As alterações hormonais normalizaram após a orquidectomia. Num caso, as alterações sexuais reverteram espontaneamente após a cirurgia, embora mantenha infertilidade. Num doente a ginecomastia regrediu espontâneamente um ano após a orquidectomia (caso 2). Em dois casos não houve regressão clínica, tendo um doente sido submetido a mastectomia, e outro recusado tratamento cirúrgico complementar.
DISCUSSÃO
Os estrogéneos séricos no sexo masculino provêm da conversão periférica de androstenediona e testosterona em estradiol (75 a 90% do total), sendo que os restantes (10 a 25%) provêm da produção directa no testículo. A aromatização da testosterona circulante em estradiol ocorre nas células de Sértoli, na idade pré-pubertária, e nas células de Leydig em idade posterior.
Este aspecto pode ser responsável pelos diferentes padrões semiológicos de apresentação dos tumores de células de Leydig. Na infância há, provàvelmente, a produção excessiva de testosterona pelas células tumorais responsável pela pubarquia prematura, aumento do tamanho do pénis, acne, aumento da massa muscular, etc. Na idade adulta existe um défice relativo dos níveis de testosterona com aparecimento de ginecomastia, impotência, diminuição da líbido, atrofia testicular contralateral, alterações da espermatogénese e infertilidade. Este estado mantido de hiperestrogenismo, que condiciona as manifestações endócrinas nos adultos, pode ser devido à produção excessiva de estradiol e/ou à aromatização da testosterona circulante pelas células tumorais, o que conduz a um aumento da percentagem de estradiol biodisponível em relação à testosterona circulante. Os níveis de estrogéneos são variáveis, inclusivé no mesmo doente, sugerindo uma produção estrogénica tumoral intermitente.
Neste tipo de tumores, em fase pré-pubertária, não há registo de malignidade, não sucedendo o mesmo na idade adulta. Na nossa série a prevalência de ginecomastia foi superior à descrita habitualmente, com estudo hormonal normal num doente e hiperestrogenismo em dois.
Houve 2 casos em que, apesar da normalização dos níveis hormonais, não houve regressão clínica espontânea da ginecomastia. Na ausência de recidiva tumoral este facto poderá estar relacionado com fenómenos de fibrose e hialinização periglandular ao nível do tecido mamário, comprometendo a regressão clínica espontânea1.
A ginecomastia pode preceder o aparecimento do tumor, em meses ou anos, e a sua presença é considerada um factor de bom prognóstico3. Regride espontâneamente em 80% dos casos após o tratamento definitivo do tumor primitivo, em semanas ou meses, de acordo com o tempo de normalização das alterações hormonais. Nos 20% restantes não há regressão espontânea, estando aconselhado o tratamento cirúrgico. Este não deve ser efectuado antes do final do primeiro ano de seguimento, pois a evolução das alterações hormonais durante este período de tempo podem ser utilizadas como um marcador de cura ou recidiva tumoral.
Os dados recentemente publicados na literatura sugerem bom controle oncológico com orquidectomia parcial4 sob controle ecográfico, em doentes com diagnóstico pré ou per-operatório de TCL, sem sinais clínicos ou histopatológicos de mau prognóstico. A população infértil tem maior incidência de tumores testiculares assintomáticos pelo que a cirurgia poupadora-de-orgão pode contribuir para a manutenção da actividade endócrina do testículo.
Estas neoplasias são quimio e radioresistentes e em casos de metastização está indicada a realização de linfadenectomia retroperitoneal5.
Os TCL têm comportamento benigno na maioria dos casos. Em doentes com ginecomastia, de causa não esclarecida deve ser excluída esta patologia testicular. A persistência da ginecomastia, após a orquidectomia, e sem evidência de recidiva tumoral, tem indicação para correcção. O tumor de células de Leydig é raro, pelo que a estratégia de seguimento não está padronizada, sugerindo-se um follow-up a longo prazo pela possibilidade de recidiva tardia.
CONFLITOS DE INTERESSE
Os autores não têm quaisquer conflitos de interesse a declarar.
Correspondência:
Dr. F. Carlos Afonso Vila.
Rua Isolino Domingues da Silva, 220, 2.º E. 4470-773 Vila Nova da Telha. Portugal.
Correio electrónico: fernandovila1@gmail.com