El Dolor Neuropático (DN) se origina como consecuencia directa de una lesión o enfermedad que afecta al sistema somatosensorial, es un problema importante de Salud Pública y una condición común, crónica, debilitante que afecta a un número signifi cativo de pacientes. La presencia del DN es sugerida por la historia clínica y el examen físico, con una localización del dolor neuroanatómicamente lógica y evidencia de daño del sistema nervioso. Los médicos de atención primaria tienen un rol crucial en realizar el diagnóstico de DN posible, evitar los retrasos en el diagnóstico y proveer una apropiada evaluación, manejo y/o oportuna derivación al especialista para mejorar los resultados, reducir los costos humanos a los pacientes, aliviando el dolor y la discapacidad subsecuente, y costos económicos a la sociedad. Debemos por lo tanto educar a los médicos generales en la detección, el diagnóstico y el manejo inicial del DN.
Neuropathic pain (NP) arising as a direct consequence of a lesion or disease affecting the somatosensory system, is an important public health problem and a common, chronic, debilitating condition that affects a signifi cant number of patients. The presence of NP is suggested by the clinical history and physical examination, revealing a location of pain that is neuroanatomically logical, with evidence of damage to the nervous system. The primary care physicians have a crucial role in the diagnosis of possible NP, avoid delays in diagnosis and provide appropriate assessment, management and / or referral to the appropriate specialist to improve outcomes, reduce the human costs to patients, relieving pain and subsequent disability and economic costs to society. We must therefore educate general practitioners in the detection, diagnosis and initial management of NP.
El objetivo de este artículo es destacar la importancia de los médicos de atención primaria de salud en el diagnóstico y tratamiento del dolor neuropático y aportar en la educación respecto de elementos básicos de su evaluación y manejo.
Definición de dolor neuropático (DN)El dolor neuropático (DN) se define como aquel dolor originado como consecuencia directa de una lesión o enfermedad que afecta al sistema somatosensorial(1). El dolor neuropático puede originarse del daño de las vías nerviosas en cualquier punto desde las terminales nerviosas de los nociceptores periféricos a las neuronas corticales del cerebro, siendo clasificado como central - cuando afecta el cerebro o médula espinal -y periférico- cuando se origina en el nervio periférico, plexo, ganglio dorsal o raíces. Según su distribución, el dolor neuropático se clasifica en localizado o difuso. Se define como dolor neuropático localizado al que se caracteriza por área(s) consistentes y circunscritas de máximo dolor asociado con signos sensitivos positivos o negativos y/o síntomas espontáneos característicos de dolor neuropático como dolor quemante (2). El dolor neuropático también se clasifica en base a la etiología del daño al sistema nervioso (tabla 1).
Clasificación del dolor neuropático
| Localización | Central (médula espinal, tronco cerebral, tálamo y corteza) Periférico (nervio, plexo, ganglio raíz dorsal, raíz) |
| Distribución | Localizado (área bien delimitada y consistente de máximo dolor) Difuso |
| Etiología | Trauma Isquemia o Hemorragia Infamación Neurotoxicidad Neurodegeneración Paraneoplásico Metabólico Défcit vitamínico Cáncer |
| Mecanismos | Descargas ectópicas Pérdida de inhibición Sensibilización Periférica Sensibilización Central |
Adaptado de IASP. Pain Clinical Updates. 2010 (24).
La prevalencia exacta del dolor neuropático es desconocida. En Europa el 20% de la población sufre de dolor crónico (3), de ellos 7% a 8% sufren de dolor predominantemente neuropático(4, 5), lo que equivale actualmente a 50 millones de personas, con una incidencia anual de casi el 1% de la población (6), de ellos solo el 40 a 60% logran un adecuado alivio del dolor (3). En Latinoamérica se observó que el 2% de la población general sufre de DN, cifra muy probablemente subestimada (7).
Independiente de la etiología, los pacientes con dolor neuropático experimentan dolor más severo que los pacientes sin él, con una intensidad de 6,4 versus 4,6 en una escala de 0 al 10 (4, 8) y en el 60% de los casos el dolor neuropático es localizado (2).
La depresión, ansiedad y trastornos del sueño son también significativamente más prevalentes en pacientes con dolor neuropático comparado con otros tipos de dolor (9). Es así como el impacto del dolor neuropático en diversos aspectos de la vida es relevante, 41% de los pacientes han sufrido dolor por más de 5 años, 60% tiene trastornos del sueño, 34% se siente deprimido, 25% está ansioso, 27% se siente constantemente debilitado, 65% ha restringido sus actividades diarias y 82% refiere impacto significativo en su calidad de vida debido al dolor (10).
Las condiciones que pueden llevar a dolor neuropático se muestran en la tabla 2, destacando la alta prevalencia de dolor neuropático en los pacientes diabéticos, con dolor lumbar y en pacientes post-operadas de cáncer de mama.
Condiciones de riesgo de dolor neuropático
| Condición | Epidemiología |
|---|---|
| Dolor Neuropático periférico | |
| Radiculopatía (lumbosacra, torácica o cervical) | 37% pacientes con Dolor Lumbar |
| Polineuropatía (diabética, alcohólica, post-quimioterapia, VIH) | 16% pacientes con Diabetes Mellitus 26% pacientes con Diabetes Mellitus 2 |
| Neuralgia post-herpética | 8% pacientes post Herpes Zoster |
| Neuralgia post-quirúrgica (dolor post-mastectomía) | 30-40% post cirugía cáncer mama |
| Trauma Nervio Periférico | 5% después de lesión n. Trigémino |
| Neuropatía Compresiva | Desconocida |
| Neuralgia Trigeminal | Incidencia 27/100.000 personas-año |
| Dolor Neuropático Central | |
| Accidente Vascular Cerebral | 8% pacientes con AVC |
| Esclerosis Múltiple | 28% pacientes con EM |
| Lesión Medula Espinal | 67% pacientes con LM |
| Dolor Miembro Fantasma | Incidencia 1/100.000 personas-año |
Adaptado de Haanpää y col. Am J Med 2009 (9).
Respecto de los pacientes diabéticos, el 85% de ellos tiene síntomas neurológicos pero solo la mitad se clasifica como neuropatía diabética por su médico tratante (11), un tercio de los diabéticos con dolor no han recibido nunca tratamiento para su DN(12). Cabe destacar que los diabéticos con neuropatía diabética dolorosa reportan significativamente menor calidad de vida comparados con aquellos sin dolor o con dolor de otro tipo (13).
El dolor post-traumático y post-quirúrgico si no son bien tratados en la fase aguda tienen potencial de progresión a dolor neuropático crónico (5, 14). El 1 a 3% de los pacientes de los pacientes sometidos a cirugía general u ortopédica cursan con dolor neuropático, siendo necesario reconocer y manejar el dolor neuropático agudo en el perioperatorio para poder aliviarlo (15, 16). Entre los pacientes con lesiones traumáticas de nervio periférico, el 66% tiene dolor y el 50% de ellos es de tipo neuropático (17). En pacientes amputados, el DN puede alcanzar hasta el 85% de los casos (18).
Importancia de la atención primaria en salud y el dolor neuropáticoEn la mayoría de los Sistemas de Salud, la atención primaria es la “puerta de entrada”, proveyendo acceso a los servicios especializados de la atención secundaria. En el Reino Unido, alrededor del 90% de las atenciones del Servicio Nacional de Salud se realizaron en la atención primaria, y en promedio cada individuo consulta a su médico general 5,5 veces por año. El dolor es motivo del 40% de las consultas de pacientes en la atención primaria cada año y aproximadamente 20% de estos pacientes ha experimentado dolor por más de 6 meses(19), incluyendo un porcentaje importante de pacientes con dolor neuropático.
En promedio en Europa hay un especialista en dolor por cada 140 pacientes con dolor crónico. Si el médico especialista en dolor evaluara todos los pacientes con DN debería ver un millón de pacientes por año, 330.000 de los cuales sufren de DN. Se requerirían 150 años de médico algólogo para ver todos los pacientes con DN en Europa (20). Actualmente, menos del 1% de los pacientes que sufre dolor crónico (3) y solo el 0,15% de la población (21) se atiende en clínicas especializadas de dolor.
El dolor, incluyendo el DN, es por ello una condición observada principalmente en la atención primaria de salud (APS). Junto con el progresivo conocimiento sobre el dolor neuropático y su prevalencia, el médico APS ha adquirido relevancia en el diagnóstico y tratamiento de éste.
Actualmente hay consenso de cómo se debe evaluar el DN en la atención primaria (19). Aunque esta evaluación detallada no puede ser realizada completamente durante la primera consulta, puede iniciarse en ella, siendo el factor más importante tener presente y contemplar dentro del diagnóstico diferencial la posibilidad de existencia de dolor neuropático.
Las razones principales por las cuales el médico APS es relevante en el manejo del DN son: El dolor neuropático (DN) es común, el DN tiene una alta prevalencia en la atención primaria de salud, el reconocimiento del DN es posible para cualquier médico clínico interesado después de un entrenamiento adecuado, el tratamiento del DN debe ser realizado sin retraso, la farmacoterapia con agentes de primera línea es simple y adecuada para médicos no especialistas, el apoyo del paciente es más fácil en la atención primaria de salud y el seguimiento es más factible en el lugar habitual de atención del paciente.
En Finlandia se lanzó en 2005 el Acceso a la Ley del Cuidado de la Salud, donde el dolor crónico fue incluido el 2007 (20), éste indica que el médico de atención primaria de salud (APS) es el principal responsable del tratamiento del dolor crónico. El médico APS es responsable por:
- -
Diagnosticar el tipo de dolor (nociceptivo, neuropático, combinación, ninguno de ellos)
- -
Diagnosticar la enfermedad que causa el dolor
- -
Aliviar el dolor y tratamiento de la enfermedad causal
- -
Evaluar la capacidad de trabajo
- -
Apoyar el enfrentamiento del dolor crónico por parte del paciente.
- -
Organizar la rehabilitación cuando es necesario.
El dolor neuropático frecuentemente es subdiagnosticado y subtratado (22, 23).
Realizar un diagnóstico identificando el tipo y origen del dolor e instituir un manejo precoz y apropiado logra resultados en salud y efectos costo-beneficiosos en la sociedad.
Frente a la sospecha de dolor neuropático, la evaluación debe considerar la historia y examen clínico, el diagnóstico de la enfermedad o evento causal y la evaluación del impacto del dolor sobre la funcionalidad (24).
- •
Reconocer el dolor neuropático: Historia
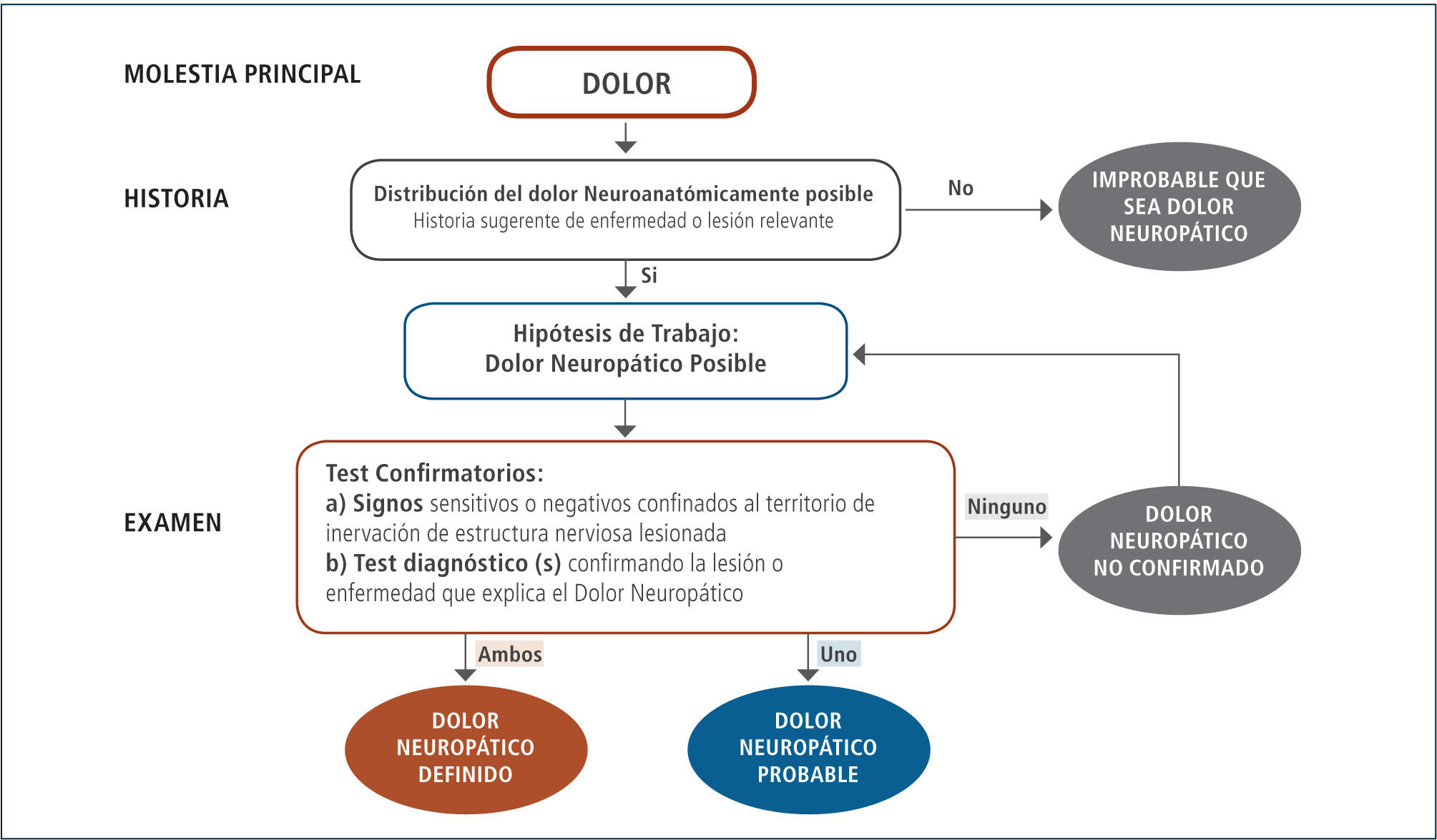
La historia debería incluir preguntas sobre la localización, intensidad, carácter y perfil temporal del dolor, junto con posibles factores desencadenantes. Los síntomas concomitantes deberían ser consultados. El proceso diagnóstico del dolor neuropático se aprecia en la figura 1, que considera como hipótesis de trabajo el dolor neuropático posible en base a una historia compatible y su localización con una distribución neuroanatómicamente posible y lógica, esto es dolor percibido dentro del territorio de inervación de un nervio, raíz o vía dañada de acuerdo a la organización somatotópica de la corteza somatosensorial primaria, la cual puede confirmarse por examen clínico y exámenes complementarios. Los dibujos del dolor son también un buen instrumento para documentar la localización. La intensidad del dolor puede ser evaluada por la escala de evaluación verbal y numérica (de cero a diez), considerando leve: 1-3; moderado: 4-6 y severa: 7-10 puntos.
Un equipo especializado en DN de Alemania (DFNS) estudió 8.000 pacientes con DN, observando diferentes patrones de dolor entre ellos aquellos con dolor persistente con leves fluctuaciones, con dolor persistente y con ataques de dolor agregado y pacientes con ataques de dolor y períodos sin dolor. En el caso que existan dos componentes de dolor -dolor persistente y ataques de dolor- la intensidad de ambos componentes deberían ser evaluados separadamente (25).
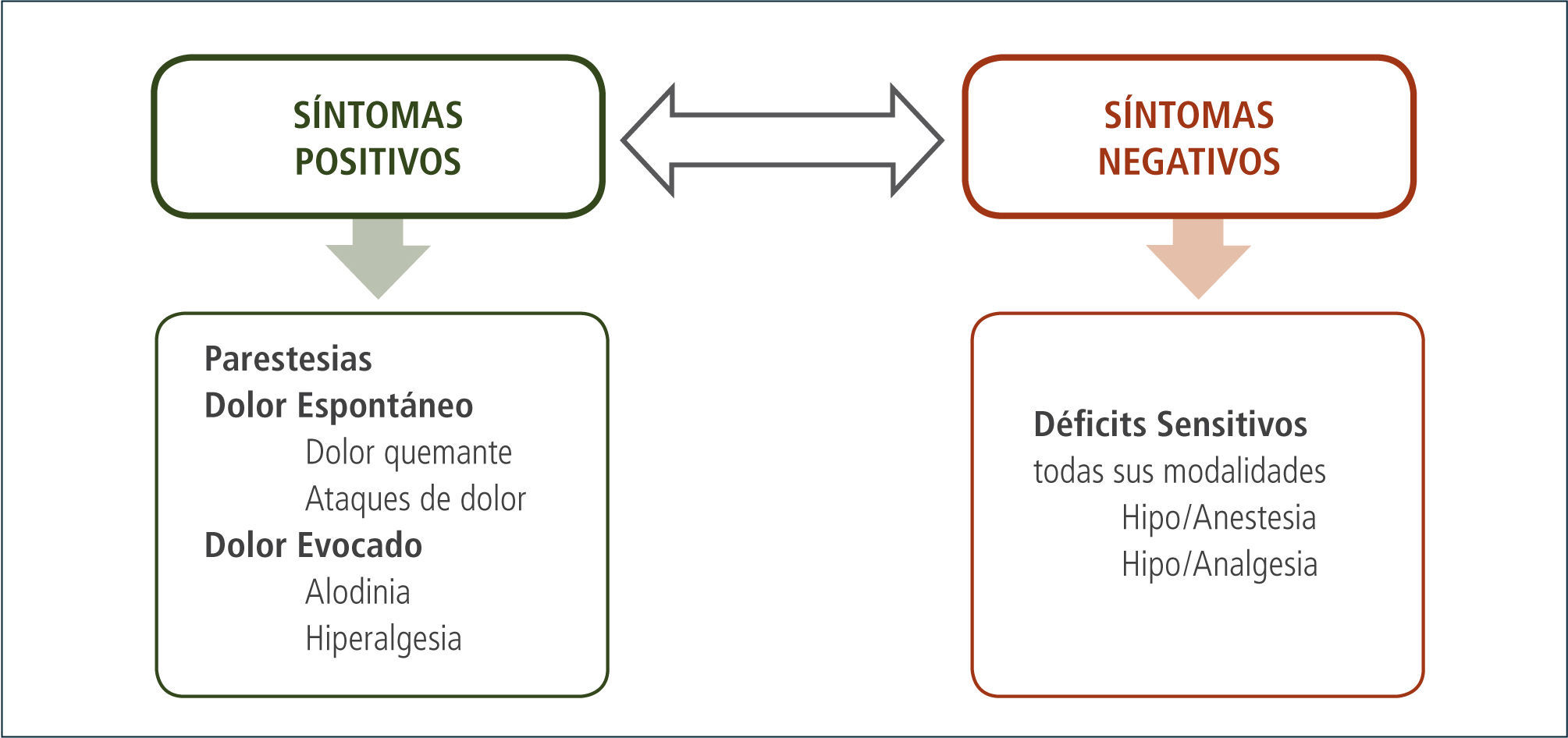
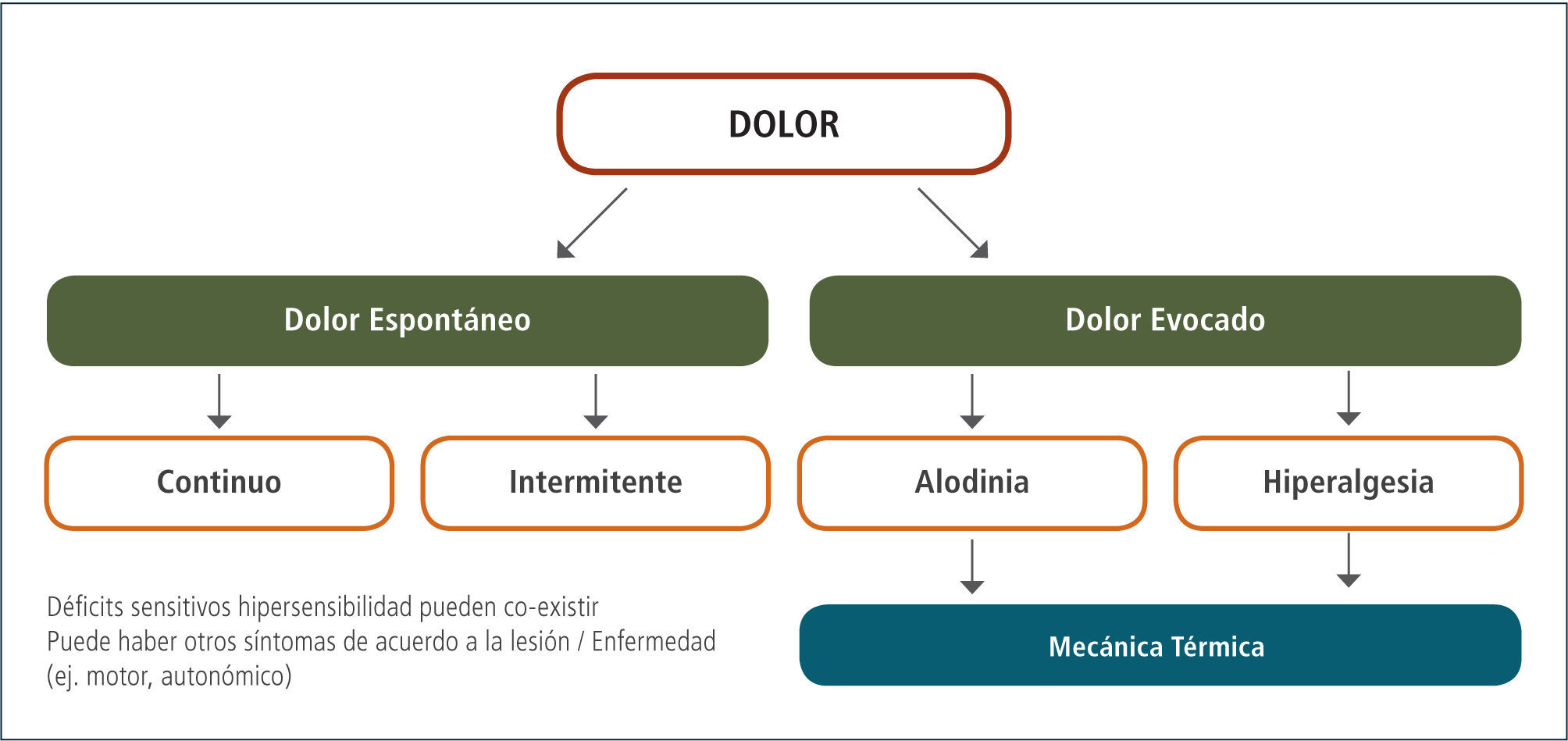
El dolor neuropático está caracterizado por dolor espontáneo y provocado, por síntomas positivos como parestesias y disestesias y signos negativos o déficits sensoriales, reflejando el daño neural (figuras 1 y 2, tabla 3). Aunque se describe a menudo como quemante, ninguna característica única del dolor es diagnóstica de dolor neuropático. Sin embargo, combinaciones de ciertos síntomas o descriptores del dolor, aumentan la posibilidad de diagnosticarlo (26).
Características Comunes Sugestivas De Dolor Neuropático
| Término | Definición |
|---|---|
| Síntomas | |
| Parestesias | Sensaciones positivas no dolorosas (hormigueo) |
| Dolor Quemante | Sensaciones de dolor espontáneo cualitativo frecuente |
| Dolor Punzante | Sensación dolorosa intensa espontánea o evocada de segundos de duración |
| Signos | |
| Hipoestesia | Sensibilidad disminuida a un estímulo |
| Hipoestesia Tactil | Sensibilidad disminuida a un estímulo táctil |
| Hipoestesia al Frío | Sensibilidad disminuida al frío |
| Hipoalgesia | Sensibilidad disminuida a un estímulo doloroso normal |
| Hiperalgesia | Sensibilidad aumentada al dolor |
| Hiperalgesia puntiforme | Hiperalgesia a un estímulo puntiforme como es pinchazo |
| Hiperalgesia Estática | Hiperalgesia a presión roma |
| Hiperalgesia al Calor | Hiperalgesia a estímulo caluroso |
| Hiperalgesia al Frío | Hiperalgesia a estímulo frío |
| Alodinia | Dolor debido a un estímulo no nociceptivo (no doloroso) |
Adaptado de Scadding JW, Treede RD. Handbook of Clinical Neurology 2006 (37).
Las herramientas de detección en base a cuestionarios simples, completados tanto por pacientes como clínicos, pueden ser usados para alertar al médico sobre la necesidad de un examen cuidadoso para la pesquisa de dolor neuropático (27) (tabla 4). El Cuestionario DN4 (28) tiene sensibilidad de 83%, especificidad de 90% y valor predictivo positivo de 89,5%, siendo es el instrumento de detección de elección en nuestro medio, dada su fácil aplicación y validación al español (29).
Ítems comunes de distintas herramientas de detección de dolor neuropático
| LANSS | DN4 | NPQ | painDETECT | ID pain | |
|---|---|---|---|---|---|
| Punzante, hormiguero | X | X | X | X | X |
| Golpe eléctrico, disparo | X | X | X | X | X |
| Caliente, quemante | X | X | X | X | X |
| Adormecimiento | X | X | X | X | |
| Dolor evocado por tacto suave | X | X | X | X | |
| Frío doloroso, dolor congelante | X | X | |||
| Cambios autonómicos | X | ||||
| Alodinia cepillado | X | X | |||
| Umbral aumentado al tacto suave | X | ||||
| Umbral aumentado al pinchazo | X | X |
Adaptado de Bennett MJ et al. Pain 2007 (27).
LANSS (*): Leeds Assessment of Neuropathic Symptoms and Signs
DN4 (#): Douleur Neuropatique 4 questions
NPQ (&): The Neuropathic Pain Questionnaire
Sin embargo, una herramienta de detección no debe reemplazar el examen clínico cuidadoso (30).
- •
Localizar la lesión: Examen neurológico
El examen clínico permite establecer la concordancia entre la historia, la distribución del dolor y otros signos neurológicos, y con ello un diagnóstico posible de dolor neuropático, de acuerdo a lo señalado previamente en la figura 3.
Diagrama de flujo de sistema de graduación para dolor neuropático
Adaptado de Treede RD y col. Neurology 2008 (1).
Identificar una enfermedad o lesión del sistema nervioso se basa en la búsqueda sistemática de anormalidades neurológicas en el examen físico. La evaluación sensitiva, guiada por la historia de localización del dolor incluye la evaluación funcional de diferentes fibras sensitivas con herramientas sencillas como un trozo de algodón, cepillo, mondadientes y diapasón. Los hallazgos en el área dolorosa son comparados con hallazgos en el área contralateral en caso de dolor unilateral y en otros sitios en el eje proximal-distal en dolor bilateral. Adicionalmente al examen sensitivo, el clínico debe realizar una evaluación motora (fuerza muscular, tono, coordinación y fluidez del movimiento), examen de los reflejos tendinosos y nervios craneanos y evaluación del sistema nervioso autónomo periférico (calor y color de la piel, función sudomotora).
Actualmente, no hay guías para el diagnóstico y evaluación de DN para médicos no especialistas (20). Es por ello que debemos ayudar a desarrollar técnicas de evaluación que sean apropiadas para la atención primaria y que eviten el retraso en el diagnóstico del DN. Hemos desarrollado una herramienta sencilla de detección de DN localizado para médicos generales, actualmente en proceso de publicación, cuyos resultados en 31 médicos de atención primaria que evaluaron 2.079 pacientes de Barcelona han sido promisorios.
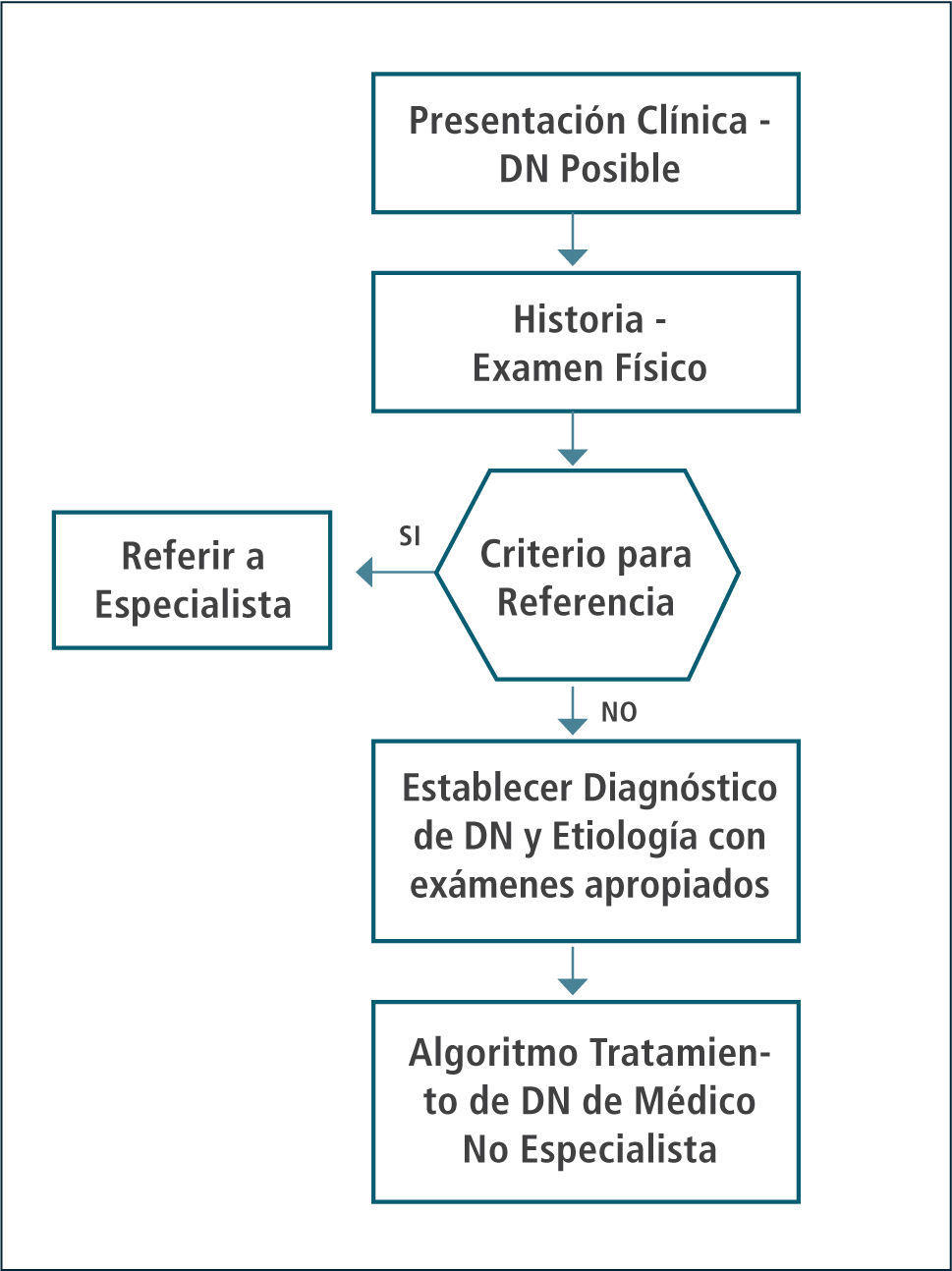
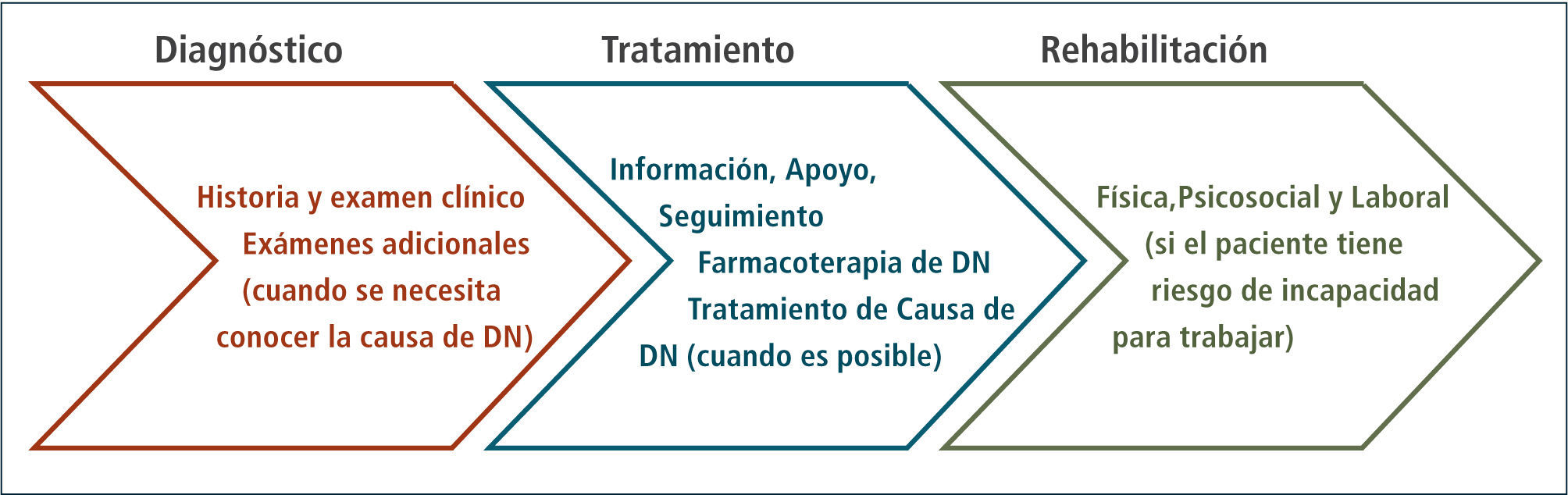
Un esquema general de evaluación y manejo precoz de dolor neuropático periférico por médicos generales se puede apreciar en la figura 4 (20).
Diagrama de flujo de sistema de graduación para dolor neuropático
Adaptado de Haanpää y col. EFIC 2013 (20).
- •
Diagnóstico de la enfermedad o evento causal:
A veces el diagnóstico es sencillo, como en el caso de DN después de una lesión quirúrgica conocida o neuralgia post-infección con herpes zoster. En estos casos no son necesarios exámenes adicionales. Si un paciente tiene dolor de localización en calcetín y guante, la polineuropatía puede ser documentada clínicamente.
La causa de la polineuropatía puede también ser determinada por exámenes de laboratorio que incluyen hemograma, velocidad de sedimentación, glucosa, creatinina, enzimas hepáticas, vitamina B12, electroforesis de proteínas séricas y función tiroidea. Otros exámenes diagnósticos deben ser solicitados por el médico especialista en dolor.
- •
Evaluar las limitaciones funcionales producidas a causa del dolor, siendo las más frecuentemente afectadas las actividades de la vida cotidiana (comer, asearse, vestirse), la marcha, subir y bajar escaleras y trastornos del sueño por dolor.
- •
Evaluar los aspectos psicosociales, trabajo, familia y vida social, necesarios para un manejo estratégico individualizado.
- •
Evaluar posibles co-morbilidades como ansiedad, depresión y discapacidad.
Los médicos APS frecuentemente refieren que debido al factor más limitante -10 minutos promedio de tiempo de consulta- la evaluación del dolor sería difícil de realizar dentro de su rutina diaria. Sin embargo, con un entrenamiento adecuado, se puede hacer un enfrentamiento diagnóstico integral para los pacientes afectados de DN que incluya una historia sucinta y examen clínico focalizado, con el conocimiento de la historia médica actual y remota del paciente. En estas condiciones, el médico general está en una excelente posición de diagnosticar dolor neuropático “posible”.
Diagnóstico diferencialUn tratamiento relevante es posible solo si el diagnóstico diferencial de la condición es realizada adecuadamente, por el contrario, un mal diagnóstico puede llevar al tratamiento en una dirección errada. Como ejemplo, la neuropatía diabética se puede confundir con claudicación intermitente, neuroma de Morton, osteoartritis, fasciitis plantar, radiculopatía y síndrome del túnel tarsiano, entre otros.
Manejo del dolor neuropáticoEl dolor neuropático crónico no tiene ningún efecto benéfico por lo cual debe ser tratado.
Su manejo debe ser un proceso fluido cuyo objetivo es la reducción del dolor, la mejoría funcional y de la calidad de vida (figura 5).
El manejo del dolor neuropático es un proceso fluido con el objetivo de reducir el dolor y mejorar la función
Adaptado de haanpää m, efic 2013 (20).
- 1)
Tratamiento precoz:
Los pacientes que sufren de dolor crónico empeoran mientras esperan tratamiento (32). En encuesta realizada en EEUU en 1.922 pacientes con DN periférico, 57% demoró dos o más años en tener un diagnóstico preciso. Las consecuencias psicosociales fueron el deterioro del ánimo, pérdida del rol social y empeoramiento de la capacidad laboral.
Por la naturaleza penosa del dolor neuropático, es inapropiado retardar la terapia que pueda brindar alivio por lo cual el tratamiento sintomático debería comenzar precozmente mientras se espera la eventual derivación al especialista.
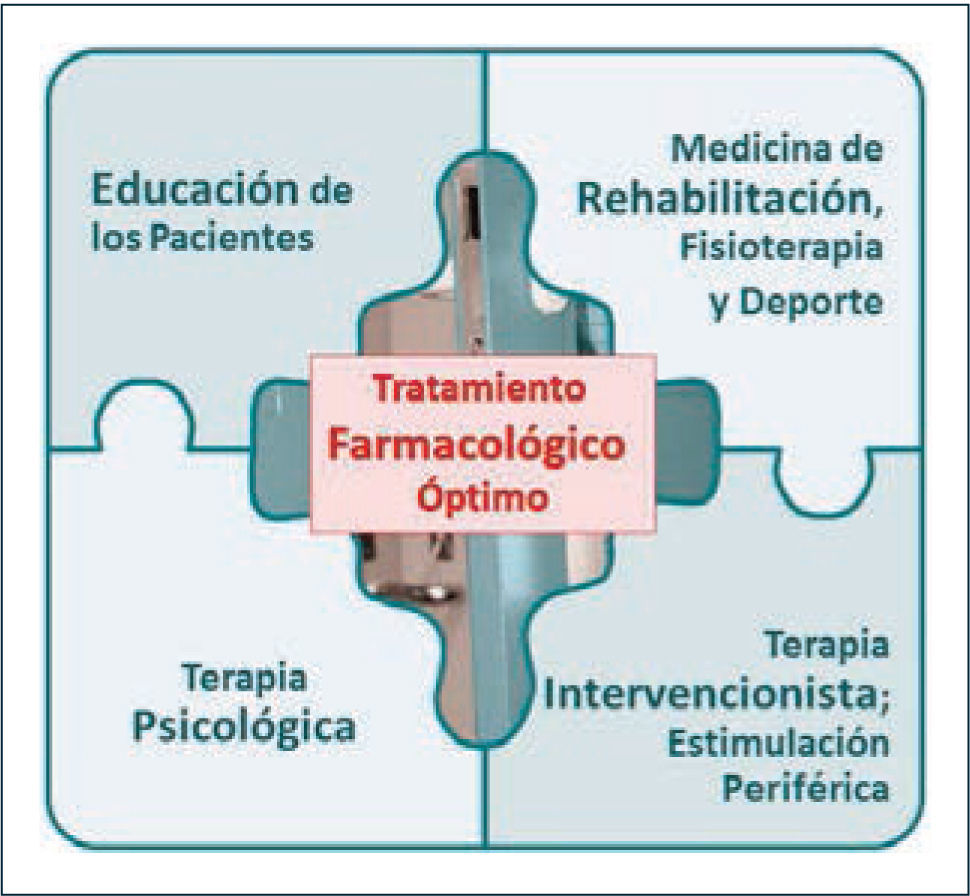
El manejo del DN debe ser multimodal, considerando todas las alternativas terapéuticas, tanto farmacológicas como no farmacológicas (figura 6).
Figura 6.Estrategias del tratamiento multimodal
Adapatado de Argoff et al. Pain Med 2009 (40).
(0.15MB). - 2)
Los medicamentos de primera línea están disponibles y son fáciles de usar en lugares con médicos no especialistas.
El DN tiende a ser prolongado. Sin embargo, algunos se pacientes pueden aliviar completamente de su dolor, y otros pueden aliviarse parcialmente con farmacoterapia y aprender a lidiar con sus síntomas. El manejo del dolor debería ser adaptado a cada paciente en la base del tipo de dolor, la enfermedad (es) causal (es) y aspectos psicosociales. La farmacoterapia sintomática basada en la evidencia es el pilar del tratamiento del DN, y debería ser titulada de acuerdo a la eficacia, posibles contraindicaciones o efectos colaterales (32, 33). Así mismo, la disminución de los fármacos debe ser lenta y progresiva.
La detección de la enfermedad causal puede garantizar un tratamiento específico (ej. medicamentos que mantengan la normoglicemia en diabéticos, para prevenir la progresión de la neuropatía y otras complicaciones) o prevención secundaria (ej. comienzo de la medicación antitrombótica y el control de factores de riesgo para la aterosclerosis después de un accidente cerebrovascular).
Las guías recientes describen el rango completo de tratamientos farmacológicos disponibles (32, 34) destacando principalmente con antidepresivos y antiepilépticos, mientras que los simples analgésicos no muestran eficacia para este tipo de dolor, (tabla 5). El médico general debe considerar la posibilidad de efectos adversos a medicamentos para la titulación y monitorización del tratamiento administrado, (tabla 6).
Tabla 5.Efectos colaterales comunes de medicación de primera línea para el tratamiento del dn
Medicación Efectos colaterales Antidepresivos tricíclicos (amitriptilina, nortriptilina, desipramina) Somnolencia
Confusión
Boca seca
Hipotensión ortostática
Subida de peso
Retención urinariaAnticonvulsivantes (gabapentina y pregabalina) Somnolencia
Vértigo, empeoramiento cognitivo o de la marcha
Edema periféricoInhibidores de la recaptación de la Serotonina y Noradrenalina (duloxetina, venlafaxina) Nausea
Vértigo
Boca seca
Disfunción
sexualParches de lidocaína 5% Reacciones cutáneas leves (enrojecimiento, edema y eritema de la piel) Adaptado de Haanpää M y col. EFIC 2013 (20).
Tabla 6.Banderas rojas y dolor crónico
Edad < 20 años o > 55 años Historia reciente de violencia o trauma Dolor no mecánico progresivo, que no cede con el descanso en cama Dolor torácico Paciente con malestar generalizado Pérdida de peso inexplicable Historia de tumoración maligna Uso prolongado de corticoesteroides Síntomas neurológicos extendidos (Incluyendo Síndrome de Cauda Equina) Deformidad estructural Fiebre Abuso de drogas, inmunosupresión, HIV Adaptado de Van Tulder et al. Eur Spine J 2006 (36).
El Reino Unido ha desarrollado guías basadas en la evidencia para el manejo del DN en lugares sin médicos especialistas, denominadas guías NICE, sin embargo se focalizan sólo en el manejo farmacológico. Estas guías recomiendan (1) Revisión precoz y frecuente para titular la máxima dosis tolerable o cambiar de tratamiento y (2) Referir precozmente a la evaluación del especialista si el diagnóstico es incierto, si las primeras dos terapias fallan, o si el dolor es severo (35).
Junto con el tratamiento farmacológico, se deben considerar las terapias no farmacológicas (ej. rehabilitación, terapia cognitiva conductual, hipnoterapia, acupuntura, entre otras). Aunque pocas son específicas para el DN, ellas no deben ser olvidadas y el rol de los otros miembros del equipo de atención primaria es relevante para su adecuada aplicación. Como en otras condiciones crónicas, para el adecuado manejo del dolor una sólida relación médico paciente y la orientación y soporte psicosocial de los pacientes son muy necesarios.
El objetivo del tratamiento es aliviar el dolor y mejorar la funcionalidad y calidad de vida. La reducción del dolor en al menos 30% se considera clínicamente relevante. En caso de estar presente, el alivio de la alodinia o hiperalgesia es relevante y con el tratamiento debe evaluarse periódicamente en los controles de seguimiento.
Los posibles efectos colaterales de la medicación, calidad del sueño, humor y limitaciones funcionales también deberían ser evaluados y registrados en el seguimiento médico, y si el tratamiento no alivia estos problemas, ellos deberían ser tratados separadamente. Para los pacientes con dolor crónico la funcionalidad y el bienestar son objetivos importantes del tratamiento.
- 3)
Apoyo y seguimiento:
El médico general conoce al paciente y sus antecedentes.
El dolor crónico, incluyendo el dolor neuropático, es una condición generalmente prolongada. Se debe definir un plan adaptado para cada paciente, incluyendo sus expectativas sobre los resultados del tratamiento. Estos pueden incluir mejoramiento de la calidad de vida, retorno al trabajo y aumento de la participación social. La comunicación y la relación médico-paciente son tan terapéuticas como cualquier medicación y el manejo de co-morbilidades relevantes, como la diabetes o la depresión, son igualmente importantes, esta última es crítica para la prevención y el tratamiento del DN.
El seguimiento es más fácil de organizar en la atención primaria, la adherencia también es mejor cuando el tratamiento es sugerido por el médico general tratante, si se le provee de suficiente información.
Dada la alta prevalencia del DN, el médico APS es muy importante en el diagnóstico precoz y tratamiento inicial, siendo capaz de realizar el manejo íntegramente a este nivel, con la adecuada capacitación; sin embargo, el médico APS debe ser capaz de identificar aquellos pacientes que requieran terapia inicial por el especialista y derivarlos oportunamente.
Sugerencias de derivación de pacientes con dn desde el médico general al especialista en dolorSe sugiere que el médico general derive al especialista cuando existan:
- 1.
Banderas Rojas(36) (tabla 7); se refieren a las causas potenciales de síntomas que requieren de tratamiento específico inmediato.
Tabla 7.Tratamientos que pueden ser realizados efectivamente en lugares con médicos no especialistas
Anticonvulsivantes - -
Gabapentina
- -
Pregabalina
- -
Carbamazepina
Localizado (tópicos) - -
Parches de lidocaína 5%
- -
TENS
Antidepresivos - -
Antidepresivos tricíclicos
- -
Duloxetina
- -
Venlafaxina
opioides - -
Tramadol
- -
¿Otros?
Adaptado de Haanpää M y col. EFIC 2013 (20).
- -
- 2.
Comorbilidades médicas complejas; tanto cardiovasculares, renales y metabólicas que dificulten el tratamiento farmacológico.
- 3.
Diagnóstico no claro; sin elementos neuropáticos categóricos o con elementos agregados que sugieran otra patología.
- 4.
Alto potencial de abuso de sustancias derivadas de opioides.
- 5.
Refractariedad a múltiples terapias de dolor, tanto farmacológicas como no farmacológicas.
- 6.
Discapacidad funcional severa, progresiva y prolongada; que deterioren en forma significativa la calidad de vida.
El dolor neuropático es común, generalmente subdiagnosticado y subtratado, su intensidad, repercusión funcional y de la calidad de vida son muy frecuentes y relevantes.
La diabetes mellitus y el dolor lumbar son las patologías que más frecuentemente se asocian a dolor neuropático. Sin embargo, es importante tener presente las causas post-traumáticas y post-quirúrgicas como potenciales generadoras de este tipo de dolor.
El dolor es el principal motivo de consulta en la atención primaria de salud, siendo frecuentemente de curso crónico. La frecuencia de DN es alta, su diagnóstico es posible de realizar por el médico APS basado en una historia sucinta y dirigida y un examen físico estandarizado, el tratamiento debe ser multimodal y multidisciplinario, iniciarse precozmente en base a fármacos de primera línea cuyo manejo está al alcance de los médicos de atención primaria, quienes deben considerar medidas no farmacológicas como la rehabilitación y la terapia cognitiva conductual. A su vez, tanto el seguimiento como el apoyo de los pacientes son más factibles de realizar en la atención primaria que en otros niveles de atención de salud.
La estructura y función de la atención primaria tiene en común entre los distintos países la necesidad de evaluar, manejar y referir a los pacientes apropiadamente.
Para lograr el desafío de enfrentar la alta prevalencia del dolor neuropático con recursos limitados, los médicos generales en la atención primaria deben ser entrenados en el diagnóstico y manejo del dolor neuropático, incluyendo los criterios de derivación para los casos más complejos o con criterios de riesgo.
AgradecimientosDeseo agradecer la valiosa colaboración de Dra. Jacqueline Dote, médico fisiatra del Instituto Teletón de Santiago y Dra. Cristina Gastó, médico internista del Hospital Geriátrico, en la revisión y sugerencias del presente artículo. Así mismo, deseo agradecer a Sra. Lorena Pasten, Jefa de Biblioteca del Hospital del Trabajador ACHS por su apoyo en la búsqueda bibliográfica.
El autor declara no tener conflictos de interés, en relación a este artículo.