La fístula entero-colónica es una rara complicación de un linfoma de origen mesentérico y una causa inusual de diarrea crónica en pacientes que no tienen inmunosupresión ni enfermedad inflamatoria intestinal. Reportamos el caso de una paciente de 68 años con cuadro de dolor abdominal y diarrea crónica que a la evaluación imagenológica y endoscópica se evidenció una fístula yeyuno-colónica. Se realizó una resección quirúrgica en bloque y el análisis histológico e inmunohistoquímico de la pieza quirúrgica evidenció un linfoma no Hodgkin B de alto grado originado de un linfonodo del mesenterio con extensión secundaria a yeyuno y colon. El diagnóstico es desafiante debido al cuadro clínico inespecífico y el amplio diagnóstico diferencial, por lo que es imprescindible una adecuada anamnesis, examen físico y evaluación imagenológica que permita caracterizar la lesión y planificar la cirugía. El pronóstico y tratamiento adyuvante dependerá del tipo de tumor y el estadio en que se encuentre. Este es el primer reporte de caso local de un paciente con una fístula yeyuno-colónica secundaria a un linfoma no Hodgkin tipo B de alto grado originado de un linfonodo del mesenterio con extensión a intestino delgado y colon.
Enterocolonic fistula is a rare complication of lymphoma of mesenteric origin and an unusual cause of chronic diarrhea in patients without immunosuppression or inflammatory bowel disease. We report the case of a 68-year-old female patient with abdominal pain and chronic diarrhea that revealed a jejunocolonic fistula on imaging and endoscopic evaluation. Surgical block resection was performed and the histological and immunohistochemical analysis of the surgical specimen evidenced a high-grade B non-Hodgkin lymphoma originating from a lymph node of the mesentery with secondary extension to the jejunum and colon. The diagnosis is challenging due to the non-specific clinical picture and the wide differential diagnosis, for which an adequate anamnesis, physical examination and imaging evaluation are essential in order to characterize the lesion and schedule surgery. The prognosis and adjuvant treatment will depend on the type of tumor and its staging. This is the first local case report of a patient with a jejuno-colonic fistula secondary to a high-grade B-type non-Hodgkin lymphoma originating from a mesenteric lymph node with extension to the small intestine and colon.
Paciente mujer de 68 años con antecedente personal de hipertensión arterial, sin antecedentes familiares de importancia. Ingresa al servicio de urgencia por dolor abdominal tipo cólico difuso de moderada a gran intensidad asociado a náuseas y diarrea de un mes de evolución, aproximadamente cinco episodios diarios, sin sangre ni mucosidad. No refiere fiebre, vómitos, transgresión alimentaria, consumo de medicamentos, anorexia, baja de peso y sudoración nocturna.
Al examen físico presenta signos vitales normales, leve distensión abdominal y dolor a la palpación difusa sin evidenciar masas ni signos de irritación peritoneal. Se maneja inicialmente con hidratación y analgesia endovenosa. Se le realiza un panel por PCR de FilmArray® gastrointestinal que dio positivo para norovirus. Presenta además hemograma donde destaca leucocitosis de 16 570 leucocitos/ml (VN: 4 400–11 300) sin desviacióna la izquierda y anemia microcítica hipocrómica [Hb 10,5g/dl (VN en mujeres: 12,3–15,3), volumen corpuscular medio (VCM) 79 fl (80,0–96,1), hemoglobina corpuscular media (HCM) 27 pg (33,4–35,5]; hipokalemia 3,42 mEq/l (3,7–5,2); hipoalbuminemia 3g/dl (3,4–5,4), proteína C reactiva 4mg/l; antígeno carcinoembrionario (CEA) 2,93 ng/ml(VN en no fumadores: 2,5ng/mL; en fumadores: 5ng/mL), calprotectina fecal 103μg/g (VN <50); hemocultivos negativos y test de antígeno COVID-19 negativo.
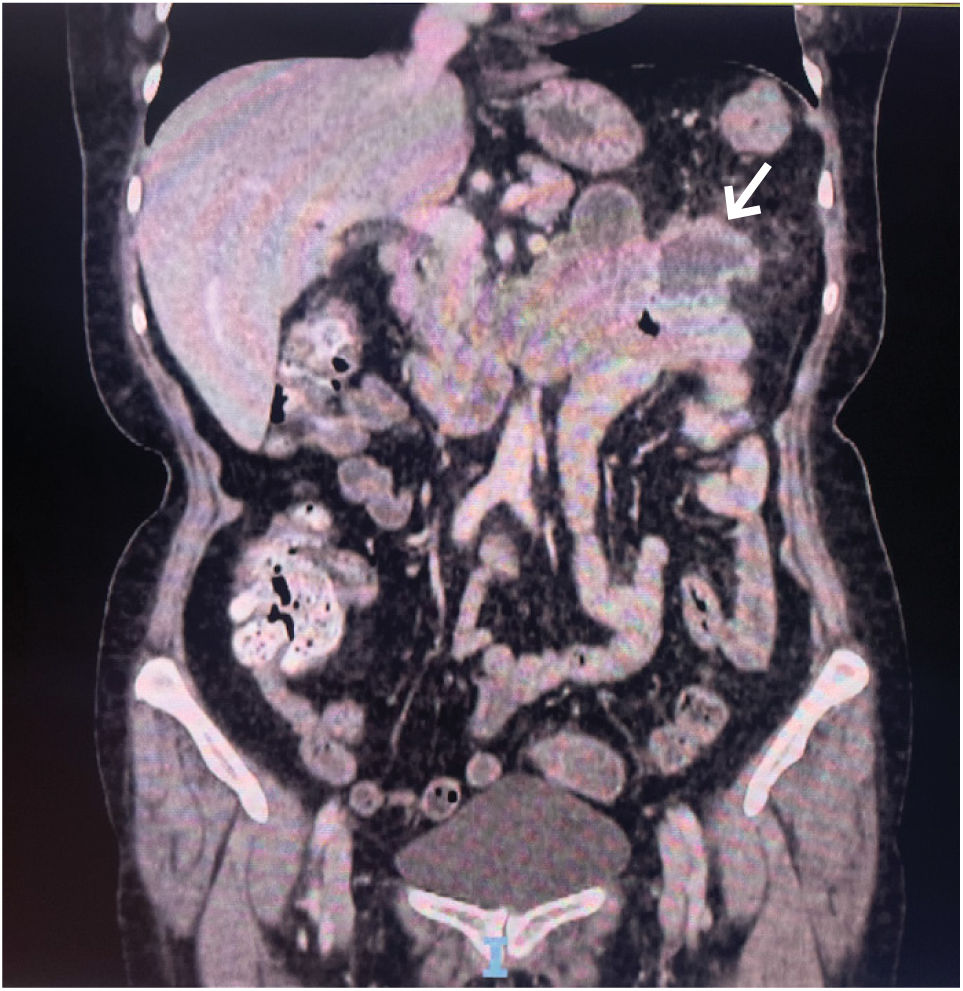
La tomografía computarizada (TC) de abdomen y pelvis con contraste evidencia un engrosamiento mural difuso del colon transverso a predominio del tercio distal, donde se identifica una colección anfractuosa con algunas burbujas en su interior de 3,9 x 3,5cm en sus ejes axiales, en íntimo contacto con el yeyuno adyacente (figura 1).
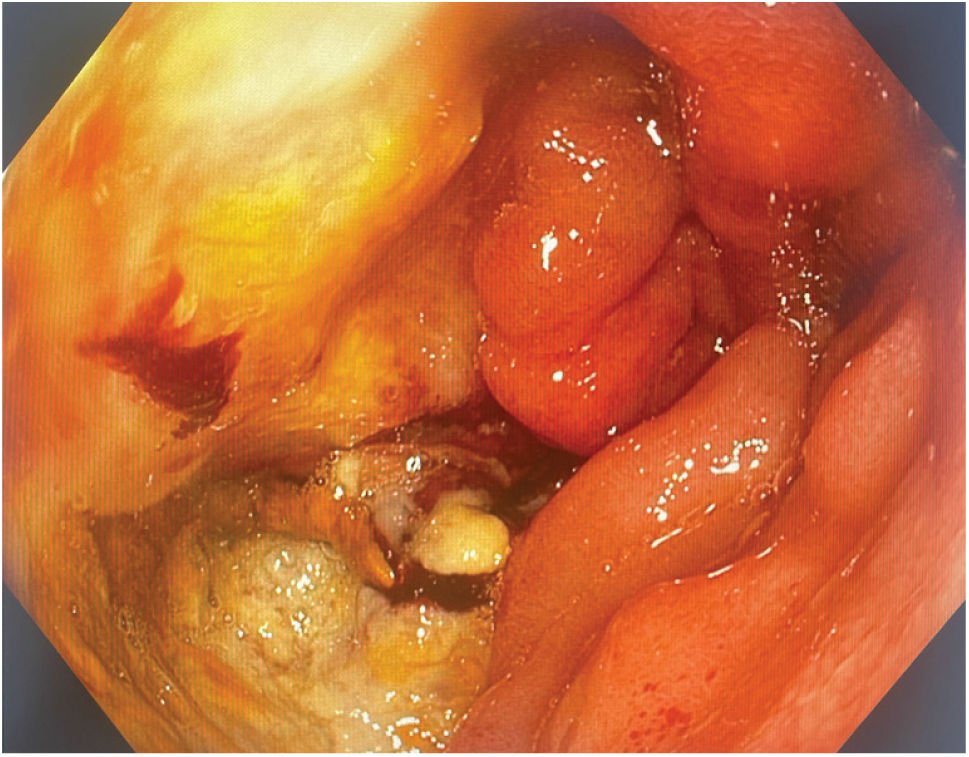
Ante la sospecha de una fístula entero-colónica, se realiza una colonoscopía donde se observa un orificio fistuloso de 2cm de diámetro en colon transverso que permitía el paso del endoscopio hacia un asa de intestino delgado con mucosa indurada recubierta de fibrina, de aspecto tumoral (figura 2). La biopsia de dicha zona informó mucosa erosionada con exudado fibrino-leucocitario, tejido conectivo fibroso reactivo, ulcerado, con foco de proliferación linfoide atípica de células de mediano a gran tamaño, altamente sospechoso de ‘neoplasia linfoproliferativa’.
Se inició tratamiento antibiótico con ceftriaxona y metronidazol recibiendo soporte nutricional parenteral preoperatorio. Se programó a cirugía electiva y se realizó una laparotomía exploradora, evidenciando una tumoración indurada de 4 x 4cm aproximadamente, de bordes irregulares, que comprometía un asa de yeyuno y el ángulo esplénico del colon, con mesenteritis circundante, sin ascitis ni exudado purulento ni implantes peritoneales ni hepáticos. Se realizó una resección en bloque de los segmentos comprometidos:1 resección de yeyuno con anastomosis entero-enteral latero-lateral mecánica;2 resección segmentaria del ángulo esplénico del colon y transverso-descenso anastomosis latero-lateral mecánica;3 resección de todo el tejido inflamatorio del mesenterio circundante.
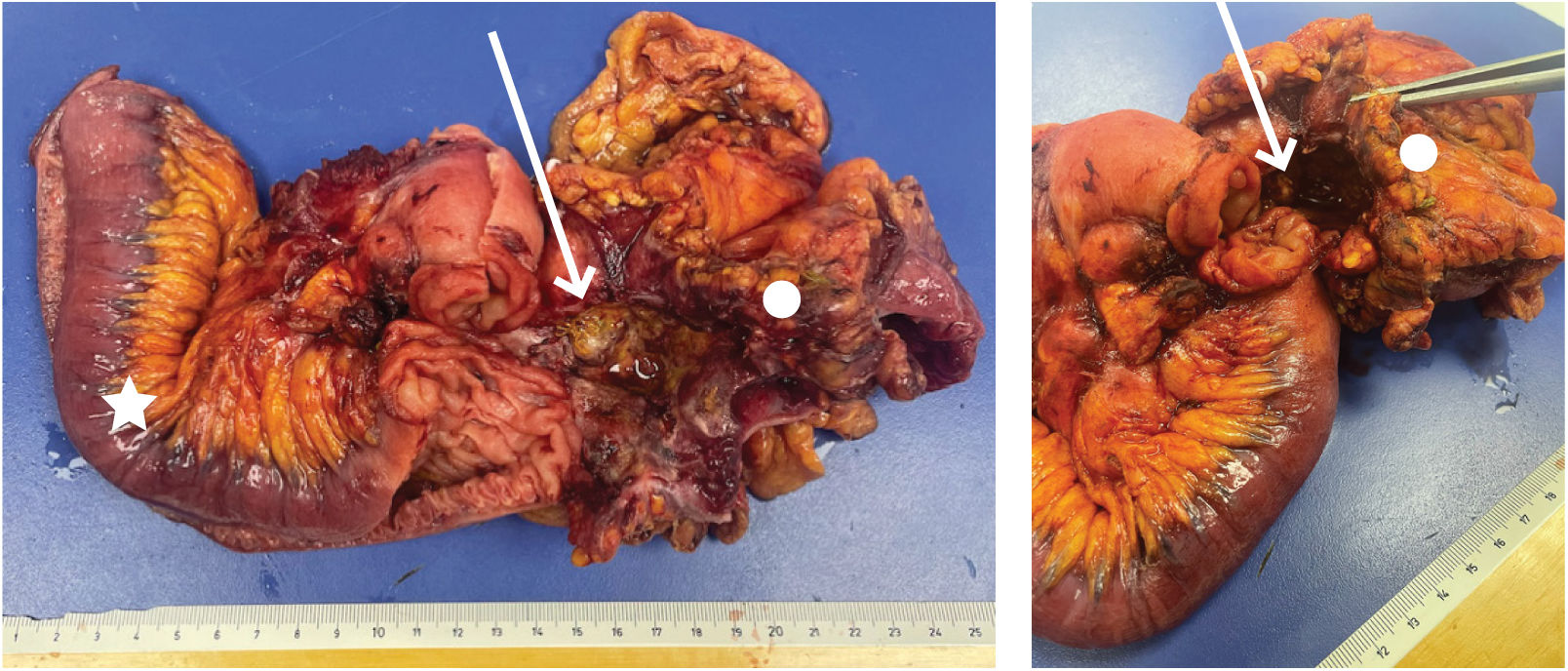
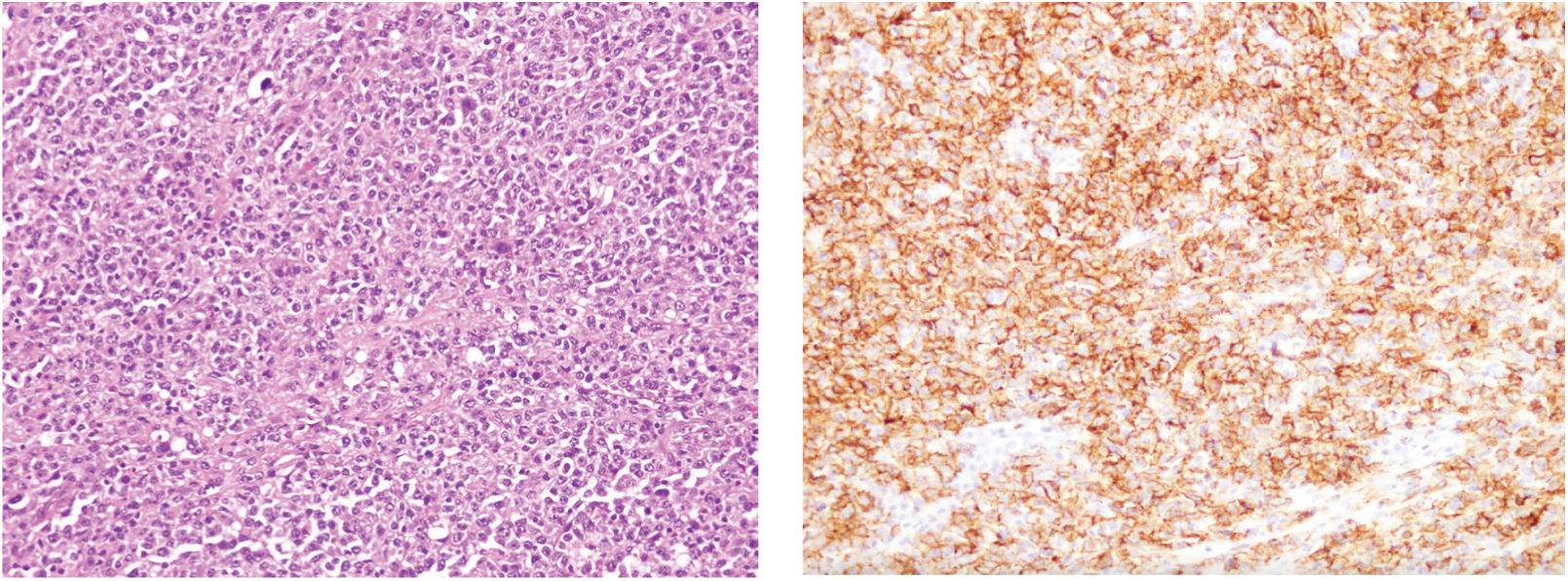
La biopsia de la pieza operatoria (mesenterio, segmento de yeyuno y de colon transverso, figura 3) demostró un linfoma no Hodgkin B de alto grado, “triple expresor” originado en un linfonodo del mesenterio con extensión secundaria a intestino delgado y colon. Inmunohistoquímicas: CD20 (+), CD3 (+), Bcl-2 (+), Bcl-6 (+), CD10 (+), MUM-1(+), Ki67 (+ en 70% de células neoplásicas), CD5 (-), Ciclina D-1 (-), CD30 (+), c-Myc (+), (figura 4).
La paciente evoluciona favorablemente, con disminución progresiva de la diarrea, siendo dada de alta en buenas condiciones al séptimo día postoperatorio, con indicación de quimioterapia posterior.
DiscusiónLas fístulas entero-colónicas suelen estar causadas por condiciones inflamatorias como la diverticulitis, pancreatitis, Enfermedad de Crohn, cuerpos extraños, cirugías previas, radiación o malignidad3. Las fístulas de origen maligno generalmente están asociadas a adenocarcinomas primarios de cérvix, ovario o colon2,4. Alrededor del 1% corresponden a una complicación de linfomas primarios del tracto gastrointestinal, destacando el linfoma no Hodgkin difuso de células grandes B en el 30% de estos casos3,5. Los factores de riesgo asociados son la inmunosupresión y la presencia de enfermedad inflamatoria intestinal6.
El diagnóstico de esta patología supone un desafío, pues las manifestaciones son inespecíficas, presentando principalmente dolor abdominal (84%), pérdida de peso (81%) y diarrea (39%)4. Esta paciente tuvo dolor abdominal difuso y diarrea acuosa de un mes de evolución, cuyo panel por PCR de FilmArray® gastrointestinal evidenció una infección por norovirus. Sin embargo, la gastroenteritis producida por este agente infeccioso suele ser autolimitada, con un corto periodo de incubación (24-48 horas) y una evolución que no suele superar los 7 días7.
La diarrea crónica se describe con una frecuencia de hasta un 5% en la población general adulta, y en pacientes inmunocompetentes generalmente ocurre en un contexto no infeccioso con un diagnóstico diferencial amplio que exige descartar malignidad8. La diarrea persistente debido a una fístula entero-colónica podría explicarse por el sobrecrecimiento bacteriano del intestino delgado a partir de la microbiota colónica; o por un fenómeno similar al síndrome del intestino corto, donde el contenido intestinal se vacía precozmente en el colon3,4.
La fístula entero-colónica es una rara complicación del linfoma, sobre todo del linfoma de origen mesentérico, y representa un estadio avanzado de la enfermedad, pues implica el crecimiento e infiltración tumoral del tejido circundante que resulta en formación de abscesos intraperitoneales y fístulas en la pared de los intestinos adyacentes4. La evaluación y diagnóstico debe contemplar una adecuada anamnesis, examen físico y estudios de imágenes como la tomografía computada con contraste, resonancia magnética, endosonografía, colonoscopia, que ayudarán en el estadiaje del tumor y la planificación quirúrgica. La diferenciación de la estirpe tumoral se basa en el análisis histológico e inmunohistoquímico, el cual es imprescindible para diferenciar de otros procesos malignos del diagnóstico diferencial de tumores mesentéricos en adultos como mesotelioma maligno, tumor estromal extragastrointestinal, los carcinomas indiferenciados y tumores neuroendocrinos5.
El tratamiento inicial debe considerar la corrección de la deshidratación y desbalance electrolítico, soporte nutricional y manejo antibiótico ante la presencia de abscesos intraabdominales, considerando la posibilidad de drenaje3. El manejo de la complicación -la fístula entero-colónica secundaria al tumor- es quirúrgico, con la exéresis del trayecto fistuloso y resección de los segmentos comprometidos en bloque9. El pronóstico y la necesidad de quimioterapia, radioterapia o inmunoterapia posterior dependerá del tipo de tumor encontrado y el estadio en el que este se encuentre6.
A la fecha, en la literatura internacional existen 10 casos reportados de pacientes con fístula yeyuno-colónica secundario a linfoma, de los cuales solo 3 corresponden a linfomas de células B y todos estos originados primariamente en el intestino y no en el mesenterio2,3,10, no existiendo publicaciones chilenas al respecto. El caso que reportamos es particular, pues la paciente no presentó ningún síntoma B (fiebre, sudoración nocturna, pérdida de peso >10% en 6 meses previos) que hiciera sospechar que se tratase de un linfoma. Asimismo, no tenía factores de riesgo como inmunosupresión ni enfermedad inflamatoria intestinal. Por último, el linfoma no Hodgkin B de alto grado diagnosticado tenía su origen de un linfonodo del mesenterio y no del tejido intestinal como en los casos reportados previamente en la literatura.
ConclusionesLa fístula entero-colónica es una rara complicación de un linfoma mesentérico y una causa inusual de diarrea crónica que hay que descartar en pacientes con cuadros no infecciosos. El estudio de imágenes es imprescindible para caracterizar la lesión y planificar la cirugía. El análisis histológico e inmunohistoquímico de la pieza quirúrgica es crucial para caracterizar la neoplasia y definir el manejo posterior. La cirugía es el manejo definitivo y debe buscar la resección en block de toda la masa tumoral y el compromiso mesentérico circundante. A nuestro conocimiento, este es el primer caso local reportado de un paciente con una fístula yeyuno-colónica secundaria a un linfoma no Hodgkin tipo B de alto grado originado de un linfonodo del mesenterio con extensión a intestino delgado y colon.
Consideraciones éticasEste reporte de caso clínico se llevó a cabo de conformidad con el Código de Ética de la Declaración de Helsinki, resguardando la privacidad y confidencialidad de los datos del paciente y contando con el consentimiento informado del mismo.
Declaración de conflicto de interésLos autores declaran no tener conflictos de interés.