En la actualidad el trasplante pulmonar es considerado el tratamiento de elección para pacientes portadores de una enfermedad pulmonar avanzada que no presenten otras patologías severas y cuya sobrevida estimada es menor a dos años. La mejoría de la técnica quirúrgica y las drogas inmunosupresoras han permitido optimizar la calidad de vida, disminuyendo las complicaciones y extendiendo así la sobrevida.
Hace 10 años Clínica Las Condes inicia su programa de trasplante pulmonar el que ha sido pionero nacional en número de injertos realizados y resultados obtenidos a largo plazo. Se realiza una revisión de las indicaciones, complicaciones precoces y tardías, capacidad física posterior al trasplante y sobrevida alejada de los pacientes trasplantados de pulmón en nuestro programa.
Currently the lung transplant is considered the treatment of choice for patients showing no other severe pathologies advanced lung disease carriers whose estimated survival rate is less than two years. The improvement of the surgical technique and immunosuppressive drugs has made it possible to optimize the quality of life, reducing complications and extending the survival rate.
For 10 years Clínica las Condes has been initiating your lung transplantation program which has been pioneering national in number made grafts and results obtained long-term. Performs a review indications, early and late complications, transplantation and survival away from transplanted patients lung our physical capacity.
El trasplante pulmonar desde fines de la década de los ochenta se ha consolidado como una alternativa terapéutica para pacientes seleccionados, portadores de una enfermedad pulmonar avanzada, refractaria a tratamiento médico, con una muy pobre calidad de vida y expectativas de sobrevida que no alcanzan los dos años (1).
El injerto pulmonar se ha considerado de mayor complejidad por condiciones como la conexión al ambiente a través de la vía aérea que facilita las infecciones, el mayor grado de inmunogenecidad respecto a otros órganos sólidos y el riesgo de isquemia de las suturas, todas complicaciones que se han ido superando en el tiempo con la profilaxis de infecciones principalmente a Citomegalovirus (CMV), con el uso de nuevos inmunosupresores de mayor potencia y más especificidad, los que disminuyen efectos colaterales como la nefrotoxicidad, la detección precoz del Rechazo Celular Agudo (RCA), del Sindrome de Bronquiolitis Obliterante (SBO) y los factores asociados a su desarrollo (2).
Desde el año 2005 ante la escasez de donantes y con el fin de optimizar los injertos se ha utilizado un puntaje para medir la gravedad del paciente en lista de espera (LAS: Lung Score Allocation) y determinar así su prioridad. Según este nuevo sistema para asignación de un órgano tienen prioridad los pacientes portadores de Fibrosis pulmonar y Fibrosis quística (3–4).
Resultados de trasplante pulmonar en CLCEl primer trasplante pulmonar se realiza en Chile en el año 1998 y posteriormente el año 1999 Clínica Las Condes inicia el desarrollo de su programa cardiopulmonar habiendo efectuado a la fecha el mayor número de injertos pulmonares en nuestro país.
El equipo de trasplante está constituído por un grupo multidisciplinario de profesionales compuesto por médicos broncopulmonares adultos y pediatras, cirujanos de tórax, enfermeras coordinadoras, psiquiatras, kinesiólogos, nutricionistas y con apoyo externo de infectólogos, intensivistas, anestesistas, cardiólogos y nefrólogos según necesidad.
Entre el año 1999 y el 2009 se han trasplantado 56 pacientes, con una edad X¯ de 55 años (r 13 – 71) y predominio del sexo masculino de 64%. En la Tabla 1 se describen las características demográficas de pacientes trasplantados pulmonares.
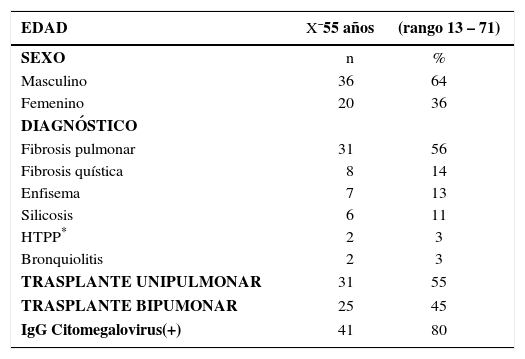
Características demográficas de 56 pacientes trasplantados pulmonares
| EDAD | X¯55 años | (rango 13 – 71) |
|---|---|---|
| SEXO | n | % |
| Masculino | 36 | 64 |
| Femenino | 20 | 36 |
| DIAGNÓSTICO | ||
| Fibrosis pulmonar | 31 | 56 |
| Fibrosis quística | 8 | 14 |
| Enfisema | 7 | 13 |
| Silicosis | 6 | 11 |
| HTPP* | 2 | 3 |
| Bronquiolitis | 2 | 3 |
| TRASPLANTE UNIPULMONAR | 31 | 55 |
| TRASPLANTE BIPUMONAR | 25 | 45 |
| IgG Citomegalovirus(+) | 41 | 80 |
La principal patología de base que motivó el trasplante pulmonar en nuestro grupo ha sido la Fibrosis pulmonar con un 56%, seguido por la Fibrosis quística, el enfisema y la silicosis pulmonar. Ver Tabla 1.
Es destacable que los pacientes aquejados de Fibrosis pulmonar, son derivados en forma tardía, ya que habitualmente se espera el deterioro espirométrico, lo cual es un signo de enfermedad avanzada y este grupo de pacientes ha presentado la mayor mortalidad en la lista de espera. La literatura recomienda la derivación precoz a un centro de trasplante en cuanto se evidencie compromiso de la saturación arterial de oxígeno < a 88 % en el examen de caminata de 6 minutos.
En la Fibrosis quística debe considerarse además de la juventud de los pacientes también su rápido deterioro sistémico con severo compromiso nutricional al presentar episodios de infecciones pulmonares a repetición, algunos de estos pacientes han requerido incluso la instalación de gastrostomía previo al trasplante.
Los pacientes portadores de EPOC constituyen nuestra tercera indicación y si bien ellos presentan una mala calidad de vida, su sobrevida es francamente mayor sin trasplante respecto a la fibrosis pulmonar y la fibrosis quística. Solo se eligen para el trasplante los pacientes con un compromiso sistémico de su enfermedad evidenciado por el índice de BODE. (Ver artículo de selección de donante y receptor de esta revista).
InmunosupresiónTodos los pacientes han recibido terapia triasociada con inhibidores de calcineurina (ciclosporina o tacrolimus), inhibidores del ciclo celular (azatioprina o micofenolato mofetil) y esteroides. Recibieron además terapia de inducción con anticuerpo monoclonal anti CD25 (Basiliximab) los últimos 35 pacientes.
Se realizan controles de niveles plasmáticos seriados de inmunosupresores, para evitar efectos subterapéuticos o toxicidad asociada. Los niveles requeridos varían en el tiempo siendo mayores durante el primer año del trasplante. El esquema de inmunosupresión se mantiene de por vida con dosis progresivamente menores.
ProfilaxisUno de los problemas del injerto pulmonar que facilita las infecciones es su comunicación al exterior a través de la vía aérea.
La profilaxis habitual ha permitido evitar o retardar la aparición de infecciones en trasplantes de órganos sólidos (5) y ésta incluye la cobertura de:
- •
Virus de tipo CMV.
- •
Virus Herpes simple.
- •
Pneumocistis Jirovecci.
- •
Nocardia.
- •
hongos.
La inmunosupresión a su vez puede provocar la reactivación de infecciones latentes de tipo viral como el Citomegalovirus (CMV), el que juega un importante papel en los trasplantes de órgano sólido y en el caso de pulmón la infección previa se ha asociado al desarrollo de un rechazo agudo y eventual rechazo crónico posterior (6).
La terapia profiláctica está compuesta de:
- •
Aciclovir por 4 meses.
- •
Valganciclovir por 4 meses (en pacientes con IgG negativo a CMV).
- •
Itraconazol por 1 año.
- •
Cotrimozaxol Forte trisemanal de mantención.
Una vez realizado el trasplante el paciente ingresa a UTI y se mantiene dormido conectado a ventilación mecánica, de la cual es retirado una vez alcanzado un intercambio de oxígeno adecuado y recuperado conciencia.
El paciente inicia precozmente su inmunosupresión la que se monitoriza con niveles plasmáticos, se efectúa profilaxis de infecciones, se retiran progresivamente los drenajes torácicos e inicia suspensión de 02. En este periodo el apoyo de kinesiólogos especializados es fundamental por la falta de reflejos pulmonares y la necesidad de rehabilitación motora progresiva. Es también en este periodo de gran importancia el manejo y educación nutricional de los pacientes que habitualmente posterior a una cirugía de esta envergadura se ve muy comprometido. Previo al alta se realiza revisión de las suturas bronquiales por medio de Fibrobroncoscopía (FBC). Se entrega además un microespirómetro portátil para medición diaria de espirometría.
SeguimientoLos pacientes se mantienen en control semanal con exámenes generales, niveles plasmáticos de inmunosupresión, radiografia de tórax y espirometría.
Entre el segundo y tercer mes los controles se realizan cada 15 días y luego mensuales durante el primer año.
El objetivo es detectar complicaciones en etapa precoz y así determinar una mayor protección del injerto. En nuestro grupo, a la fecha existen pacientes en seguimiento con un periodo posterior al trasplante desde 3 meses a 9 años.
ComplicacionesEn nuestra experiencia podríamos clasificarlas como inmediatas, precoces y tardías; si ocurren antes o después de 6 meses del trasplante.
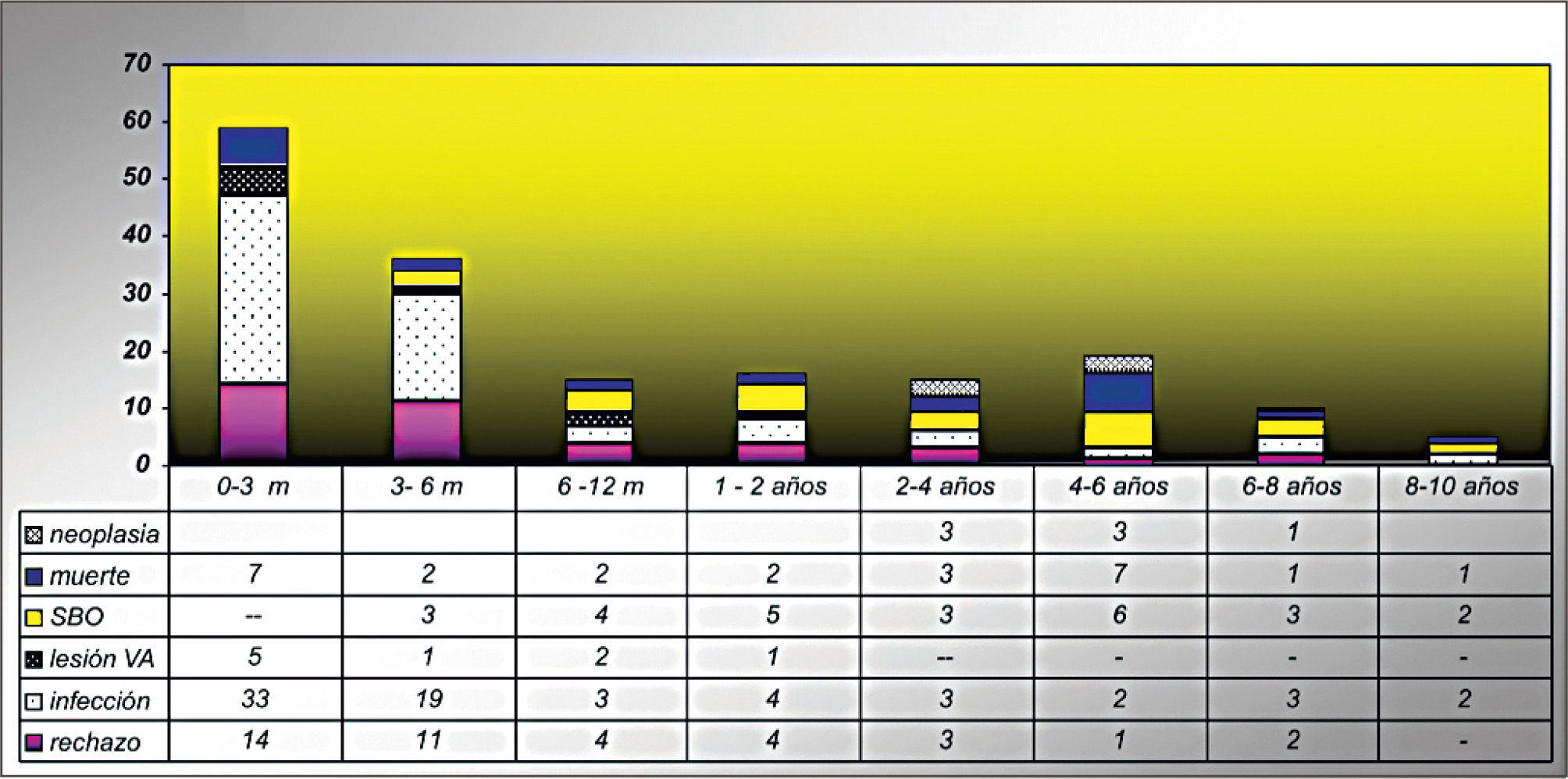
Hemos observado que el mayor número de complicaciones se presenta el primer año con un 63%.
InmediatasOcurren desde el intraoperatorio y están relacionadas al acto quirúrgico en donde pueden presentarse los mayores sangramientos y se inicia la etapa de reperfusión del pulmón injertado.
a.–Disfunción primaria de injerto (DPI)Es una de las complicaciones precoces más temida y puede presentarse entre un 10–20% en diferentes grados de severidad, se caracteriza por infiltrados pulmonares difusos e insuficiencia respiratoria (7).
En nuestra experiencia la DPI severa se ha presentado en 8 de 56 pacientes que han requerido de apoyo con Circulación extracorpórea (ECMO), el 50% de los pacientes sobrevivió a esta complicación.
b.– Rechazo hiperagudoSe presenta en pacientes previamente sensibilizados (PRA alto), provoca fenómenos de trombosis vascular e insuficiencia respiratoria severa (8).
Esta complicación la hemos observado en 2 pacientes, en ellos se realizó plasmaféresis y apoyo con ECMO, sin embargo ambos fallecieron antes de 72 horas.
PrecocesOcurren después de la primera semana y las más frecuentes son: infecciones, rechazo celular agudo (RCA) y lesiones de sutura.
a.– InfeccionesLas fuentes de infección pueden venir desde el donante (se encuentra en muerte cerebral conectado a ventilación mecánica), del receptor y facilitado por las múltiples líneas vasculares utilizadas en UCI y asociado a la inmunosupresión. Los gérmenes predominantes son bacterias (9).
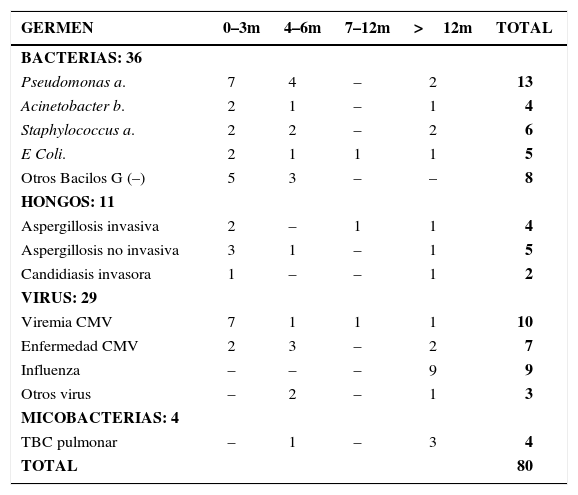
En nuestra casuística de 56 pacientes hubo 33 episodios de infecciones en los tres primeros meses, con predominio de foco pulmonar y bacterias del tipo Pseudomonas a ver Tabla 2.
Infecciones en 56 pacientes trasplantados pulmonares: tipo de germen y tiempo post trasplante
| GERMEN | 0–3m | 4–6m | 7–12m | >12m | TOTAL |
|---|---|---|---|---|---|
| BACTERIAS: 36 | |||||
| Pseudomonas a. | 7 | 4 | – | 2 | 13 |
| Acinetobacter b. | 2 | 1 | – | 1 | 4 |
| Staphylococcus a. | 2 | 2 | – | 2 | 6 |
| E Coli. | 2 | 1 | 1 | 1 | 5 |
| Otros Bacilos G (–) | 5 | 3 | – | – | 8 |
| HONGOS: 11 | |||||
| Aspergillosis invasiva | 2 | – | 1 | 1 | 4 |
| Aspergillosis no invasiva | 3 | 1 | – | 1 | 5 |
| Candidiasis invasora | 1 | – | – | 1 | 2 |
| VIRUS: 29 | |||||
| Viremia CMV | 7 | 1 | 1 | 1 | 10 |
| Enfermedad CMV | 2 | 3 | – | 2 | 7 |
| Influenza | – | – | – | 9 | 9 |
| Otros virus | – | 2 | – | 1 | 3 |
| MICOBACTERIAS: 4 | |||||
| TBC pulmonar | – | 1 | – | 3 | 4 |
| TOTAL | 80 |
Las infecciones por hongos precoces se presentaron en 6 pacientes dos aspergillosis invasivas, 3 no invasivas y una candidiasis sistémica.
Las infecciones virales en este periodo fueron exclusivamente por CMV, en dos casos enfermedad invasora y en siete sólo reactivación del virus sin compromiso de otros órganos.
b.–RechazoEl rechazo celular agudo (RCA) se presenta en general después de la primera semana y puede alcanzar hasta el 50% de los pacientes en el primer año, este puede ir desde episodios asintomáticos a cuadros severos (10).
En 27 pacientes se identificaron 39 episodios de rechazo agudo (X¯ 1,4 episodios por paciente), 70% el primer año post trasplante.
Durante los tres primeros meses post trasplante se confirmó un episodio de RCA por biopsia transbronquial en 14 pacientes. El tratamiento consistió en Metilprednisolona 1g por 3 días.
c.–Lesiones de vía aéreaLa zona de anastomosis bronquial ha sido una de las principales causas de morbi-mortalidad en el trasplante pulmonar, asociado en general a la técnica quirúrgica y a la isquemia regional. Se describe que alrededor del 20% de los pacientes presentan alguna complicación (11).
En nuestro grupo en 7 pacientes ocurrieron en forma precoz, todos cercanos a la sutura, 5 de ellos con estenosis que requirieron FBC seriadas para realizar dilatación bronquial y en 3 de ellos instalación de Stent endobronquial y en un caso cirugía con reanastomosis bronquial con excelente resultado clínico.
TardíasSon complicaciones manifestadas después del sexto mes, persistiendo aún el RCA, aparecen los episodios de rechazo crónico (SBO), algunas lesiones de vía aérea, infecciones y neoplasias.
a.–SBOConstituye la principal complicación a largo plazo y la que determina la sobrevida del injerto. En la evolución del trasplante pulmonar se describe la aparición de SBO en alrededor de hasta un 50% a 5 años (12–13), en diferente grado de severidad. Los factores descritos como de riesgo son el antecedente de RCA, infecciones de tipo CMV y actualmente asociado al RGE (14–15).
En nuestro grupo hemos identificado 18 pacientes (32%) quienes desarrollaron SBO. En 7 pacientes moderado y en 6 de ellos severo; con una sobrevida X¯ de 18,5 meses desde el momento del diagnóstico. De los factores de riesgo asociados al desarrollo de SBO: 13 pacientes (72%) presentaron RCA previo y 4 de ellos en dos oportunidades. En nuestra serie, la mitad de los pacientes tenía antecedentes de RGE demostrado por phmetría pretrasplante y en dos pacientes posterior al injerto.
b.–Lesiones de vía aérea tardíaSe presentaron en dos pacientes con lesiones de tipo malacia en la zona de sutura, lo que llevó a instalación de stent endobronquial corrigiendo completamente esta complicación.
c.– InfeccionesDespués de los seis primeros meses disminuyen los episodios de infección en forma progresiva con 24 casos a 9 años de seguimiento. En este periodo se demostraron 3 episodios de tuberculosis (un paciente portador de silicosis con 2 episodios), aparecen los virus comunitarios: 5 casos de influenza común y el año 2009, 4 casos de influenza AH1N1.
d.– NeoplasiasEl uso de inmunosupresión prolongada puede facilitar el desarrollo de enfermedades neoplásicas en forma tardía (16).
En nuestro grupo, siete pacientes (12,5%) desarrollaron enfermedad neoplásica de predominio cutáneo. Hubo tres pacientes con adenocarcinoma, uno de ellos gástrico al 5° año, uno pulmonar al 4° año y uno prostático al 5° año.
Otro paciente al quinto año desarrolló un Linfoma de células T que respondió favorablemente a la terapia y al año posterior desarrolló un Mieloma múltiple muy agresivo que le ocasionó la muerte.
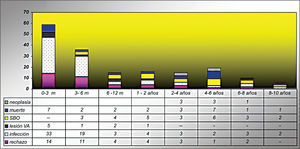
En general las complicaciones del trasplante pulmonar disminuyen progresivamente en el curso del tiempo, presentándose en nuestra experiencia el 63% de ellas durante el primer año (17). Ver Figura 1.
Capacidad física posterior al trasplanteLas patologías de base que culminan en un trasplante pulmonar lo hacen por la severa alteración del intercambio gaseoso que lleva a un deterioro progresivo de la capacidad física del paciente y dependencia absoluta de 02 aún en reposo.
En esta etapa el paciente debe abandonar su trabajo, los estudios y limitar su actividad progresivamente.
Test de caminata de 6 minutosSi bien la espirometría ha sido considerada como el examen que puede llevar a la decisión de un trasplante, su deterioro es en general tardío en patologías como la fibrosis pulmonar. Es por esto que se ha incorporado la medición del test de caminata de 6 minutos (TC6m) como un indicador de la severidad de la enfermedad (18). En este examen además de la distancia caminada es muy relevante observar el compromiso de la saturación de 02 lo que permite establecer un pronóstico previo al deterioro espirométrico y a su vez realizar una derivación precoz a un equipo de trasplante (19).
Una vez que el paciente se ha trasplantado el TC6m es un importante indicador de la capacidad física y se correlaciona mejor con las actividades de la vida diaria que la espirometría.
En nuestros pacientes el TC6m pre trasplante fue en x 260mts (no todos los pacientes logran realizarlo por su insuficiencia repiratoria).
En nuestro seguimiento a largo plazo el TC6m es mayor a 400mts: a 1, 3 y 5 años en 22, 20 y 13 pacientes respectivamente.
Actividad físicaProbablemente el principal efecto posterior al trasplante es la suspensión de oxígeno y la mejoría de la capacidad física en forma progresiva. En la primera etapa los pacientes se encuentran vinculados al Programa de Rehabilitación de Clínica Las Condes, lo que les permite un entrenamiento progresivo con monitorización cardiovascular.
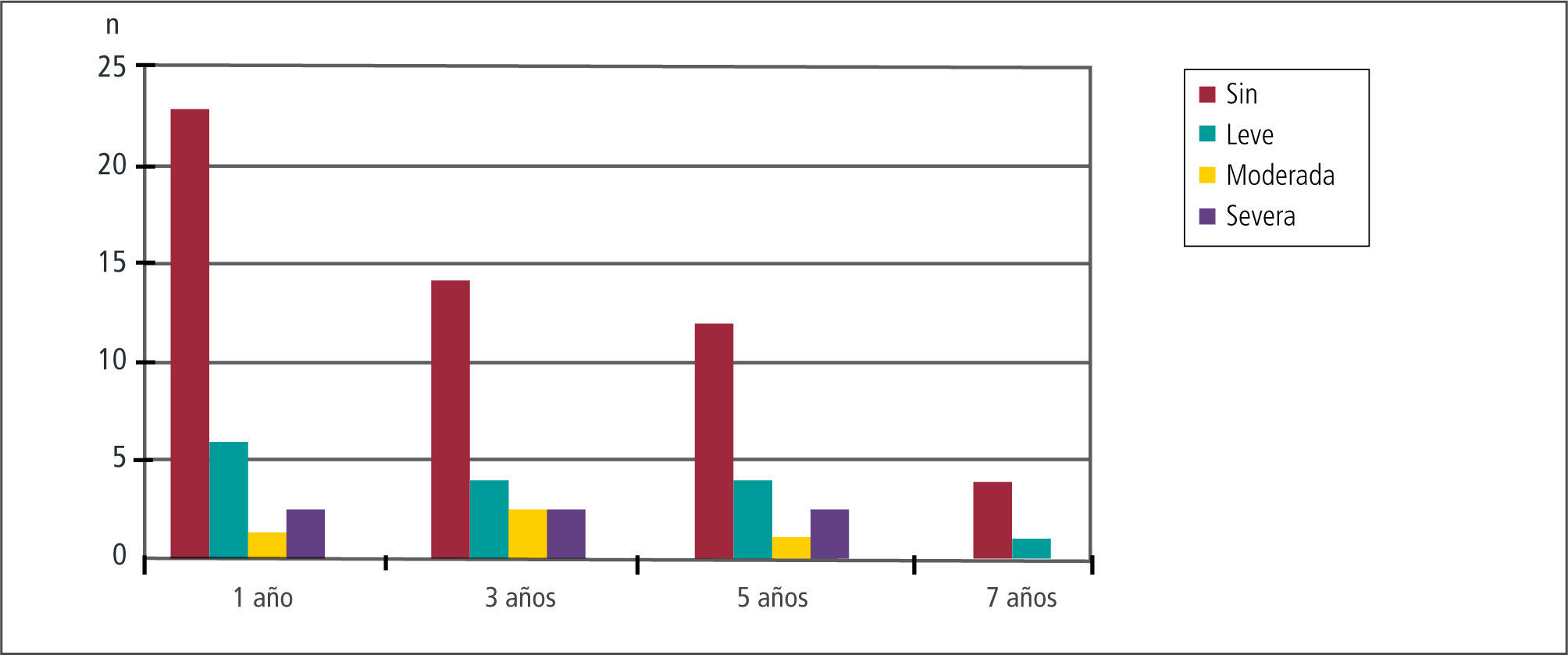
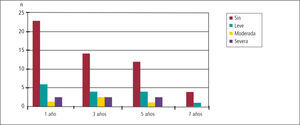
De los pacientes en seguimiento a 1, 3, 5 y 7 años la actividad física, no se encuentra limitada en 26, 16, 6 y 4 pacientes respectivamente.
Sólo los pacientes que han presentado un SBO severo han requerido el uso de oxígeno nuevamente y en nuestro grupo lo han necesitado 7 pacientes.
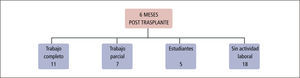
Ver Figura 2 tipo de limitación post trasplante.
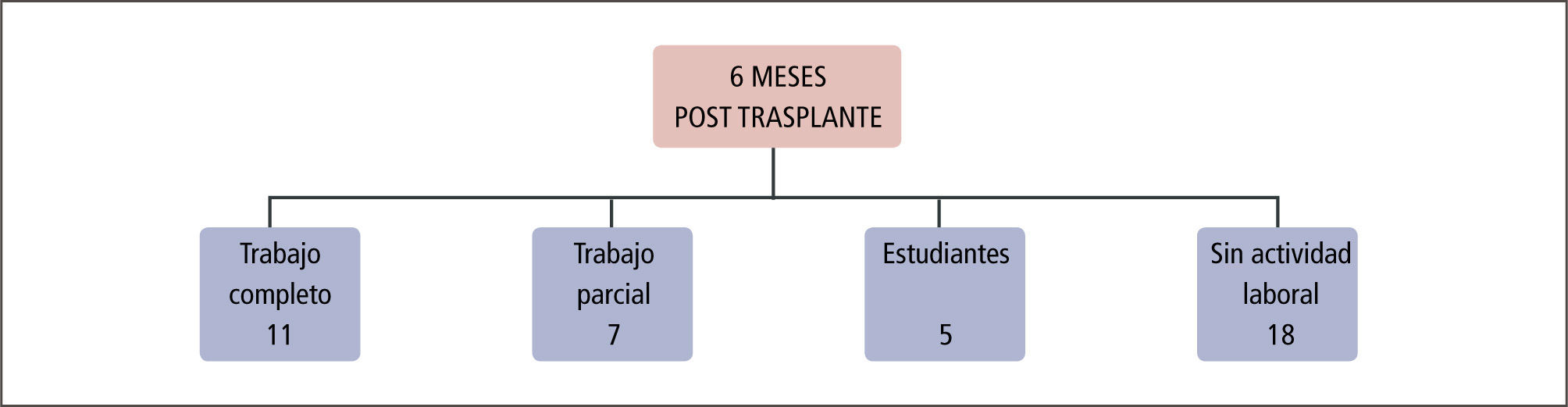
Actividad laboralUna vez superados los primeros 6 meses post trasplante, los pacientes en buenas condiciones pueden reinsertarse a su actividad laboral o estudiantil.
En nuestro grupo a los 6 meses posteriores, once pacientes realizan actividad laboral con jornada completa, siete de ellos lo hacen con jornada parcial y cinco jóvenes vuelven a estudiar.
En nuestro grupo han sido trasplantados 8 pacientes por Fibrosis quística y a la fecha 3 de ellos realizan estudios universitarios y otro ejerce jornada completa como kinesiólogo. Es importante destacar este grupo de pacientes, ya que la Fibrosis quística avanzada, requiere múltiples hospitalizaciones para terapia antibiótica con un alto costo económico, familiar y social.
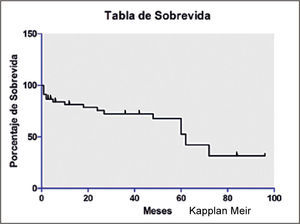
SobrevidaUn paciente candidato a trasplante es aquel cuya sobrevida estimada por su patología de base no sobrepasa los 2 años. Los resultados iniciales mostraron que menos del 50% de los pacientes superaban los 5 años posterior al trasplante (20). Con los nuevos esquemas inmunosupresores y el diagnóstico precoz de las complicaciones se ha observado una mejoría progresiva alcanzando alrededor de un 60% a 5 años, 30% a 10 años y 20 % a 20 años (21).
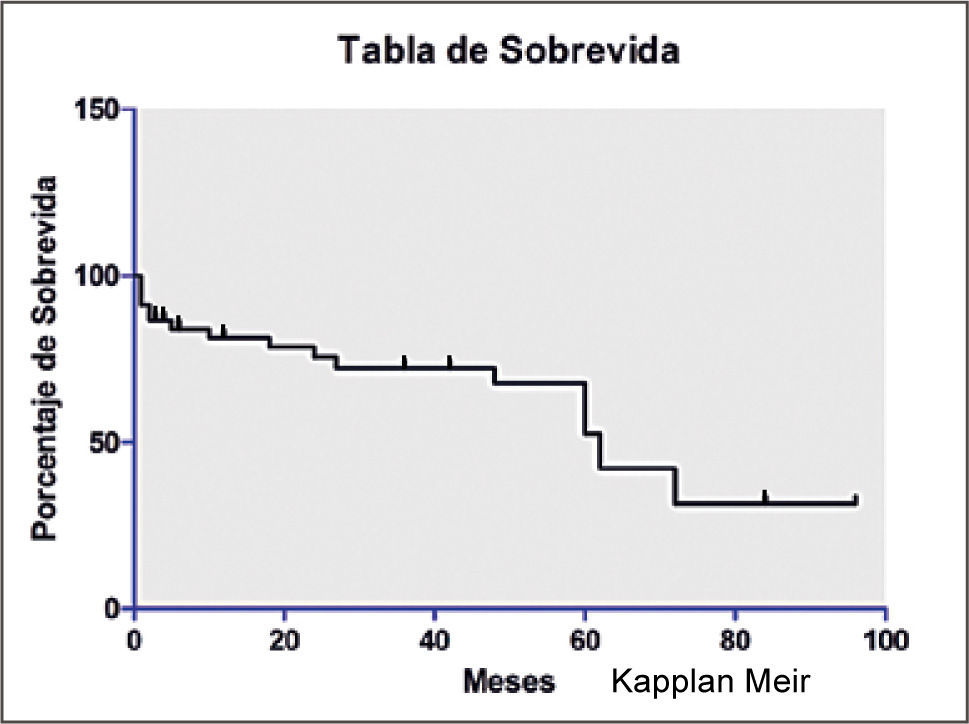
En nuestro grupo la sobrevida estimada por Kaplan Meier global al año, 3, 5 y 10 años es de 79%, 66%, 55% y 11% respectivamente, lo cual es muy semejante a lo reportado por la literatura. Ver figura 3.
Causas de mortalidadConsiderando los tres los primeros meses como el periodo precoz posterior al trasplante nuestras principales causas de mortalidad fueron: dos pacientes con sepsis a gram negativo, dos pacientes con hemoptisis masiva (lesión aspergillar), dos disfunciones primarias de injerto y una hemorragia cerebral secundaria a un aneurisma no conocido previamente.
Entre las causas de mortalidad tardía, la principal fue la insuficiencia respiratoria secundaria a un SBO en etapa avanzada en ocho pacientes, tres pacientes con neumonia refractaria seguido de tres pacientes con enfermedad neoplásica.
ComentarioEl principal resultado observado en los pacientes trasplantados pulmonares es el cambio en su calidad de vida, permitiéndoles en su gran mayoría la independencia absoluta del oxígeno, lo que facilita la inserción familiar y laboral en forma evidente.
Los grandes problemas iniciales fueron las complicaciones asociadas a las lesiones de sutura que provocaron la muerte de muchos pacientes en los programas pioneros, pero con la mejoría de las técnicas quirúrgicas y principalmente por evolución de los nuevos inmunosupresores estos problemas se han superado en forma progresiva dando paso en la actualidad al gran dilema que es la escasez de donantes, esto último ha conducido a la priorización de pacientes en las listas de espera según puntaje de gravedad.
Es destacable que entre las indicaciones de trasplante pulmonar en nuestro grupo aparece la silicosis en seis pacientes, considerando el ambiente minero de nuestro país este puede ser un grupo de riesgo en un futuro próximo. En la literatura existen solo escasos reportes de trasplante pulmonar en esta patología (22).
En nuestro medio la tarea es aún ardua, debido principalmente a la falta de cobertura económica para la gran mayoría de los pacientes que requieren un trasplante pulmonar, la no existencia de programas de salud pública que consideren esta alternativa terapéutica, la limitación de exámenes para pacientes hipersensibilizados y la escasez progresiva de donantes efectivos.
A lo anterior debe mencionarse el muy escaso desarrollo de los programas de trasplante pulmonar pediátrico, principalmente en niños secuelados por adenovirus o con Fibrosis quística avanzada, para este grupo el acceso a un donante en muerte cerebral es muy ocasional, y debe plantearse en un futuro próximo el trasplante con donante vivo relacionado.
A pesar de las dificultades mencionadas, Clínica Las Condes cuenta con un programa de trasplante pulmonar pionero a nivel nacional, con resultados comparables a grandes centros internacionales y se basa principalmente en la conformación de un equipo multidisciplinario con un gran compromiso con los pacientes del programa.
La autora declara no tener conflictos de interés, en relación a este artículo.