La vacunación es la medida preventiva más costo-efectiva para evitar las enfermedades infecciosas inmunoprevenibles, a nivel individual y comunitario. Los riesgos biológicos laborales, deben ser manejados en un sistema de gestión del riesgo, donde la vacuna es el elemento clave de protección personal (EPP) específico cuya provisión y uso obligatorio tiene normas legislativas referidas a la entrega por el empleador, la capacitación en la prevención y el uso por el trabajador. En Chile, hay 8.364.282 trabajadores según datos de Superintendencia de Seguridad Social (SUSESO). La Ley 16.744 y sus Decretos Supremos (DS) indican las condiciones que se deben mantener en los lugares de trabajo y el derecho a saber por parte del trabajador; también existen circulares del Ministerio de Salud que incluyen situaciones y grupos especiales laborales a vacunar, pero es necesaria una normativa que oriente a trabajadores dependientes e independientes y a empleadores sobre qué vacunas colocar, en qué situaciones y a quiénes dependiendo de la actividad laboral. En este artículo, hacemos una reseña de la situación legal, de recomendaciones en otros países y enumeramos algunas vacunas que podrían implementarse en la población expuesta a riesgo.
Vaccination is the most cost-effective measure for immune-preventable infectious diseases, at individual and community level. Biological occupational hazards must be faced in a risk management system, where the vaccine is a specific key as an element of personal protection, whose provision and obligatory use has legislative norms related to the delivery by the employer, the training in the prevention and the use by the worker. Several countries count with technical guides for vaccination in the working population. In Chile in 2018, there were 8.364.282 workers according with Superintendence of Social Security. Law 16.744 and Supreme Decrees indicate the environmental conditions for workers and the right to know the risks; also, Ministry of Health has issued circulars where some working conditions need specific vaccination. Is for that reason that is necessary a regulation that guides dependent and independent workers and employers on when and which vaccines must be used depending on the labor activity. In this article, we review the legal situation, other guides in different countries and list some vaccines that could be implemented in the population at specifical risks.
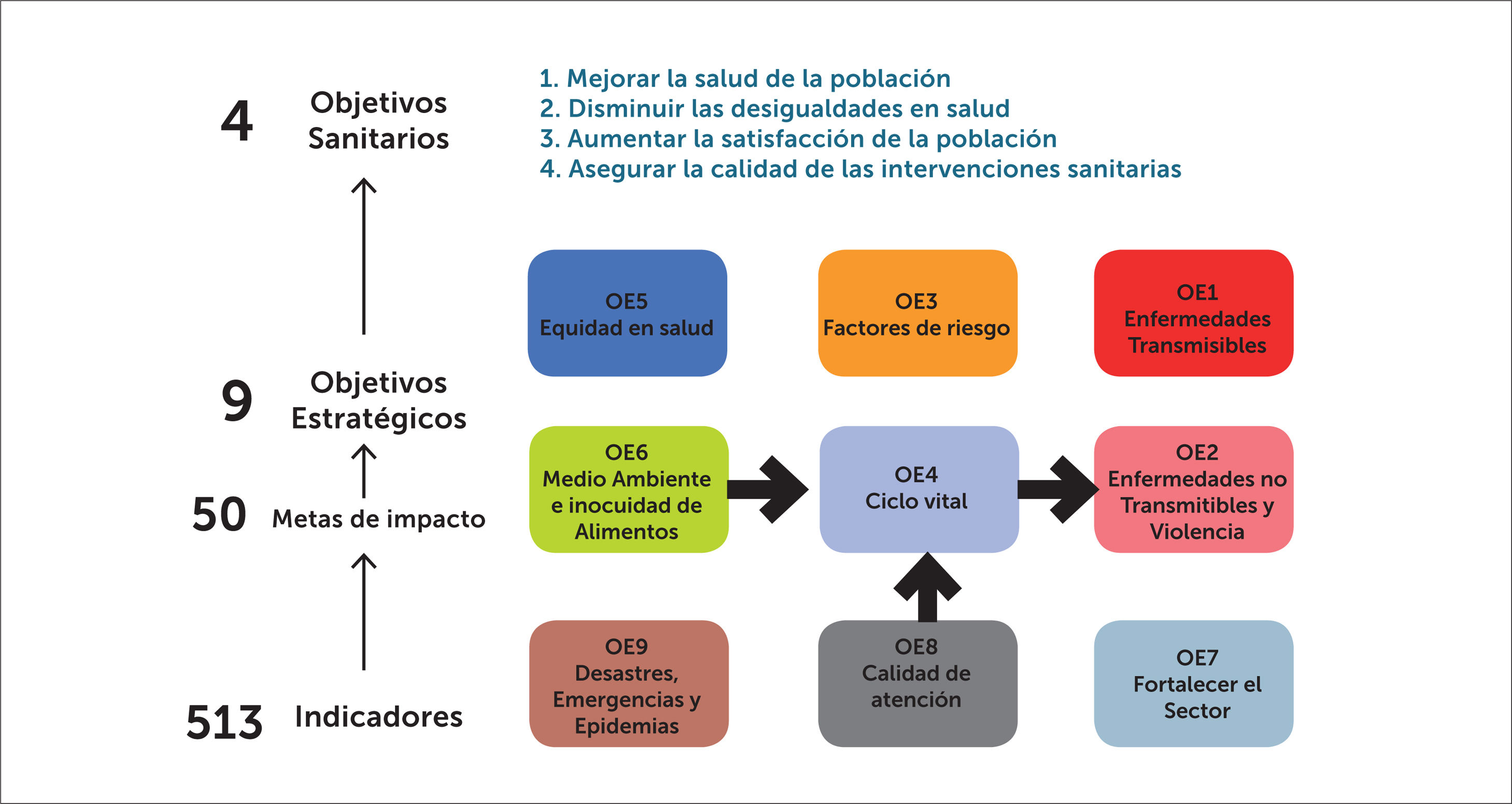
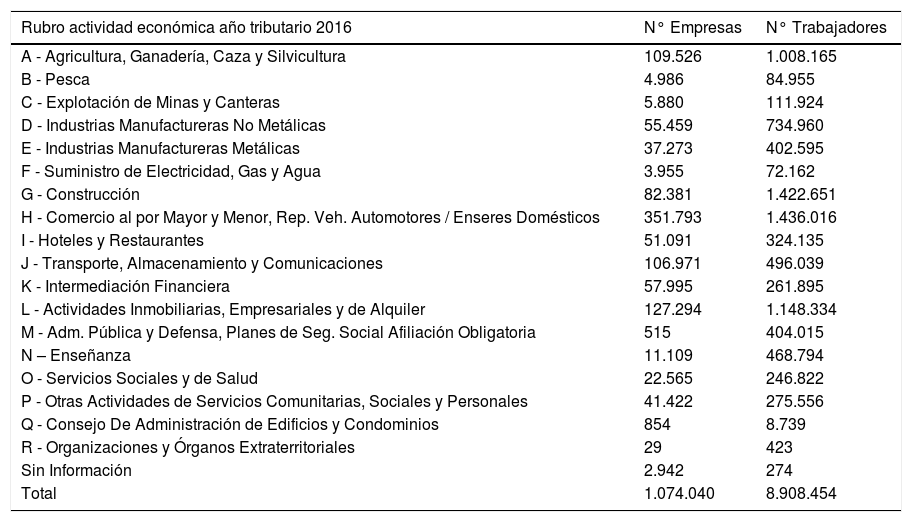
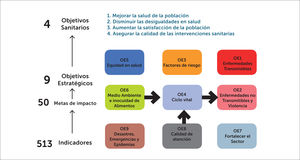
Durante el ciclo vital las vacunas son la medida de salud pública más efectiva y con mayor beneficio para la humanidad en la prevención de enfermedades. En la “Estrategia Nacional de Salud” de Chile1, el proceso de vacunación es relevante. Incluye nueve objetivos estratégicos donde actuar: enfermedades transmisibles; enfermedades crónicas no transmisibles/accidentes/violencia; factores de riesgo; ciclo vital; medio ambiente e inocuidad alimentaria, equidad; fortalecimiento del sector de la salud; calidad de atención; y desastres/emergencias/epidemias (figura 1). En Chile, al año 2018, había 8.364.282 trabajadores, agrupados en 18 rubros de la actividad económica (tabla 1), según datos de la Superintendencia de Seguridad Social, SUSESO, de los cuales 6.105.926 (73%) estaban protegidos por la Ley 16.7442. Según la información de la Encuesta Nacional de Salud 2018, se podría extrapolar que el perfil de salud de los adultos en edad laboral (20-64 años) en Chile, incluye tabaquismo (30,7 a 40,4%); sedentarismo (81,2 a 93%); sobrepeso y obesidad (58% a 81%); y sindrome metabólico (40,1%), lo cual da un perfil de alto riesgo cardiovascular poblacional. Adicionalmente, la exposición a riesgos ocupacionales puede presentar sinergia en las enfermedades crónicas, que también pueden agravarse por infecciones inmunoprevenibles3.
Estadísticas de empresas por rubro de actividad económica, según Servicio de Impuestos Internos, Chile 2016
| Rubro actividad económica año tributario 2016 | N° Empresas | N° Trabajadores |
|---|---|---|
| A - Agricultura, Ganadería, Caza y Silvicultura | 109.526 | 1.008.165 |
| B - Pesca | 4.986 | 84.955 |
| C - Explotación de Minas y Canteras | 5.880 | 111.924 |
| D - Industrias Manufactureras No Metálicas | 55.459 | 734.960 |
| E - Industrias Manufactureras Metálicas | 37.273 | 402.595 |
| F - Suministro de Electricidad, Gas y Agua | 3.955 | 72.162 |
| G - Construcción | 82.381 | 1.422.651 |
| H - Comercio al por Mayor y Menor, Rep. Veh. Automotores / Enseres Domésticos | 351.793 | 1.436.016 |
| I - Hoteles y Restaurantes | 51.091 | 324.135 |
| J - Transporte, Almacenamiento y Comunicaciones | 106.971 | 496.039 |
| K - Intermediación Financiera | 57.995 | 261.895 |
| L - Actividades Inmobiliarias, Empresariales y de Alquiler | 127.294 | 1.148.334 |
| M - Adm. Pública y Defensa, Planes de Seg. Social Afiliación Obligatoria | 515 | 404.015 |
| N – Enseñanza | 11.109 | 468.794 |
| O - Servicios Sociales y de Salud | 22.565 | 246.822 |
| P - Otras Actividades de Servicios Comunitarias, Sociales y Personales | 41.422 | 275.556 |
| Q - Consejo De Administración de Edificios y Condominios | 854 | 8.739 |
| R - Organizaciones y Órganos Extraterritoriales | 29 | 423 |
| Sin Información | 2.942 | 274 |
| Total | 1.074.040 | 8.908.454 |
Disponible en: http://www.sii.cl/estadisticas/empresas_rubro.htm
En el mundo anualmente ocurren 374 millones de accidentes laborales y mueren 2,78 millones por accidentes y enfermedades relacionadas con el trabajo, equivalente a una carga económica de 3,94% del PIB global. Es necesario crear conciencia de la importancia de proteger la salud de los trabajadores, del riesgo de adquirir algunas enfermedades transmisibles, contribuyendo a evitar muertes prematuras, discapacidad y consultas médicas, entre otras4. De este modo, se describen dentro de los objetivos de vacunar a la población laboral el prevenir las enfermedades directamente relacionadas con los riesgos ocupacionales; evitar el ausentismo laboral; proteger a los trabajadores con comorbilidades del riesgo de padecer determinadas enfermedades transmisibles; y evitar que los trabajadores sean fuente de contagio de enfermedades transmisibles para otros trabajadores, su familia o para otros miembros de la comunidad.
Es por esto, que la prevención, conceptualizada en salud del trabador, en distintos niveles, es una herramienta estratégica para gestionar el riesgo y así evitar el daño5. La prevención primordial, es el nivel más adecuado donde actuar. Consiste en controlar y cautelar que no se generen agentes de riesgo que afecten la salud del trabajador, en las etapas anteriores a instalar un proceso productivo. Si el riesgo está presente, la prevenciónprimaria, consiste en mantenerlo en niveles en que la epidemiología indica que no habría daño durante una vida laboral de exposición, pero el individuo debe asumir conductas protectoras. Si el riesgo supera los límites legales6, se debe proceder a la prevenciónsecundaria, protegiendo al trabajador con elementos de protección personal (EPP). Si se produce el daño, el nivel de prevenciónterciario, incluye el manejo clínico, evitar la progresión, la rehabilitación y manejo de secuelas.
El financiamiento y otorgamiento de las prestaciones preventivas, curativas y económicas relacionadas con salud laboral, según la Ley 16.744 de Accidentes del Trabajo y Enfermedades Profesionales7 es a través de organismos administradores de la Ley (OAL) como lo son el Instituto de Salud Laboral (ISL), equivalente OAL del Estado; Mutualidades como la Asociación Chilena de Seguridad (ACHS), Mutual de Seguridad de la Cámara Chilena de la Construcción (MCChC), Instituto de Seguridad del Trabajo (IST); y OAL con administración delegada (Codelco, Pontificia Universidad Católica). A esta Ley están afiliados todos los trabajadores con contrato y desde el 2019, los trabajadores independientes que emiten boletas a honorarios8. De esta forma, la vacunación de la población laboral tendría como vías de financiamiento al Estado, a través del Programa Nacional de Inmunizaciones (PNI) y a los empleadores para las vacunas contra agentes de riesgo específicos que no están incluidas en PNI.
En el Código del Trabajo9, Libro II “De la Protección a los Trabajadores”, artículo 184 se indica que “El empleador estará obligado a tomar todas las medidas necesarias para proteger eficazmente la vida y salud de los trabajadores, informando de los posibles riesgos y manteniendo las condiciones adecuadas de higiene y seguridad en las faenas, como también los implementos necesarios para prevenir accidentes y enfermedades profesionales”. En el artículo 154 se indica que la empresa debe contar con un “Reglamento Interno de Orden, Higiene y Seguridad” y se enumeran las disposiciones que debe contener, indicando que deben incluirse “las normas e instrucciones de prevención, higiene y seguridad que deban observarse en la empresa o establecimiento”, lo que implica que se deben definir los EPP según el riesgo; y también deben incluirse “las sanciones que podrán aplicarse por infracción a las obligaciones que señale este reglamento, las que sólo podrán consistir en amonestación verbal o escrita y multa de hasta el veinticinco por ciento de la remuneración diaria”10. El incumplimiento por parte de la empresa de no contar con un reglamento interno que contenga las cláusulas establecidas como las sanciones descritas implica una falta “grave”, que da origen a multas, dependiendo del número de trabajadores de la empresa. También es “falta gravísima”, el incumplimiento de los artículos 184, incisos 1° y 2°, y 506 del Código del Trabajo, que hacen referencia a “no mantener las condiciones adecuadas de seguridad y salud laboral al no vigilar que los trabajadores cumplan correctamente los procedimientos de trabajo, establecidos por la empresa para el puesto de trabajo o proceso”11.
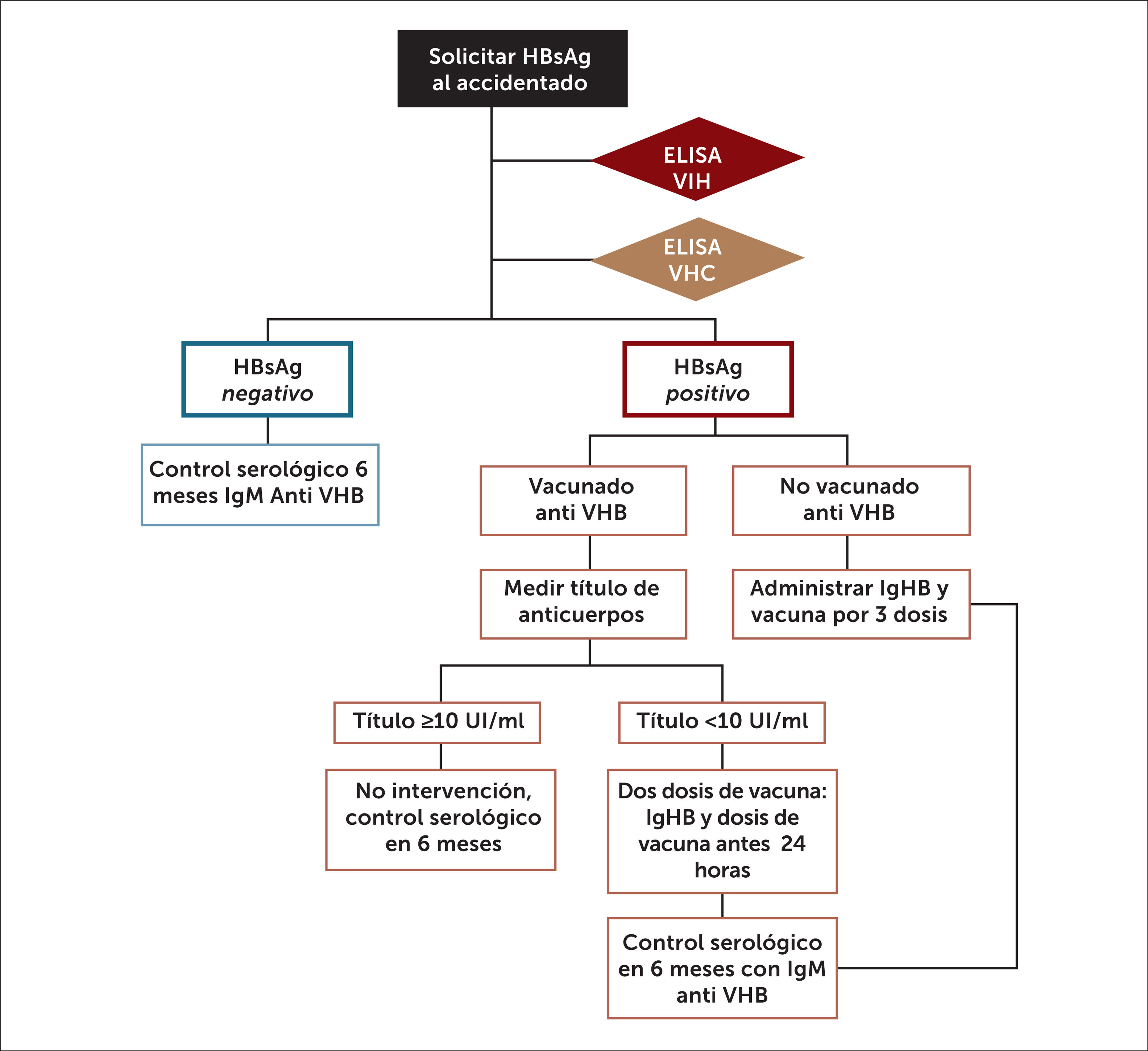
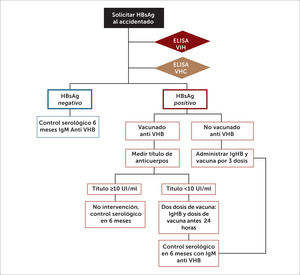
RIESGOS BIOLÓGICOSEl riesgo biológico laboral de microorganismos patógenos incluye a los genéticamente modificados, cultivos celulares y endoparásitos humanos que pueden causar infección, alergia o toxicidad en el trabajador expuesto. Estos riesgos deben ser manejados con un sistema de gestión que evite o disminuya la exposición. Los EPP son la barrera entre el agente y el trabajador y deben cumplir criterios de idoneidad definidos por el Instituto de Salud Pública (ISP)12. El Decreto Supremo (DS) 594/1999, artículo 53 indica que el empleador debe proporcionar a los trabajadores libres de costo, los EPP adecuados al riesgo, y que los trabajadores deberán usarlos en forma permanente mientras se encuentren expuestos6. En Chile se desconoce cuántos trabajadores están expuestos a riesgos biológicos. La población objetivo del MINSAL durante la campaña de influenza 2019, incluyó 402.384 trabajadores agrícolas, criaderos de cerdos y personal de salud público y privado13. En el Centro Información Toxicológica Universidad Católica, CITUC, entre 2006 y 2009, el riesgo biológico más frecuente reportado fue la autoinoculación con vacunas usadas en salmonicultura y, en segundo lugar, las picaduras y mordeduras. Dentro de éstas últimas, la mordedura de Loxoceleslaeta es la más frecuente14. En el personal de salud, los accidentes cortopunzantes son de vital importancia y cuentan con protocolos específicos para su manejo. En la figura 2 se presenta un algoritmo en caso de accidente cortopunzante, contaminado con sangre o secreciones de paciente con HBsAg+.
Las vacunas son un EPP de tipo biológico que protegen contra agentes de riesgo biológicos inmunoprevenibles, equivalente a un EPP de tipo físico como un protector auditivo, zapatos de seguridad y/o guantes que protegen contra traumas acústicos y accidentes. En este contexto legal, la vacunación es imperativa para el personal expuesto, ya que es una medida costo-efectiva en la prevención de enfermedades transmisibles inmunoprevenibles. Cuando un trabajador se incorpore a una nueva empresa con exposición a riesgos biológicos, el nuevo el empleador deberá verificar que el trabajador cuente con el esquema completo de vacunación y si aún se encuentra en el tiempo de inmunidad que otorga la vacuna correspondiente. Cuando no se cumpla algunas de estas condiciones el nuevo empleador deberá vacunar al trabajador.
RECOMENDACIÓN DE VACUNAS E INMUNIZACIONESInternacionalmente, la vacunación a los trabajadores es una norma. Varios países han incorporado, recomendaciones según actividad y vacunas a utilizar15-19. La revisión 2006-2015 de las infecciones laborales en Estados Unidos mostró que las actividades con más frecuencia de casos fueron el personal de salud, de laboratorio, el trabajo con animales y trabajadores de servicios públicos20. En Chile, el documento del ISP, “Situación de vacunación de trabajadores y trabajadoras”, indica que los grupos de trabajadores expuestos a riesgo y susceptibles de vacunación preventiva son el personal sanitario, personal que ocupa puestos claves en la comunidad (bomberos, socorristas, policías, protección civil); trabajadores de laboratorios clínicos, y de investigación microbiológica; trabajadores de instituciones cerradas como cárceles, centros geriátricos, y de discapacitados psíquicos; trabajadores docentes, en especial jardines infantiles y guarderías; personal de limpieza en contacto con residuos; trabajadores en contacto con aguas contaminadas, colectores, aguas estancadas, aguas servidas, saneamiento ambiental; trabajadores en centros de producción o manipulación de alimentos; trabajadores de limpieza, lavandería, recolección de residuos; trabajadores no sanitarios expuestos a sangre, pinchazos u otros fluidos contaminantes como manicuristas, podólogas y personas que realizan tatuajes; trabajadores en contacto con animales salvajes (zoológicos, animalarios); mineros; veterinarios; y trabajadores agropecuarios21.
Además de la normativa de protección cuando se está expuesto a riesgo biológico y la obligatoriedad de usar el EPP, que en este caso, sería la vacuna, existe otra normativa legal dada por el Ministerio de Salud a través del Decreto 865 Exento del 26 de septiembre 2015, que modifica al decreto n°6 exento del 2010. En este decreto 865 se define que la vacunación es obligatoria para las enfermedades inmunoprevenibles de la población del país.
Si bien las vacunas están dirigidas a microrganismos específicos, una misma vacuna puede ser preventiva o terapéutica, tener distintos objetivos y fuentes de financiamiento. Algunas condiciones para mencionar corresponden a:
a) Vacunas como elemento de protección personal, por riesgo específico, con financiamiento por el empleador: vacunas por riesgo de exposición o accidente laboral como hepatitis B, hepatitis A, enfermedad meningocócica y tétanos; y vacunas para personal que viaja a zonas con endemia o mayor incidencia de infecciones específicas como fiebre amarilla o encefalitis japonesa.
b) Vacunas para proteger al trabajador y evitar que sea riesgo para otros o disminuir ausentismo laboral por ser personal crítico o sistema de beneficio para el personal, con financiamiento por el empleador: vacuna influenza anual, vacuna antineumocócica, vacuna contra papiloma humano (VPH) y vacuna contra hepatitis B en trabajadores sexuales; y vacuna contra Coxiella burnetti para trabajadores de ganadería bovina.
c) Vacunas en trabajadores que son población objetivo de campañas financiadas por el Estado a través del PNI: vacuna influenza en las campañas estatales, acorde a sus definiciones anuales de poblaciones de riesgo, como, por ejemplo, embarazadas, >65 años, enfermedades crónicas, personal de salud, personal de industria avícola y criadores de cerdos, personal de salud pública incluidas FF.AA. y voluntarios. En casos de brotes epidemiológicos: vacuna antimeningococo en personal de salud, de laboratorio, en profesores, parvularias, personal de cárceles; y vacuna antipertussis en estrategia capullo.
d) Vacunas en casos especiales de hacinamiento en albergues y cárceles, financiadas por el Estado a través del PNI: hepatitis A, hepatitis B, meningocócica.
e) Vacunas para evitar que el trabajador contamine y así asegurar la calidad de productos procesados como alimentos, financiadas por el empleador: fiebre tifoidea, hepatitis A.
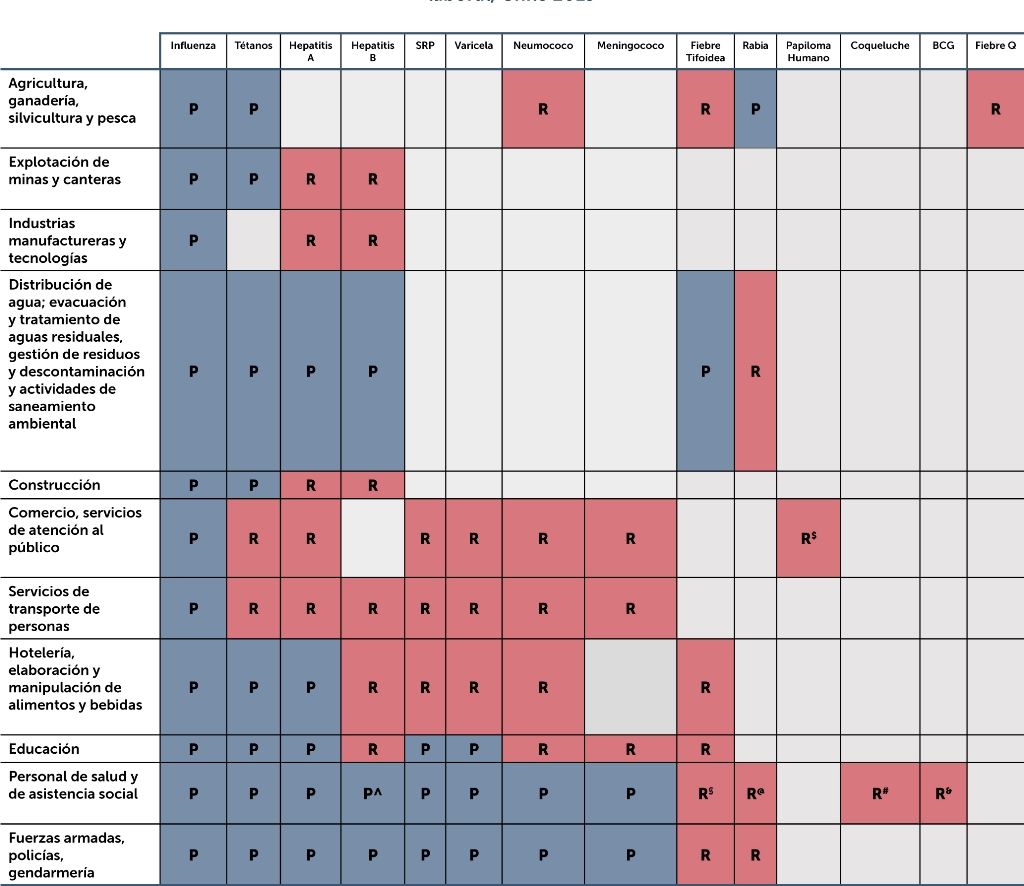
VACUNAS SEGÚN RIESGO LABORAL ESPECÍFICOSegún las recomendaciones internacionales, en Chile, hay variadas vacunas, según tipo de exposición laboral, las que se presentan en la tabla 3. El primer objetivo es que los trabajadores posean sus vacunas rutinarias al día. En el caso de las trabajadoras gestantes, deben y pueden recibir las vacunas inactivadas definidas para proteger a la madre, al feto y al recién nacido durante las primeras semanas de vida. Es importante tener presente que la embarazada no debe recibir vacunas vivas atenuadas.
Además, se debe considerar que las vacunas requieren de un tiempo entre 7-14 días, para inducir títulos de anticuerpos protectores, lo que podría acortarse en situaciones de dosis de refuerzo. También, la magnitud de esta respuesta inmune puede decaer en el tiempo, por lo que se debe tener en cuenta que, si persiste la exposición, se debe evaluar la necesidad de dosis de refuerzo, según recomendaciones específicas. La situación de bomberos en nuestro país requiere un análisis por separado, porque no poseen empleador y desarrollan tareas con riesgos laborales semejantes a los rescatistas, con reiteradas exposiciones. En Estados Unidos, se estima que los bomberos poseen entre 9% y 14% más de cáncer y de riesgo de morir por cáncer que el resto de la población22. Por ello, en este grupo se podría plantear el recibir vacunas contra hepatitis A y B, fiebre tifoidea, neumococo, refuerzos de tétanos, influenza anual, además de su calendario programático al día20,23.
InfluenzaLa influenza es un problema de salud pública global. Es una enfermedad inmunoprevenible, altamente transmisible con elevado potencial epidémico; tiene alta variabilidad antigénica y posibilidad de intercambio genético entre los virus de origen humano y animal y se estima que anualmente afecta entre un 5-15% de la población mundial. El estudio “Estimación de Carga de Influenza Asociado a Hospitalizaciones y Muerte. Chile 2012-2014” realizado por MINSAL estimó que por influenza anualmente, 5320 personas se hospitalizaron y 447 personas fallecieron24. Respecto de la incapacidad laboral, el año 2018, el 14.2% de las licencias médicas por enfermedad común correspondieron a enfermedades respiratorias y ello significó 929.629 días de reposo laboral25. Se utiliza la vacuna inactivada para prevenir complicaciones de la influenza, la cual debe repetirse anualmente, incorporando grandes grupos poblacionales y de exposición laboral con vacuna trivalente inactivada. Se incluyó en el PNI para adultos desde los 65 años, enfermos crónicos y personal de salud, a partir del año 1982.
Dentro de los grupos objetivos de la vacunación contra influenza del PNI para el 2020, se incluyen los siguientes categorías, que pueden considerar a adultos en edad laboral, como el personal del área de la salud, lo que incluye al personal de salud de las Fuerzas Armadas y de orden, y a los alumnos en práctica y voluntarios del sistema público y privado; trabajadores de avícolas y de criaderos de cerdos; personal que trabaja en jardines infantiles; alumnos de escuelas de formación de las FF.AA., Carabineros y PDI; trabajadores/as sexuales; bomberos; establecimientos de atención cerrada, como el servicio nacional de menores y establecimientos psiquiátricos, y personal de apoyo que desempeñe funciones en estos establecimientos; todas las embarazadas, independiente de su edad de gestación; personas de 65 años y más; personas con diabetes; enfermedades pulmonares crónicas, como el asma bronquial, EPOC, fibrosis quística y fibrosis pulmonar; cardiopatías congénitas, reumática, isquémica y miocardiopatías de cualquier causa; enfermedades neuromusculares congénitas o adquiridas que determinan trastornos de la deglución o del manejo de secreciones respiratorias; hipertensión arterial en tratamiento farmacológico; obesidad mórbida; insuficiencia renal en etapa 4 o mayor; insuficiencia renal en diálisis; insuficiencia hepática crónica; enfermedades autoinmunes como lupus, escleroderma, artritis reumatoide, enfermedad de Crohn; cáncer en tratamiento con radioterapia, quimioterapia, terapias hormonales o medidas paliativas de cualquier tipo; infección por VIH; y finalmente, inmunodeficiencias congénitas o adquiridas26. Sin embargo, también es recomendable en otras condiciones laborales, para disminuir el riesgo de influenza y el ausentismo laboral. Durante el 2019 se alcanzó una cobertura global del 89%, destacando un 98% en personal de salud, 94% en embarazadas, 68,3% en mayores de 65 años y 119% en trabajadores de avícolas y de criaderos de cerdos, entre otros27. En nuestro país se dispone además de formulaciones inactivadas tetravalentes, sin preferencia actual por sobre la vacuna trivalente. Existen otras formulaciones, que pueden incluir adyuvantes, dosis reforzadas, vivas atenuadas inhaladas, tanto tri como tetravalentes, pero que no están disponibles en este momento en Chile.
TétanosEl toxoide tetánico protege contra toxinas de Clostridiumtetani, cuyas esporas están presentes en forma ubicua en suelo, superficies húmedas, heces de animales y humanos. En nuestro PNI la vacuna antitetánica está disponible desde 1975, administrándose actualmente a los 2, 4, 6 meses, con refuerzos a los 18 meses, 1° básico, 8° básico y en embarazadas desde las 28 semanas de gestación. En exposición por accidente, se usa inmunoglobulina antitetánica y vacuna en esquema según tipo de herida y antecedente de vacunación. Si el trabajador tiene esquema completo o refuerzo desde hace más de 10 años, se debe usar toxoide tetánico. Las mordeduras por animales se consideran heridas sucias, por lo que también requieren de vacunación con toxoide tetánico28,29 (tabla 2). En el caso de realizar una serie primaria de vacunación en adultos, se recomiendan administrar 3 dosis, de manera que las dos primeras queden espaciadas con 1 a 2 meses de diferencia, y la tercera dosis se administre al menos 6 a 8 meses después de la segunda dosis. Algunos países recomiendan administrar las 3 dosis con un mínimo de 1 mes de diferencia entre ellas30.
Esquema de vacunación antitetánica según tipo de herida y antecedente de vacunación
| Antecedentes de vacunación con componente antitetánico | Herida limpia | Herida sucia | ||
|---|---|---|---|---|
| Toxoide tetánico | Inmunoglobulina antitetánica | Toxoide tetánico | wInmunoglobulina antitetánica | |
| Esquema completo y/o refuerzo hace menos de 5 años | No | No | No | No |
| Esquema completo y/o refuerzo hace menos de 5 a 10 años | No | No | Si1 | No |
| Esquema completo y/o refuerzo hace más de 10 años | Si1 | No | Si1 | No |
| Sin antecedentes de vacuna o desconocido | Si2 | No | Si2 | Si3 |
§ Disponible en https://www.leychile.cl/Navegar?idNorma=1082177.
Sugerencia de vacunas prioritarias y recomendadas para trabajadores, entre 18 y 65 años, según actividad laboral, Chile 2019*
*Las vacunas que se exponen a continuación son una recomendación y solo consideran el riesgo laboral, no las comorbilidades que se tengan de base, las cuales deben ser resueltas a través del PNI utilizando las “Recomendaciones para la vacunación de pacientes con necesidades especiales por patologías o situaciones de riesgo”, programas GES, y Ley Ricarte Soto, respectivas.
P: vacunas prioritarias; R: vacunas recomendables
^ Se considera medir títulos en caso de riesgo de exposición sostenido y vacunación durante tabaquismo activo, obesidad o inmunodeficiencia concomitante, además de situaciones post-exposición.
§ Considerar en trabajadores de laboratorio en contacto con S typhi y personal de saneamiento ambiental
@ Considera vacunación pre-exposición solo a veterinarios y al personal de salud que trabaja con virus rábico. En el caso de los trabajadores de salud ambiental se considera su uso post-exposición si lo requirieran
$ Incluye a trabajadores sexuales y de establecimientos de entretenimiento con potencial riesgo de contacto sexual
# Incluye a en personal de salud, principalmente en unidades de neonatología y maternidad
& Evaluar de manera excepcional en trabajadores no vacunados con BCG, que presenten exposición a cepas de M tuberculosis multi-resistente
Esquemas de vacunación sugeridos
Influenza: 1 dosis, repetir anualmente
Tétanos: 3 dosis en primovacunación (0, 1 y 6 meses) o 1 dosis de refuerzo c/10 años
Hepatitis A: 2 dosis, separadas por 6 meses
Hepatitis B: 3 dosis, 0, 1 y 6 meses.
SRP: 2 dosis en los no vacunados; 1 dosis de refuerzo en susceptibles. Considerar tamizaje. No usar en inmunosuprimidos
Varicela: 2 dosis, 0 y 2 meses, en los susceptibles no vacunados. Considerar tamizaje. No usar en inmunosuprimidos
Neumocócica: 1 dosis de vacuna polisacárida 23 valente o conjugada 13 valente
Meningocócica: 1 dosis de vacuna conjugada tetravalente contra serogrupos ACWY, o 2 dosis (0 y 2 meses) de vacuna recombinante de 4 componentes contra serogrupo B
Fiebre Tifoidea: 1 dosis, vacuna de polisacárido Vi
Rabia: esquema de 3 dosis para pre-exposición (0, 7 y 28 días); y 5 dosis en post-exposición (0, 3, 7, 14 y 28 días)
Virus Papiloma Humano: 3 dosis, 0, 2 y 6 meses
Coqueluche: 3 dosis en primovacunación (0, 1 y 6 meses) o 1 dosis de refuerzo c/10 años, con formulación acelular y presentación combinada
BCG: 1 dosis
Fiebre Q: 1 dosis, sin refuerzos. Considerar tamizaje previo a su administración. No usar en embarazadas.
Vacuna inactivada, muy segura e inmunogénica, con esquema de 2 dosis para adultos, separadas por al menos 6 meses. En Chile, la hepatitis A se presenta como endemia intermedia, distribuyéndose de manera heterogénea en el país, con ciclos epidémicos que desde 1990 ocurren cada 3-5 años, siendo el último durante el 2017-2018, asociándose a transmisión fecal-oral31. Desde el año 2005, el 70% de los casos se han presentado en sujetos mayores de 15 años. Nuestro PNI inició la vacunación universal contra hepatitis A con 1 dosis a los 18 meses desde el 201832. Desde el punto de vista laboral, su indicación está enfocada principalmente en manipuladores de alimentos y en personal que trabaja en evacuación y tratamiento de aguas residuales, descontaminación y actividades de saneamiento ambiental, entre otras. Existe una vacuna combinada para hepatitis A y B, pudiendo usarse en esquema de 3 dosis, 0, 1 y 6 meses.
Hepatitis BVacuna recombinante contra el virus de la hepatitis B (VHB). Chile es país de baja endemicidad, afectando al 0,15% de la población; el grupo de 20-39 años concentra el 58% de los casos33. El riesgo de infección laboral está dado por transmisión percutánea cuyo riesgo de enfermar en accidente de alto riesgo, sin vacuna ni protección es del 30%33. El hepatocarcinoma y la cirrosis hepática a largo plazo son considerados enfermedades profesionales, si el trabajador se infectó por la exposición en su actividad laboral. La medida preventiva más eficaz, es la vacunación, cuya eficacia es del 85 a 90% posterior a la tercera dosis. Se considera inmunizado aquel sujeto que alcanza títulos de anticuerpos anti HBs ≥10 UI/ml, los cuales pueden declinar con el tiempo, pero frente a nueva exposición se produce una respuesta inmune adecuada33. La vacuna está disponible en nuestro PNI desde el 2005, administrándose actualmente en recién nacidos, 2, 4, 6 meses, con refuerzo a los 18 meses, por lo que nuestros adolescentes hasta los 15 años debieran estar vacunados contra VHB. El año 2010, se amplía a otros grupos de riesgo: personal clínico, hemodializados, portadores hepatitis C y hemofílicos. El Decreto Exento MINSAL N° 865/2015, que dispone vacunación obligatoria contra enfermedades inmunoprevenibles34, agrega que deben vacunarse contra hepatitis B, quienes son contactos de personas portadoras de hepatitis B, peritoneo-dializados, insuficiencia renal crónica, las personas con VIH, las trabajadoras sexuales y personas víctimas de abuso sexual. En este último caso, si el trabajador es víctima de abuso en su trabajo o en el trayecto a, o, desde su trabajo, el evento pasaría a ser considerado o un accidente del trabajo o un accidente de trayecto y es cubierto por la Ley 16.744. El esquema preventivo para el trabajador es 0, 1 y 6 meses, sin requerir dosis de refuerzo, transcurridos diez años desde la inmunización34,35. En caso de interrupción del esquema vacunal entre la primera y segunda dosis, se debe administrar cuanto antes, espaciándola por al menos 4 meses con la tercera dosis. Si esta interrupción ocurre entre la segunda y tercera dosis se debe poner al día cuanto antes. En casos específicos, en que se requiera completar inmunización en períodos más breves, se puede utilizar el esquema acelerado 0, 7 y 21 días, con dosis de refuerzo a los 6 o 12 meses. En ningún caso se requiere reiniciar esquemas vacunales. Existe un protocolo para manejo post exposición por accidente con fluidos biológicos que considera el estado vacunal del trabajador y la positividad de la fuente. En caso de accidente de riesgo con paciente fuente positiva y trabajador no vacunado o con títulos anti HBs <10 UI/ml se debe usar inmunoglobulina contra hepatitis B (IgHB) asociado a vacunación antes de 24 horas, con seguimiento serológico por 6 meses35,36. En la figura 2 se incluye el flujograma de manejo incluido en la Guía MINSAL 2013 sobre Manejo y tratamiento de infección por virus hepatitis B36.
Sarampión, rubéola, paperasSe utiliza vacuna tres vírica, que contiene virus vivos atenuados de sarampión, rubéola y parotiditis. Fue introducida en Chile desde 1991. Se administra programáticamente a los 12 meses y 1° básico; en caso de viaje, desde los 6 meses en niños que tienen menos de 2 dosis. Desde el 2011 a la fecha se administra vacuna tresvírica a todo viajero que haya nacido entre 1971 y 1981, especialmente aquellos que se desplazan a zonas donde estos virus sean endémicos o existan brotes. Si no hay antecedente de dos dosis de vacuna en trabajadores, se recomienda vacunar directamente o según tamizaje de susceptibilidad37. En Chile, se han hecho campañas de puesta al día los años 1992, 1996 y 1997 a las que se agregaron campañas de seguimiento cada 5 años desde el 2000 para niños entre 1 y 5 años 11ms 29 días. Debido al aumento de casos en el mundo y el ingreso de casos importados, durante el año 2019, se realizó una campaña de vacunación para el grupo entre 20 y 24 años.
Ante un brote o caso importado de sarampión se recomienda la administración de una dosis a los contactos en las primeras 72 horas.
El personal de salud debiera tener inmunidad para parotiditis, sarampión y rubéola por haber sido vacunado con vacuna tres vírica o tener evidencia de inmunidad con serología IgG, de lo contrario, el trabajador debiera recibir dos dosis de vacuna, separadas por 28 días38. La vacunación del personal sanitario es fundamental. El estudio de un brote en Arizona que afectó a dos hospitales significó 15.210 horas de trabajo perdidas y tuvo un costo de US$ 800.000 39. También es costo-efectiva. Dos dosis tienen una efectividad de 99%. El año 2017 hubo un aumento de casos en Italia y el estudio de Coppetta mostró que el 22,3% de los casos se presentaron en el ambiente hospitalario y que el 6,6% del personal de salud se infectó. También observaron poca adherencia a la vacuna. Durante un año pusieron en vigilancia a 2.940 trabajadores sanitarios y mediante serología IgG y antecedente de no vacunación, se identificaron 450 trabajadores susceptibles que fueron vacunados. Los autores compararon el costo de la campaña de vacunación con tamizaje previo para identificar los susceptibles y sin tamizaje previo. El usar tamizaje que también tiene costo, significó un ahorro de €146.262. por lo que ellos sugieren usar la vacunación tres vírica solo en trabajadores susceptibles mediante la identificación previa de ellos a través de serología.
La vacuna tres vírica está contraindicada en el embarazo y en inmunodeprimidos, por ser una vacuna a virus vivos40. El embarazo debe posponerse 28 días post-vacunación. En caso de haberse administrado 1 dosis, estando embarazada, no es razón para suspender el embarazo.
VaricelaVacuna viva atenuada de virus varicela zoster, incorporada al PNI desde el 202041. Recomendable en 2 dosis, separadas por 8 semanas, para personas sin antecedentes de haber tenido la enfermedad ni de vacunación, contactos con familiares de personas inmunocomprometidas, personas que viven o trabajan en ambientes en los que su transmisión es probable (ej. profesores, trabajadores de salas cunas y jardines infantiles, funcionarios de salud), residentes y personal de instituciones (ej. asilos); y personas que viven o trabajan en ambientes en los que se reconoce un mayor riesgo de la transmisión (ej. universitarios, reclusos, funcionarios carcelarios, personal militar, funcionarios de salud)17,42. En caso de brotes institucionales podría utilizarse vacuna en los susceptibles, antes de las 96hrs de contacto. En el caso de susceptibles inmunocomprometidos, embarazadas, recién nacidos cuya madre presenta varicela entre 5 días antes y 2 días después del parto, y prematuros hospitalizados no se recomienda la vacuna, sino que se debe usar inmunoglobulina específica hiperinmune43. La vacuna de varicela está contraindicada durante el embarazo44.
NeumococoExisten vacunas conjugadas y polisacáridas, contra neumococo. La vacunación en adultos se inició en campañas el 2007 con vacuna polisacárida 23 valente (PSV23) para adultos >75 años, introduciéndose el 2010 en el PNI para adultos de 65 y más años45. En lactantes, se incorporó desde el 2011 con vacuna conjugada 10 valente y desde el 2017 con vacuna 13 valente (PCV13). En el caso de personas con enfermedades crónicas, se recomienda el uso secuencial de PCV13 y PSV23, espaciadas por 8 semanas o 1 año, según edad y comorbilidad35. Las coberturas de PSV23 en nuestro país para adultos mayores de 65 años varían desde un 30,8% hasta 60,5%46. La vigilancia del ISP de enfermedad neumocócica invasora para el periodo 2007-2017 en este mismo grupo de personas, demostró que el 72,8% de las cepas estaban incluidas en la vacuna PSV23 y el 57,7% en la PCV13. En base a esta información y a la baja eficacia de PCV13 en serotipos no vacunales en mayores de 65 años47, se ha considerado importante mantener la vacuna PSV23 en el PNI y reforzar su adherencia, antes de modificar su indicación46. No hay actividades económicas específicas que aumenten el riesgo de neumonía por neumococo, pero neumopatías ocupacionales como silicosis y otros, la mayor expectativa de vida y disminución de ingresos que está prolongando la edad de retiro laboral, implica que habrá una población mayor con inmunosenescencia y más riesgo de enfermar, que podría recibir esquema de vacuna conjugada y después de 1 año, vacuna polisacárida. Este esquema secuencial y el mejor momento para vacunar a los adultos mayores de 50 años, antes de que se establezca la inmunosenescencia todavía no está claro, y aún se discute a nivel nacional e internacional17,48,49.
MeningococoEl meningococo se transmite persona a persona por gotitas, con secreciones o elementos contaminados que contactan la vía respiratoria o conjuntiva, aumentando su riesgo con el hacinamiento50,51. En Chile, existen vacunas conjugadas tetravalentes contra serogrupos A, C, W e Y y vacuna recombinante contra serogrupo B. Desde el 2012 se inició la administración de vacuna tetravalente conjugada en niños entre 9 meses y 4 años, incorporándose el 2014 al calendario nacional a los 12 meses de edad52. En este mismo periodo se utilizaron adicionalmente vacunas polisacáridas tetravalentes para personal de salud de los servicios de urgencia pediátricos y parte del personal de laboratorio microbiológico53. La vacuna recombinante contra meningococo B, 4CMenB, se utiliza en adultos en esquema de 2 dosis, separadas por 2 meses, sin tope de edad. La necesidad de dosis de refuerzo de esta vacuna no está establecida, pero podría ser utilizada de forma semejante a vacunas conjugadas tetravalentes, cada cinco años, si es que persiste el factor de riesgo de exposición. La circular 32/2014 MINSAL indica que debe vacunarse el personal de laboratorio microbiología, servicio de urgencia, unidad de paciente crítico y de aislamiento de los establecimientos públicos y privados54. Dada la epidemiología de la enfermedad meningocócica de los últimos años, con predominio de circulación de los serogrupos W y B en los últimos 8 años, los riesgos son semejantes, independientes del serogrupo, por lo que la cobertura debiera incluir ambos tipos de vacunas, para serogrupos ACWY y B 17,55-57.
Fiebre tifoideaLa fiebre tifoidea ha experimentado un fuerte descenso desde las altas endemias en la década de 1950 hasta tasas menores a 1 por 100.000 habitantes, durante el 2018. Esta disminución se acentuó desde 1992 debido a los logros en saneamiento básico, a partir de la Campaña de Prevención contra el Cólera58. Existen vacunas viva atenuada oral e inactivada inyectable, para proteger contra infección sistémica causada por Salmonellatyphi. Su transmisión es fecal-oral, por contacto entre individuos o a través del agua o de alimentos contaminados. La vacuna parenteral de polisacárido Vi está indicada a partir de los 2 años en viajeros a regiones donde es endémica, convivientes de portadores de S. typhi de zonas con alta incidencia de infección y trabajadores de laboratorio en contacto con bacterias y de saneamiento ambiental17.
RabiaVacuna inactivada contra el virus de la rabia. Su reservorio son los animales como murciélagos, perros, gatos y visones. Desde 1960 Chile ha incorporado la vacunación en humanos a través del programa nacional de control de rabia, el cual también incluye vacunaciones masivas de población canina, lográndose liberar de rabia humana producida por variante canina desde 1972. Por este motivo, actualmente en Chile no existe riesgo de rabia trasmitida a humanos por mordeduras caninas ni felinas, pero sí por murciélagos, cuyo último caso en humanos fue confirmado en 1996, logrando ser declarado libre de rabia humana desde 201059,60.
Según la norma técnica N°169 MINSAL, la vacuna preexposición se administra sólo quienes están expuestos a alto riesgo permanente con virus vivo de rabia, como veterinarios, funcionarios SEREMI o de servicios de salud que por razones laborales estén expuestos a animales susceptibles de trasmitir rabia, de estaciones cuarentenarias, de laboratorios de rabia o de programas de control de rabia. El esquema recomendado es de tres dosis, a tiempo 0, 7 y 28 días. De persistir la exposición, estos funcionarios deben recibir una dosis de refuerzo, e idealmente monitorear los niveles de anticuerpos neutralizantes cada 6 a 24 meses, repitiendo la dosis si estos están bajo 0,5 UI/ml17,61.
La vacunación post-exposición es gratuita en los establecimientos públicos y privados en convenio, consistiendo en cinco dosis, a los 0, 3, 7, 14 y 28 días. Su indicación es para aquella persona mordida, rasguñada o lamida en piel lesionada y/o mucosa por un animal sospechoso o diagnosticado rabioso; persona mordida por un animal vagabundo que desaparezca o muera posterior a la mordedura; persona mordida por un animal mamífero silvestre; persona mordida o que haya estado en contacto con murciélagos como manipulación a manos desnudas voluntaria o involuntariamente, haya entrado a lugares cerrados donde viven colonias sin usar protección respiratoria, o presencia de murciélagos en habitación, esto último ya que la mordida del murciélago no siempre es perceptible, sobre todo mientras la persona duerme. En caso de individuos previamente inmunizados sólo se requieren dosis los días 0 y 3, no siendo necesaria la aplicación de inmunoglobulina antirrábica humana (IGR). Si el accidente es de alto riesgo, sin vacunación preexposición, está indicado usar IGR, 20 UI/kg en la herida y el resto intramuscular en glúteo.
En general, las vacunas anti-rábicas inactivadas son seguras y bien toleradas. Las reacciones anafilácticas son excepcionales, siendo más frecuentes al recibir la dosis de recuerdo. Dada la gravedad del cuadro clínico, que puede llevar a la muerte si no se trata con inmunoprofilaxis específica, no existen contraindicaciones en el caso de mordedura por animal con rabia. El embarazo y lactancia no constituyen contraindicación para la profilaxis postexposición si está indicada.
Virus Papiloma HumanVacuna inactivada contra virus papiloma humano (VPH). El PNI incorporó la vacuna tetravalente desde el 2014 en 4° y 5° básico, inicialmente solo para mujeres, ampliándose para varones desde el 2019. Esta vacuna no contiene ADN viral, no es infecciosa ni oncogénica. Los genotipos oncogénicos incluidos son el 16 y 18 y los genotipos 6 y 11 para verrugas genitales. La protección contra infección por VPH depende de la cantidad de anticuerpos producidos por el huésped, la disponibilidad en el sitio de la infección y la persistencia de anticuerpos neutralizantes en el tiempo que protegen contra una nueva infección con ese mismo serotipo. La inmunogenicidad lograda por la población vacunada es mayor que la que lo logra por la infección en forma natural. Más del 99% de las mujeres entre 15 y 24 años responden a la vacunación con anticuerpos séricos contra los tipos de VPH contenidos en las vacunas62. En mujeres entre 15 y 26 años se demostró eficacia clínica para infecciones persistentes y neoplasias intraepiteliales (NIE) de cuello uterino mayores tipo 2 o 3, utilizando esquemas de tres dosis63. Su eficacia disminuye al aumentar la edad de vacunación primaria y si existe infección previa por genotipos vacunales64. En el caso de las mujeres entre 24 a 45 años, la eficacia evaluada por protocolo fue del 88,7% y del 47,2% en el grupo por intención de tratar, en base a infecciones persistentes, lesiones extragenitales y NIE 1+ relacionadas con los genotipos 6, 11, 16 o 1862. Ninguna vacuna antiVPH ha demostrado ser completamente efectiva, ni reemplazan el tamizaje con papanicolau.
En la población laboral, debiera incluirse a los trabajadores sexuales como vacuna preventiva hacia el trabajador y para quienes tienen contacto con ellos. Actualmente está indicada como vacuna post exposición en caso de víctimas de violencia sexual pudiendo ser considerada como accidente del trabajo o de trayecto. Esta vacuna es profiláctica y no terapéutica, por lo que su indicación, en el caso que ya estuviera infectado, previene la reinfección. El esquema recomendado para personas no vacunadas entre 9 años y 13 años es de 2 dosis, con un intervalo de 12 meses entre ellas, y desde 14 años en adelante se utilizan 3 dosis, administradas a los 0, 2 y 6 meses65.
CoquelucheVacuna inactivada, incorporada en Chile desde 1954 en lactantes, luego el 2013 se incorporó programáticamente para alumnos de 8° básico y desde octubre del 2017 en embarazadas desde la semana 28 de gestación, ambas en formulación dTpa29,66. En los últimos años, la proporción de casos en mayores de 10 años se ha incrementado, asociado a la disminución de sus títulos protectores, por lo que su actividad epidemiológica puede variar, pudiendo asociarse a brotes epidémicos, los que tienen mayor repercusión en la población menor de 1 año66,67. Su recomendación puede enfocarse en personal de salud, principalmente en unidades de maternidad, neonatología y pediatría42. Los adultos con antecedente de vacunación desconocida deben recibir un esquema de 3 dosis, separando las dos primeras por 4 semanas al menos y la tercera dosis a los 6-12 meses después de la segunda dosis. En caso de vacunación incompleta se debe recibir solamente las dosis faltantes67.
BCGVacuna BCG, incorporada en Chile desde 1927. Se usa dosis única en recién nacidos. Su eficacia en adultos y contra tuberculosis (TBC) pulmonar es un tema de controversia, por lo que no se considera habitualmente, excepto en sujetos no vacunados en situaciones específicas de prevención de tuberculosis latente o clínica por cepas muti resistentes a antimicrobianos68. Los trabajadores expuestos al bacilo de Koch o Mycobacterium tuberculosis, que atienden pacientes infectados o procesan muestras, tienen mayor riesgo de infección, lo que no significa enfermedad. De los infectados, un 5% desarrollará enfermedad en los 2 años siguientes y otro 5% en los años venideros. Los programas de vigilancia de trabajadores expuestos como personal de salud usan las siguientes estrategias: prueba de conversión de tuberculina (PPD), pruebas de liberación de interferón gama y tamizaje de sintomáticos respiratorios con radiografía de tórax y baciloscopias69.
La Norma Técnica MINSAL 2014 para el control y eliminación de la tuberculosis en Chile70, indica que todo individuo que se incorpora a actividades con riesgo de TBC, debe tener al ingreso una prueba de tuberculina o PPD (derivado proteico puridicado), examen de expectoración y radiografía de tórax. Si hay sospecha de contagio, se repetirá el PPD si éste fue negativo previamente. Si hay viraje y se descarta TBC activa, se indicará quimioprofilaxis. Se considera positivo un viraje igual o mayor a 10-15mm. Como herramienta de vigilancia en trabajadores expuestos, esta prueba tiene problemas de efectividad de detectar conversión, porque en los países en vías de desarrollo, en que la vacuna es obligatoria, a lo menos, el 50% de las personas tiene PPD+ al ingreso, por lo que el seguimiento sería solo para quienes tuvieron PPD– previamente. La conversión del PPD serviría como seguimiento en personas no vacunadas de países con baja endemia. En los países con alta endemia, también es difícil la interpretación porque no diferencia entre exposición previa o TBC activa. La vacuna BCG está contraindicada en el embarazo.
Fiebre QLa fiebre Q es una zoonosis, altamente transmisible, producida por Coxiellaburnetii, la cual se asocia a morbimortalidad significativas en adultos y niños. La transmisión a las personas ocurre principalmente por inhalación de polvo, gotas o aerosoles de fluidos de animales infectados, como placenta, líquido amniótico, leche, deposiciones y ocasionalmente por ingestión, exposición percutánea, transfusión o contacto sexual. Habitualmente la transmisión se da en contexto laboral, en personas que trabajan con ganado bovino, ovino o caprino, o por cercanía geográfica con áreas contaminadas con tejidos o deposiciones del reservorio70. El primer brote en Chile se describió en 1998. Posteriormente se han producido brotes en distintos lugares, especialmente el Sur de Chile70-73. Nuevos brotes en el sur podrían abrir la discusión respecto del uso de una vacuna inactivada para optimizar su control, sin embargo, no disponemos actualmente de ella. El protocolo de vigilancia ambiental y de trabajadores del MINSAL, considera las medidas preventivas de aseo y desinfección de instalaciones, elementos de protección personal, manejo de la ropa de trabajo y consumo de leche y alimentos73.
Australia es el único país del mundo que ha producido y registrado una vacuna contra la fiebre Q para uso humano. Se utiliza en dosis única, sin necesidad de refuerzos. A pesar de sus exitosos resultados en su país de origen74 su efectividad solo se ha demostrado en adultos jóvenes sanos, y no en personas con factores de riesgo cardiovascular o pacientes con comorbilidades más grave75. Está contraindicada en embarazadas y en alérgicos al huevo. La vacuna está recomendada para personas susceptibles que trabajan con ganado bovino, ovino o caprino, o productos de estos animales, por ejemplo, trabajadores de mataderos y visitantes, personal veterinario, trabajadores de corral, agricultores, esquiladores, transportadores de animales, trabajadores de laboratorio que manejan muestras veterinarias potencialmente infectadas o visitan mataderos. Su principal indicación está en trabajadores agropecuarios en zonas endémicas o en pacientes quienes han tenido endocarditis, usuarios de prótesis valvulares cardíacas, con importantes anomalías cardíacas congénitas, incluidas aquellas que requirieron injertos, o con defectos estructurales de la válvula aórtica o mitral, aneurisma de la aorta, injertos vasculares, y/o enfermedad vascular periférica grave76. El riesgo de infectarse con fiebre Q es mayor en los primeros años de exposición, por lo que los trabajadores deben vacunarse lo antes posible preexposición a la bacteria, idealmente con tamizaje de susceptibilidad77. Por otro lado, la vacunación de personas que ya han montado una respuesta inmune contra el patógeno puede provocar reacciones adversas graves, como abscesos estériles y síntomas sistémicos de inflamación. Actualmente existe incertidumbre respecto de la seroprevalencia de fiebre Q en nuestra población, por lo que se deben realizar más estudios previos a la toma de decisiones para optimizar las medidas que ayuden a su control78.
Fiebre amarillaEs una enfermedad viral, transmitida a través de picaduras de mosquitos Aedesaegypti infectados. Hay zonas endémicas en el mundo, 42 países en América y África y países que exigen la vacunación antes del ingreso. Los trabajadores cuya actividad signifique viajes a zonas con riesgo, deben estar inmunizados contra la fiebre amarilla. Las actividades laborales incluyen comercio exterior, agentes de turismo, militares, diplomáticos, organizaciones internacionales y otros. Se requiere 1 dosis de vacuna para tener inmunidad de por vida y debe ser administrada al menos 10 días antes del viaje79, porque la producción de anticuerpos comienza al 5° día y los niveles protectores se logran al 10° día. El objetivo de la vacunación es evitar que el trabajador haga la enfermedad grave porque tiene alta letalidad. Es una vacuna a virus vivo atenuado, que se producen en huevos embrionados de pollo. Puede tener efectos adversos serios y además no está disponible permanentemente debido a que su fabricación es compleja. En caso de disponibilidad restringida de vacuna, OMS sugiere usar 1/5 de la dosis cuya protección sería de 1 año80,81. No debe aplicarse a trabajadoras embarazadas o que estén amamantando, personas con inmunodeficiencia severa y alergia grave al huevo. También hay que evaluar si se coloca a un trabajador mayor de 60 años para mayor riesgo de efectos adversos82.
Encefalitis japonesaEs una enfermedad viral transmitida por picadura de mosquitos Culextarsalis infectados. El virus es un arbovirus del género flavivirus perteneciente a la familia flaviviridae. Está relacionado con los virus del dengue, fiebre amarilla y virus del Nilo Occidental. La tasa de letalidad de la enfermedad puede llegar al 30% y los pacientes recuperados pueden quedar con secuelas neuro-psiquiátricas como convulsiones, debilidad de la neurona motora superior e inferior, signos cerebelosos y extrapiramidales, déficits cognitivos y problemas de conducta, entre otros. Trabajadores de laboratorio expuestos a este virus y trabajadores que deban desplazarse a zonas rurales del Pacífico Occidental, sureste asiático y zona norte de Australia, tienen riesgo de infectarse, especialmente en la época de los monzones y en brotes y si permanecerán al menos por 1 mes. Es endémica en 24 países. Según el informe del Comité Asesor sobre Prácticas de Inmunización (ACIP)83, la vacuna aprobada por FDA y disponible en EE.UU. es la vacuna derivada del cultivo celular Vero inactivado derivada de la cepa atenuada del virus SA14-14-2 JE propagada en células Vero (Ixiaro [JE-VC]). Cada dosis de 0,5ml contiene 6 unidades de antígeno de virus purificado JE, inactivado y aproximadamente 250μg de hidróxido de aluminio como adyuvante. En personas entre 18 y 65 años, se administran 2 dosis vía intramuscular con lapso entre 7 y 28 días para la segunda dosis (esquema acelerado). Para el grupo de 65 años y más las dosis deben ser administradas en los días 0 y 28. La segunda dosis debe ser dada al menos 1 semana antes de la exposición84. Ningún estudio controlado ha evaluado la seguridad, inmunogenicidad o eficacia de JE-VC en mujeres embarazadas. En Australia y otros países asiáticos está aprobada una vacuna viral quimérica YF-JE atenuada viva (IMOJEV®). Se administra una dosis única de 0,5ml subcutánea desde los 12 meses de edad. Hasta los 17 años se requiere un refuerzo 1 o 2 años después. En los adultos, la dosis de refuerzo se podría colocar después de 5 años. Contraindicada en inmunocomprometidos y no se ha evaluado su seguridad en el embarazo85.
RECOMENDACIONES ESPECÍFICAS PARA EL PERSONAL DE SALUDAdvisory Committee on Immunization Practices, Centers for Disease Control and Prevention (CDC), Association for Professionals in Infection and Epidemiology, Inc (APIC), American College of Physicians (ACP) han recomendado las siguientes vacunas para el personal de salud86:
- •
Todos deben estar inmunizados contra sarampión, rubéola, parotiditis y varicela.
- •
Todos los expuestos a sangre y fluidos corporales deben estar inmunizados contra hepatitis B.
- •
Todo el personal que trabaja en un recinto de salud debe vacunarse anualmente contra la influenza.
- •
Todos deben tener una dosis de Tdap.
- •
Debe ofrecerse a todo el personal de salud, las vacunas recomendadas para los adultos en función de la edad y otros factores de riesgo individuales. Tétanos, Td (toxoide diftérico), neumococo, vacuna contra papiloma humano (VPH). En las personas de 60 y más años, ofrecer a vacuna Zoster (el mismo virus de varicela zoster atenuado vivo, pero con 14 veces más la concentración de virus) ACIP87.
- •
El personal con riesgo específico y el personal de laboratorio debe tener las vacunas polio, meningococo, BCG, rabia, tifoidea y hepatitis A.
La migración es un fenómeno global. Desde el 2011 el flujo de migrantes aumentó progresivamente en Europa. La revisión sistemática publicada por Mipatrini D. 2007, muestra que la población de migrantes y refugiados tiene menores tasas de vacunación que la población en Europa. Las causas se relacionan con las bajas coberturas de vacunación en los países de origen. Una vez en Europa, el problema es el acceso a la vacunación porque: se movilizan geográficamente y no pueden completar los esquemas que requieren dosis múltiples; no conocen su estado de inmunización previo; algunos países que los reciben, también tienen crisis económicas; las personas no quieren registrarse por miedo a problemas legales; no hay coordinación entre los sistemas de salud de países vecinos o de dónde provienen para contar con la información y ello se traduce finalmente en que no se vacunan o en duplicación de dosis88.
En EE.UU. se ha implementado una estrategia de salud pública para inmigrantes y refugiados. En el primer caso, en que la inmigración es programada se realiza un manejo fuera de EE.UU. donde se detecta TBC, parasitosis y se conoce el estado vacunal. Esos temas se resuelven antes del ingreso a EE.UU. En el caso de los refugiados, en el plazo de 1 a 3 meses, se evalúa el estado de salud, se realiza el tamizaje para distintas enfermedades y respecto de la vacunación se complete la historia de inmunizaciones según las guías del país de origen y se realiza puesta al día Esta estrategia, no es posible en todas partes porque no se logra el seguimiento para completar las series de vacunas89.
En Chile, al 31 de diciembre 2019 según el Instituto Nacional de Estadísticas (INE) había alrededor de 1,5 millones de personas extranjeras que residen en Chile90. El año 2014, eran 410.988. Venezuela y Perú son los países de origen que aportan con el mayor porcentaje de personas. Del total de extranjeros residentes, 1.256.970 personas están en edad laboral entre 19 y 69 años90. La migración es un determinante social de la salud y no es un riesgo per se. Pero los migrantes son vulnerables a la inequidad y las condiciones en que migran son las que generan el riesgo91. Respecto de la vacunación, las personas migrantes, aunque no posean cédula de identidad chilena (RUN) y no tengan recursos, pueden acceder en forma gratuita a las prestaciones de la red pública de salud, en igualdad de condiciones que los chilenos. Estas prestaciones incluyen las vacunas del PNI92. En los niños hasta 14 años, en que no se conoce el estado vacunal, MINSAL a través del Ord B27/N°4638 de la Subsecretaría de Salud Pública, emitió el documento “Calendario de Puesta al día en Inmunizaciones. Chile 2018” y con ello, es posible completar los esquemas en caso de calendarios incompletos93. En marzo 2019, MINSAL realiza la campana “Ponte al Día” para todos los niños menores de 14 años, migrantes y chilenos, tengan sus vacunas al día.
Desafíos de vacunación laboral en ChileLa vacunación en trabajadores expuestos es una herramienta preventiva eficaz y ayudaría a aumentar el efecto de protección comunitaria para algunas vacunas y patologías específicas. Para ello, es necesario desarrollar una guía de vacunación preventiva y terapéutica para las personas que trabajan expuestas a riesgos biológicos, de manera que se estandarice el uso de este EPP preventivo. Nuestro PNI ha avanzado en recomendaciones para la vacunación gratuita de pacientes con necesidades especiales por patologías o situaciones de riesgo35, aunque no estén en GES ni Ley Ricarte Soto. Sin embargo, debemos avanzar en definir los esquemas de vacunación para grupos especiales de trabajadores como los bomberos, las embarazadas, inmigrantes, trabajadores con esquemas incompletos o desconocidos, trabajadores de 60 y más años, trabajadores sexuales y de establecimientos de entretenimiento con potencial riesgo de contacto. En este proceso debiera integrarse al sistema de Registro Nacional de Inmunizaciones del MINSAL y coordinar con la SUSESO para el intercambio de información que permita medir la cobertura preventiva de la inmunización en los trabajadores. En los últimos años, varias empresas han avanzado hacia convertirse en “empresa saludable” y ofrecen programas de vacunación a sus empleados para la prevención de enfermedades más allá de los riesgos laborales. En este escenario, es un gran aporte el rol del Médico del Trabajo y el aporte de la Sociedad Chilena de Medicina del Trabajo, ya que pueden conjugar las acciones de salud común y salud laboral, con lo que se lograría aumentar las coberturas de vacuna en Chile, prevenir las enfermedades infecciosas y conseguir una organización más saludable y, en última instancia, más feliz y productiva, permitiendo concluir la etapa laboral con una mejor condición de salud global.
Declaración de conflicto de interésGabriela Moreno no refiere conflictos de interés. Rodolfo Villena ha participado en proyectos de investigación en vacunas para GSK y consultorías para Pfizer y Sanofi Pasteur.
FinanciaciónLos autores declaran que no han recibido financiación externa para redactar este artículo.