Se presenta el caso de una mujer de 51años con antecedentes de disnea progresiva, palpitaciones y dolor torácico de 4meses de evolución que fue ingresada por disnea de reposo y tos. El dímeroD se encontraba elevado y la tomografía computarizada demostró defecto de repleción del tronco pulmonar y de la rama derecha de la arteria pulmonar. El ventrículo derecho se encontraba dilatado, con función sistólica severamente deprimida y presión pulmonar sistólica estimada superior a 100mmHg. El cuadro fue interpretado como un episodio de embolismo agudo sobre una enfermedad crónica tromboembólica. A pesar del tratamiento fibrinolítico y anticoagulante, la situación clínica sufrió un rápido deterioro. El intento de trombectomía percutánea y angioplastia resultaron fallidos y la paciente presentó disociación electromecánica que precisó soporte con oxigenación extracorpórea de membrana.
Se realizó tromboendarterectomía pulmonar de urgencia bajo circulación extracorpórea. El estudio histopatológico confirmó el diagnóstico de sarcoma intimal de la arteria pulmonar. Se comentan algunos aspectos relacionados con la clínica, el diagnóstico y el tratamiento de este tumor.
The case is presented of a 51year-old female who was admitted due to a four months history of worsening dyspnoea and cough. She also reported intermittent palpitations and chest pain. Her past medical history was insignificant for any major co-morbidities. On admission, D-dimer levels were elevated and computed tomographic scan showed a filling defect in the pulmonary trunk extending into the right pulmonary artery. Cardiac ultrasound showed severely dilated right ventricle with severe diastolic dysfunction and an estimated systolic pulmonary artery pressure of more than 100mmHg. The patient was diagnosed with acute pulmonary embolism on top of chronic pulmonary thromboembolic disease. Despite adequate anticoagulation and fibrinolytic therapy, the patient continued to deteriorate clinically. Urgent percutaneous thrombectomy was attempted, but was unsuccessful. The patient later developed an episode of cardiac arrest that required veno-arterial extracorporeal membrane oxygenation support.
The patient underwent urgent surgical thromboendarterectomy under cardiopulmonary bypass, and the patency of the main pulmonary branches was re-established. The histopathological examination of surgical samples confirmed the diagnosis of pulmonary intimal sarcoma. Some aspects, including the clinical findings, diagnosis, and management of this rare tumour are discussed in this case report.
El sarcoma intimal primario de la arteria pulmonar (SIPAP) es un tumor maligno raro originado en la túnica íntima de la arteria pulmonar1,2. El cuadro clínico y los hallazgos hemodinámicos y radiológicos hacen que con frecuencia el SIPAP sea confundido con otros procesos vasculares pulmonares, como la hipertensión arterial pulmonar crónica tromboembólica, el embolismo pulmonar agudo, la mediastinitis fibrosante, las enfermedades de Takayasu y de Behçet y la hipertensión arterial pulmonar primaria1-3. Por este motivo, en numerosas ocasiones el diagnóstico final de SIPAP se lleva a cabo a partir del estudio histopatológico del material obtenido en una intervención quirúrgica o en la autopsia2,4.
Se describe el caso de una paciente con SIPAP e hipertensión pulmonar que inicialmente fue diagnosticada de embolismo pulmonar. La paciente fue sometida a tratamiento fibrinolítico y tromboextracción percutánea fallidos, precisando el implante de un oxigenador extracorpóreo de membrana (ECMO) venoarterial como puente a la realización de una tromboendarterectomía quirúrgica.
Caso clínicoSe trata de una mujer de 51años, sin antecedentes de interés y en tratamiento crónico con fluoxetina. Debutó con febrícula y síncope, siendo diagnosticada de golpe de calor. Tres meses más tarde consultó por disnea de esfuerzo, molestias retroesternales, palpitaciones y mareos. En la exploración se detectó un soplo sistólico en el mesocardio y una ligera anemia microcítica de probable origen ginecológico. Se pautó hierro por vía oral y la paciente fue remitida a cardiología. En el ecocardiograma transtorácico se observó una insuficiencia tricúspide ligera con una presión arterial pulmonar sistólica (PAPS) estimada de 60mmHg, dilatación del ventrículo derecho y excursión sistólica del plano del anillo tricuspídeo de 18mm. No se detectaron cortocircuitos ni otro tipo de anomalías.
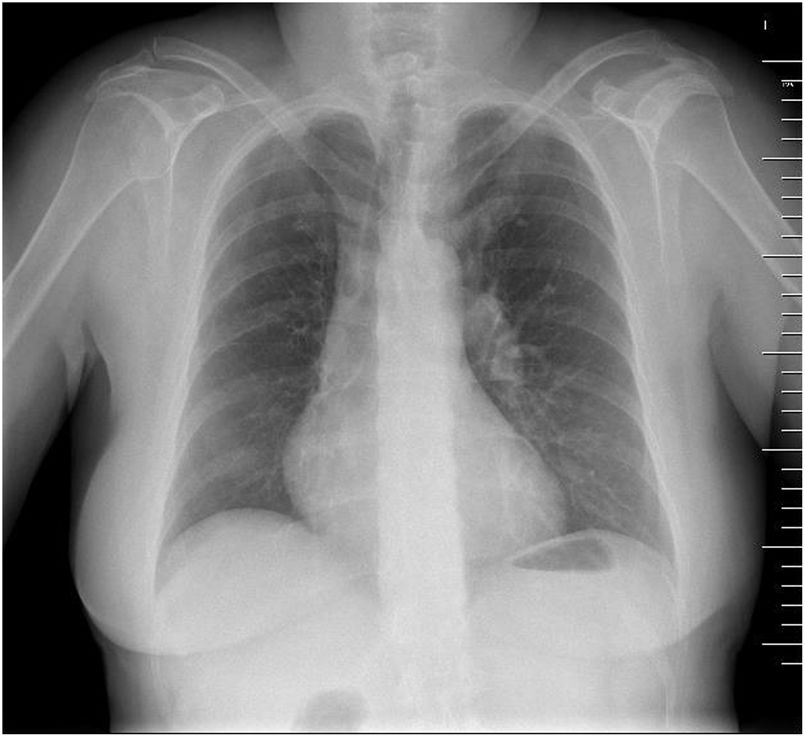
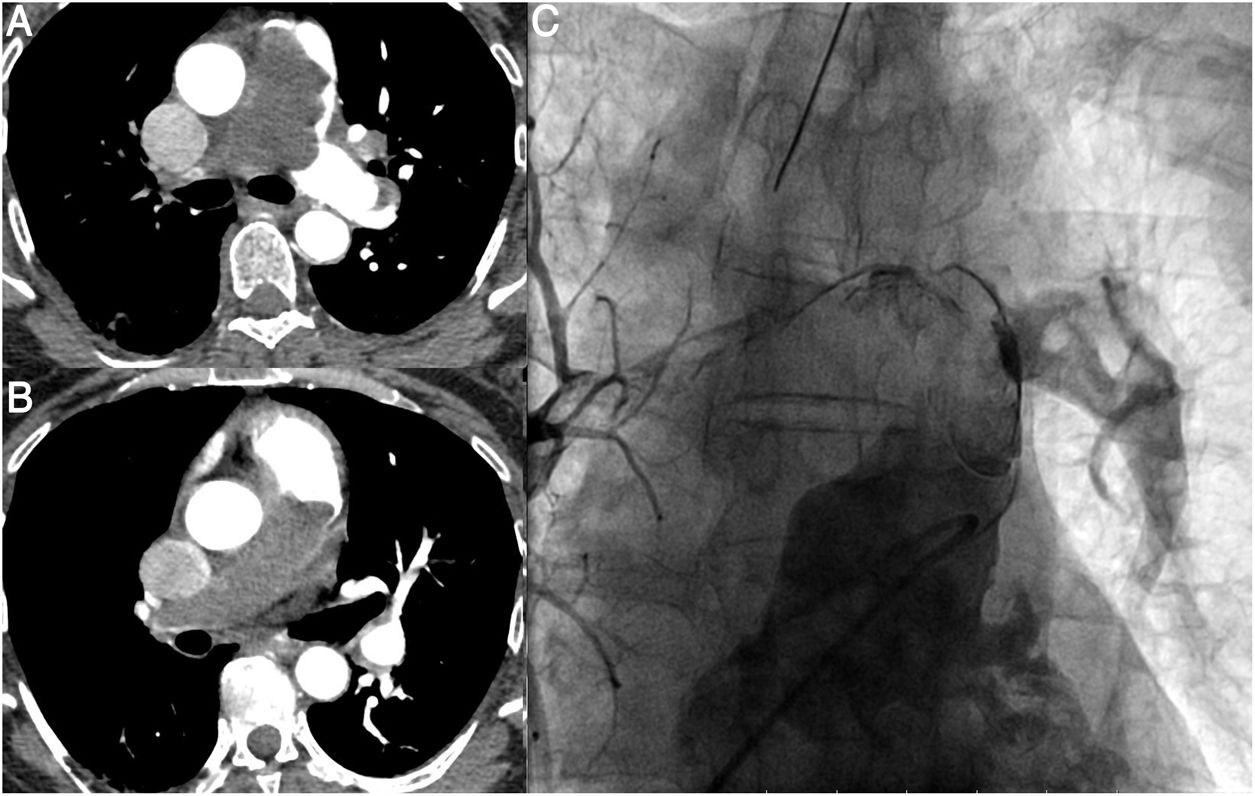
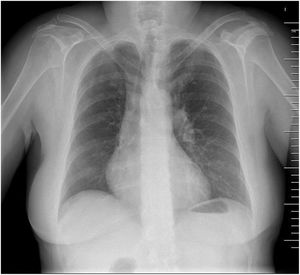
Dos meses después la paciente acudió a urgencias por empeoramiento clínico, refiriendo disnea de pequeños esfuerzos y tos seca. En la exploración se observó taquicardia sinusal a 110lpm y saturación del 92%. En la analítica se constató un dímeroD elevado (1.935ng/ml) y una PaO2 de 56mmHg. La radiografía de tórax reveló amputación del hilio derecho (fig. 1) y la tomografía computarizada, un defecto de repleción del tronco arterial pulmonar y de la rama derecha (fig. 2). El ecocardiograma demostró cavidades izquierdas normales y ventrículo derecho dilatado con función deprimida, TASE de 10mm, acinesia de la pared libre, aplanamiento del septo interventricular, dilatación del tracto de salida del ventrículo derecho y del tronco de la arteria pulmonar con insuficiencia valvular pulmonar ligera, dilatación de la cava inferior e insuficiencia tricúspide moderada con PAPS estimada de 109mmHg. La paciente fue diagnosticada de episodio de tromboembolismo pulmonar agudo superpuesto a un cuadro de tromboembolismo crónico y se administró tratamiento anticoagulante y fibrinolítico, sin que se observara mejoría. Una semana después la paciente fue remitida a nuestro centro.
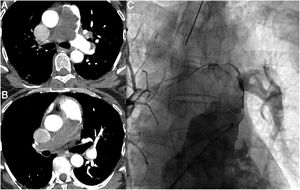
A)Tomografía computarizada. Obliteración del tronco pulmonar. La arteria pulmonar izquierda está permeable. B)Tomografía computarizada. Obliteración de la arteria pulmonar derecha. C)Ventriculografía derecha. Suboclusión del tronco pulmonar y de la rama derecha. La rama lobar inferior izquierda está preservada.
Al ingreso, la paciente presentaba disnea de reposo y taquipnea con PaO2 de 57mmHg a pesar de gafas de alto flujo. Transcurridas 24h sufrió agravamiento de la hipoxia y se indicó tratamiento percutáneo en la sala de hemodinámica. La arteriografía pulmonar demostró oclusión casi completa del tronco pulmonar, de la rama principal y de las ramas lobares derechas y de la rama lobar superior izquierda con recanalización distal (fig. 2). Durante las maniobras de tromboextracción y angioplastia de los vasos pulmonares —que resultaron fallidas— la paciente sufrió disociación electromecánica, precisando maniobras de reanimación cardiopulmonar prolongadas e implante percutáneo de una ECMO venoarterial. La paciente fue remitida a cirugía cardiaca para intervención urgente.
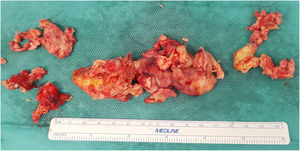
Se realizó un abordaje mediante esternotomía media. Después de la apertura de la cavidad pericárdica se observó dilatación y disfunción graves del ventrículo derecho, sin derrame pericárdico, así como dilatación del tronco de la arteria pulmonar sin signos de inflamación ni infiltración parietal. Bajo circulación extracorpórea y paro electromecánico del corazón mediante pinzamiento aórtico y administración de cardioplejía se realizó arteriotomía del tronco de la arteria pulmonar, ramas derecha e izquierda y ramas lobares. La luz de los vasos pulmonares se encontraba ocupada por un material organizado, consistente y firmemente adherido a la pared vascular. Mediante disección con espátula se realizó tromboendarterectomía del tronco pulmonar, ramas principales y lobares (fig. 3).
Finalizada la intervención, se observó mejoría del intercambio gaseoso y de la función ventricular derecha. Se avanzó un catéter de Swan-Ganz y se calculó una PAPS de 29mmHg. A pesar de la mejoría, se decidió continuar con soporte ECMO de modo preventivo hasta transcurridas 36h, y se retiró sin incidencias. La paciente no despertó después de la intervención, si bien cabe destacar que la concentración plasmática de enolasa neuronal específica en una muestra extraída antes de su traslado al quirófano fue de 96,6ng/ml. Se realizó resonancia magnética cerebral, en la que se detectaron múltiples lesiones sugestivas de encefalopatía hipóxica, por lo que se decidió limitar el esfuerzo terapéutico y la paciente falleció una semana más tarde.
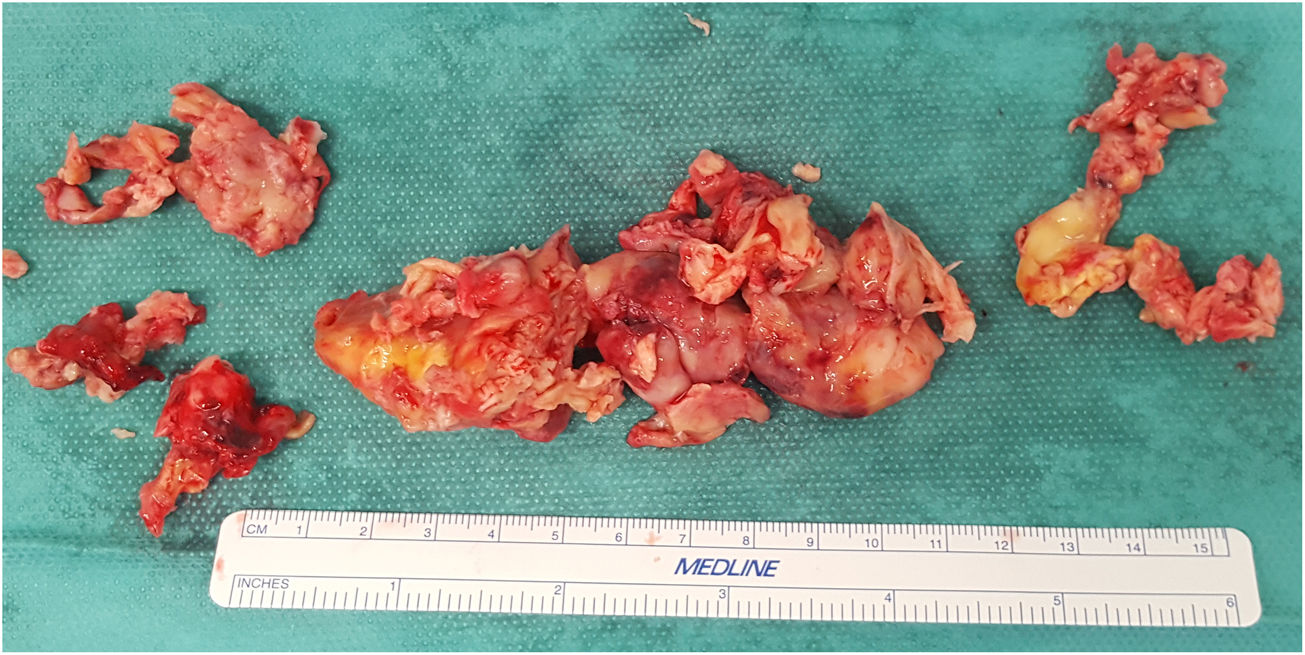
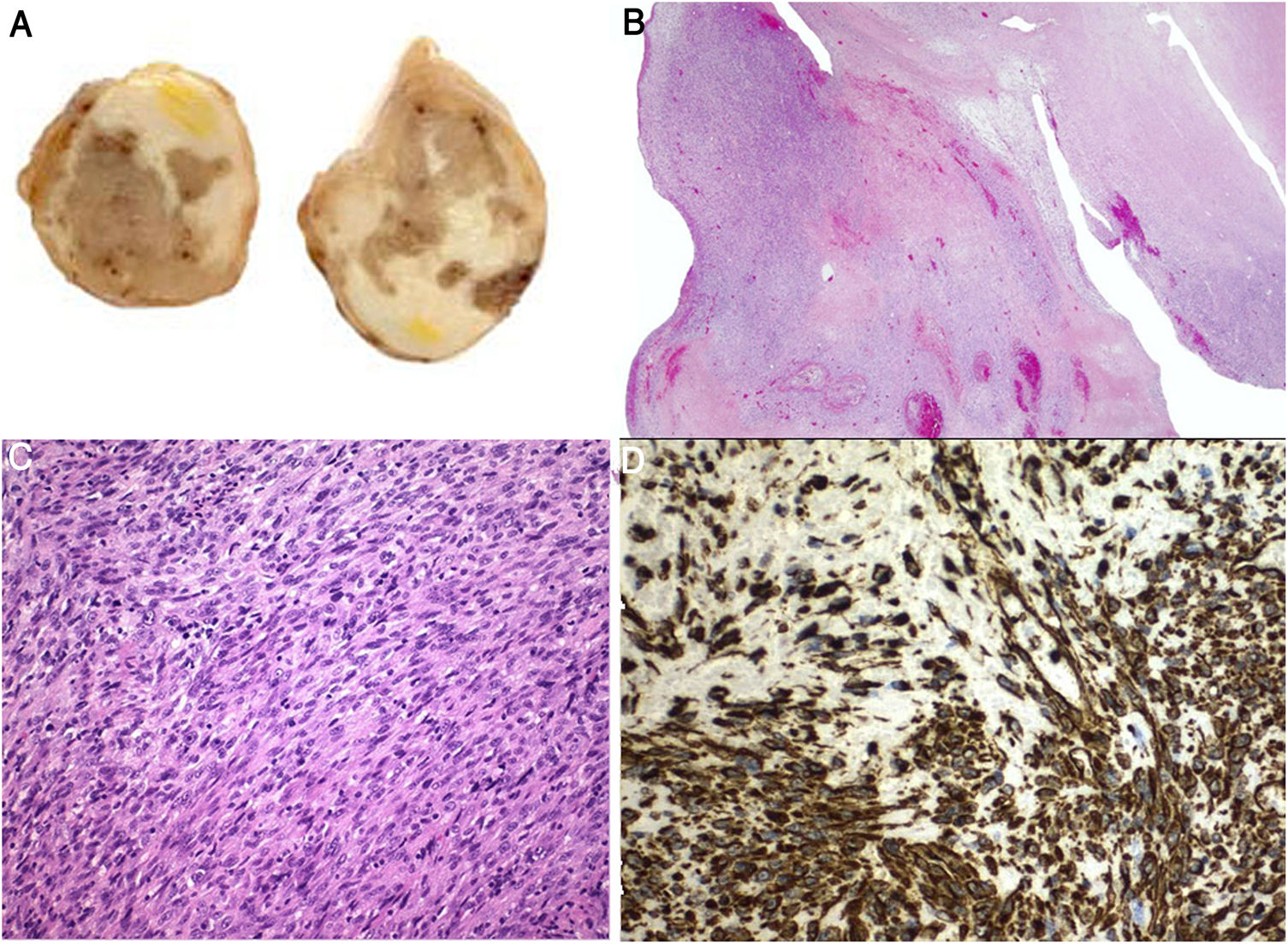
En el estudio anatomopatológico del material extraído (fig. 4) se observó material fibrinohemático entremezclado con focos de proliferación de células de características malignas con morfología predominantemente fusiforme, polimorfismo nuclear y actividad mitótica (13mitosis/10campos gran aumento), así como varios focos de necrosis. En el estudio inmunohistoquímico se apreció intensa positividad para vimentina, así como para CD34, CD10, CD99, MDM2 y CK AE1-AE3. Los marcadores de diferenciación muscular (actina de músculo liso, desmina y miogenina), neural/melanocítica (S100 y HMB45) y hematolinfoide (CD45-LCA, CD68, CD21 y CD23) resultaron negativos, así como la expresión de CD31, WT-1, HHV8, C-Kit y CDK4. Realizado estudio mediante FISH, no se observaron translocaciones en EWS y SYT ni amplificación para MDM2. El conjunto de hallazgos histopatológicos y moleculares apoyaron el diagnóstico de tumor mesenquimal maligno concordante con un SIPAP.
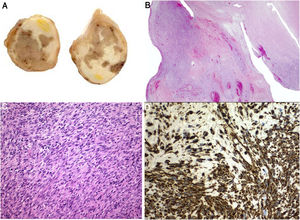
Estudio anatomopatológico. A)Aspecto macroscópico del material extraído. Sección transversal al eje del vaso. B)H-E 2,5×. Material fibrinohemático con focos de proliferación celular. C)H-E 20×. Células malignas de aspecto fusiforme y polimorfismo celular. D)Inmunohistoquímica. Se aprecia intensa positividad para vimentina.
El SIPAP se suele originar en la íntima del tronco de la arteria pulmonar o de las ramas principales1-3. Excepcionalmente puede originarse en la válvula pulmonar4. Afecta con mayor frecuencia a mujeres en la quinta y sexta décadas de la vida. Habitualmente presenta un crecimiento endoluminal anterógrado con trombosis superpuesta proximal y distal, tromboembolismo distal y embolia tumoral metastásica1-3. En ocasiones el tumor puede extenderse retrógradamente hacia la válvula pulmonar y el tracto de salida del ventrículo derecho5. La infiltración parietal es infrecuente1-3,6.
El crecimiento del tumor y la trombosis in situ sobreañadida provocan la obliteración progresiva de la luz vascular. A pesar de que el dímeroD suele encontrarse elevado7, la administración de anticoagulantes y fibrinolíticos no mejora la sintomatología o bien lo hace de un modo transitorio al actuar sobre el componente trombótico superpuesto al tumor6.
El SIPAP no suele dar síntomas hasta que el tumor se encuentra avanzado y provoca una obstrucción vascular grave1. Se calcula que en el momento del diagnóstico hasta el 50% de los pacientes puede presentar metástasis a distancia1. El pronóstico de los pacientes con SIPAP, a pesar de la resección completa del tumor, es malo, con una supervivencia media inferior a 2años2,3,6.
Clínica y radiológicamente el SIPAP suele confundirse con la hipertensión arterial pulmonar crónica tromboembólica1-3,7. Se ha observado que hasta el 4% de los pacientes intervenidos de tromboendarterectomía pulmonar por hipertensión tromboembólica padecen en realidad un SIPAP8. Por otro lado, entre el 20 y el 80% de los pacientes con SIPAP son preoperatoriamente etiquetados como hipertensión tromboembólica1-3,6.
El cuadro clínico de los pacientes con SIPAP, consistente en disnea progresiva, dolor torácico, síncope e insuficiencia cardiaca derecha, se asemeja a la hipertensión crónica tromboembólica1-3,6,7. Sin embargo, los pacientes con SIPAP presentan una evolución clínica más rápida, y además suelen carecer de antecedentes de embolismo pulmonar y de trombosis venosa profunda1,7. Es posible que la tomografía de emisión de positrones ayude a distinguir ambos procesos, ya que, a diferencia del tromboembolismo crónico, el SIPAP presenta captación activa1,7.
La caracterización anatomopatológica de los sarcomas intimales indiferenciados precisa la utilización de una amplia batería de marcadores fenotípicos y moleculares para diferenciarlos de otros tumores, como fibrosarcomas, angiosarcomas y sarcomas derivados de células musculares9.
La tromboendarterectomía proporciona mejoría clínica, hemodinámica y gasométrica en los pacientes con hipertensión pulmonar y obliteración arterial pulmonar, ya sea de causa embolica o tumoral. Sin embargo, en algunos casos al finalizar la intervención la presión arterial pulmonar se mantiene elevada, y este hecho puede ser debido a la afectación de los pequeños vasos inaccesibles a la cirugía o bien al edema secundario a la reperfusión o al trauma quirúrgico10. En estas situaciones el soporte postoperatorio con ECMO venoarterial es una técnica rutinaria que permite una retirada progresiva del apoyo cardiorrespiratorio2,9. Sin embargo, la utilización de ECMO preoperatorio como puente a la tromboendarterectomía es excepcional, reservándose para pacientes con inestabilidad hemodinámica, presión pulmonar similar a la sistémica e hipoxia grave a pesar de tratamiento máximo10.
El caso presentado puede contribuir a establecer una indicación más precoz del soporte con ECMO como puente a la cirugía en los casos de embolia pulmonar de alto riesgo que no responden a trombólisis, en los pacientes inestables con hipertensión pulmonar —ya sea de causa tumoral o tromboembólica— candidatos a tromboendarterectomía pulmonar, y en los casos de intervencionismo cardiaco que tratan embolias de pulmón agudas de alto riesgo sin respuesta a la anticoagulación y la fibrinólisis.
Responsabilidades éticasEste trabajo ha sido aprobado por el comité ético del hospital. Por tratarse de una paciente fallecida, no precisa consentimiento informado para su publicación.
FinanciaciónNinguna.
Conflicto de interesesNo se declara ninguno.