A partir del descubrimiento de las moléculas de histocompatibilidad y su papel como elementos de restricción de la respuesta inmune, los estudios de asociación de estos genes y diversas enfermedades han cobrado gran interés, en especial en aquellas patologías en las que el sistema inmune desempeña un papel preponderante en la etiología y en la evolución del cuadro clínico1.
La aterosclerosis es una enfermedad inflamatoria, porque es mucho más que la simple acumulación de lípidos en la pared arterial. Sus lesiones abarcan una serie de respuestas celulares y moleculares específicas, las cuales aparecen desde las etapas iniciales de la enfermedad2. La intensidad y persistencia de esta respuesta inflamatoria podría estar determinada genéticamente3.
Se sabe que el infarto de miocardio y en general toda la patología aterosclerótica tiene un componente hereditario importante4,5. En la última década las técnicas de biología molecular han permitido identificar numerosos genes responsables del aumento del riesgo. Estos polimorfismos genéticos están siendo considerados como los nuevos factores de riesgo para la aterosclerosis coronaria, y han hecho pensar en la hipótesis de que la suma de los que resultan desfavorables en presencia de un ambiente propicio podría facilitar la aparición de esta enfermedad típicamente poligénica y multifactorial5. Dentro de estos genes o grupos de genes podría estar implicado el complejo mayor de histocompatibilidad (MHC) o sistema HLA (acrónimo de Human Leucocyte Antigens), por ser el principal elemento en el reconocimiento antigénico y en la iniciación de la respuesta inmune, y sus antígenos podrían servir como marcadores de susceptibilidad para desarrollar enfermedad coronaria de acuerdo con el perfil genético individual.
Este estudio tiene como objetivo determinar si existe asociación entre el sistema HLA y la enfermedad coronaria en pacientes con antecedentes de infarto de miocardio y factores de riesgo tradicionales e historia familiar de cardiopatía isquémica (CI).
Material y métodos
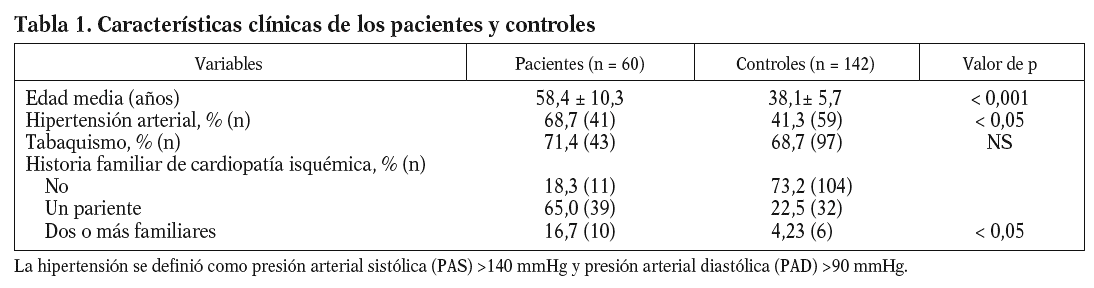
Se realizó un estudio de casos y controles con 60 pacientes varones seleccionados al azar, de entre 38 y 72 años de edad, con historia de uno o más infartos de miocardio, diagnosticados según criterios clínicos y electrocardiográficos con antecedentes de hipertensión arterial, tabaquismo y/o historia familiar de CI, procedentes de servicios de cardiología de 3 centros médicos de la ciudad de La Habana. Se excluyeron los pacientes con antecedentes de enfermedad cerebrovascular y autoinmune. Como controles se seleccionó a 142 donantes voluntarios, supuestamente sanos y no relacionó, sin evidencias clínicas de enfermedad cardíaca ni autoinmune, y que representaban los principales componentes raciales de la población cubana6 (tabla 1).
En el grupo de pacientes se estudió la relación entre los antígenos de significación encontrados y las variables: número de infartos, edad de ocurrencia del episodio, tabaquismo, hipertensión arterial e historia familiar de CI. Se establecieron 3 grupos de edad: de 38 a 49, de 50 a 64 y mayores de 65 años. Se consideró fumador al sujeto que fumaba uno o más cigarrillos al día, que lo había hecho durante un año o más y que había fumado durante el último año. Como no fumador al que nunca había fumado o que lo había hecho 2 años antes o más de iniciarse este estudio. Se consideró hipertenso al paciente que recibía tratamiento o refirió habérsele diagnosticado la enfermedad. Para el análisis de la historia familiar de CI se consideró primer grado de parentesco (padres o hermanos).
La determinación serológica de los antígenos HLA clase I y II se realizó mediante la técnica de microlinfocitotoxicidad en 2 pasos7,8 modificada para doble fluorescencia9. Las células mononucleares periféricas se obtuvieron mediante la técnica de Böyum modificada10, y la separación de los linfocitos T y B se realizó por fibra de nylon11. Los linfocitos T se ajustaron a 2 3 106 células/ml, y los B, a 2,5 3 106 células/ml, haciéndose reaccionar con sueros específicos anti-HLA clase I y II, respectivamente, en presencia de suero de conejo como fuente de complemento. La lectura de las placas se realizó en un microscopio invertido de doble fluorescencia (sistema Patimed-Leica)9.
Análisis estadístico
Se calcularon las frecuencias antigénicas (f) y haplotípicas (fh) para pacientes y controles utilizando un software de genética de poblaciones12. La significación estadística de la asociación se calculó mediante la prueba de x2 para un valor de p # 0,05. El grado de asociación se determinó a través de los odds ratio (OR) como una aproximación para estimar los riesgos relativos que confiere la presencia de la variable en relación con su ausencia, y sus correspondientes intervalos de confianza (IC) del 95%13.
Se calculó la fracción etiológica (FE) para determinar qué porcentaje del OR es atribuible al antígeno considerado, si el riesgo se debe o no al marcador estudiado, o es debido a otro en desequilibrio de ligamiento con él13. Mediante el análisis de independencia y asociaciones antigénicas (AIAA) se determinaron las asociaciones significativas, la independencia o no de un antígeno respecto a otro, y si es debido o no al fenómeno de desequilibrio de ligamiento (D)14.
La relación entre los antígenos de susceptibilidad y las variables independientes se analizó con el método de aproximación logarítmica o prueba G (Microsoft Excel 2000 y Statgra phics Plus 2.1 1996).
Resultados
Para pacientes y controles se utilizaron 117 sueros anti-HLA de clase I, mono u oligoespecíficos, y 68 de clase II, los cuales representan las especificidades HLA serológicas más frecuentes de la población cubana15.
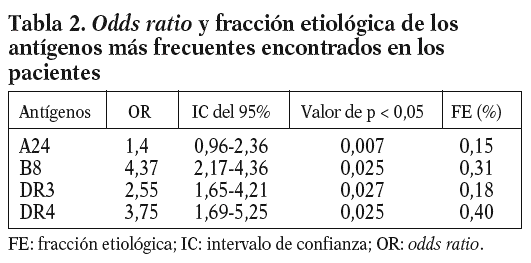
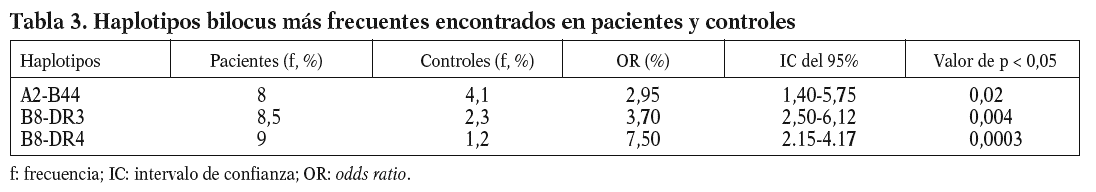
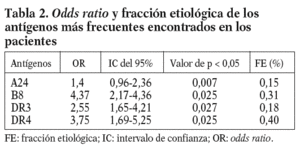
Los antígenos significativamente más frecuentes fueron: HLA-DR4, DR3, B8 y A24. Sin embargo, la FE permitió definir una verdadera asociación para el DR4 y el B8 (tabla 2). El antígeno menos frecuente con respecto al grupo control fue el B15 (1,66 frente al 16,66%; p < 0,001), cuyo OR de 0,14 (IC del 95%, 0,41-1,82; p < 0,027) y fracción preventiva de 0,12 indicaron una asociación negativa para el infarto de miocardio, pudiendo considerarse como marcador de protección. Los haplotipos bilocus más frecuentes significativamente fueron: B8-DR4, B8-DR3 y A2-B44 (tabla 3).
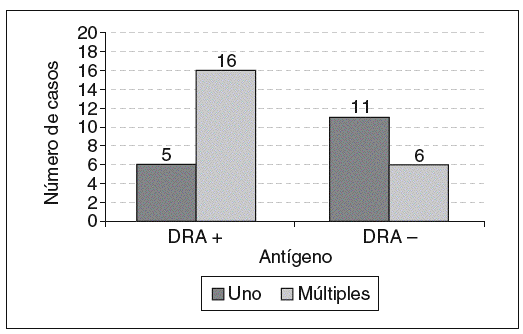
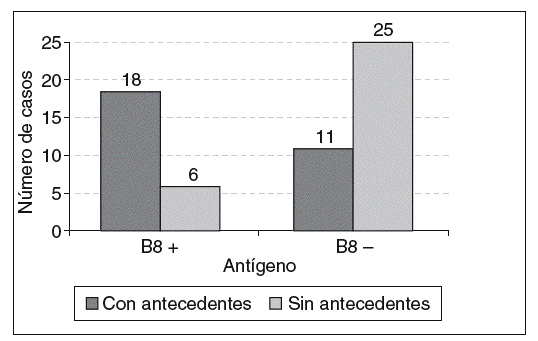
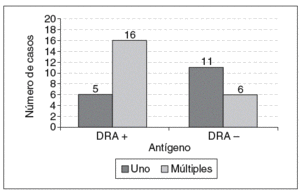
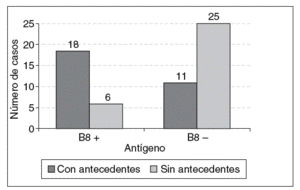
No se encontraron diferencias significativas entre pacientes positivos y negativos para ninguno de los 2 antígenos de susceptibilidad para las variables edad de ocurrencia del infarto, hipertensión arterial y tabaquismo. Para el número de infartos hubo significación para el antígeno DR4 (p = 0,0025), con una prevalencia de 2 episodios en los pacientes con este marcador (61%) (fig. 1). El fenotipo B8 resultó significativo para la historia familiar de CI (p = 0,004) (fig. 2).
Figura 1. Relación del antígeno HLA-DR4 con el número de infartos de miocardio (p = 0,0025).
Figura 2. Relación del antígeno HLA-B8 con los antecedentes familiares de cardiopatía isquémica (p = 0,004).
Discusión
No existe un criterio definitivo sobre la asociación del sistema HLA con las cardiopatías, pues los antígenos de susceptibilidad comunicados son diversos (A3, A24, B8, B51, B52, DR1, DR4, DR7)16-20. Las discrepancias encontradas se deben fundamentalmente a diferencias raciales.
En este estudio se encontró asociación entre el sistema HLA y el infarto de miocardio para los antígenos HLA-DR4 y B8. La FE para el A24 indica que por sí solo no constituye un antígeno de susceptibilidad. Su elevada frecuencia en los pacientes se debe a un sesgo racial por la alta presencia de individuos caucásicos. Este antígeno es característico de este grupo étnico y frecuente en la población cubana (28,18%; p = 0,017). En el caso del DR3, la FE indica la posibilidad de desequilibrio de ligamiento con otro alelo, por lo que también fue descartado.
No se consideró de susceptibilidad el haplotipo A2-B44, porque la significación se debe a su alta frecuencia en la población cubana15. El AIAA indicó la presencia de desequilibrio de ligamiento (D = 2,8%; p = 0,0003), lo cual afianzó nuestro criterio de exclusión y confirmó el de susceptibilidad para los haplotipos B8-DR4 (D = 1,0%; p = 0,014) y B8-DR3 (D = 1,9%; p = 0,0007).
Relación de los antígenos HLA-DR4 y B8 con la edad de ocurrencia del episodio, la hipertensión arterial y el tabaquismo
El fenotipo HLA no parece aportar predisposición para el desarrollo temprano de infarto de miocardio, y el aumento de la mortalidad por esta causa con la edad depende de otros factores de riesgo, como por ejemplo la historia materna y paterna de enfermedad cardiovascular21.
Para la hipertensión arterial se han identificado varios genes candidatos en los cromosomas 2q, 6q, 5q y 9q22. Otros autores han encontrado altas frecuencias para los antígenos B35, DR4 y DR7 en hipertensos caucásicos23-26, y para el DRB1*03 en afroamericanos, así como de genes MHC clase III26. Este estudio no encontró asociación con ningún antígeno de susceptibilidad, aunque sería útil incorporar un mayor número de pacientes hipertensos para llegar a un criterio definitivo, considerando la cantidad de antígenos HLA presentes en nuestra población15.
Un estudio molecular detectó en caucásicos el primer polimorfismo MHC asociado con el tabaquismo, que incluye a 2 genes del sistema de complemento y al gen del factor de necrosis tumoral alfa (TNF-a). Éstos aparecen ligados al haplotipo HLA A1-B8-DR3, el cual posee una baja frecuencia en la población sana y un incremento en las enfermedades autoinmunes asociadas al HLA27,28. En este estudio, a pesar de encontrar OR significativamente elevados para el B8 y para el haplotipo B8-DR3, no puede afirmarse o negarse una asociación HLA debido al reducido número de pacientes fumadores que encontramos con este fenotipo (12%).
Relación de los antígenos HLA-DR4 y B8 con el número de infartos y la historia familiar de cardiopatía isquémica
Hasta donde sabemos, no existen comunicados previos que relacionen el número de infartos con el sistema HLA. Nosotros encontramos que el 76,1% de los pacientes con fenotipo DR4 experimentaron múltiples infartos, y es posible que esta molécula posea una mayor restricción para péptidos "aterogénicos" de gran afinidad capaces de inducir una respuesta inflamatoria.
Está demostrado que la historia familiar de CI tiene una prevalencia de 2 a 5 veces mayor entre los individuos con cardiopatías que entre los sujetos normales29, y que el riesgo aumenta cuando el accidente ha ocurrido en un familiar de primer grado21. En este estudio, cerca del 50% de los pacientes B8 positivos refirieron este antecedente, lo cual apoya la hipótesis acerca del efecto de determinados genes individuales como portadores de predisposición para el desarrollo de la enfermedad coronaria. Entre ellos pudiera incluirse el antígeno B8, si se considera su baja frecuencia en la población normal y su relación con los procesos inflamatorios de carácter autoinmune.
Relación de la enfermedad coronaria con la autoinmunidad
Las observaciones que apoyan el vínculo entre inmunidad y aterosclerosis provienen de estudios epidemiológicos en pacientes con trastornos autoinmunes. Se ha encontrado la ocurrencia de mutaciones en genes no propios de la respuesta inmune pero que están en desequilibrio de ligamiento con alelos MHC-II (DR y DP), así como la presencia de autoanticuerpos anticardíacos asociados al antígeno DR430-33.
Se conoce que el TNF-a, cuyo gen está ubicado en la región MHC clase III, puede ser sintetizado por los cardiomiocitos y macrófagos del miocardio en respuesta a una lesión, y se demuestra su presencia en el 88% de las lesiones ateroscleróticas y su ausencia en el miocardio normal34. El alelo TNF-A1 se ha asociado con el haplotipo A1-B8-DR3, para una elevada producción de TNF-a35,36.
En este estudio, la presencia de los antígenos DR4 y B8 y de los haplotipos B8-DR3 y B8-DR4 nos hace sugerir que el fenómeno autoinmune pudiera estar presente en la enfermedad coronaria como un proceso subyacente. Es posible que la susceptibilidad aportada por moléculas HLA particulares esté dada por la conformación de sus epítopos y el grado de afinidad para la unión con la célula T, durante la presentación de péptidos antigénicos, que provoquen estados de autoinmunidad. El TNF-a, al favorecer la expresión exagerada de moléculas MHC-II incrementaría esta respuesta, que ya ha sido observada en enfermedades crónicas, y es posible que en estas patologías los procesos autoinmunes se desarrollen paulatinamente y a largo plazo.
Para llegar a resultados concluyentes sobre la posible susceptibilidad de los genes MHC para la enfermedad coronaria, sería útil realizar estudios genéticos moleculares que permitan reforzar o anular este criterio.