La cirugía valvular aórtica aislada mínimamente invasiva mediante miniesternotomía superior se está generalizando debido a ventajas respecto a la cirugía convencional. Analizamos los resultados a 2 años en nuestro centro tras la implementación de la técnica en noviembre del 2013.
MétodosEstudio observacional analítico retrospectivo de 92 pacientes consecutivos intervenidos de sustitución valvular aórtica aislada por estenosis aórtica severa, desde noviembre del 2013. Se obtuvieron 2 grupos (grupo miniesternotomía y grupo convencional) de 40 pacientes mediante puntuación de propensión para su comparación (objetivo primario compuesto de 6 complicaciones cardíacas y cerebrovasculares mayores, y secundarios como tiempos de circulación extracorpórea e isquemia, tiempo intubación, sangrado en 24h, transfusiones y supervivencia).
ResultadosLa mediana de los tiempos de circulación extracorpórea e isquemia fueron 15 y 10 min más largos en el grupo miniesternotomía (89 [75-110] y 74 [64-90] vs. convencional 65 [55-73] y 55 [47-63] min, respectivamente, p<0,001). El grupo miniesternotomía presentó menores complicaciones mayores (12,5% vs. 30% convencional, p=0,05, odds ratio 0,32; intervalo de confianza del 95% 0,09-0,93), menor sangrado en las primeras 24 h (304±150 vs. 506±300ml, p<0,001) y menores necesidades transfusionales (0,8±0,2 vs. 1,6±0,3 concentrados de hematíes/paciente, p=0,04). No existieron diferencias en tiempo de intubación, estancia hospitalaria, mortalidad ni supervivencia.
ConclusionesLa sustitución valvular aórtica aislada por miniesternotomía presenta una reducción de la morbimortalidad, lo que recomendaría su utilización frente a la cirugía convencional siempre que sea factible. Son precisos nuevos ensayos clínicos para confirmar estos datos.
Minimally invasive aortic valve surgery using the upper mini-sternotomy is becoming more popular in our ¿country?, due to its advantages over conventional median sternotomy. An analysis is presented on the outcomes in our centre for the two years after the implementation of the technique in November 2013.
MethodsAn observational analytical retrospective study was conducted on 92 consecutive patients who underwent isolated aortic valve replacement due to severe aortic stenosis after November 2013. Propensity score matching with “nearest neighbour matching” protocol was performed to obtain two groups of 40 patients (mini-sternotomy group and conventional group) for comparison (Primary combined end-point of 6 major adverse cardiac and cerebrovascular events, and secondary end-points such as cardiopulmonary bypass and cross-clamp times, intubation time, bleeding in first 24hours, transfusions, and survival).
ResultsMedian cardiopulmonary bypass and cross-clamp times were 15 and 10minutes longer in the mini-sternotomy group (89 [75–110] and 74 [64–90] versus conventional group 65 [55–73] and 55 [47–63] minutes, respectively, P<.001). The mini-sternotomy group had less major complications events (12.5% versus 30% conventional group, p=.05, Odds Ratio 0.32; 95% Confidence Interval; 0.09 -0.93), bleeding in 24hours (304±150ml vs. 506±300ml conventional, p<.001) and transfusion requirements (0.8±0.2 vs. 1.6±0.3 packed red blood cells per patient p=.04). No differences were found in intubation time, hospital stay, mortality, or survival.
ConclusionsIsolated aortic valve replacement using mini-sternotomy shows a reduction in morbidity and mortality, so we recommend its use instead of conventional surgery, whenever possible. Further clinical trials are needed to confirm these data.
Como consecuencia del envejecimiento progresivo de la población, el número de cirugías sobre la válvula aórtica debido a enfermedad degenerativa se ha multiplicado1, a la vez que ha disminuido la mortalidad2. La cirugía convencional (CC) a través de esternotomía media completa representa todavía hoy en día el «patrón oro».
La cirugía mínimamente invasiva (CMI) es, según la American Heart Association, aquella que se realiza por una pequeña incisión en el tórax que no sea una esternotomía media convencional3. Su aplicación para la sustitución valvular aórtica (SVA) fue descrita inicialmente en 19934 y popularizada a partir de 19965-8. Existe múltiple variedad de técnicas, incluyendo accesos paraesternal derecho6, esternotomías transversas7, hemiesternotomías en «T» invertida o en «J»8, minitoracotomías anteriores derechas9 e infraaxilares derechas10. La hemiesternotomía superior en J (miniesternotomía o MINI) y la minitoracotomía anterior derecha son las más utilizadas. Hoy en día, numerosos estudios retrospectivos11-16 y metanálisis15-16 han comunicado una reducción en el sangrado postoperatorio, transfusiones, fibrilación auricular (FA) postoperatoria, tiempo de intubación, estancia en unidades de cuidados intensivos, estancia hospitalaria, disminución del dolor e incluso disminución en la mortalidad precoz11-16 y tardía14. En este artículo, comparamos los resultados obtenidos con CMI aórtica a través de MINI (grupo MINI) frente a CC con esternotomía media completa (grupo CC) tras la implantación de la CMI en nuestro centro desde noviembre del 2013, mediante un estudio pareado por puntuación de propensión que incluye el período de curva de aprendizaje de todo un servicio.
MétodosDesde noviembre del 2013 hasta agosto del 2015, 92 pacientes fueron intervenidos de SVA aislada programada por estenosis aórtica severa aislada, o doble lesión aórtica con predominio de estenosis severa, de manera consecutiva. Los datos fueron obtenidos de manera prospectiva de las historias digitales de salud de los pacientes, previo consentimiento informado.
Debido a la presencia de diferencias significativas entre grupos (tabla 1, características preoperatorias de datos no pareados), se diseñó un «propensity score» (puntuación de propensión) mediante el protocolo «nearest neighbour matching» para identificar y emparejar casos y controles apropiados mediante un modelo de regresión logística binaria basada en 15 variables preoperatorias (edad, sexo, índice de masa corporal, hipertensión arterial, diabetes mellitus, dislipidemia, enfermedad pulmonar obstructiva crónica, arteriopatía periférica, accidente vascular cerebral preoperatorio, insuficiencia renal crónica, valor de creatinina preoperatoria, cardiopatía isquémica, fracción de eyección del ventrículo izquierdo preoperatoria, gradiente medio preoperatorio y EuroScore logístico), obteniéndose 2 grupos similares y comparables de 40 pacientes en cada grupo, grupo MINI y grupo CC.
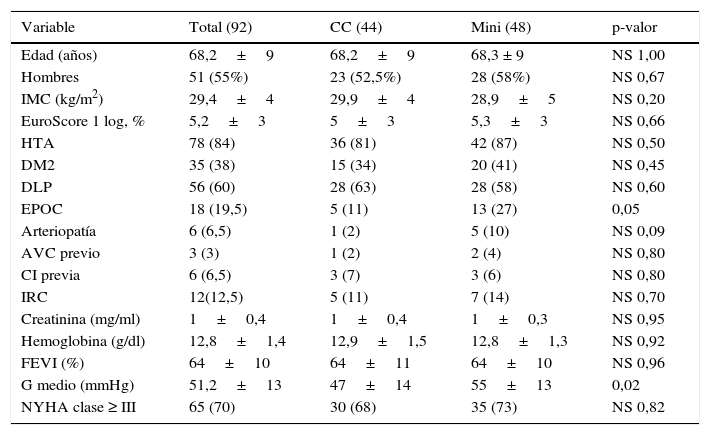
Características preoperatorias, muestra total
| Variable | Total (92) | CC (44) | Mini (48) | p-valor |
|---|---|---|---|---|
| Edad (años) | 68,2±9 | 68,2±9 | 68,3 ± 9 | NS 1,00 |
| Hombres | 51 (55%) | 23 (52,5%) | 28 (58%) | NS 0,67 |
| IMC (kg/m2) | 29,4±4 | 29,9±4 | 28,9±5 | NS 0,20 |
| EuroScore 1 log, % | 5,2±3 | 5±3 | 5,3±3 | NS 0,66 |
| HTA | 78 (84) | 36 (81) | 42 (87) | NS 0,50 |
| DM2 | 35 (38) | 15 (34) | 20 (41) | NS 0,45 |
| DLP | 56 (60) | 28 (63) | 28 (58) | NS 0,60 |
| EPOC | 18 (19,5) | 5 (11) | 13 (27) | 0,05 |
| Arteriopatía | 6 (6,5) | 1 (2) | 5 (10) | NS 0,09 |
| AVC previo | 3 (3) | 1 (2) | 2 (4) | NS 0,80 |
| CI previa | 6 (6,5) | 3 (7) | 3 (6) | NS 0,80 |
| IRC | 12(12,5) | 5 (11) | 7 (14) | NS 0,70 |
| Creatinina (mg/ml) | 1±0,4 | 1±0,4 | 1±0,3 | NS 0,95 |
| Hemoglobina (g/dl) | 12,8±1,4 | 12,9±1,5 | 12,8±1,3 | NS 0,92 |
| FEVI (%) | 64±10 | 64±11 | 64±10 | NS 0,96 |
| G medio (mmHg) | 51,2±13 | 47±14 | 55±13 | 0,02 |
| NYHA clase ≥ III | 65 (70) | 30 (68) | 35 (73) | NS 0,82 |
AVC: accidente vascular cerebral; CI: cardiopatía isquémica; DLP: dislipidemia; DM2: diabetes mellitus tipo 2; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; G medio: gradiente medio transaórtico; HTA: hipertensión arterial; IMC: índice de masa corporal; IRC: insuficiencia renal crónica; NS=no significativo; NYHA: New York Heart Association.
Media±DE, frecuencia absoluta (frecuencia relativa, %).
Estadísticamente significativo si p ≤ 0,05.
Los análisis estadísticos de puntuación de propensión fueron realizados con R software versión 3.0.1 (R Foundation for Statistical Computing, Vienna, Austria). La eficiencia del pareado fue del 86,9% (80/92). Se realizó un análisis de sensibilidad utilizando el método Rosenbaum, que fue satisfactorio.
El resto de los datos fueron analizados con el paquete estadístico SPSS® (versión 15.0). Se realizó un test de Kolmogorov-Smirnov para comprobar la normalidad de las variables. Los valores de las variables cuantitativas se expresan mediante medias±desviación estándar (SD) o medianas (rango intercuartílico), según la distribución de la variable sea o no simétrica y normal. Las variables cualitativas se presentan como frecuencias absolutas (número) y frecuencias relativas (porcentaje).
El test «t» de Student fue utilizado para los análisis estadísticos cuantitativos para muestras independientes. En caso de ausencia de normalidad, se aplicó la correspondiente prueba no paramétrica U de Mann-Whitney. Se utilizó la prueba de la chi al cuadrado para comparación de los datos cualitativos, con corrección de Fisher cuando fue necesario. Se consideraron significativas las diferencias con una p ≤ 0,05.
El objetivo primario del estudio fue diseñado en función del tamaño de la muestra disponible para aumentar las probabilidades de encontrar diferencias entre grupos, debido a la escasa frecuencia de cada complicación aislada, siendo por tanto un objetivo compuesto. Consiste en la comparación de la incidencia en ambos grupos de 6 complicaciones cardiovasculares, cerebrovasculares e infecciosas mayores (complicaciones MACCE). Este objetivo primario consta de mortalidad de cualquier causa, accidente vascular cerebral, infarto agudo de miocardio, hemorragia o taponamiento cardíaco posquirúrgico, insuficiencia renal aguda clasificación Acute Kidney Injury Network (AKIN) ≥ 2 (incremento de creatinina mayor del 100% [el doble] respecto al basal y/o diuresis< 0,5ml/kg/h durante más de 12 h) e infecciones graves, como endocarditis infecciosa, sepsis, neumonía nosocomial o mediastinitis, de acuerdo con los criterios y definiciones del Valve Academic Research Consortium 217.
Los objetivos secundarios del estudio fueron la comparación de los tiempos operatorios de circulación extracorpórea (CEC) e isquemia, tiempo de intubación y cantidad de sangrado en ml/24h, necesidad de transfusión durante las primeras 72h, número de bolsas de concentrados de hematíes/paciente transfundidos y supervivencia (log Rank de Mantel-Cox).
Técnica quirúrgicaTodos los pacientes recibieron el mismo tipo de anestesia y monitorización. Las intervenciones se realizaron con CEC en hipotermia leve a 34°C, con canulación central arteriovenosa y pinzamiento aórtico estándar, utilizando cardioplejía hemática fría (4°C) intermitente cada 20 min de manera anterógrada y/o retrógrada.
En el grupo CC se realizó una herida en piel de unos 20cm, seguida de esternotomía media completa de manubrio a xifoides, con canulación venosa en la aurícula derecha (AD, cánula estándar de 32 French) y arterial en aorta. Cardioplejía anterógrada y/o retrógrada, según criterio del cirujano.
En el grupo MINI, la herida en piel de unos 8-10cm se realizó desde el ángulo de Louis esternal en sentido caudal, seguida de una hemiesternotomía ampliada en «J» desde la escotadura supraesternal hasta el cuarto espacio intercostal derecho, con cuidado de no lesionar el paquete mamario del mismo lado. La cardioplejía fue siempre anterógrada y la canulación venosa en AD (cánula estándar) o cava superior (cánula triple puerto de 29 French), si la visibilidad era subóptima. Se utilizó infusión de CO2 en el campo operatorio durante la CEC para facilitar el purgado de aire de las cavidades cardíacas al no tener acceso directo a los ventrículos. En todos los casos MINI se colocaron palas externas de desfibrilador. Colocación de aspirador de izquierdas en vena pulmonar superior derecha en todos los casos.
La elección del abordaje fue criterio exclusivo de cada cirujano, si bien al final del primer año todos los integrantes del servicio habían superado la curva de aprendizaje. La técnica de implante y el tipo valvular no variaron entre grupos. Los criterios de extubación, transfusión y tiempo de ingreso en cuidados intensivos fueron los mismos, según el criterio de los anestesistas encargados de los cuidados críticos postoperatorios en función de los protocolos hospitalarios.
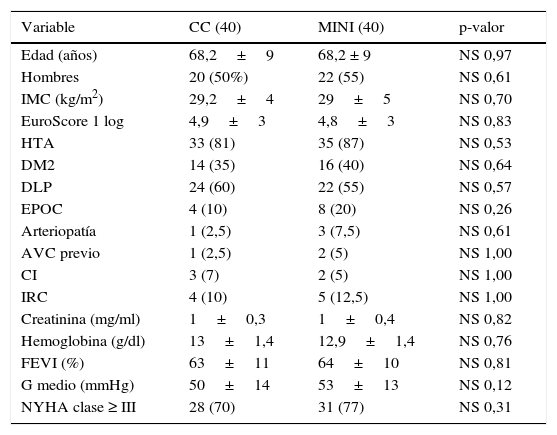
ResultadosEn la tabla 1 se reflejan las características preoperatorias de la totalidad de la muestra. El paciente tipo fue varón en un 55%, con sobrepeso, un EuroScore medio de 5, hipertenso y dislipidémico, con estenosis aórtica severa, gradiente medio de 50mmHg y grado funcional New York Heart Association III. Existieron diferencias preoperatorias en la presencia de enfermedad pulmonar obstructiva crónica (27% vs. 11%, p=0,05) y en el valor del gradiente medio (55±13 vs. 47±14, p=0,02), mayores en el grupo MINI. La distribución por sexo, la distribución de factores de riesgo cardiovascular, así como la situación clínica preoperatoria de los pacientes, fueron similares. Tras el emparejamiento por puntuación de propensión, no existieron diferencias preoperatorias entre grupos, como puede apreciarse en la tabla 2.
Características preoperatorias tras emparejamiento
| Variable | CC (40) | MINI (40) | p-valor |
|---|---|---|---|
| Edad (años) | 68,2±9 | 68,2 ± 9 | NS 0,97 |
| Hombres | 20 (50%) | 22 (55) | NS 0,61 |
| IMC (kg/m2) | 29,2±4 | 29±5 | NS 0,70 |
| EuroScore 1 log | 4,9±3 | 4,8±3 | NS 0,83 |
| HTA | 33 (81) | 35 (87) | NS 0,53 |
| DM2 | 14 (35) | 16 (40) | NS 0,64 |
| DLP | 24 (60) | 22 (55) | NS 0,57 |
| EPOC | 4 (10) | 8 (20) | NS 0,26 |
| Arteriopatía | 1 (2,5) | 3 (7,5) | NS 0,61 |
| AVC previo | 1 (2,5) | 2 (5) | NS 1,00 |
| CI | 3 (7) | 2 (5) | NS 1,00 |
| IRC | 4 (10) | 5 (12,5) | NS 1,00 |
| Creatinina (mg/ml) | 1±0,3 | 1±0,4 | NS 0,82 |
| Hemoglobina (g/dl) | 13±1,4 | 12,9±1,4 | NS 0,76 |
| FEVI (%) | 63±11 | 64±10 | NS 0,81 |
| G medio (mmHg) | 50±14 | 53±13 | NS 0,12 |
| NYHA clase ≥ III | 28 (70) | 31 (77) | NS 0,31 |
AVC: accidente vascular cerebral; CI: cardiopatía isquémica; DLP: dislipidemia; DM2: diabetes mellitus tipo 2; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; G medio: gradiente medio transaórtico; HTA: hipertensión arterial; IMC: índice de masa corporal; IRC: insuficiencia renal crónica; NS=no significativo; NYHA: New York Heart Association.
Media±DE, frecuencia absoluta (frecuencia relativa, %).
Estadísticamente significativo si p ≤ 0,05.
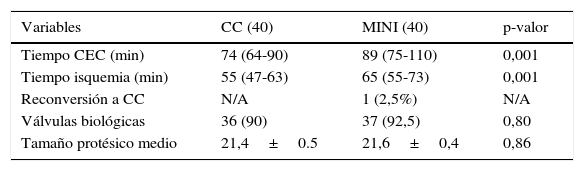
En la tabla 3 se exponen los resultados operatorios de la muestra emparejada. Destacamos la presencia de diferencias estadísticamente significativas en la mediana de los tiempos de CEC e isquemia. Estos fueron 15 y 10 min más largos en el grupo MINI (89 [75-110] y 74 [64-90] vs. CC 65 [55-73] y 55 [47-63] min, respectivamente, p<0.001). Solo hubo una reconversión por visualización subóptima al inicio de la cirugía y se utilizaron en más del 90% de los casos bioprótesis, sin existir diferencias en cuanto a tamaños protésicos implantados (21,4±0,5mm CC vs. 21,6±0,4mm, p=0,86).
Resultados operatorios: grupos pareados
| Variables | CC (40) | MINI (40) | p-valor |
|---|---|---|---|
| Tiempo CEC (min) | 74 (64-90) | 89 (75-110) | 0,001 |
| Tiempo isquemia (min) | 55 (47-63) | 65 (55-73) | 0,001 |
| Reconversión a CC | N/A | 1 (2,5%) | N/A |
| Válvulas biológicas | 36 (90) | 37 (92,5) | 0,80 |
| Tamaño protésico medio | 21,4±0.5 | 21,6±0,4 | 0,86 |
CC: cirugía convencional; CEC: circulación extracorpórea; N/A: no aplicable; NS=no significativo.
Frecuencia absoluta (%), mediana (rango intercuartílico).
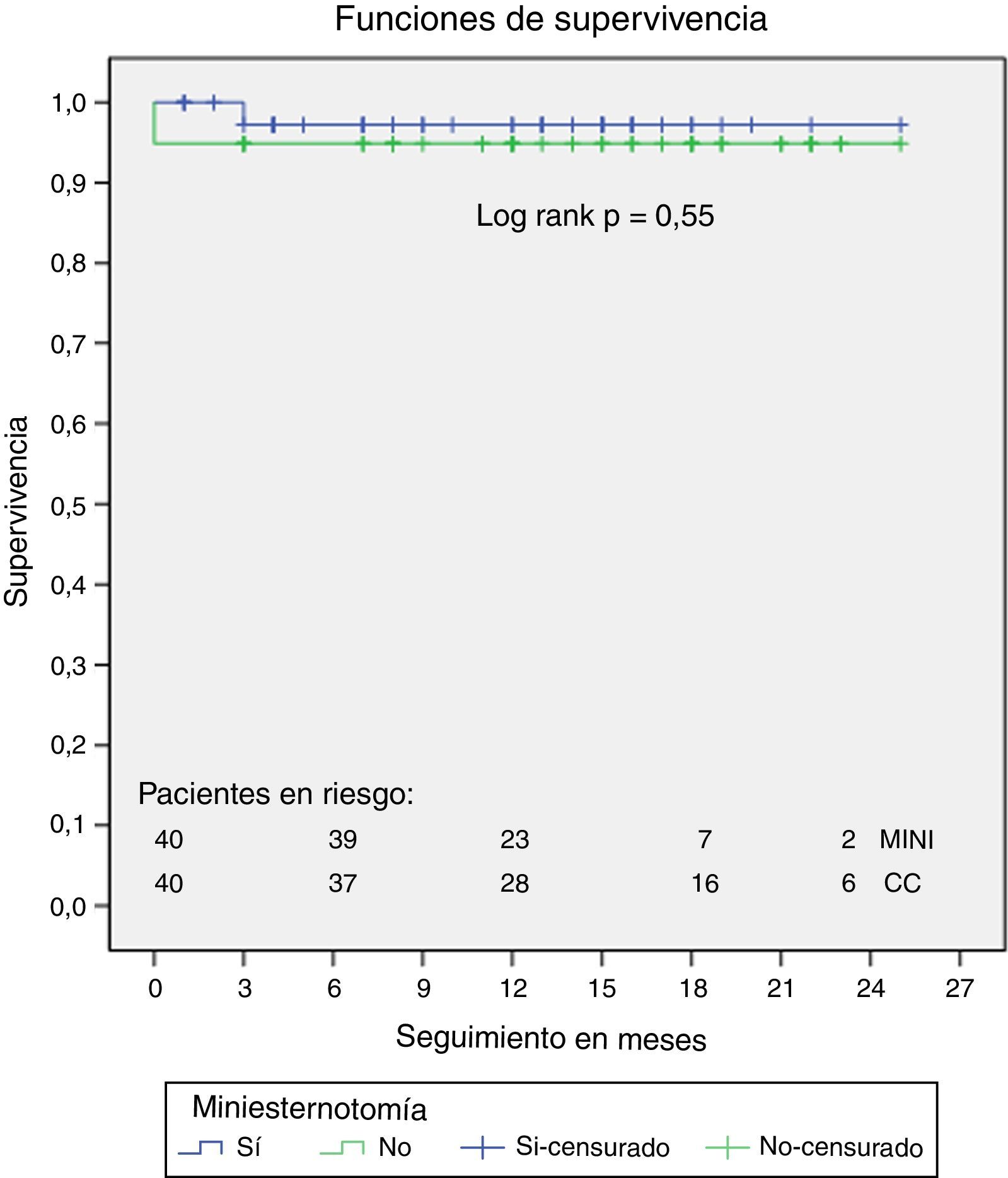
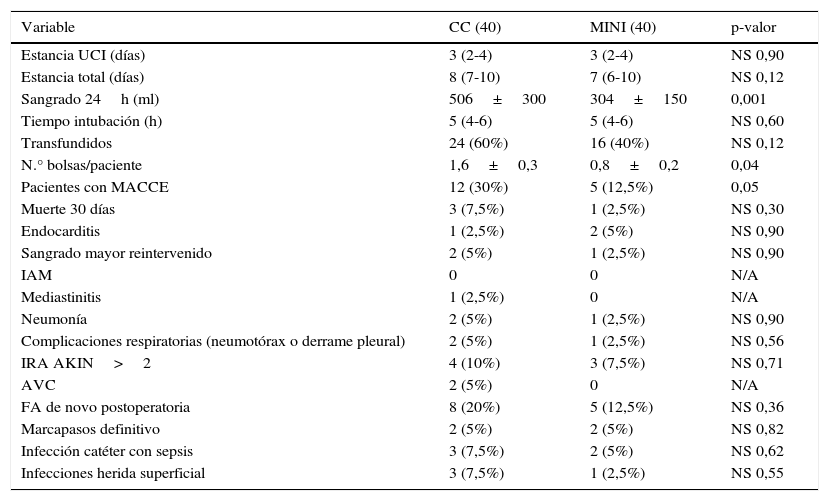
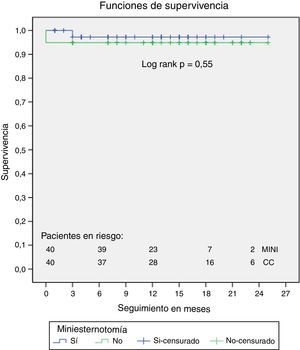
Los resultados postoperatorios se recogen en la tabla 4. El grupo MINI presentó menor mortalidad precoz, pero sin alcanzar la significación estadística (1 vs. 3 casos, p=0,30). El análisis de la incidencia de complicaciones no demostró diferencias significativas a pesar existir una tendencia a presentar menos complicaciones el grupo MINI. Sin embargo, sí se encontraron diferencias significativas en el objetivo primario de incidencia de complicaciones MACCE más infecciones graves, a favor del grupo MINI (12,5% vs. 30% CC, p=0,05), siendo la utilización de esta técnica factor protector para complicaciones MACCE (OR 0,32; IC del 95%, 0,09-0,93, p=0,05). También existieron diferencias significativas en cuanto a una menor cantidad de sangrado en las primeras 24 h (304±150ml grupo MINI vs. 506±300ml grupo CC, p<0,001) y menores necesidades transfusionales (0,8±0,2 vs. 1,6±0,3 concentrados de hematíes/paciente, p=0,04) en aquellos pacientes que precisaron de una transfusión (60% CC vs. 40% MINI, p=0,12 NS). No existieron diferencias en tiempo de intubación (mediana de 5 h por grupo), estancia en recuperación posquirúrgica (mediana 3 días por grupo), estancia hospitalaria (tendencia a un día menos de ingreso el grupo MINI, mediana 7 [6-10] MINI vs. 8 [7-10] CC, p=0,12 NS) ni supervivencia a 24 meses (log Rank p=0,55 NS, fig. 1).
Resultados postoperatorios: grupos pareados
| Variable | CC (40) | MINI (40) | p-valor |
|---|---|---|---|
| Estancia UCI (días) | 3 (2-4) | 3 (2-4) | NS 0,90 |
| Estancia total (días) | 8 (7-10) | 7 (6-10) | NS 0,12 |
| Sangrado 24h (ml) | 506±300 | 304±150 | 0,001 |
| Tiempo intubación (h) | 5 (4-6) | 5 (4-6) | NS 0,60 |
| Transfundidos | 24 (60%) | 16 (40%) | NS 0,12 |
| N.° bolsas/paciente | 1,6±0,3 | 0,8±0,2 | 0,04 |
| Pacientes con MACCE | 12 (30%) | 5 (12,5%) | 0,05 |
| Muerte 30 días | 3 (7,5%) | 1 (2,5%) | NS 0,30 |
| Endocarditis | 1 (2,5%) | 2 (5%) | NS 0,90 |
| Sangrado mayor reintervenido | 2 (5%) | 1 (2,5%) | NS 0,90 |
| IAM | 0 | 0 | N/A |
| Mediastinitis | 1 (2,5%) | 0 | N/A |
| Neumonía | 2 (5%) | 1 (2,5%) | NS 0,90 |
| Complicaciones respiratorias (neumotórax o derrame pleural) | 2 (5%) | 1 (2,5%) | NS 0,56 |
| IRA AKIN>2 | 4 (10%) | 3 (7,5%) | NS 0,71 |
| AVC | 2 (5%) | 0 | N/A |
| FA de novo postoperatoria | 8 (20%) | 5 (12,5%) | NS 0,36 |
| Marcapasos definitivo | 2 (5%) | 2 (5%) | NS 0,82 |
| Infección catéter con sepsis | 3 (7,5%) | 2 (5%) | NS 0,62 |
| Infecciones herida superficial | 3 (7,5%) | 1 (2,5%) | NS 0,55 |
AKIN: Acute Kidney Injury Network; AVC: accidente vascular cerebral; CEC: circulación extracorpórea; FA: fibrilación auricular de novo; IAM: infarto agudo de miocardio; IRA: insuficiencia renal aguda; MACCE: complicaciones mayores cardíacas y cerebrovasculares mayores; NS=no significativo; UCI: unidad de cuidados intensivos; N/A: no aplicable.
Frecuencia absoluta (%), mediana (rango intercuartílico), media±DE.
Resultado estadísticamente significativo si p ≤ 0,05.
Los beneficios de la CMI aórtica han sido ampliamente publicados, pero no se ha producido una generalización de su utilización debido a que los ensayos clínicos no los han confirmado, al estar mal diseñados respecto a su objetivo primario. Para detectar diferencias del 2% en mortalidad entre técnicas (principal end-point en cirugía cardíaca) son precisos cerca de 1.200 pacientes por cada grupo de estudio, lo que hace muy compleja su realización y provoca la proliferación de estudios retrospectivos pareados con puntuación de propensión.
El presente trabajo es un análisis retrospectivo de una población de pacientes subsidiarios de SVA pertenecientes al «mundo real», los cuales fueron pareados mediante puntuación de propensión y divididos en 2 grupos en función de si fueron operados con CC o con CMI. Esta serie es una de las escasas publicaciones sobre la materia acerca de este tema en España, a excepción del grupo del Hospital General de Valencia, publicado en 2013 y 201511,13, y del ensayo clínico de Aris et al.6 en 1999.
Por lo que se refiere al objetivo primario de comparar la incidencia de complicaciones MACCE en ambos grupos, los pacientes operados mediante CMI presentaron un menor porcentaje (12% vs. 30%), lo que representa el principal hallazgo del estudio y concuerda con la literatura publicada hasta la fecha11-16.
Asimismo, los metaanálisis previos15,16 detectaron un menor tiempo de intubación en los pacientes intervenidos, una menor mortalidad y una menor estancia en la UCI y hospitalaria a favor de la CMI. A pesar de la ausencia de significación estadística en nuestro estudio en cuanto a mortalidad y estancia hospitalaria, probablemente por el insuficiente tamaño de la muestra, se aprecia una tendencia favorable a menor mortalidad (3 casos CC frente 1 MINI, todos con complicaciones graves), menor tiempo de ingreso hospitalario (un día menos, mediana 7 días MINI vs. 8 días CC), sin existir diferencias en cuanto a tiempo mediano de intubación (5 h ambos grupos), estancia en UCI (3 días de mediana cada grupo) ni comorbilidades analizadas por separado.
En cirugía cardíaca, las transfusiones de hemoderivados son un factor predictivo de aumento de la morbimortalidad postoperatoria18, por lo que su reducción puede tener un gran impacto en los resultados. Uno de los hallazgos secundarios más importantes en este estudio son la menor pérdida de sangre durante las primeras 24 h tras la cirugía (202ml menos, p<0,001), con menores requerimientos transfusionales para los pacientes intervenidos con MINI (un 20% menos, que precisan la mitad de bolsas de concentrados de hematíes que con CC). Estos hallazgos son consistentes con los obtenidos por el grupo de Paredes et al.13 y con metanálisis15,16 y estudios previos19, donde las transfusiones se reducen a la mitad.
Otro factor importante observado en el grupo MINI es la menor tendencia de FA de novo postoperatoria (20% vs. 12.5%, p=NS), cardiovertida en la inmensa mayoría de casos con éxito (10/12, 83%). A pesar de que la etiología de la FA es compleja y multifactorial, esta reducción ya se ha visto en otros tipos de CMI, como la minitoracotomía anterior derecha, debido una menor manipulación de las estructuras20.
La técnica de MINI permite al cirujano mantenerse en la zona de confortabilidad quirúrgica, debido a la familiaridad de la exposición, acortando la curva de aprendizaje. Esto facilita enormemente la reconversión a CC en caso de complicación. La reconversión a esternotomía media durante una CMI suele ser debida a una mala exposición que dificulta la realización segura del reemplazo valvular. La tasa de reconversión está en torno al 3% en la literatura, similar a la observada en nuestra serie (2,5%).
En nuestra experiencia, los datos de morbimortalidad hospitalaria y supervivencia a 2 años demuestran que la CMI se puede realizar de forma segura y con resultados al menos tan buenos como los de la CC.
En 2015, el grupo de Borger et al.14, en un estudio de 477 pares de pacientes pareados mediante puntuación de propensión, encontró una mayor supervivencia estadísticamente significativa tanto precoz (0,4% MINI vs. 2,3% CC, p=0,013) como tardía (a 8 años MINI 77,7±4,7% vs. 72,8± 3,1% CC, p=0,034), siendo la MINI un factor independiente de supervivencia no solo a corto, sino también a largo plazo (OR=0,47; IC del 95%, 0,26-0,87), a expensas de solo 3-5min extra de tiempos de isquemia y CEC. Estos hallazgos deberán ser confirmados con otros estudios de cohortes actuales de pacientes, preferentemente ensayos clínicos.
Con la reciente introducción en el mercado de las válvulas Sutureless (Perceval S®, LivaNova, Londres, Reino Unido) o Rapid Valve Deployment (Edwards Intuity®, Edwards Lifesciences, Irvine, EE. UU.), los tiempos de CEC e isquemia se han reducido hasta un 45%, mejorando la morbilidad quirúrgica21,22. La unión de estas nuevas bioprótesis junto con la técnica de MINI puede motivar la designación de un nuevo «patrón oro» de la cirugía valvular aórtica aislada en un futuro cercano.
Limitaciones del estudioEste trabajo presenta los resultados de un único centro y tiene las limitaciones propias de los estudios retrospectivos. Al ser un estudio de pareado mediante puntuación de propensión, se puede haber pasado por alto la medición de variables ocultas e interdependientes, pero, sin embargo, nos ha permitido estudiar una población de pacientes aórticos «del mundo real». El hecho de que el estudio haya sido realizado durante la fase de «curva de aprendizaje» de la técnica mínimamente invasiva para muchos de los cirujanos puede haber influido en los resultados atenuando las bondades se esta técnica.
ConclusionesEn nuestra limitada experiencia, la CMI se asocia a ciertas ventajas más allá de lo cosmético frente a la CC, como son la menor aparición de complicaciones MACCE, menor sangrado postoperatorio durante las primeras 24 h y menor necesidad de transfusión. Los tiempos de isquemia y CEC fueron significativamente mayores en el grupo MINI (15 y 10 min extra, respectivamente).
En cualquier caso, son precisos ensayos clínicos aleatorizados para confirmar estos hallazgos para poder considerarla la técnica de elección para la SVA.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.