Se presenta el caso de un varón de 74 años con hipertensión arterial complicada con cardiopatía hipertensiva y vasculopatía arterial periférica, diabetes mellitus tipo 2 (DM2) de más de 15 años de evolución, obesidad grado i, enfermedad renal crónica (ERC) estadio IIIB y fibrilación auricular crónica. Jubilado, con adecuada situación sociofamiliar. Durante años, mantenía una actitud de negación de su enfermedad y mala adherencia a estilos de vida saludables y a los tratamientos farmacológicos. Presentaba un adecuado control metabólico de su DM2 con una HbA1c del 6,3% pero con un marcado deterioro de la función renal, habiendo pasado el filtrado glomerular de 43,2ml/min a 39,1ml/min en los últimos 4 meses. Por todo ello, se suspendió el tratamiento con metformina 850mg/12 h y glibenclamida 5mg/12 h y se pautó repaglinida 1mg antes de cada comida y linagliptina 5mg/24 h.
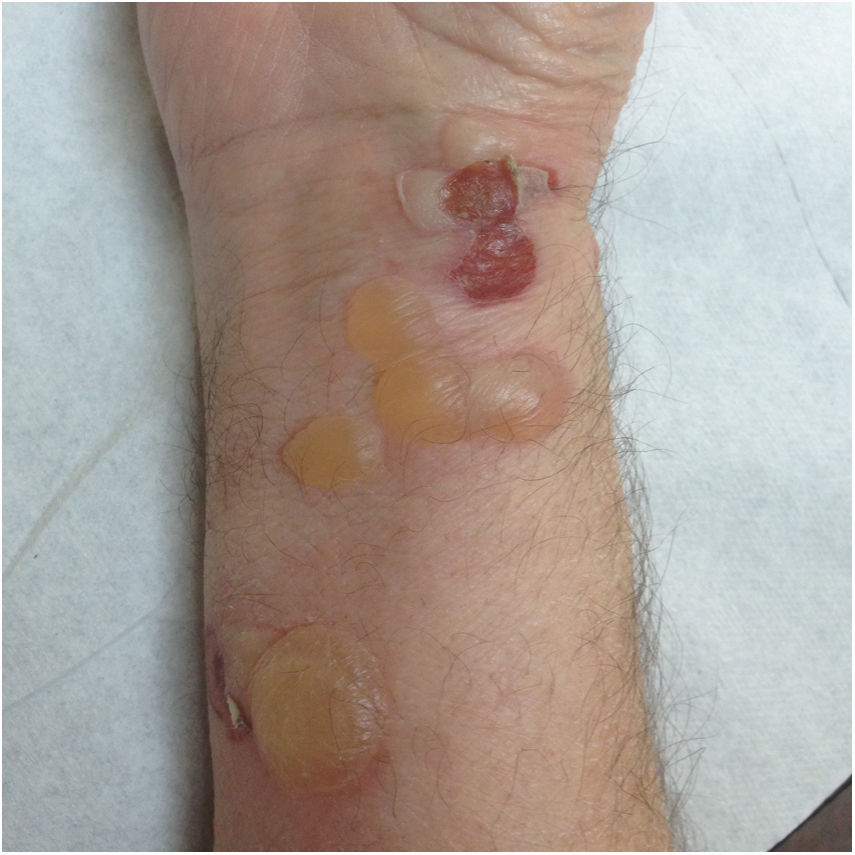
Dos semanas después de dicho cambio, acude al centro de salud por aparición de erupción cutánea polimorfa en placas eritematosas amplias, pruriginosas, en tronco y extremidades, que se etiquetó como «eritema a filiar». Cuatro días después acudió al servicio de urgencias por aparición sobre las placas, de ampollas tensas de contenido seroso sobre base urticariforme, sin afectación de mucosas (fig. 1). Valorado por el dermatólogo de guardia, y tras descartar clínicamente otras entidades, como el lupus eritematoso bulloso, el pénfigo vulgar, la dermatitis herpetiforme y el eritema multiforme ampolloso, se planteó como primera posibilidad diagnóstica el penfigoide ampolloso1 (PA) y como posible etiología una reacción adversa a linagliptina, recientemente pautada. Aunque el diagnóstico de PA es clínico, en este caso se realizó una biopsia que mostró:
- –
Histopatología compatible con PA:
- 1.
Perilesional: intenso edema de dermis papilar.
- 2.
Intralesional: infiltrado inflamatorio de intensidad variable con abundantes eosinófilos.
- –
Inmunofluorescencia directa negativa: hecho poco concordante, ya que se generan IgG frente a los BP 230 y BP 180 de la unión dermoepidérmica, observándose un depósito lineal.
Este resultado, algo inespecífico, permitió, sin embargo, un diagnóstico de presunción de PA secundario a linagliptina, por lo que se suspendió la linagliptina y se pautó metilprednisolona tópica sobre las lesiones 2 veces al día, demorando la decisión de iniciar un corticoide por vía oral dado que presentaba DM2. Al empeorar el cuadro clínico con aparición de nuevas lesiones en prácticamente todo el cuerpo, el paciente acudió a su médico de familia que pautó prednisona 30mg, dosis única por vía oral en el desayuno. Se recomendó control glucémico diario antes del almuerzo2, objetivándose glucemias en torno a 300mg/dl, por lo que se inició tratamiento con insulina NPH antes del desayuno, que en los días posteriores se fue titulando.
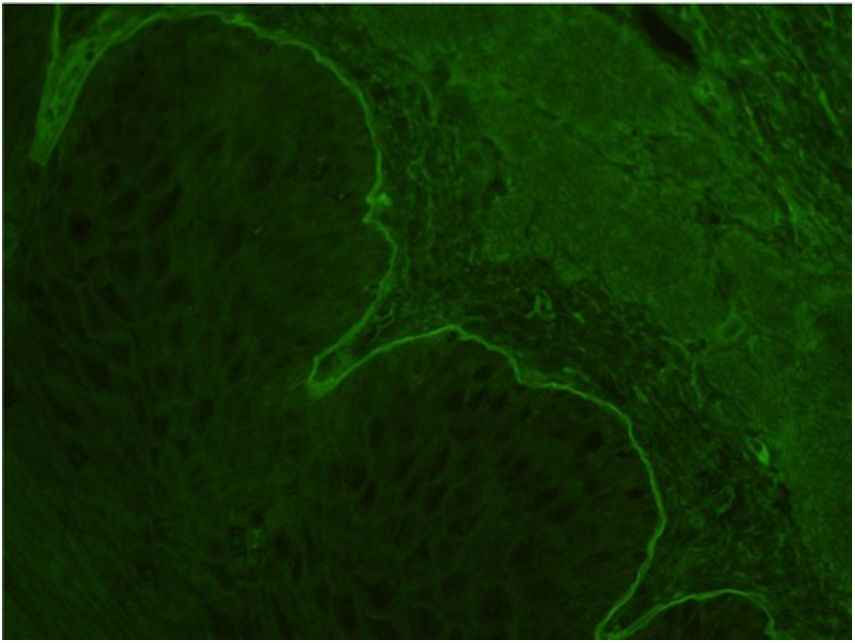
El cuadro dermatológico mejoró muy escasamente de manera que para su confirmación diagnóstica se amplió el estudio mediante inmunofluorescencia indirecta que fue positiva (depósitos de anticuerpos circulantes antimembrana basal en subepidermis) (fig. 2) y el test ELISA también positivo a título de 1/10 (método semicuantitativo para detectar anticuerpos anti-BP180, cuyo título no se correlaciona con la gravedad del cuadro). Se inició tratamiento con azatioprina 50mg/día (se suspendió el tratamiento con prednisona), experimentando una evidente mejoría clínica que era casi completa en 3 semanas. Tras la supresión de los corticoides, se mantuvo una dosis única diaria de 12 UI de insulina glargina 300 por la mañana como único fármaco hipoglucemiante.
El PA es la enfermedad ampollosa autoinmune más frecuente y suele afectar a ancianos plurimedicados. Existen 2tipos de PA en los que los fármacos pueden desempeñar un papel etiopatogénico diferente3:
- –
PA primario o autoinmune. La enfermedad se desarrolla, o no, en función de determinados estímulos externos (desencadenantes), como los fármacos. Son cuadros crónicos que evolucionan a PA ampollar idiopático aunque se suspenda el fármaco. En nuestro caso, la presencia de anticuerpos confirmó el origen. El mecanismo histopatológico es el depósito de autoanticuerpos (IgG) dirigidos contra proteínas de los hemidesmosomas BP 230 y BP 180: la unión de autoanticuerpos al antígeno BP 180 desencadena la liberación de IL-6 e IL-8, y la activación del complemento que induce la quimiotaxis de células inflamatorias, liberando proteasas responsables de la separación dermoepidérmica (ampolla).
- –
PA secundario. Provocado directamente por un agente externo (sin proceso autoinmune concomitante), como traumatismos, quemaduras, vacunas y «por fármacos». En este caso, son cuadros ampollares agudos que ceden al suspender el fármaco.
El tratamiento del PA son los corticoides tópicos, orales y, en casos graves o resistentes, los inmunosupresores (azatioprina, ciclofosfamida, micofenolato) o anti-CD 20 (linfocito B). También la plasmaféresis o las inmunoglobulinas por vía intravenosa en cuadros más graves y resistentes1.
Lo interesante del caso es que se trata de un evento escasamente descrito en la literatura y, en general, más frecuentemente descrito con otros inhibidores de la enzima DPP4 (IDPP-4)4-6, pero no tanto con linagliptina7,8. Además, existen dudas de si la relación de causalidad entre los IDDP-4 y el PA se produce estando en asociación con metformina o por sí solos. Nuestro caso corroboraría la posibilidad de PA en relación con linagliptina sin metformina4,5. En este caso, aunque no podemos asegurar fehacientemente la relación causa-efecto entre la toma del IDPP-4 y la aparición del PA, si evaluamos la causalidad con la escala de Naranjo podemos afirmar que la relación es «probable».
En resumen, se trata de un caso de PA probablemente secundario a linagliptina que pone de manifiesto muchos de los retos a los que se enfrenta el médico de familia en el cuidado de las personas, retos como:
- –
Conocer los principales efectos adversos de los fármacos9, hecho complejo a veces cuando no son muchos los casos descritos. De ahí la importancia de su comunicación al sistema de farmacovigilancia cuando se identifican y de su difusión.
- –
Determinar el balance riesgo-beneficio de iniciar un tratamiento. ¿Era necesario pautar linagliptina en un paciente de 74 años con pluripatología (enfermedad cardiovascular establecida, ERC, etc.), una DM2 de larga evolución y una HbA1c de 6,3%? Según las actuales recomendaciones10, quizá no hubiera sido necesaria una pauta tan intensiva dado el adecuado grado de control metabólico (HbA1c 6,3%) en un paciente de sus características.
- –
La adherencia es otro de los grandes retos. El paciente descrito presentaba una comprobada dificultad para el cumplimiento para los tratamientos farmacológicos desde hacía años. Optar por pautas sencillas contribuye a mejorar este aspecto y quizá la pauta con repaglinida más linagliptina no era especialmente sencilla (4 «pastillas», administración cada 8 h, riesgo de hipoglucemia), si bien este hecho no parece haber tenido que ver con el cuadro descrito.
Para la realización de esta publicación y la utilización de imágenes, se han seguido los protocolos del centro de trabajo, se cuenta con el consentimiento del paciente y se ha respetado la privacidad del mismo.
Conflicto de interesesNo ha existido fuente de financiación ninguna ni conflicto de intereses.