138 - TRATAMIENTO DE LA ARTRITIS REUMATOIDE CON FILGOTINIB: DATOS DE SEGURIDAD EN LA SEMANA 156 DE UN ESTUDIO DE EXTENSIÓN ABIERTO DE FASE 2B
1Parc Taulí Hospital Universitari, Sabadell. 2University of California, San Diego, School of Medicine, La Jolla, CA (EEUU). 3University Hospital KU Leuven, Leuven (Bélgica). 4Oregon Health and Science University, Portland, OR (EEUU). 5Gilead Sciences, Inc., Foster City, CA (EEUU). 6Galapagos NV, Mechelen (Bélgica). 7Schlosspark-Klink University Medicine, Berlin (Alemania). 8Stanford University, Palo Alto, CA (EEUU).
Introducción: El filgotinib (FIL) es un inhibidor de janus quinasas 1 selectivo y oral que ha demostrado su efectividad y buena tolerancia en pacientes con distintas enfermedades inflamatorias. DARWIN 3 (D3) es un estudio abierto, en curso, de extensión a largo plazo de fase 2b que evalúa la seguridad y eficacia de FIL en artritis reumatoide (AR).
Métodos: Pacientes con AR y respuesta inadecuada a metotrexato (MTX) que completaron los estudios de 24 semanas DARWIN 1 (D1: FIL+MTX) o DARWIN 2 (D2: FIL monoterapia) participaron en D3. Los pacientes recibieron FIL 200 mg/día o 100 mg/día. Se presenta el análisis preliminar en la semana 156 (S156). La tasa de eventos está calculada como eventos totales/años totales de exposición a FIL.
Resultados: 877 pacientes completaron D1 y D2. 739 pacientes se reclutaron para D3 (497: D1; 242: D2). La mayoría eran mujeres: 81,5%/81,8%; blancas: 75,3%/74,8%; y de edad media: 53/52 años (D1/D2). En la S156, 59,9% de pacientes permanecieron en el estudio. Los motivos más frecuentes para suspensión fueron: eventos adversos (AEs: 26,5%), solicitud del paciente (9,1%). La exposición total a FIL fue de: 2.203 pacientes-año; exposición media ± DE: 3,04 ± 1,22 años (FIL+MTX) y 2,86 ± 1,21 años (FIL monoterapia). Los AEs surgidos durante el tratamiento (TEAE): 419 (84,3%) pacientes en FIL+MTX y 203 (83,9%) pacientes en FIL monoterapia; TEAE graves: 45 (9,1%) y 33 (13,6%) pts, respectivamente. Las tasas de AEs de interés especial permanecieron bajas en la S156 (tabla). Se registraron 5 muertes (FIL+MTX: 2, FIL monoterapia: 3), 0 tras la S132. Se mostró eficacia clínica en la S156 en FIL+MTX y FIL monoterapia respectivamente medido en ACR20 (87,2%/89,7%), ACR50 (72,4%/63,0%), ACR70 (45,5%/40,0%), DAS28(CRP) ≤ 3,2 (69,0%/64,7%) y DAS28 (CRP) < 2,6 (53,4%/45,6%).
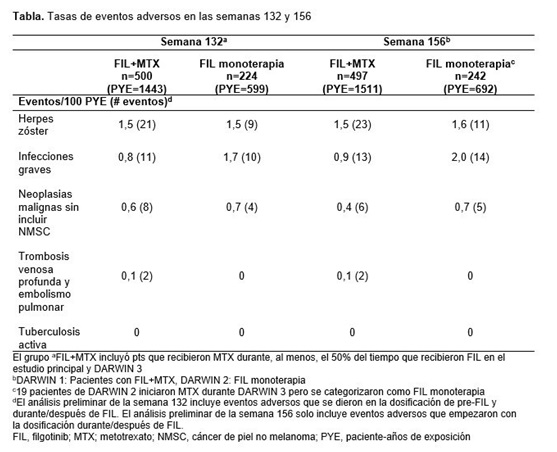
Conclusiones: FIL ha tenido buena tolerancia; no surgieron nuevas señales de seguridad. No se observaron diferencias en seguridad en pacientes que recibieron FIL+MTX o FIL monoterapia. Se mantuvo la eficacia hasta la S156 en ambos grupos de tratamiento.








